Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión On-line ISSN 1561-3011
Rev Cubana Invest Bioméd v.21 n.1 Ciudad de la Habana ene.-mar. 2002
Instituto Nacional de Endocrinología
Determinación de la hormona luteinizante (LH) en plasma por un método inmunoenzimático
Dra. Edelis Castellanos Puerto, Dra. María Celeste Arranz Calzado, Dra. Bertha V. Rodríguez Pendás, Dra. Gema García Dafonte y Dr. Roberto M. González Suárez
Resumen
Se presentaron los resultados del montaje y la estandarización de un método inmunoenzimático (EIA) para la determinación de la hormona luteinizante (LH), que utiliza un anticuerpo policlonal y un anticuerpo monoclonal producidos ambos en el laboratorio. Este EIA tipo sandwich de LH, demostró ser preciso, sencillo, rápido y sensible (0,7 U/L), que tiene un rango dinámico entre 0,8 a 100 U/L para la detección de LH en plasma. La validación clínica del método se realizó en 151 muestras, 21 de hombres sanos entre los 20 y 35 años de edad, 20 mujeres sanas en edad fértil en las 3 etapas diferentes del ciclo menstrual, 20 embarazadas entre las 9 y 30 semanas de gestación, 20 niños prepuberales, 20 mujeres posmenopáusicas. Se compararon los resultados obtenidos usando este método con la determinación efectuada por el método de radioinmunoanálisis (RIA) de referencia (HRP-OMS), empleado en el Instituto Nacional de Endocrinología de Cuba y se obtuvo una correlación de 0,67 y una pendiente de 0,58. El método desarrollado representa una alternativa (no isotópica) para la determinación de LH en plasma.
DeCS: HL/análisis; TECNICAS PARA INMUNOENZIMAS/métodos; TEST DE ELISA; PLASMA.
Las hormonas gonadotrópicas: luteinizante (LH), folículo estimulante (FSH) se producen y secretan por la hipófisis, y la gonodatropina coriónica (HCG) es de origen placentario; la LH y la FSH son las que regulan la función reproductora en los mamíferos y ejercen sus acciones primarias sobre las gónadas.1 La LH estructuralmente tiene 2 cadenas polipeptídicas, la cadena alfa (a) y la cadena beta (b) que es la encargada de la especificidad de acción a los receptores de cada hormona.2 Su cuantificación es útil para la predicción y determinación de la ovulación, además para el estudio y tratamiento de la infertilidad y la planificación familiar.3 También es útil en el diagnóstico y pronóstico de los pacientes con tumores pituitarios secretores de gonodatropinas, específicamente de LH.4
En este trabajo se propuso como principal objetivo validar el método inmunoenzimático, correlacionar los valores de LH obtenidos en el ELISA con los métodos de referencia (RIA) y evaluar sus parámetros operativos y de calidad en las condiciones de laboratorio; para lo cual se diseñó un sistema inmunométrico tipo sandwich que emplea un anticuerpo policlonal de alta avidez como elemento de captura, un anticuerpo monoclonal de alta especificidad y un sistema de amplificación que asegura una alta sensibilidad al ensayo.
Métodos
Montaje y validación del ensayo
Primero se produjeron y caracterizaron los reactivos primarios, se seleccionaron las concentraciones y los tiempos de incubación para calibrar el sistema y establecer parámetros de normalización.
Las hormonas LH, TSH y FSH fueron obtenidas en el Instituto Nacional de Endocrinología (INEN) y calibradas contra los estándares internacionales de la OMS. La HCG fue donada por los laboratorios "Mario Muñoz" IMEFA. Los restantes reactivos fueron químicamente puros obtenidos de Merck o BDH.
Anticuerpos
El antisuero policlonal anti LH 1046 fue obtenido en el INEN. La reactividad cruzada para la TSH resultó de 10 %, para FSH 8 % y para la HCG de 29 %.
Los anticuerpos monoclonales usados fueron el AcM-Lh LD4 y BG7. Su actividad inmunológica se evaluó en trabajos previos por RIA y por ELISA de IgG de ratón.5 Sus concentraciones fueron determinadas también por el método de Lowry con la utilización de BSA como estándar.6 A partir del estándar de LH liofilizado se prepararon concentraciones para los diferentes puntos de la curva de calibración del ensayo: 0,8; 1,6; 3,2; 6,25; 12,5; 25; 50 y 100 U/L de LH en tampón del ensayo.
Para la especificidad se determinó la reacción cruzada en el EIA con la utilización de hormonas puras de FSH, TSH y HCG a concentraciones desde 1 000 ng/mL hasta 1 ng/mL, las cuales fueron enfrentadas en el ensayo como curvas patrones al igual que el estándar de LH en un mismo ensayo.7
La validación clínica del ensayo se realizó de acuerdo con los valores obtenidos en sujetos en los que no se encontraron enfermedades ni afecciones endocrinas o estaban sometidos a tratamiento hormonal, los cuales tenían diversas condiciones fisiológicas como hombres sanos entre 20 y 35 años de edad (n= 21), mujeres fértiles sanas entre 20 y 35 años de edad (n= 20) que tuvieran ciclos menstruales regulares (28-30 d), mujeres en estado posmeno-páusico, sanas, mayores de 50 años que no menstruaran por lo menos desde 3 años atrás (n= 20), niños prepúberes (hembras y varones) entre los 9-11 años (n= 20), embarazadas sanas sin complicaciones entre los 20 y 35 años de edad, con edades gestacionales entre las 9-22 semanas (n= 20). Se utilizaron 3 controles de calidad previamente preparados para el RIA-LH INEN, con diferentes concentraciones de LH alto, medio y bajo, según los valores de la curva estándar.
Resultados
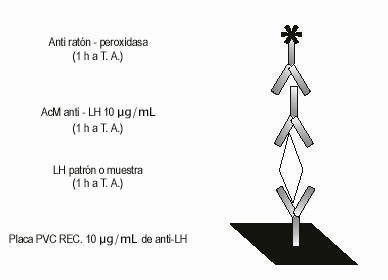
En la figura 1 se muestra esquemáticamente el ensayo. Las condiciones escogidas fueron de 10 ug/mL de anticuerpo policlonal (AcP) en el recubrimiento y 10 ug/mL del monoclonal (AcM); ambos clones se comportaron igual en cuanto a sensibilidad (B) y rango dinámico, además ninguno reconocía a la FSH, la TSH y la HCG ni aun a altas concentraciones como 1 000 ug/mL.
Fig. 1. Procedimiento del método conjugado.
Tabla. Niveles de LH en situaciones fisiológicas
| ELISA | RIA | |||||
| Diagnóstico | N | X | DE | N | X | DE |
| Hombres sanos | 21 | 4,1 | 7,38 | 21 | 3,1 | 3,49 |
| Mujeres: | ||||||
| - Fase pre-ovulación | 17 | 1,9 | 1,6 | 17 | 3,7 | 2,28 |
| - Fase peri-ovulación | 17 | 7,2 | 6,2 | 17 | 13,9 | 15,8 |
| - Fase pos-ovulación | 17 | 2,6 | 2,5 | 17 | 4,3 | 1,9 |
| Embarazadas | 20 | 0,9 | 0,3 | 20 | 303 | 170 |
| posmenopáusica | 20 | 22,1 | 14,3 | 20 | 33,7 | 19,1 |
| Niños prepúberes | 20 | 1,35 | 1,85 | 20 | 4,56 | 6,19 |
El límite de detección calculado en 22 ensayos independientes fue de 0,7 U/L de LH. La exactitud se obtuvo con una recuperación entre 85 - 103 % en 3 ensayos diferentes con un CV entre 5 y 6 %. En el análisis del paralelismo se observa que entre la curva que describe los valores obtenidos por dilución seriada de las muestras (B) y la curva patrón (A) existe paralelismo (fig. 2), el cual se corrobora al aplicarle el programa estadístico de comparación de rectas que demostró que ambas son rectas paralelas y coincidentes. A pesar de no encontrar reacción cruzada en los ensayos de RIA en fase sólida y fase líquida en estudios anteriores,5 a altas concentraciones de FSH, TSH y HCG (1 000 ng/mL); se encontró reacción cruzada en el ELISA para la HCG.
Fig. 2. Calibración y paralelismo MICROELISA de LH.
Para mostrar la precisión del ELISA de LH en plasma humano se usaron controles de calidad alto, medio y bajo, con coeficientes de variación aceptables para este tipo de método.
El análisis de regresión entre los resultados de la determinación por RIA y ELISA se muestra en la figura 3. Se observa que la pendiente es de 0,58, la regresión de 0,67 y el intercepto de 2,1. La tabla muestra los resultados obtenidos en sujetos en situaciones fisiológicas conocidas en las que se modifican las concentraciones de LH, donde se pueden ver además las oscilaciones de un ciclo menstrual completo en ambos métodos.2
Fig. 3. Análisis de regresión de las muestras de LA por RIA y ELISA
Discusión
La reactividad cruzada del EIA con la HCG se atribuye a la presencia del AcP en el recubrimiento y fue de 29 %, por lo que estudios posteriores se deben encaminar a sustituir el AcP por un AcM, que reconozca un epitope diferente de la hormona para no limitar su uso.
Los resultados del EIA fueron inferiores en 50 % a los del RIA debido a las diferencias entre las especificidades de los Acs utilizados en cada método,7 pero el ensayo fue más sensible (0,7 U/L) que el RIA de uso actual (1,1 U/L), lo cual permite el monitoreo de casos con bajas concentraciones de LH como sucede al inicio de la pubertad y en casos patológicos.8,9
La sensibilidad de este método permitiría realizar la determinación de LH en orina, pues la toma de la muestra es más fácil al igual que su procesamiento.10
El amplio rango de este ensayo (0,7- 100 U/L) también permite la dosificación de altas concentraciones de LH en estados fisiológicos como la menopausia y en la detección de algunos tumores hipofisarios.3,4
Los resultados de este trabajo son comparables con los estudios multicentros realizados por otros investigadores10,11 donde se emplean métodos enzimáticos y no instrumentales, por lo que este EIA sería una alternativa no isotópica para la determinación de LH.
Summary
The results of the mounting and standardization of an immunoenzimatic assay (IEA) to determine LH by using a polyclonal antibody and a monoclonal antibody, produced both at the laboratory, are shown. This sandwich IEA of LH proved to be accurate, simple, rapid and sensitive (0.7 U/L) with a dynamic range from 0.8 to 100 U/L for the detection of LH in plasma. The clinical validation of the method was made in 151 samples, 21 of sound males aged 20-35, 20 of sound females at fertile age in the 3 different stages of the menstrual cycle, 20 of pregnant women between 9 and 30 months of gestation, 20 of prepuberal children and 20 of postmenopausal women. The results were compared by utilizing this method with the determination obtained by the radioimmunoanalysis (RIA) reference method (HRP-WHO) used at the National Institute of Endocrinology of Cuba. A correlation of 0.67 and a slope of 0.58 were attained. The method developed represents an alternative (non-isotopic) for the determination of LH in plasma.
Subject headings: LH/analysis; IMMUNOENZYME TECHNIQUES/methods; ENZIME-LINKED IMMUNOSORBENT ASSAY; PLASMA.
Referencias bibliográficas
- Daughady WH. Hormonas glicoproteicas. En: Daughady WH. Tratado de Endocrinología. 5ta. ed. La Habana: Editorial Científico-Técnica, 1987:88-91.
- Charles WM. The antigenic structure of the human glicoprotein hormone alpha subunit. Caracterization of anti-alpha monoclonal antibodies. Endocrinology 1990;127(6):2977-84.
- Mateo de Acosta O. Manual de diagnóstico y tratamiento en Endocrinología y Metabolismo. La Habana: Editorial Científico-Técnica, 1985.
- White MC. LH and FSH secretion and response to Gn. Rh and patients whith clinically functionaless pituitary adenoma. Clin Endocrinol 1990;32(6):681-9.
- Rodríguez B, Machado AJ, Arranz MC. Obtención y caracterización parcial de anticuerpos monoclonales generados contra la hormona luteinizante humana. Biotecnol Aplic 1997;14:101-5.
- Lowry DH, Rosebrougth NL, Parr AL, Randall RJ. Protein measurement whith Folin Phenol Reagent. J Biol Chem 1951;139:765-6.
- Lordey H. Validation of highly specific and sensitive RIA for Lutropin, gonatropin and free alpha subunit in unextrated urine. Clin Chem 1990;36(2):340-4.
- Mardersbecher S, Wolf H, Gerth R, Berger P. Increased ELISA sensitivity using a modified method for conjugating horseradish peroxidase to monoclonal antibodies. J Immunol Methods 1992; 152(1):9-13.
- Andino Valdés NA. Radioinmunoensayo de LH y FSH. Valores normales en una muestra de la población cubana masculina sana. Rev Cubana Obstet Ginecol 1980;6:319.
- Weiss P, Zech H, Peter H, Fritzche H. Abbot Imx and Serono MAIA close assays compared for entropin determinations in urine. Clin Chem 1992;38(11):280-3.
- Thijssen JH, Wood WG, Kessler AC, Griesser HN, Bauer O, Bieglmayer C. Multicenter evaluation of new enzime-linked immunoassay of FSH and LH in serum or plasma. Clin Chem 1991;37(7):1257-63.
Recibido: 16 de febrero de 2000. Aprobado: 12 de abril de 2001.
Dra. Edelis Castellanos Puerto. Instituto Nacional de Endocrinología. Zapata y D, El Vedado, Ciudad de La Habana, Cuba. CP 10400.