Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión On-line ISSN 1561-3011
Rev Cubana Invest Bioméd v.21 n.1 Ciudad de la Habana ene.-mar. 2002
Instituto de Ciencias Básicas y Preclínicas Victoria de Girón
Valores de alfa-fetoproteína en pacientes con hepatitis viral crónica
Dra. Zulema Adorna Carmenate y Dra. Mercedes Gámez Fonseca
Resumen
Se determinó alfa-fetoproteína (AFP) sérica en 59 pacientes con el objetivo de conocer sus niveles y la variación en el tiempo. Estos pacientes tenían diagnóstico de hepatitis viral crónica B o C, confirmado por biopsia hepática. La AFP se midió cada 4 meses durante 1 año mediante electroquimioluminiscencia en un analizador automático. En la determinación inicial 100 % presentó cifras normales. En las mediciones evolutivas se mantuvo en rango normal, excepto en 2 casos con valores ligeramente elevados. Se observó tendencia al aumento en la segunda medición en 37,5 % de los pacientes con actividad necroinflamatoria severa y fibrosis marcada según biopsia. Se concluye que el porcentaje de pacientes con valores normales de AFP en la hepatitis viral crónica es elevado, y no se modifica significativamente en el tiempo.
DeCS: HEPATITIS VIRAL HUMANA/enzimología; ALFAFETOPROTEINAS/análisis; INMUNOENSAYO/métodos.
La alfa-fetoproteína (AFP) es una glicoproteína que está incluida dentro de las pruebas que permiten evaluar la función hepática, específicamente la capacidad biosintética del hígado. Se asemeja a la albúmina y pertenece al grupo de proteínas fetales. En adultos sanos, con exclusión de mujeres embarazadas, se presenta en concentraciones muy bajas, solo detectadas por métodos inmunológicos muy sensibles.1 Se sabe que en los tumores desarrollados en tejidos que tienen componentes estructurales embrionarios, es posible detectar una neosíntesis considerable de AFP. Tal es el caso del carcinoma hepatocelular (CHC), entidad patológica en la que se reporta internacionalmente hasta 70-90 % de pacientes con AFP sérica elevada.2 También puede encontrarse elevada en otros tumores malignos como son: tumor de células germinales, carcinomas gástrico, pancreático, esofágico, de vejiga y de recto. Con excepción del tumor de células germinales, en general muestran valores por debajo de 350 - 400 UI/mL.3
En las últimas 2 décadas varios investigadores han reportado niveles séricos elevados de AFP en pacientes con hepatitis viral crónica, con cirrosis o sin ella.1,4-6 Estos estudios han arrojado una gran variación en cuanto al grado de elevación de la AFP y la proporción de pacientes que presentan esta anomalía.
En Cuba, en 1990 se llevó a cabo una investigación por el Centro de Inmunoensayos, en la que se utilizó la determinación de AFP en el pesquisaje de neoplasias en una población mayor de 50 años supuestamente sana (Centro de Inmunoensayos. Resumen de los principales resultados obtenidos. Enero 1990. CIE. La Habana, Cuba). Sin embargo se desconoce cómo se comporta esta variable en nuestros pacientes con hepatitis viral crónica, lo cual pudiera ser útil en el seguimiento evolutivo de esta enfermedad.
El propósito de este trabajo consistió en conocer los valores de AFP que presentan los pacientes con hepatitis B o C, y su variación en el tiempo.
Métodos
Se llevó a cabo un estudio obser-vacional prospectivo en pacientes con hepatitis viral crónica B o C, a los que se les determinó AFP en suero. Esta variable se midió evolutivamente cada 4 meses durante un año.
La muestra estuvo integrada por 59 pacientes, con edades comprendidas entre 16 y 76 años, que asistieron a la consulta de hepatología del Servicio de Gastroenterología del Hospital Clinico-quirúrgico "Hermanos Ameijeiras", a los cuales se les diagnosticó hepatitis viral B o C crónica. El muestreo realizado fue de tipo discrecional.
Se consideraron crónicos aquellos pacientes que presentaron antígeno de superficie positivo por más de 6 meses (hepatitis B) o aquellos que presentaron anticuerpos contra el virus C por más de 6 meses y valores de transaminasas elevados (hepatitis C). Este diagnóstico estuvo confirmado además por la biopsia hepática indicada por el gastroenterólogo.
Se excluyeron del estudio los pacientes menores de 15 años, pacientes con hepatitis aguda, hepatopatías de otra etiología, doble infección B y C, tumores productores de AFP diagnosticados y embarazadas. En ningún caso habían recibido tratamiento antiviral previo.
La distribución de los pacientes en estudio según tipo de hepatitis y sexo fue como se muestra en la tabla 1. Por las características de su enfermedad, una gran proporción de estos pacientes es de difícil seguimiento. Esto influyó en que la muestra en las determinaciones evolutivas estuviera conformada como se presenta en la tabla 2.
Tabla 1. Distribución de pacientes según tipo de hepatitis y sexo
| Sexo | Hepatitis B | Hepatitis C | Total |
| Femenino | 6 | 19 | 25 (42 %) |
| Masculino | 18 | 16 | 34 (58 %) |
| Total | 24 (41 %) | 35 (59 %) | 59 |
Tabla 2. Total de pacientes en cada determinación de AFP
| AFP 1 | AFP 2 | AFP 3 | AFP 4 | |
| Pacientes | 59 | 32 | 14 | 7 |
En el seguimiento de estos enfermos se repitieron las determinaciones de AFP cada 4 meses hasta el año; por lo que se contó con 4 valores de esta variable al finalizar el tiempo de estudio.
La AFP fue determinada en el analizador automático Elecsys 2010, mediante inmunoensayo de electroquimioluminiscencia (EQL) con técnica sandwich.7 Se consideró normal la AFP sérica hasta el valor de 11,5 UI/mL. Para realizar el análisis de los datos se utilizó el software SYSTAT 7.0. Se realizó una prueba pareada y análisis de observaciones repetidas para determinaciones evolutivas de AFP. Se calcularon estadísticas descriptivas (que incluyen media, mediana, desviación estándar e intervalo de confianza 95 %) para la variable cuantitativa AFP.
Resultados
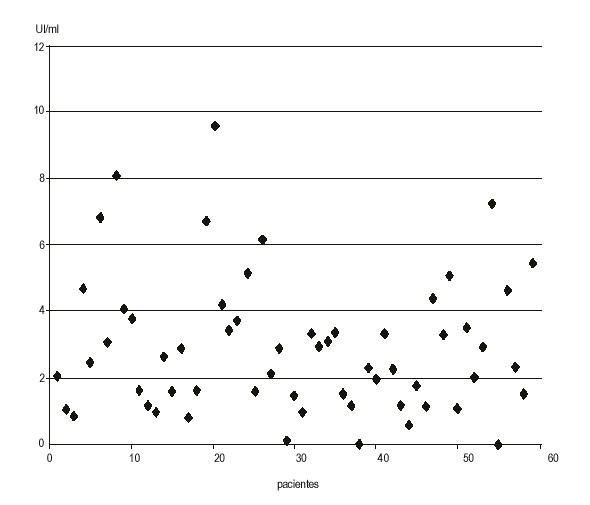
Todos los pacientes presentaron cifras dentro del rango normal en la determinación inicial de AFP. La dispersión de los valores obtenidos se muestra en la figura 1.
Fig.1. Dispersión de los valores iniciales de alfa-fetoproteína.
El valor medio de esta variable para los 59 pacientes fue de 2,92 UI/mL (mediana 2,46; desviación estándar 2,04).
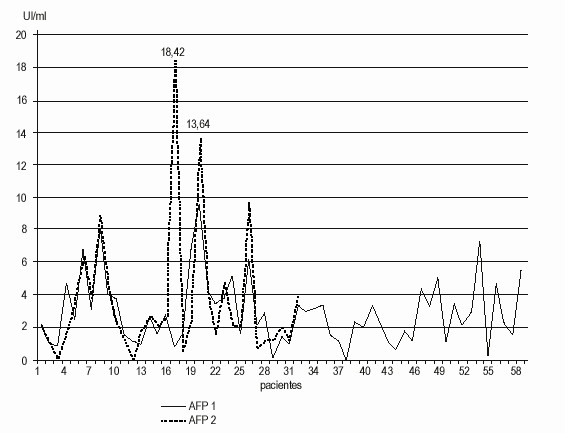
Según el tipo de hepatitis, se obtuvieron los resultados iniciales de AFP (UI/mL) mostrados en la tabla 3. En las mediciones evolutivas la AFP se mantuvo dentro del rango normal, excepto en 2 casos (13,64 y 18,42 UI/mL).
Tabla 3. Valores iniciales de AFP según tipo de hepatitis
| Tipo de hepatitis | Media | Mediana | Desviación estándar |
| B | 3,31 | 2,91 | 2,45 |
| C | 2,65 | 2,32 | 1,69 |
La variación de las cifras de AFP2 con respecto a AFP1, analizada mediante prueba pareada, no resultó significativa (t= -.464, p= .646). Esto se corroboró con un análisis de observaciones repetidas para la AFP que dio como resultado que no hay cambio temporal significativo (F= .245, p= .787). Sin embargo, se observó una tendencia al aumento en la segunda determinación en 3 casos (fig. 2).
Fig.2. Evolución de la alfa-fetoproteína en las dos primeras determinaciones.
Discusión
Si bien han sido numerosos los hallazgos de AFP elevada en pacientes con hepatitis viral crónica, la mayoría de los reportes plantean la presencia de esta anomalía en un amplio rango que va desde el 11 hasta 58 %.4,8-10 Además, el nivel de corte empleado en los distintos estudios no ha sido siempre el mismo. Por lo general se ha considerado la AFP elevada por encima de los 10 ng/mL, aunque existen pequeñas diferencias que dependen de las normas empleadas en cada laboratorio.
En este estudio, a pesar de que en la determinación inicial de AFP todos los pacientes presentaron cifras normales (menores o iguales que 11,5 UI/mL ó 13,8 ng/mL respectivamente), en la segunda medición 2 pacientes tuvieron valores moderadamente alterados. Esto representa 6,25 % del total de pacientes a los que se les realizó una segunda medición de AFP. Además, los niveles alcanzados por estos casos con AFP alterada coinciden con lo descrito por otros autores, porque se plantea que la mayoría de estos pacientes presenta ligera o moderada elevación de la AFP.11-15
Los resultados aquí obtenidos son similares a los de Stransk en 1993, que de 83 pacientes con hepatitis viral crónica sin cirrosis estudiados, solo 7,2 % tuvo la AFP alterada.5
En 1995, Sherman midió AFP en 1 069 pacientes con hepatitis viral crónica B, y en la determinación inicial 4 % tenía AfP igual o mayor que 20 ng/ml14 En ese año, Tong y otros describieron AFP elevada solamente en 10 % de sus casos, que incluso presentaban ya cirrosis hepática.14
En un estudio realizado por Forones, con la finalidad de conocer el comportamiento de la AfP en las distintas situaciones clínicas en las que puede elevarse, de 81 pacientes incluidos con hepatitis viral crónica solo 13,5 % tenía AFP> 15 ng/mL.9 Al investigar la microheterogeneidad de la AFP, Raedle y otros contaron en su muestra con 14 % de pacientes con hepatitis viral crónica que tenían AFP> 20 ng/mL.10 Asimismo Fattovich reporta que 43 % de sus pacientes cirróticos compensados tuvieron valores de AFP elevada.15
Bayati, en 1998, tuvo 13 % de sus pacientes con hepatitis viral crónica C sin cirrosis con AFP alterada.9 En 1999, Peng encontró que 89,3 % de sus pacientes con hepatitis viral crónica por virus C tenían AFP menor que 20 ng/mL, e incluso 34,3 % tenía valores inferiores a 5 ng/mL.11
Aunque no hubo variación significativa de los niveles de AFP en el tiempo, se observó una tendencia al aumento en la segunda determinación en 3 casos de un total de 8 pacientes (37, 5 %), en los que coincidieron actividad necroinflamatoria severa y fibrosis marcada o cirrosis. Consideramos que en este tipo de pacientes sí puede resultar útil el seguimiento cada 4 o 6 meses con determinación sérica de AFP, en coincidencia con lo propuesto por Izzo en 1998 al plantear que el seguimiento con AFP y ultrasonografía debe ser reservado para pacientes con hepatitis crónica con un alto grado de actividad, fibrosis o ambas.16 Este ha sido el intervalo de seguimiento planteado por varios autores para pacientes considerados con riesgo de presentar un CHC.17-19
Se concluye que el porcentaje de pacientes con valores de AFP no se modifica significativamente, en el tiempo estudiado.
Summary
The serum alpha-fetoprotein (AFP) was determined in 59 patients aimed at knowing its levels and variation with time. These patients had a diagnosis of chronic viral hepatitis B or C, confirmed by liver biopsy. AFP was measured every 4 months during a year by electrochemoluminiscence in an automatic analyzer. 100 % had normal figures in the initial determination. A normal range was maintained in the evolutive measures, excepting 2 cases with slightly elevated values. A trend toward increase was observed in the second measurement in 37.5 % of the patients with severe necroinflammatory activity and marked fibrosis according to biopsy. It was concluded that the percentage of patients with normal values of AFP in chronic viral hepatitis is elevated and that it is not significantly modified with time.
Subject headings: HEPATITIS, VIRAL, HUMAN/enzimology; ALPHA-FETO PROTEINS/analysis: IMMUNOASSAY/methods.
Referencias bibliográficas
- Abelev GI. 25 Years of the study of alpha-fetoprotein. Ontogenez 1989;20(6):607-15.
- Abelev GI, Eraiser TL. Cellular aspects of alpha-fetoprotein reexpression in tumors. Semin Cancer Biol 1999; 9(2):95-107.
- Abelev GI, Sell S. Tumor markers. Introduction. Semin Cancer Biol 1999 Apr; 9(2):65-5.
- Weinberg DS, Malet PF. Chronic hepatitis C and markedly elevated serum alpha-fetoprotein; complete response to treatment with alpha interferon. Am J Gastroenterol 1994;89(8):1253-54.
- Stransk YJ, Zichova M, Vodak M. Assessment of alpha-fetoprotein in chronic HbsAg carriers and in HbsAg negative cirrhosis of the liver. Sb Lek 1993;94(4):311-5.
- Saito S, Ikeda K, Koida I. The diagnosis of HCC determined by pattern of alpha-fetoprotein bands separated by Con A affinity electrophoresis. Nippon Shokakibyo Gakkai Zasshi 1994 91(8):1301-8.
- Operators Manual. Elecsys 2010 System. Edition Boehringer Mannheim 1998;58-65.
- Forones NM, Queiros LA, Ferraz ML. AFP in hepatic tumors and benign liver diseases. Rev Assoc Med Bras 1995;41(2):91-3.
- Bayati N, Silverman AL, Gordon SC. Serum alpha-fetoprotein levels and liver histology in patients with chronic hepatitis C. Am J Gastroenterol 1998;93(12):2452-6.
- Raedle J, Roth WK, Oremek G. Anti-p53 autoantibodies in hepatitis C virus infected patients. Anticancer Res 1997 17(4):3079-81.
- Peng YC, Chan CS, Chen GH. The effectiveness of serum alpha-fetoprotein level in anti-HCV positive patients for screening hepatocellular carcinoma. Hepatogastroenterology 1999; 46(30):3208-11.
- Goldstein NS, Blue D, Hankin R, Hunter S, Bayati N. Serum alpha-fetoprotein levels in patients with chronic hepatitis C. Relationships with serum alanine aminotransferase values, histologic activity index, and hepatocyte MIB-1 scores. Am J Clin Pathol 1999;111:811-6.
- Sherman M, Peltekian KM, Lee C. Screening for hepatocellular carcinoma in chronic carriers of hepatitis B virus. Hepatol 1995;22(2):432-8.
- Tong M, El-Farra NS, Reikes AN. Clinical outcomes after transfusion-associated hepatitis C. N Engl J Med 1995;332:1463-6.
- Fattovich GF, Giustina G, Degos F. Morbidity and mortality in compensated cirrhosis type C: a retrospective follow-up study of 384 patients. Gastroenterology 1997;112:463-72.
- Izzo F, Chemona F, Ruffolo T, Palaia R. Outcome of 67 pacients with hepatocellular cancer detected during screening of 1 125 patients with chronic hepatitis. Ann Surg 1998;227(4):513-8.
- Tsai JF, Jeng JE, Ho MS, Chang WY. Effect of hepatitis C and B virus infection on risk of hepatocellular carcinoma: a prospective study. Br J Cancer 1997;76(7):986-74.
- Yang B, Zhang B, Xu Y. A prospective study of early detection for primary liver cancer. Chung Hua Chung Liu Tsa Chih 1996;18(6):442-444.
- Lemoine A, Azoulay D, Jezequel-Cuer M, Debuire B. Hepatocellular carcinoma. Pathol Biol (Paris) 1999;47(9):903-10.
Recibido: 20 de julio de 2001. Aprobado: 11 de octubre de 2001.
Dra. Zulema Adorna Carmenate. Instituto de Ciencias Básicas y Preclínicas Victoria de Girón. Avenida 146. No. 3102, esquina a 31, teparto Cubanacán, municipio Playa, Ciudad de La Habana, Cuba. CP 11600.