INTRODUCCIÓN
La culminación del Proyecto Genoma Humano, que requirió y fomentó el desarrollo de las tecnologías ómicas, ha conducido a la emergencia de un modelo denominado de medicina genómica, medicina molecular, medicina de precisión o medicina personalizada. Si bien tales términos no son estrictamente sinónimos, tienen entre sus elementos comunes la consideración de las características individuales de los pacientes para agruparlos en subpoblaciones, de acuerdo con su susceptibilidad a una enfermedad, el riesgo de padecerla o su respuesta a un tratamiento específico.1
Las tecnologías ómicas incluyen la genómica, la transcriptómica, la proteómica, la metagenómica, la metatranscriptómica y la metabolómica, así como la farmacogenómica y la bioinformática, entre otras.2) Estas se caracterizan por el empleo de equipamientos y metodologías específicamente desarrollados, la capacidad de procesamiento simultáneo de numerosas muestras y el análisis de los grandes conjuntos de datos experimentalmente generados.
Dichas tecnologías han ampliado los límites de las acciones sanitarias y, si se toma como ejemplo el diagnóstico, permiten la pesquisa prenatal y no invasiva, la evaluación de la predisposición o el riesgo, tanto de enfermedades de herencia mendeliana como complejas, en individuos aparentemente sanos, así como la toma de decisiones sobre las terapias, a partir de poseer o no receptores o dianas específicos, y de variaciones farmacogenómicas a nivel individual.3
En el campo de las terapias, por ejemplo, una encuesta realizada a oncólogos vinculados a un proyecto de medicina genómica reveló que las dos terceras partes de los profesionales consideraron que, en los próximos cinco años, estas tecnologías tendrían un impacto significativo en el descubrimiento de nuevos fármacos. También, más de la mitad reconoció sentir confianza en la información obtenida sobre el genoma de un paciente para la toma de decisiones relativas al tratamiento.4
La implementación de la medicina genómica o personalizada requiere de la preparación del personal sanitario para la investigación, la evaluación, la aprobación y la toma de decisiones en relación con la información disponible para los sistemas de salud sobre el genoma de los pacientes.5 La falta de preparación de los profesionales sanitarios para acceder a, interpretar y utilizar la información genómica ha sido reconocida como uno de los principales obstáculos para la integración de las tecnologías ómicas en la práctica clínica.4,6
Un número significativo de médicos no tiene los conocimientos para interpretar, incluso, las pruebas genéticas más sencillas.7) El panorama es más complejo con la disponibilidad de ensayos dirigidos a los consumidores (direct-to-consumers, DTC, en inglés), los altos costos de los ensayos genómicos, los aspectos éticos y el escepticismo en relación con su validez y utilidad.3,8,9
En el caso de Cuba, que no dispone aún de las tecnologías ómicas en su sistema de salud, se aspira a su progresiva introducción bajo el principio de beneficiar a toda la población.10) En relación con la enseñanza en la carrera Medicina en el país, la asignatura Genética Médica se imparte en el cuarto semestre, en el segundo año académico, y se extiende por 18 semanas lectivas;10 entre sus contenidos se incluyen la organización del genoma humano y su interacción con el ambiente, las tecnologías diagnósticas como FISH (del inglés fluorescent in situ hydridization), PCR (Polymerase chain reaction) y la secuenciación, así como la farmacogenómica. Algunas de estas tecnologías son mencionadas también en las asignaturas Biología Molecular, Informática Médica y Farmacología, pero no aparecen en las materias del área clínica (Medicina Interna, Pediatría u otras).
En este trabajo se presenta una primera aproximación a la evaluación de los conocimientos de los profesionales médicos sobre tales tecnologías.
MÉTODOS
Se aplicó un cuestionario estructurado, anónimo y autoadministrado, de selección múltiple, con diez preguntas abiertas o cerradas, sobre conocimientos en relación con las tecnologías ómicas, a médicos que comenzaron sus estudios en especialidades clínicas y quirúrgicas en el Hospital General Docente “Dr. Ernesto Guevara de la Serna”, de la provincia cubana de Las Tunas, seleccionados por muestreo no probabilístico intencional entre los residentes de nuevo ingreso: su número representó la mitad de los nuevos ingresos a estudios de especialización en la institución. Se recogió como dato personal la vía de entrada a la residencia: directa (recién graduados de la formación inicial en Medicina) y segunda especialidad (ya obtenido el grado de especialista en Medicina General Integral); en este último caso se indagó en el número de años de experiencia laboral.
Se consideraron como variables los conocimientos sobre técnicas de diagnóstico molecular, genes para el diagnóstico de enfermedades, farmacogenómica, y secuenciación del genoma completo y sobre recursos bioinformáticos con información del genoma. En todos estos casos los indicadores fueron: Conoce, No conoce o No recuerda. Otras variables incluidas resultaron la información recibida sobre el genoma y las tecnologías ómicas, y el interés en actividades formativas sobre estos temas, con indicadores Sí/No. Se solicitaron ejemplos de genes para diagnóstico, pruebas farmacogenómicas y recursos bioinformáticos, en caso de respuestas afirmativas para las preguntas respectivas.
La información obtenida a partir de la aplicación del cuestionario se procesó por medio del programa Microsoft Office Excel 2010, y se expresó con estadística descriptiva, a través de frecuencias absolutas y relativas.
Antes de la aplicación del cuestionario, a los participantes se les informó acerca de los objetivos y las características de la investigación, y se les solicitó su consentimiento para participar. No se documentó información alguna que revelara su identidad.
RESULTADOS
De los 53 médicos residentes que participaron en el estudio, 29 (54,7 %) se habían graduado tras concluir su formación médica inicial, mientras los 24 restantes (45,3 %) habían ejercido en la atención primaria de salud y tenían el grado de especialistas en Medicina General Integral. De este último grupo, la experiencia laboral varió desde 2 hasta 22 años de práctica profesional, con un promedio de 8,9 años.
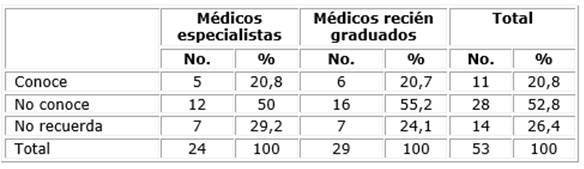
Entre las técnicas de diagnóstico molecular incluidas en la indagación se combinaron ensayos de biología molecular con otros basados en tecnologías ómicas: reacción en cadena de la polimerasa, Southernblot, hibridación fluorescente in situ, microarrays y secuenciación de nueva generación. La reacción en cadena de la polimerasa fue reconocida por más de la tercera parte de los participantes, mientras que los microarrays y la secuenciación genómica, solo por cinco de ellos (tabla 1). En general, el 37,7 % de la muestra declaró no recordar ninguna de las técnicas mencionadas, de quienes el 60 % fueron médicos que ya habían ejercido en la asistencia sanitaria.
Tabla 1 Conocimientos sobre técnicas de diagnóstico molecular
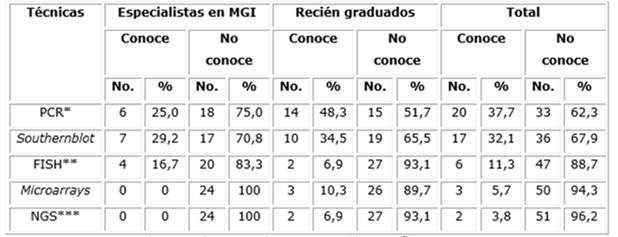
Nota: *PCR: polimerase chain reaction,**FISH: fluorescent in situ hybridization,***NGS: next generation sequencing.
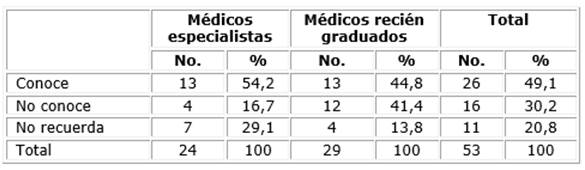
El 52,8 % de los encuestados respondió no conocer sobre la detección de algún gen para el diagnóstico de enfermedades o del riesgo de padecerlas (tabla 2). Sin embargo, solo seis de quienes se manifestaron afirmativamente (54,5 %), mencionaron un ejemplo (BRCA, del inglés BReastCAncer, en cinco casos y la hemoglobina S en otro).
Para evaluar los conocimientos sobre farmacogenómica se preguntó sobre la existencia de pruebas genéticas requeridas para la prescripción de algún medicamento: 40 residentes (75,5 %: 18 graduados como especialistas en MGI y 22 recién graduados) reconocieron no saber de ninguna. De los 4 que afirmaron conocer al respecto, 3 (75 %) no brindaron ningún ejemplo de ensayo con tal objetivo y el resto mencionó una prueba no utilizada para ese fin. Ninguno nombró algún medicamento donde se hubiera recomendado la determinación de variantes alélicas o polimorfismos, que influyeran en la prescripción o la dosificación del fármaco.
En la tabla 3 puede observarse que el 49,1 % de los residentes conocía que era posible estudiar el genoma completo de un paciente, con proporciones similares para las dos categorías de residentes.
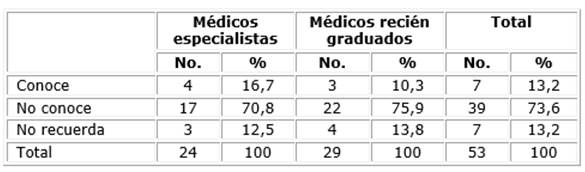
El 73,6 % de los participantes manifestó no conocer sobre sitios web o bases de datos relacionados con el genoma humano (tabla 4). Entre quienes respondieron afirmativamente, ninguno pudo ejemplificar con un recurso bioinformático en particular.
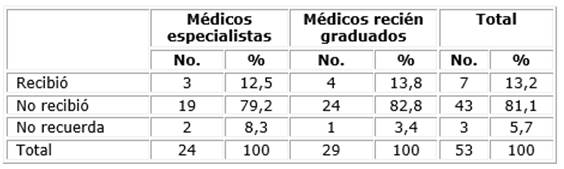
Entre los residentes que afirmaron no haber recibido información sobre el genoma y sus tecnologías de estudio, predominaron los recién graduados, que representaron el 82,8 % (tabla 5).
El 90,6 % de los residentes mostró interés en participar en actividades formativas sobre el genoma humano o las tecnologías ómicas.
DISCUSIÓN
Se presenta el primer reporte en Cuba sobre la exploración de conocimientos en médicos en relación con las tecnologías ómicas y su utilidad en la práctica clínica, de acuerdo con lo revisado por los autores del estudio. Esta aproximación es relevante como punto de partida para considerar las estrategias necesarias para la introducción e implementación de la medicina genómica en el país, que pasa por la preparación de los recursos humanos, y que demanda múltiples indagaciones.11
No son muchos los datos disponibles sobre edad, experiencia y otras características de los profesionales que son encuestados en este tipo de estudio.11) Una revisión sistemática encontró que solo en el 34,1 % de los reportes se brindó información relativa a la edad, mientras que en el 45,5 % se mencionaron los años de experiencia; ello dificultó dilucidar y comparar la influencia que pueden tener los factores demográficos, psicológicos y profesionales en la efectividad de la formación, y el desempeño en genómica y las ramas afines.12
En un estudio sobre un grupo de médicos que participaron en actividades formativas en genómica, estuvieron representadas 17 especialidades, más de la mitad de las cuales se vinculaban a la asistencia primaria y más del 70 % de los encuestados sobrepasaban los 40 años.13) En otro reporte, todos los encuestados llevaban al menos 12 años de experiencia laboral.4) Los profesionales recién graduados deben asimilar mejor la capacitación en genómica,12) si bien en nuestro estudio fueron precisamente los médicos recién graduados los que mostraron menor conocimiento sobre las tecnologías ómicas.
La disponibilidad de pruebas genéticas y genómicas es creciente, tanto por indicación facultativa como por las DTC, y los pacientes esperan que sus médicos de asistencia puedan interpretarlas, incluso aquellas más complejas como las relacionadas con la secuenciación.4,14,15 El acceso del público general a información sobre el tema en los medios demanda la necesidad de que los doctores puedan orientar al respecto, interpretar sus resultados y decidir sobre la remisión a otros especialistas.8,13 Todo ello pasa, en primer lugar, por la formación que reciben, los conocimientos que adquieren y las habilidades que desarrollan, para lo cual el presente estudio representa un punto de partida.
Se espera que las pruebas genómicas proporcionen la mayor parte de la información relevante para la práctica médica.8 Hay varias iniciativas para evaluar y aportar las evidencias requeridas sobre la validez y utilidad de este tipo de ensayos, como el caso de EGAPP (del inglés Evaluation of Genomic Applications in Practice and Prevention)14) y la más reciente Public Health Genomics Knowledge Base (https://phgkb.cdc.gov/PHGKB/).16
En un grupo de médicos californianos, encuestados sobre la utilización de este tipo de pruebas, el 26,5 % reconoció indicarlas con una frecuencia mayor a mensual;13) tal escenario pudiera presentarse en un futuro para el sistema cubano de salud, por lo que no debe demorar la preparación de los profesionales de la salud, tanto en la formación inicial como permanente.
La secuenciación de nueva generación fue la tecnología diagnóstica menos conocida entre los médicos encuestados en el presente trabajo. Sin embargo, su diversidad de aplicaciones se reflejó en el hecho de que más de 100 publicaciones por mes refirieron su utilización.17 Un número creciente de instituciones de salud la ofrecen dentro de sus servicios diagnósticos de rutina en enfermedades como el cáncer y las infecciones, o en la genética clínica,17) al tiempo que se reconocen como un complemento de la insustituible historia clínica.15) No obstante, existen cuestionamientos sobre sus potencialidades, particularmente en el caso de la pesquisa neonatal.9 Es la secuenciación, como los otros aspectos abordados en el cuestionario empleado, uno de los contenidos a considerar en las actividades y tareas docentes que se diseñen con fines formativos de estudiantes y profesionales de la salud.
El conocimiento de los genes implicados en las enfermedades humanas tiene importancia para la comprensión de la fisiopatología, la disponibilidad de ensayos diagnósticos, la evaluación del pronóstico y como posibles dianas terapéuticas. El 89,2 % de los profesionales que participaron en esta investigación mostraron no conocer sobre este tema. Puede tenerse una idea de la relevancia del asunto en el hecho de que el Colegio Americano de Genética y Genómica Médicas ha divulgado una lista de 59 genes relacionados con condiciones genéticas prevenibles.18
La creencia de que las enfermedades genéticas monogénicas o raras son las únicas donde se aplica esta información y la escasa formación en genética, se han propuesto como explicaciones para la baja percepción de su importancia por parte de los médicos.19
La farmacogenómica es una de las aplicaciones más promisorias e inmediatas a extender entre las tecnologías ómicas en la práctica clínica,9,20) incluso en las condiciones actuales del sistema cubano de salud, y que debe considerarse también para las actividades formativas. La décima parte de todos los medicamentos aprobados por la Agencia de Medicamentos y Alimentos de Estados Unidos (FDA, por sus siglas en inglés), contiene advertencias sobre su farmacogenética en la información a los consumidores,21 y se estima una disminución de entre 60000 y 144000 ingresos en España por concepto de reducción de los efectos adversos mediados por las variaciones genéticas.22 Fue esta, sin embargo, una de las áreas con mayor desconocimiento entre los médicos encuestados en esta investigación.
Tal situación resulta similar a lo ya reportado en otros trabajos. Desde hace casi tres lustros, en Estados Unidos se ha recomendado la inclusión de la farmacogenómica como contenido en la formación de profesionales de la salud, en todos los cursos que lo permitan;23) cinco años después, el Departamento de Salud de ese país reconocía que los médicos no poseían conocimientos para interpretar la información relacionada con esta área.1) Mediante el empleo de PubMed y Google no fue posible localizar ninguna referencia bibliográfica sobre la enseñanza de la farmacogenética en España, según autores de ese país.22
La formación de los profesionales de la salud en farmacogenómica se ha identificado como uno de los “cuellos de botella” para su implementación en la práctica médica.1) Por ello, se ha recomendado a las escuelas de Medicina incorporar más contenidos sobre esta disciplina, para lo cual hay ejemplos disponibles en la literatura,22,23 aunque no está claro si con ello se logre el impacto esperado.1) Las actividades prácticas, en particular la posibilidad de genotipaje personal, pueden incrementar la motivación y la confianza en esta tecnología,24 lo que no es posible en todos los escenarios docentes, particularmente en los países en desarrollo, más allá de los cuestionamientos éticos de ese tipo de actividad docente.
Cerca de la tercera parte de los médicos que participaron en esta investigación declararon no saber de la posibilidad de la secuenciación del genoma de los individuos. En la actualidad esta tecnología diagnóstica reduce sostenidamente el tiempo de su realización y los costos son cada vez más bajos,19 al punto que se espera que su ejecución se siga simplificando.25,26 Su empleo o interpretación por el personal sanitario no capacitado puede conducir a diagnósticos imprecisos y gastos de recursos.26
Menos de la sexta parte de los profesionales encuestados estaba al tanto de los recursos bioinformáticos que pueden tener utilidad para su práctica clínica. La bioinformática es otra de las tecnologías ómicas que ya se ha señalado como una necesidad formativa,27) bajo la consideración de que los cambios educativos que se implementen deben facilitar el manejo de los volúmenes de datos científicos ya disponibles, su interpretación y la toma de decisiones.10) Baste mencionar un ejemplo a tono con la farmacogenómica para recordar que tales recursos pueden potenciar el aprendizaje: la base de datos PharmGKB (https://www.pharmgkb.org/).23
Si bien la mayoría de los médicos que participaron en esta investigación no fueron capacitados sobre las tecnologías ómicas, un significativo número mostró interés por recibir tal formación. Una situación similar ha sido identificada en otros estudios para profesionales que no se dedican a la genética,12) mientras que menos del 20 % de otra muestra reportó haber recibido entrenamiento formal en genética.28) Incluso entre oncólogos vinculados a la genómica, se comenta el escaso conocimiento sobre estas nuevas tecnologías.4
En general, los médicos que ejercerán su práctica profesional durante el siglo xxi requerirán mucho más que un conocimiento básico sobre la genética humana; en tal sentido, la formación médica inicial en muchas instituciones no parece prepararlos.4,19,22 La universidad médica es el sitio ideal para tal formación,4) e internacionalmente se demanda una reforma educativa que integre los contenidos sobre genética y genómica a todo el continuum del currículo, dado que un solo curso no puede preparar a los futuros médicos.3) Entre otros, la Asociación norteamericana de Profesores de Genética Humana y Médica ha publicado un currículo base, que incluye competencias específicas para las tecnologías ómicas (microarrays, la secuenciación, los recursos bioinformáticos, entre otros).29
Algunas iniciativas han sido implementadas para cubrir esa brecha de conocimiento en profesionales de la salud, como en la Escuela de Medicina de Mount Sinai y el Colegio Baylor de Medicina.8) En Italia, sin embargo, más de un tercio de las escuelas dedicadas al posgrado en Salud Pública no tienen siquiera un curso sobre genómica.5
Las universidades médicas deben mantener una actualización continua de sus programas como respuesta a los rápidos avances en la genómica.2,11,28) Debe recordarse que el “analfabetismo ómico” puede ser determinante en las actitudes negativas hacia la genómica.4 No pueden obviarse del análisis de su implementación, los costos relativos a las actividades educativas,11 la disponibilidad de fuentes de financiamiento y la comunicación con el público.30
La formación médica posgraduada está altamente fragmentada, y habitualmente resulta bajo el número de residentes en cada especialidad, lo que dificulta la integración de las tecnologías ómicas entre sus contenidos.15) En Estados Unidos, por ejemplo, hay 46 programas acreditados de residencia en Genética Médica y Genómica.11) Como sucedió en nuestro estudio, haber cursado una residencia anterior, particularmente Medicina General Integral, no promueve un nivel de conocimientos adecuado sobre genética y genómica. Junto a su mayor alcance en términos de matrículas, tales argumentos justifican que es mejor hacerlo desde la formación inicial, pues en ella se preparan los profesionales del mañana.25) Debe servir como alerta que, en el período 2014-2016, solo el 0,2 % de los estudiantes de Medicina de segundo año en Estados Unidos, consideraban la posibilidad de un entrenamiento futuro en genómica.11) Por ello, el mejor momento para la educación siempre es el actual.15
Los resultados aquí presentados connotan la necesidad de un abordaje más profundo e integrador de tales contenidos desde la formación inicial. A pesar de las dificultades y limitaciones para la implementación de la medicina genómica, la mayoría de los médicos están interesados en incrementar sus conocimientos sobre genómica y desean adoptarla en su desempeño profesional,4,25,31 como sucedió en nuestro estudio, realizado en Cuba, un país en vías de desarrollo. Nuestra nación es reconocida por la calidad de la formación de sus recursos humanos en salud, e igualmente sucede con la genética médica, lo cual constituye un factor que facilitará la integración de las tecnologías ómicas a la práctica médica.10,32
Como la muestra estudiada procede de un único hospital, debe tenerse en cuenta que los datos aquí presentados no son necesariamente representativos del fenómeno estudiado a nivel del Sistema Nacional de Salud. Se trata, no obstante, de un primer acercamiento, que aporta información de interés y que alerta sobre la necesidad de la inclusión de contenidos relacionados con la genómica y las tecnologías ómicas en la formación médica inicial.
Los médicos que iniciaron estudios de especialización, tanto recién graduados como los que ya tenían experiencia laboral en la atención primaria, mostraron tener conocimientos insuficientes sobre estas tecnologías. Ello puede limitar la implementación de acciones para la introducción de la medicina genómica. Se requiere, por tanto, de la inclusión de contenidos en la educación médica para preparar a los profesionales de la salud, desde su formación inicial, en los principios, las aplicaciones y la interpretación de las tecnologías ómicas en la práctica clínica.