Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Oftalmología
versión impresa ISSN 0864-2176
Rev Cubana Oftalmol vol.23 supl.2 Ciudad de la Habana 2010
INVESTIGACIONES
Evaluación del equipo de interferometría óptica de coherencia parcial Lenstar en la biometría ocular
Evaluation of Lenstar partial coherente optical interferometry device in the ocular biometry
Iramis Miranda HernándezI; Juan Raúl Hernández SilvaII; Marcelino Rio TorresIII; Yanele Ruiz RodríguezI; Jenny Del Amo FreireIV; Acelia Bisnubia VargasIV
IEspecialista de II Grado en Oftalmología. Especialista de I Grado en Medicina General Integral. Aspirante a investigador. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
IIEspecialista de II Grado en Oftalmología. Doctor en Ciencias. Profesor asistente. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
IIIEspecialista de II Grado en Oftalmología. Doctor en Ciencias. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
IVLicenciada en Optometría y Óptica. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
RESUMEN
OBJETIVOS: Comparar y evaluar la biometría ocular con el nuevo equipo de interferometría óptica de coherencia parcial (Lenstar) con el equipo de interferometría óptica de baja coherencia IOL Master y también con los sistemas topográficos Galilei y Pentacam.
MÉTODOS: Se realizó un estudio descriptivo, transversal, en 120 ojos de 60 pacientes. Para el cálculo del lente intraocular se tomaron mediciones con un nuevo biómetro Lenstar LS 900 (Haag Streit AG) y con el IOL Master V.5 (Carl Zeiss Meditec AG). Se compararon mediante el análisis de regresión lineal y correlación de Pearson. También se compararon las medidas con las obtenidas por los equipos topógrafos Galilei y Pentacam. RESULTADOS: Existe una alta correspondencia en los valores biómetricos de longitud axial, queratometría y profundidad de la cámara anterior entre los equipos Lenstar e IOL Master. También se encontró una buena correspondencia entre las medidas de profundidad de cámara posterior y queratometría entre Lenstar y los topógrafos Galilei y Pentacam.
CONCLUSIONES: El nuevo biómetro Lenstar, provee resultados que se correlacionan muy bien con aquellos obtenidos con los equipos IOL Master, Pentacam y Galilei. El equipo Lenstar es un equipo preciso que brinda información adicional por lo que es útil en la cirugía de catarata y la cirugía refractiva.
Palabras clave: Lente intraocular, biometría, Interferometría óptica, Lenstar.
ABSTRACT
OBJECTIVES: To compare and to evaluate the ocular biometry taken by a new optical partial coherence interferometry device (Lenstar),the low coherence optical interferometry equipment (ILO Master) and the topographic systems Pentacam y Galilei.
METHODS: A descriptive cross-sectional study was conducted in 120 eyes from 60 patients. For the IOL calculation, the necessary measurements were taken with the new optical biometer Lenstar LS 900 (Haig Streit AG) and with the IOL Master V5 (Carl Zeiss Meditec AG). The results were evaluated using the linear regression analysis and Pearson´s correlation. The measures were then compared to those taken by topographic devices Galilei and Pentacam.
RESULTS: There existed high correlation in biometric measurements of axial length, keratometry and anterior chamber depth between the Lenstar and the IOL Master. Good correlation was also found for the Keratometry and anterior chamber depth between the Lenstar and the topographs Pentacam and Galilei.
CONCLUSION: The new biometer LENSTAR provided results that correlated very well with those of the IOL Master, Pentacam and Galilei systems. Lenstar is a precise device offering additional features that will be helpful for any cataract or refractive surgery.
Key words: Intraocular lens (IOL), biometry, optical interferometry, Lenstar.
INTRODUCCIÓN
La determinación de las distancias intraoculares, especialmente la longitud axial del ojo (ALX), es necesaria en procesos relacionados con la cirugía oftalmológica, sobre todo en la cirugía de cataratas. Hasta hace unos años, la ultrasonografía AScan a 10 mHz era la técnica de medición más difundida, con una resolución aproximada de 0,10 mm. Cuando esta técnica se realiza en condiciones óptimas, los valores obtenidos se consideran fiables y altamente precisos, como cuando se realiza mediante la técnica de inmersión, sin embargo la medición es menos exacta cuando se realiza mediante la técnica de contacto ya que resulta en una longitud axial falsamente corta y resultados variables por la compresión que experimenta la cornea al entrar en contacto con el instrumento.1-4
Debido a las características negativas de este procedimiento, desde la década de los años ochenta (siglo XX) se comenzó a estudiar la factibilidad de medir distancias intraoculares mediante una nueva técnica que constituía –y aún sigue siendo– un terreno fértil para la investigación y el desarrollo: la interferometría de coherencia parcial.5
El fundamento teórico de este método no es otro que el del uso del fenómeno de interferencia para medir distancias en términos de la longitud de onda de la luz. El uso de la interferometría de coherencia parcial para la medición de la longitud axial del ojo humano fue reportado en 1986, por un colectivo de científicos del Institut für Medizinische Physik de la Universidad de Viena.6
El desarrollo del método conocido como interferometría de coherencia parcial y su empleo en la biometría del ojo humano, han hecho posible la obtención de mediciones aproximadamente cinco veces más exactas que las brindadas por los antiguos biómetros como los ultrasonógrafos.3
En la cirugía de catarata varios aspectos tendrán un impacto en el resultado refractivo posoperatorio final. Estos son la medición de diferentes parámetros oculares que tienen un gran peso en la consecución de buenos resultados. Una cuidadosa optimización de las constantes de la lente intraocular (LIO) y las fórmulas usadas para el cálculo de la potencia óptica de la misma influyen en el resultado refractivo final. Se ha probado que el mayor peso en todas las fórmulas para conseguir resultados emetropizantes al implantar un lente intraocular lo tiene, además del cálculo fiable de la longitud axial, la queratometría. Estos parámetros o variables constituyen las principales fuentes de error biométrico que deriva en un poder incorrecto del lente intraocular.7,8
Existen otros parámetros complementarios que son especialmente útiles en otras fórmulas como el grosor del cristalino, el diámetro corneal mediante la medición del diámetro visible o la distancia limbo-limbo o blanco-blanco (WTW). Estas variables tienen importancia como predictores de la posición efectiva del lente (ELP) en la fórmula Holladay II, especialmente útil en pacientes hipermétropes.7,9
Justamente en estos procedimientos de medición es que intervienen los biómetros basados en el sistema de la interferometría de coherencia parcial (ICP). De estos, el equipo IOL Master (Carl Zeiss, Jena, Alemania), es el primer equipo comercializado basado en este sistema. Es un biómetro óptico de no contacto, que tiene más de 10 años de experiencia a nivel internacional. Se ha convertido en la norma de referencia de la biometría lo cual se debe a la fiabilidad, exactitud y seguridad de las mensuraciones obtenidas con el objetivo de calcular el poder dióptrico del lente intraocular en la cirugía de catarata. Calcula la longitud axial (ALX), profundidad de la cámara anterior (ACD), queratometría y la distancia blanco-blanco, este último de gran utilidad en cirugía refractiva.10,11
Recientemente, la firma Hagg Streit (AG, Koeniz, Alemania), presentó un nuevo equipo basado en el principio de la interferometría óptica de coherencia parcial, el cual está siendo probado por diferentes instituciones por la calidad de las mensuraciones para el cálculo del LIO. Se trata del equipo Lenstar, biómetro de no contacto que realiza 9 mediciones diferentes en un mismo disparo. Provee mediciones que son útiles en pacientes candidatos tanto de cirugía de catarata como en cirugía refractiva.12
El equipo Lenstar utiliza un diodo superluminiscente (SLD) de larga longitud de onda (820 nm), como fuente de luz, lo que permite una adecuada penetración en cristalinos de dureza moderada.13-19
Por tratarse de un método óptico, depende de la facilidad de propagación de la luz en el ojo, por tanto patologías que perjudiquen o impidan la propagación de la luz, igualmente impedirán la medida de la ALX.15-17
Proporciona el cálculo de la lente intraocular (software Eyesuite). Es especialmente útil en ojos con altas miopías, afáquicos o que contengan aceite de silicona. Se realizan 16 escaneos como medida principal y facilita valores de los diferentes elementos de la parte más externa del ojo. El escaneo rápido del ojo hace que si se pierde en algún momento la fijación no se anula la medición y el examen continúa cuando se reestablece la misma. Este equipo es altamente sensible por lo que puede ser difícil de realizar en pacientes con maculopatías, nistagmus o poco colaborativos.15-17
Las mediciones obtenidas con el equipo Lenstar son la paquimetría, queratometría (K), diámetro pupilar, excentricidad del eje visual, distancia blanco-blanco (WTW), profundidad de cámara anterior (ACD), espesor del cristalino (LT), longitud axial (ALX) y el espesor de la retina.
Las reflexiones de las diferentes estructuras del ojo humano, tales como, la córnea, el cristalino y la retina, son interferométricamente superpuestas sobre la reflexión de los brazos de referencia. Una señal de interferencia de la interfase reflectiva es generada cuando el rayo de medida está fijado por el paciente y cuando este está perpendicular a la interfase. Debido a la separación temporal de las interferencias la ACD, el LT y la ALX son medidos en un solo procedimiento de posición. Este instrumento además puede medir las medidas del radio de curvatura corneal en el meridiano plano (R2) e inclinado (R1) y analiza un patrón de 32 diodos emisores de luz, los cuales están dispuestos en dos anillos con 16 puntos de medidas cada uno.15-17
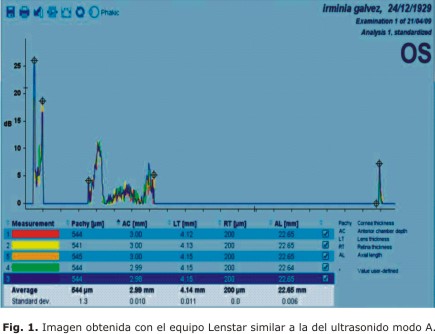
Las medidas son representadas en un gráfico que refleja el promedio de las mediciones realizadas (cinco en total) y la desviación estándar (DE) de cada una. El gráfico obtenido recuerda la imagen del ultrasonido modo A y los picos corresponden a la superficie anterior y posterior de la córnea, cápsula anterior y posterior del cristalino y la retina (fig. 1).
En el Instituto Cubano de Oftalmología "Ramón Pando Ferrer"por la importancia que comprende el uso de este tipo de sistema para el cálculo del poder dióptrico del lente intraocular, nos propusimos el objetivo de iniciar un estudio para su evaluación. Realizamos la comparación y evaluación de las medidas obtenidas con este nuevo biómetro con las obtenidas con el equipo IOL Master así como las obtenidas con sistemas topográficos Pentacam y Galilei basados en la tecnología Scheimpflug con experiencia de uso.13 La tecnología Scheimpflug utiliza dos cámaras giratorias con este principio y sus imágenes precisas permiten analizar las estructuras del ojo desde la parte anterior de la córnea hasta la cápsula posterior del cristalino.13,14 Sus aplicaciones más importantes están relacionadas con la validación de candidatos para cirugía refractiva, cirugía personalizada con base topográfica y la documentación de la catarata por medio de la densitometría.
MÉTODOS
Se realizó un estudio descriptivo transversal con un grupo de pacientes atendidos en el Centro de Microcirugía Ocular del Instituto Cubano de Oftalmología "Ramón Pando Ferrer", con edades comprendidas entre 40 y 75 años de edad, sanos que fueron sometidos a la línea preoperatoria para cirugía de catarata entre los meses de mayo de 2009 a mayo de 2010. Se estudiaron 60 pacientes (120 ojos). Este es el número de casos mínimo insertado en el estudio que el diseño del equipo exige para probar sus resultados y aceptar su eficacia.
Los valores biométricos se tomaron por el mismo observador y previa información de la naturaleza del estudio con el consentimiento del paciente que aceptó participar. Fue aprobado por el Comité de Ética de la institución y ajustado al cumplimiento cabal con las normas de Helsinki para experimentación en humanos.
Se tomaron el mismo día las mensuraciones con los equipos Lenstar e IOL Master, y en otra consulta con los equipos Galilei y Pentacam.
Se incluyeron en el estudio pacientes con diagnóstico de catarata que presentaban dureza del núcleo lenticular de II a IV+ (dado por el sistema LOCS), así como un conteo celular endotelial de 2 000 células/mm2 ( ± 100 células/mm2).
A cada paciente se le realizaron las siguientes mensuraciones (recomendadas por los fabricantes para probar la eficacia del equipo).
a) IOL Master (Versión: 3.02.0304):
– Longitud axial (5 mediciones por ojo).
– Profundidad de la cámara anterior (1 medición por ojo).
– Queratometría (3 mediciones por ojo: R1 meridiano más curvo- R2 meridiano más plano).
– Distancia blanco-blanco (3 mediciones por ojo).
b) Lenstar LS 900 (Versión: 0.9.3):
– Longitud axial (5 mediciones por ojo).
– Profundidad de la cámara anterior (5 medición por ojo).
– Queratometría (5 mediciones por ojo).
– Eje o axis corneal.
– Distancia blanco-blanco (5 mediciones por ojo).
Equipos Galilei (Ziemer, Suiza) y Pentacan (Oculus, Alemania):
– Queratometría (3 mediciones por ojo).
– Eje o axis corneal.
– Profundidad de la cámara anterior (3 mediciones por ojo).
Se excluyeron aquellos pacientes que presentaban afecciones que podrían comprometer la realización del examen por presentar mala fijación como pacientes con maculopatías, nistagmus o poco colaborativos. Los criterios de salida fueron individuos que en el transcurso del estudio presentaron alguna afección oftalmológica.
Los resultados se expresan en medias (± desviación estándar). Se realizó el análisis de regresión lineal y el cálculo de coeficiente de Pearson. Se consideró 95 % como nivel de significación.
RESULTADOS
Este estudio comparó las medidas clínicas obtenidas con el equipo IOL Master con las del equipo Lenstar de la ALX, R1, R2, ACD y WTW.
Con el Lenstar es posible determinar también el espesor del cristalino (LT), este dato no lo mostramos en este trabajo.
En este estudio el comportamiento de las cataratas según su tipo fue de: 73,3 % nucleares, 23,3 % corticonucleares y un 3,3 % opacidades periféricas.
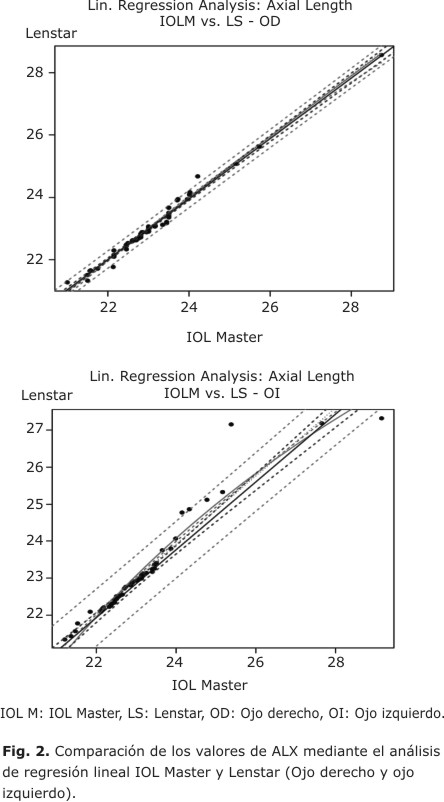
Se analizaron los 120 ojos. Los valores medios de ALX obtenidos fueron de 22,9 ± 2,48 con el Lenstar y 22,82 ± 2,49 con el IOL Master. Los resultados fueron altamente correspondientes y exactos entre los mismos, principalmente en pacientes con ALX entre 22-26 mm. En ALX mayores de 26 mm fueron más inexactos (fig. 2).
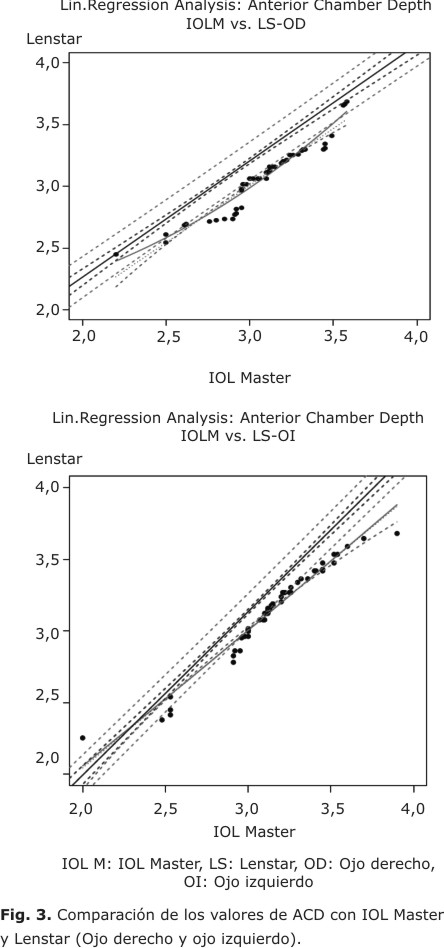
La comparación de la medida de la ACD fue posible en los 120 ojos estudiados. La media de la ACD fue de 2,91 ± 0,38 con el Lenstar y de 3,06 ± 0,40 con el IOL Master. El IOL Master realiza la medición desde el epitelio corneal hasta la cápsula anterior del cristalino. El Lenstar realiza la medición de la ACD desde el endotelio corneal hasta la cápsula anterior del cristalino (ACD anatómica). Para realizar el cálculo del LIO suma los valores paquimétricos y la ACD. Este valor fue el que tomamos para realizar la comparación, Estos resultaron altamente correspondientes cuando analizamos el valor total obtenido (fig. 3).
La ACD también fue comparada con los topógrafos Pentacam y Galilei. Los resultados mostraron buena correspondencia. Estos fueron: Lenstar 2,91 ± 0,38, Pentacam 2,94 ± 0,29 y Galilei 2,95 ± 0,29.
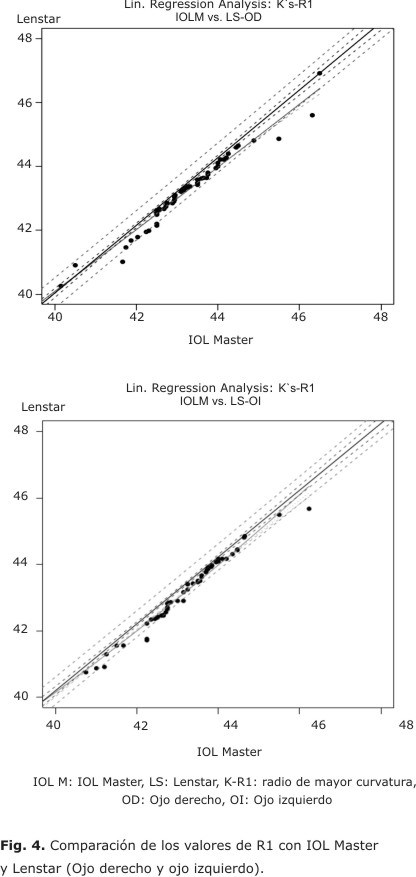
En relación con la queratometría, las medias de las medidas obtenidas de R1 fueron de 42,44 ± 4,14 y de R2 43,15 ± 4,22 con el Lenstar. Con el IOL Master fueron de R1 42,66 ± 4,17 y R2 43,87 ± 4,26. Observamos una alta correspondencia de las medidas obtenidas entre ambos (fig. 4).
La correspondencia de los valores de queratometría (R1 y R2) entre el Lenstar y los equipos Pentacam y Galilei fue buena aunque menor que con el equipo IOL Master. Las diferencias no fueron estadísticamente significativas. Pentacam R1 43,05 ± 1,59 y R2 43,66 ± 1,59. Con el Galilei R1 42,90 ± 1,48 y R2 43,63 ± 1,52 (fig. 5).
El eje o axis fue de 103,08 ± 56,77 con el Lenstar, de 103,32 ± 55,12 Pentacam y de 106,70 ± 67,63 con el Galilei; se observó al igual que en las medidas anteriores una alta correspondencia de los valores obtenidos.
La distancia WTW fue de 11,59 ± 1,57 con el Lenstar y de 11,72 ± 1,15 con el IOL Master. Presentaron una alta correspondencia.
DISCUSIÓN
Este dispositivo de interferometría se encuentra calibrado frente a sistemas de alta resolución, por lo que se realiza una medida análoga a la de un sistema A de inmersión.
Las medidas obtenidas de la LAX fueron correspondientes entre ambos equipos (Lenstar-IOL Master) con un alto grado de correspondencia entre los valores obtenidos. Estos fueron más exactos en ojos con ALX normales (23-24 mm), sin embargo, algo inexactos en ALX extremas (ojos ALX > 24 mm). Esto puede deberse a que en pacientes con ALX altas, pacientes miopes tienen el epitelio pigmentario más fino y la capa de monocélulas al tener menor grosor oponen menos interferencia al rayo por lo que los resultados son más inexactos.
Por tratarse de un método óptico, depende de la facilidad de propagación de la luz en el ojo, por tanto patologías que perjudiquen o impidan la propagación de la luz, igualmente impedirán la medida de la ALX. De aquí la dificultad para realizar el examen en pacientes con opacidades cristalineanas de densidad media alta de manera similar que con el IOL Master.20
En marzo 2009 fue publicado un estudio clínico comparativo realizado por el doctor Auffarth. Aplicó la correlación de Spearman para evaluar y comparar la efectividad del equipo Lenstar. Reveló una alta correlación en las medidas de la ALX y queratometría y una menor correlación para la ACD pero las diferencias no fueron estadísticamente significativas.21 Estos resultados coinciden con los obtenidos en nuestro estudio.
El equipo Lenstar está basado en el principio de reflectometría óptica de baja coherencia utiliza un diodo superluminiscente.18,19 El equipo IOL Master usa el principio de la interferometría óptica de coherencia parcial en la configuración de un rayo de luz doble y esto se efectúa mediante un láser diodo multimodo. Debido a las diferentes características espectrales se obtiene una mayor resolución con el uso del SLD comparado con el láser diodo multimodo.15,22
El cálculo del coeficiente de Pearson fue cercano a 1 para las medidas de ALX, ACD, R1, R2 y WTW, entre el IOL Master y el Lenstar. Las medidas de ACD, R1, R2 entre topógrafos y el Lenstar evidenciaron que el coeficiente de Pearson también fue cercano a 1.Todos los resultados se confirmaron mediante el análisis de regresión, y se determinó una buena asociación entre las variables correlacionadas.
Las mediciones Scheimpflug de la ACD con los equipos Galilei y Pentacam son exactas y tienen una buena repetibilidad en comparación con la interferometría de coherencia parcial Lenstar. Sin embargo, debido a la alteración de la luz al pasar a través de superficies de refracción, la imagen se distorsiona. Esto puede llevar a una subestimación de la profundidad de la cámara anterior en los ojos pseudofáquicos.13,14
Los resultados obtenidos en este trabajo coinciden con los alcanzados en otros estudios publicados en el año anterior en algunas universidades de Alemania,22 lo que demuestra que este sistema de interferometría es un instrumento confiable, efectivo y reproducible para el cálculo del lente intraocular. Además es un equipo preciso que brinda información adicional por lo que es útil en la cirugía de catarata y la cirugía refractiva.
REFERENCIAS BIBLIOGRÁFICAS
1. Orts Vila P, Devesa Torregrosa P, Tañá Rivero P. Interferometría de coherencia parcial. Estudio comparativo entre la interferometría de coherencia parcial y la biometría ultrasónica para el cálculo de la lente intraocular. Microcirugía Ocular. 2001;1
2. Carrera Sánchez JC, Barojas Weber E. Comparación de eficacia y límites entre el IOLMaster y el ultrasonido de inmersión, en el cálculo del lente intraocular en pacientes con catarata. Rev Mex Oftalmol. 2009;83(6):360-5.
3. Ademwada A, Natrajan S. Ocular Biometry and Intraocular Lens Power Calculations in Microphaco. En: Garg A, editor. Mastering the Art of Bimanual Microincision Phaco (Phakonit/MICS). Nueva Delhi: Jaypee Brothers Medical Publishers; 2005.p.69-76.
4. Rajan MS, Keilhorn I, Bell JA. Partial coherence laser interferometry vs conventional ultrasound biometry in intraocular lens power calculations. Eye. 2002;16(5):5526.
5. Hitzenberger CK. Optical Measurement of the Axial Eye Length by Laser Doppler Interferometry. Investigative Ophthalmology & Visual Science. 1991;32(3):616-24.
6. Fercher AF, Mengedoht K, Werner W. Eye length measurement by interferometry with partially coherent light. Optics Letters. 1988;13(3):186-8.
7. Gale RP, Saha N, Johnston RL. National Biometry audit. Eye. 2004;18(1):63-6.
8. Olsen, T. Prediction of the effective postoperative (intraocular Lens) anterior chamber depth. J Cataract Refract Surg. 2006;32(3):419-24.
9. Soler Fernández FL, Pascual Segarra J. Fuentes de Error en Queratometría y Biometría. En: Centurión V. El Libro del Cristalino de las Américas. Brasil: Livraria Santos; 2007. p. 95-111.
10. Tehrani M, Krummenauer F, Kumar R, Dick HB. Comparison of biometric measurements using partial coherence interferometry and applanation ultrasound. J Cataract Refract Surg. 2003 Apr;29(4):747-52.
11. Findl O, Kriechbaum K, Sacu S, Kiss B, Polak K, Nepp J, et al. Influence of operator experience on the performance of ultrasound biometry compared to optical biometry before cataract surgery. J Cataract Refract Surg. 2003 Oct;29(10):1950-5.
12. Buckhurst PJ, Wolffsohn JS, Shah S, Naroo SA, Davies LN, Berow EJ. A new optical low coherence reflectometry device for ocular biometry in cataract patients. Br J Ophthalmology. 2009;93(7):949-53.
13. Ucakhan ÖÖ, Özkan M, Kanpolat A. Corneal thickness measurements in normal and keratoconic eyes: Pentacam comprehensive eye scanner versus noncontact specular microscopy and ultrasound pachymetry. J Cataract Refract Surg. 2006;32(6):970-7.
14. Lackner B, Schmidinger G, Pieh S, Funovics MA, Skorpik C. Repeatability and Reproducibility of Central Corneal Thickness Measurement with Pentacam, Orbscan, and Ultrasound. Optom Vis Sci. 2005 Oct;82(10):892-9.
15. Drexler W, Findl O, Menapace R, Rainer G, Vass C, Hitzenberger CK, et al. Partial coherence interferometry: a novel approach to biometry in cataract surgery. Am J Ophthalmol. 2003;126(4):524-34.
16. Santodomingo-Rubido J, Mallen EA, Gilmartin B, Wolffsohn JS. A new non-contact optical device for ocular biometry. Br J Ophthalmol. 2002;86(4):45862. 17. Böhnke M, Widmer S, Wälti R. Real-time pachymetry during photorefractive keratectomy using optical low-coherence reflectometry. J Biomed Opt. 2001;6(4):4127.
18. Schmid GF. Axial and peripheral eye length measured with optical low coherence reflectometry. J Biomed Opt. 2003;8(4):655-8.
19. Bohnke M, Master BR, Walti R, Ballif JJ, Chavanne P, Gianotti R, et al. Precision and reproducibility of measurements of human corneal thickness with rapid optical low-coherence interferometry (OLCR). J Biomed Opt. 1999;4:152-6.
20. Bjeloš Ronèeviæ M, Bušiæ M, Èima I, Kuzmanoviæ Elabjer B, Bosnar D, Miletiæ D. Comparison of optical low-coherence reflectometry and applanation ultrasound biometry on intraocular lens power calculation. Graefe's Arch for Clin and Exp Ophthalmol [serie en Internet]. 2010 [citado 15 de junio de 2010 ];248(1):[aprox.10 p.]. Disponible en: http://www.springerlink.com/content/61254152K4003755/fulltext.pdf
21. Holzer MP, Mamusa M, Auffarth GU. Accuracy of a new partial coherence interferometry analyzer for biometric measurements. Br J Ophthalmol. 2009;93(6):807-10
22. Rohrer K, Frueh BE, Wälti R, Clemetson IA, Tappeiner C, Goldblum D. Comparison and Evaluation of Ocular Biometry Using a New Noncontact Optical Low-Coherence Reflectometer. Ophthalmology. 2009;116(11):2087-92.
Recibido: 29 de enero de 2011.
Aprobado: 15 de febrero de 2011.
Dra. Iramis Miranda Hernández. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". Ave. 76 No. 3104 entre 31 y 41 Marianao, La Habana, Cuba. Correo electrónico: iramis.miranda@infomed.sld.cu