Introducción
El nanoftalmo es una anomalía del desarrollo; una condición rara, siempre bilateral. Comúnmente se presenta con un patrón hereditario autosómico recesivo.1 Se caracteriza por ser un ojo diminuto, con una excepción: el cristalino que ha sido reportado de tamaño normal o un poco más grande.1
Todo ojo de tamaño menor de 21,0 mm de longitud anteroposterior (AP) debe ser considerado como potencialmente nanoftálmico. Hay autores que plantean menor de 20,5 mm. A consecuencia de tener una longitud antero-posterior corta y un poder refractivo relativamente normal (córnea y cristalino), el ojo nanoftálmico es extremadamente hiperópico de +8 a +20,0 o más.1
El grosor escleral es un importante elemento a tener en consideración en ojos pequeños. La esclera es más gruesa en su parte posterior y mide aproximadamente 1,0 mm en un ojo de tamaño medio. La esclera se adelgaza en su porción anterior y mide aproximadamente 0,6 mm a nivel del ecuador, y la zona más delgada, de aproximadamente 0,3 mm, corresponde a la región escleral justo posterior a la inserción de los músculos rectos. En el nanoftalmo el grosor escleral medido por ecografía B es mayor de 1,7 mm en todos los casos, y en muchos pacientes es mayor a 2,5 mm.2
Estos ojos tienen una importante tendencia a desarrollar glaucoma de ángulo cerrado. Hay varios mecanismos involucrados en esto, como el bloqueo pupilar, el iris plateu, la expansión coroidea y el desplazamiento anterior del lente.3) Cuando ocurre el cierre angular es de difícil manejo porque no responde al tratamiento convencional. Los mióticos empeoran con frecuencia el bloqueo pupilar por relajación zonular, mientras la iridotomía láser y la iridoplastia pueden ser beneficiosas inicialmente, pero no es suficiente para controlar la presión intraocular (PIO).3,4
La cirugía de catarata en el nanoftalmo está asociada a un alto riesgo de complicaciones, tanto refractivas por lo difícil de realizar el cálculo del LIO (lente intraocular), como quirúrgicas por las condiciones de esos ojos. De igual forma, la cirugía del glaucoma con técnicas filtrantes puede ser desastrosa por la fluctuación de la PIO a causa de un bloqueo ciliar posoperatorio y una efusión uveal, muy temida por los cirujanos. Es más recomendable la extracción del cristalino en etapas tempranas, pero siempre que existan evidencias de aumento de la PIO que no se controle con una sola medicación, o de una catarata.3,4,5
Presentación de caso
Paciente femenina de 49 años de edad, quien acudió a la consulta por disminución lenta y progresiva de la visión en ambos ojos. Presenta antecedentes patológicos personales de hipertensión arterial esencial y antecedentes patológicos oculares de queratocono y glaucoma.
Al examen oftalmológico, los datos positivos para el diagnóstico fueron: segmento anterior con cámara anterior estrecha; iridotomías periféricas; catarata corticonuclear densa (dificultaba la observación del fondo); fondo de ojo con disco oblicuo y excavación 0,6 en el ojo derecho (OD) y 0,9 en el ojo izquierdo (OI). Las tensiones oculares elevadas; tensión ocular (TO) con corrección por paquimetría).
Chequeo preoperatorio de catarata
Agudeza visual sin corrección: En ambos ojos cuenta dedos a 2 metros.
Refracción dinámica: OD + 12,50-1,00 X 950 (0,4); OI + 12,50-0,50 X 850 (0,25) visión lateral.
Tensión ocular con corrección: OD: 22 mmHg; OI: 28 mmHG.
IOL máster 700:
Queratometría (K): OD 52,41; 51,61. OI 52,24; 52,00.
Cámara Anterior (CA): OD 2,58; OI 2;61.
Longitud Axial (LA): OD 16,93; OI 16,72.
Hoffer Q: LIO 47,0 dioptrías.
Se realizó la facoemulsificación de la catarata del ojo derecho por ser el de mejor pronóstico visual para colocar piggyback con LIO de mayor graduación en existencia en saco de 32,0 dioptrías (D) y LIO de menor graduación en sulcus de 15,0 D, previo tratamiento hipotensor con manitol y acetazolamida.
Complicación transquirúrgica
Hipertensión ocular, con estrechamiento marcado de la cámara anterior en el momento de colocar el segundo LIO, pero que no impidió el acto. Se indicó tratamiento hipotensor después de la cirugía.
Evolución posquirúrgica
Evolución de las 24 h: Cámara anterior formada; córnea transparente sin pliegues de la descemet; aparición de membrana inflamatoria prelental. Se indicó tratamiento local con esteroide, antinflamatorio no esteroideo, antibiótico, hipotensor (timolol 0,5 %) y se colocó inyección subconjuntival con betametasona.
Evolución a los 7 días: Cámara anterior formada; membrana prelental en fase de reabsorción; la paciente refería buena visión. Se mantuvo el tratamiento antinflamatorio, hipotensor y antibiótico.
Evolución a los 21 días: Cámara anterior ligeramente estrecha en relación con las consultas anteriores; resto pequeño de la membrana sobre el LIO; tensión ocular con corrección OD 29 mmHg. Se mantuvieron los antinflamatorios adecuando las dosis y se asoció la dorzolamida 3 veces al día.
Evolución a los 30 días: Se mantenían las tensiones elevadas y se decidió realizar la cirugía filtrante de glaucoma. Al mes de la cirugía de catarata se realizó trabeculectomía (TBT).
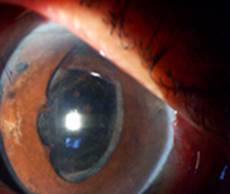
Evolución a los 15 días: La paciente presentaba cámara anterior muy estrecha y la periferia contactaba con la córnea (Fig. 1, 2 y 3).

Fig. 1 A las 24 h se observa cámara anterior estrecha. Tensión ocular con corrección 12 mmHg. Se indican midriáticos.

Fig. 3 A los 15 días se observa la cámara anterior muy estrecha. La periferia contacta con la córnea.
Se diagnosticó un glaucoma maligno, y se interconsultó con especialistas de Retina. Tomografía de coherencia óptica (OCT) 361,4; edema macular quístico 366; retina aplicada; disco oblicuo; excavación 0,6. Mácula con membrana epirretinal (MER) celofánica. Se realizó hialoidectomía con Yag láser y se ingresó con tratamiento parenteral hipotensor.
Biomicroscopia: Cámara muy estrecha, solo el área central no contactaba. Se realizó vitrectomía por pars plana; se repuso la cámara anterior y se rompieron las sinequias anteriores.
Evaluación al mes posvitrectomía pars plana: Se logró el control de la PIO y mantener la cámara anterior formada. Al mes, aún con medicamentos, la biomicroscopia mostraba: midriasis irregular por sinequias posteriores aisladas, cámara anterior amplia, mejoría de la visión. Tensión ocular con corrección 19 mmHg. Retinopatía diabética ojo derecho (RD OD) -2,50-2,50 x 85 (0,3) (Fig. 4).
Evaluación al año
Se logró el control de la PIO con dos medicamentos hipotensores; cámara anterior amplia y mejoría significativa de la agudeza visual. Tensión ocular con corrección: 16 mmHg; RD OD -1,75-1,50 x 85 (0,6) (Fig. 5).
Discusión
Los pacientes con nanoftalmo presentan dificultades en la conducta médica (hipermetropías, ambliopía y glaucoma) y quirúrgica (síndrome de efusión uveal, maculopatía quística y glaucoma maligno por síndrome misdireccional de acuoso), así como un elevado riesgo de descompensación corneal e iritis.5,6,7
La cirugía de catarata en el nanoftalmo debe realizarse cuando el cristalino lo justifique por opacidad o por intumescencia, que reduce los espacios y provoca riesgo de un glaucoma agudo,5,6 como en el caso que nos ocupa. Debe realizarse un estudio minucioso ocular y compensar enfermedades coexistentes previo a la decisión quirúrgica. La paciente presentó, como consecuencia de la cirugía, complicaciones bien descritas en la bibliografía, que debemos evitar en este tipo de caso y prepararnos para enfrentarlo.
Revisamos la bibliografía, analizamos restrospectivamente paso a paso y concluimos que nos faltaron procederes que hubieran evitado estas complicaciones, como la evaluación del espesor escleral previo a la cirugía.2 En los ojos en cuya ecografía se observa un aumento del grosor esclero-coroideo se pueden realizar esclerectomías profilácticas anteriores;8,9 indicar esteroides orales previo a la cirugía y realizar vitrectomía vía pars plana antes de la trabeculectomía.9