Introducción
El coronavirus dos del síndrome respiratorio agudo severo (SARS‐CoV‐2), surge en Wuhan, China en diciembre de 2019 y la enfermedad que produce se denomina COVID-19. Esta se disemina de forma rápida por todo el mundo y la Organización Mundial de la Salud (OMS) la declara como una pandemia el 11 de marzo de 2020. 1 Al inicio, el SARS-CoV-2 se cataloga como un virus respiratorio debido a que los primeros pacientes presentan un síndrome gripal, que en la mayoría de los casos evolucionan a una neumonía grave.
De este modo los esfuerzos iniciales se enfocan en manejarlo como tal, pero a medida que la pandemia progresa y se incrementan los casos, el virus revela un mayor espectro de manifestaciones clínicas. Como consecuencia de ello aumentan las notificaciones de pacientes infectados con SARS-CoV-2, sobre todo, con afecciones respiratorias, cardíacas, neurológicas, endocrinas y renales. 2
Los virus respiratorios causan infecciones que, según sus manifestaciones clínicas se clasifican en agudas y localizadas. Es decir provocan la alteración o necrosis del epitelio en un lapso aproximado de una a dos semanas durante el cual permanecen localizados en el tracto respiratorio. 3 Así pues, estas manifestaciones se observan durante infecciones producidas por adenovirus, rinovirus, virus sincitial respiratorio, coronavirus estacionales, virus parainfluenza y el virus influenza, 4 aunque en este último, existen informes esporádicos de su afinidad por otros órganos. 5 El tropismo tisular que presenta el SARS-CoV-2 es mayor y tiene características que distan mucho de ser solo un virus respiratorio, por lo que se asemejan más a los virus que producen infecciones generalizadas, en las que el sistema respiratorio representa la vía de ingreso, en la cual puede o no producir lesiones aparentes, como es el caso del virus del sarampión, la varicela, el virus Epstein-Barr y algunos enterovirus. 6
Las diferentes manifestaciones extrapulmonares evidenciadas en el curso de la COVID-19, así como las complicaciones posteriores a la infección, sugieren que el virus no solo está circunscrito o localizado en el epitelio pulmonar, tal y como sucede con los virus respiratorios, sino que tiene un tropismo mayor por otros órganos (Figura 1).
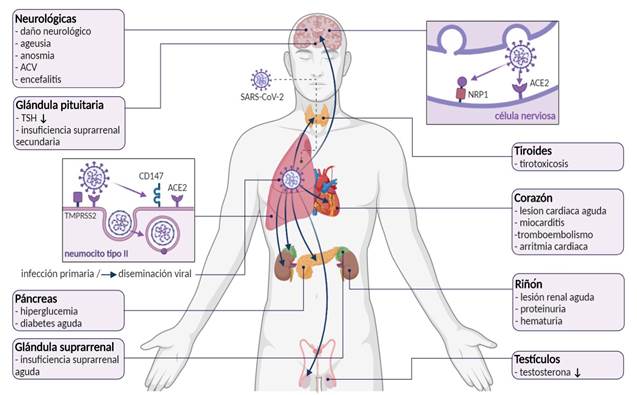
Figura 1 Curso bifásico y manifestaciones extrapulmonares de la COVID-19. El virus SARS-CoV-2 utiliza el tracto respiratorio como sitio inicial de replicación (fase inicial) y luego se propaga a otros órganos de los sistemas neurológico, cardiovascular, endocrino y renal principalmente, al provocar daño directo e indirecto (fase tardía).
Todavía no es posible determinar si las secuelas que sufren los pacientes que superan las infecciones por el SARS-CoV-2 son temporales o permanentes, pero una mejor comprensión del espectro de las manifestaciones, así como de la fisiopatología que las acompaña permiten abordar el tratamiento clínico de los pacientes infectados por este virus.
Métodos
La búsqueda y el análisis de la información se realizaron en un periodo de 65 días, desde el 23 de agosto hasta el 27 de octubre de 2020. Se emplearon los siguientes términos: Coronavirus AND COVID-19 AND SARS-CoV-2 AND virus replication AND tissue tropism AND neurologic manifestations OR cardiovascular diseases OR endocrine system diseases OR kidney diseases. No se aplicaron restricciones de idioma.
A partir de la información obtenida se realizó una revisión bibliográfica de un total de 197 artículos publicados en las bases de datos MEDLINE accedido desde PubMed, SciELO, LILACS. Así mismo, se tomaron en cuenta artículos publicados en repositorios de pre impresión como medRxiv, BioRxiv, e informes de la Organización Mundial de la Salud. Mediante el gestor de búsqueda y administrador de referencias Mendeley Desktop 1.19.4., se eliminaron los duplicados y aquellos que no se ajustaban al objetivo del estudio, para la revisión se seleccionaron 63 artículos.
Desarrollo
SARS-CoV-2: un virus respiratorio diferente:
Los virus respiratorios que afectan con mayor frecuencia a los seres humanos pertenecen a las familias Picornaviridae, Orthomyxoviridae, Paramyxoviridae y Coronaviridae.4 En cuanto a la enfermedad que producen, se caracteriza por ser aguda y localizada. 7 No es habitual que las infecciones respiratorias virales afecten zonas distintas al tracto respiratorio y sobre todo que se detecten durante periodos prolongados, salvo en algunos casos producidos por el virus de la influenza. 8,9 Por otra parte, los virus del sarampión, la rubéola, el virus Epstein-Barr y ciertos enterovirus como los coxsackievirus utilizan el tracto respiratorio como sitio inicial de replicación y lo infectan de forma inaparente, para luego diseminarse a otros órganos en busca de sus respectivas dianas, un mecanismo que en cierta medida se observa en los casos asintomáticos respiratorios que debutan con accidente cerebrovascular o miocarditis en SARS-CoV-2, tal como se describe más adelante.
SARS-CoV-2 puede invadir el parénquima pulmonar y no producir síntomas en alrededor del 80 % de los pacientes, 10 incluso muchos de ellos pueden presentar anomalías por imágenes de tomografía computarizada de tórax. 11 Lo más inquietante al respecto es que, alrededor del 50 % de los individuos asintomáticos infectados por SARS-CoV-2 también presentan estas anomalías radiográficas, incluidas las mencionadas opacidades en vidrio deslustrado. 12 Un hecho sin precedentes en las infecciones producidas por los virus respiratorios. 13
En los casos moderados y severos de la COVID-19, el daño no parece estar relacionado con la neumonitis viral, sino que se produce en gran medida por el sistema inmune en su intento por contener la infección y que reacciona de forma desproporcionada, al generar en algunos casos la llamada tormenta de citocinas. 14 Esto, sumado a la extensa formación de coágulos que pueden obstruir los alvéolos, son los principales responsables de las complicaciones respiratorias. 15 Aunque el pulmón es el principal órgano dañado por el virus, la COVID-19, ahora se considera una enfermedad sistémica que afecta a una amplia gama de otros órganos vitales. Es poco claro si la lesión de los órganos y tejidos en pacientes con la COVID-19 es consecuencia directa o indirecta de la infección por el virus. Sin embargo, SARS-CoV-2 posee afinidad por varios receptores entre los que se consideran el ACE2, CD147, CD26; 16,17 y la neuropilina-1 (NRP1) como se pudo observar en la figura anterior. (18 Todos ellos respaldan la posibilidad de un daño directo a otros órganos humanos vitales. 15
La infección por SARS-CoV-2 presenta un probable curso bifásico con persistencia y capacidad de reinfección:
Las características clínicas de la COVID-19 son heterogéneas y dependientes del hospedero. Al principio sugieren que la infección es inocua en los niños, ya que éstos no presentan la enfermedad respiratoria de forma aparente, sin embargo, luego determinan que algunos síndromes estaban presentes, lo que revela que el tracto respiratorio no es el objetivo final de SARS-CoV-2 en este grupo etario. 19 De este modo se propone que en la primera fase de la infección el virus aprovecha los receptores presentes en las vías respiratorias para ingresar al hospedero y llevar a cabo una primera replicación en este lugar, en dependencia si la vía respiratoria infectada (superior o inferior) se producen las primeras manifestaciones de la enfermedad, cuya exacerbación o complicación se dará en un número reducido de infectados que presentan condiciones de riesgo y comorbilidad. 20
Luego de la replicación inicial, el virus migra a otros órganos dentro del hospedero, donde en una fase tardía realiza una segunda replicación y se establece o no, en dependencia de la presencia de factores aún no estudiados según se muestra en la figura anterior. La evidencia de que el virus tiene tropismo tisular por muchos órganos distintos al tracto respiratorio se expone más adelante.
El 87 % de los pacientes que requieren atención hospitalaria por la COVID-19, sufren al menos un síntoma relacionado con la enfermedad casi dos meses después y más de la mitad experimentan fatiga. 21 Incluso algunos investigadores definen la existencia de la COVID-19 postaguda a la enfermedad, aquella que se extiende más allá de las tres semanas desde el inicio de los primeros síntomas y la COVID-19 crónica para la enfermedad que se prolonga más allá de las 12 semanas. 22 Estos datos revelan que el virus puede persistir en el organismo luego de alcanzar su sitio final de replicación. Según el investigador Tim Spector, del King's College de Londres, citado por Gajagher J, 23 una posibilidad es que el virus (tras la primoinfección) se haya eliminado de la mayor parte del cuerpo, pero se mantenga en pequeños focos. Si hay diarrea prolongada, el virus se encuentra en el intestino, si hay pérdida del olfato, está en los nervios. Es decir los síntomas persistentes de la enfermedad dependen del sitio de replicación secundaria.
La persistencia es un atributo poco descrito para los virus respiratorios de importancia clínica, y solo se notifica en las infecciones respiratorias producidas por rinovirus. 24 Un hecho que tiene repercusiones de interpretación en la detección viral mediante pruebas moleculares, ya que la detección de ARN de los rinovirus es frecuente en individuos sanos y son necesarios estudios de transcriptómica para detectar infecciones agudas y activas. 25
En este contexto la persistencia de SARS-CoV-2 en el organismo requiere un cambio de paradigma y enfoque en el manejo de la COVID-19, tanto en el diagnóstico de laboratorio como clínico debido a la necesidad de atender y hacer el seguimiento a las manifestaciones extrapulmonares.
La determinación de que el virus SARS-CoV-2 produce reinfecciones es reciente. 26 Esto indica que, la exposición previa al virus puede no garantizar la inmunidad total en todos los pacientes, lo que plantea un desafío para el desarrollo y la aplicación de vacunas. No obstante, los casos de reinfección se señalan también para otros virus respiratorios, con características heterogéneas en dependencia del agente viral y el lapso en que se susciten. Son esporádicas para el virus de la influenza, 24 y muy frecuentes en los rinovirus donde se detecta asociación significativa con la enfermedad pulmonar obstructiva crónica (p=0,04) y el asma (p=0,02). 27 De este modo, el virus SARS-CoV-2 posee características poco usuales algunas de las cuales son exclusivas de este nuevo virus.
SARS-CoV-2 y su tropismo tisular a nivel extrapulmonar:
Una de las primeras alteraciones extrapulmonares descritas en la COVID-19 corresponde a los trastornos quimiosensoriales del gusto (hipogeusia/ageusia) y el olfato (hiposmia/anosmia), donde las manifestaciones prevalentes asociadas al sistema nervioso periférico y que aparecen de modo súbito, incluso en los pacientes asintomáticos y en ausencia de obstrucción o secreción nasal. 28 Existen reportes de disfunciones olfativas y gustativas hasta en un 85,6 y 88 % de los pacientes infectados, respectivamente. 29 Se propone que las alteraciones del olfato pueden servir como marcadores tempranos de infección. 29 Inclusive la persistencia de la anosmia por más de 20 días parece estar asociada a un curso severo de la enfermedad. 30
Respecto al sistema nervioso central diversos informes proporcionan evidencia directa de la neuroinvasión del SARS-CoV-2, desde la aparición del primero de ellos en Japón, 31 así como reportes de meningitis/encefalitis después de la COVID-19 donde confirman la presencia del SARS-CoV-2 en los tejidos cerebrales y en las células endoteliales capilares, según las autopsias. 32
El bulbo olfatorio es la única parte del sistema nervioso central (SNC) que no está protegida por la duramadre y representa una probable ruta de ingreso para el SARS-CoV-2, al usar el epitelio olfatorio como vía de entrada, ya que expresa los receptores ACE2, TMPRSS2 y NPR1, necesarios para el ingreso viral y el transporte axonal retrógrado, según se aprecia en la descripción a de la (Figura 2). 33
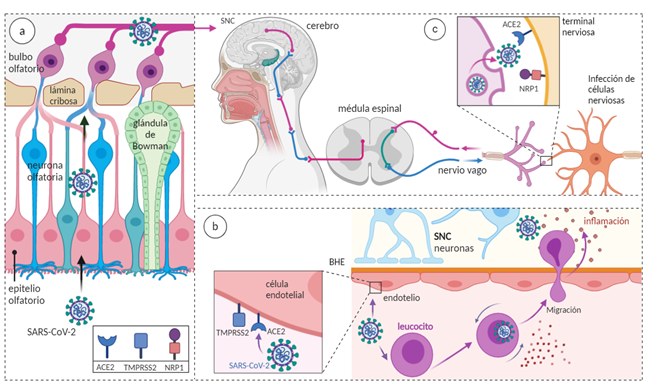
Figura 2 Mecanismos de invasión al SNC. a) SARS-CoV-2 puede ingresar empleando el epitelio olfatorio; b) a través de la ruta hematógena c) o utilizando el nervio vago con mecanismos de transporte axonal retrogrado y la diseminación transináptica. Figura modificada a partir de: Neurological Aspects of SARS-CoV-2 Infection: Mechanisms and Manifestations. Front Neurol. 2020;11:1039.
Los cambios de señal observados en el tallo cerebral y el tálamo pueden representar una infiltración central a través del sistema trigémino. 32 La neuroinvasión también se puede producir a través del transporte axonal retrógrado y la diseminación transináptica del SARS-CoV-2 desde los mecanorreceptores y quimiorreceptores situados en el pulmón hacia el centro cardiorespiratorio medular, lo que puede explicar la participación del tronco encefálico. 34
Un mecanismo de neuroinvasión poco probable del SARS-CoV-2, es a través de la ruta hematógena, dentro de los leucocitos infectados o por invasión directa a las células endoteliales de la barrera hematoencefálica (BHE) después de la viremia, aunque la ausencia del virus en la sangre no respalda esta vía de ingreso.
El infarto agudo de miocardio y el accidente cerebrovascular (ACV) se detectan con frecuencia durante el inicio de la pandemia. 35 Los primeros indicios que vinculan al virus con el daño cardíaco surgen a principios de 2020, cuando se notifica la primera muerte de un paciente con COVID-19 a causa de un ataque cardíaco. 36 Posterior a ese episodio se confirma el daño directo del SARS-CoV-2 al miocardio en un niño enfermo. 37 La autopsia detecta partículas virales dentro de varios tipos de células (cardiomiocitos, células endoteliales del endocardio, macrófagos, neutrófilos y fibroblastos), lo que demuestra que el SARS-CoV-2 es un agente causal importante de miocarditis como se observó en la figura 1 y ahora en (Figura 3).
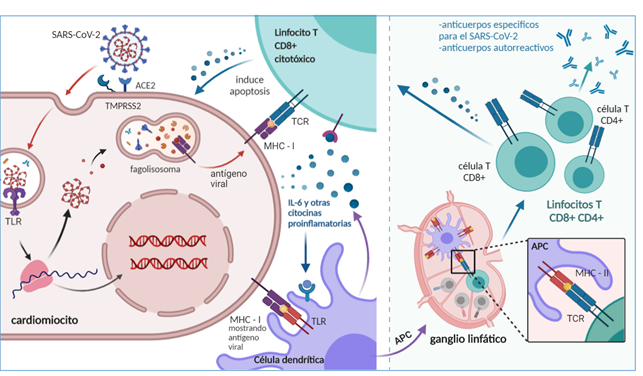
Figura 3 Mecanismos propuestos para la miocarditis por COVID-19. SARS-CoV-2 puede lesionar al miocardio por infección directa al cardiomiocito o por mecanismos de respuesta a la infección. Figura modificada a partir de: Molecular Biology and Pathogenesis of Viral Myocarditis. Annu Rev Pathol Mech Dis. 2008;3(1):127-55.
En la actualidad existen informes de que la lesión miocárdica es común en pacientes con la COVID-19 y representa entre el 7 al 23 % de los casos asociados a una mayor tasa de morbilidad y mortalidad, 38 frecuente en pacientes obesos o con alguna enfermedad preexistente como la hipertensión o la diabetes mellitus, 39 aunque también se presentan casos de miocarditis fulminante en pacientes jóvenes sin enfermedades previas. 40 Los mecanismos propuestos para la miocarditis en la COVID-19 se presentaron en la figura 3.
Los pacientes con enfermedades agudas suelen desarrollar hiperglucemia. En la COVID-19 la hiperglucemia observada en los pacientes hospitalizados puede ser un factor de riesgo mayor que la diabetes preexistente. 41 Por ahora, los análisis postmortem no demuestran una asociación directa del virus con la hiperglucemia, lo que significa que otros factores pueden estar implicados, como la alteración de la respuesta inmune o la hipersecreción de glucocorticoides producto del estrés celular. 42,43) A pesar de que hay estudios de autopsias que demuestran lesión en las células foliculares y parafoliculares de la tiroides en los pacientes con SARS-CoV, 44 y autopsias de tiroides en pacientes con SARS-CoV-2, 45 todavía no muestran el daño directo del virus en la tiroides.
A diferencia de otros órganos, el receptor ACE2 en las células testiculares (células germinales, células de Sertoli y células de Leydig), tiene una mayor expresión, convirtiéndolas en susceptibles a la infección por SARS-CoV-2. Esto puede tener efecto en el desarrollo sexual masculino y el inicio de la espermatogénesis. (46 Por otro lado, la expresión de ACE2 en los tejidos reproductivos femeninos como los ovarios, el útero, endometrio, la vagina y placenta es baja, lo que sugiere una menor susceptibilidad femenina, (47 pero hasta este momento el impacto del sexo en la COVID-19 es aún un tema de debate. 48
El receptor ACE2, se expresa en los tejidos suprarrenales. 49 Estudios de autopsias en SARS-CoV identifican el efecto citopático directo del virus en las células suprarrenales. 50 En SARS-CoV-2, los estudios postmortem identifican lesiones suprarrenales moderadas con infiltrado mononuclear, 51 pero no la presencia del virus in situ. Por otro lado, se evidencia daño directo del SARS-CoV-2 en el riñón, tanto en podocitos, 52 células del epitelio tubular proximal y distal, 52,53 lo que puede explicar, en parte, la disfunción renal observada en los pacientes hospitalizados por la COVID-19.
En cuanto a la lesión renal y la proteinuria observada en los pacientes con la COVID-19, surgen dos posibilidades. Por una lado, que el daño directo del virus en los podocitos que expresan ACE2, 52 altere la homeostasis local del sistema renina angiotensina aldosterona, eleva los niveles de angiotensina II, cuyas propiedades inflamatorias en el glomérulo hace que el podocito adopte un fenotipo disfuncional, donde al reestructurar su citoesqueleto e internalizar la nefrina, provoca su desprendimiento basal. La segunda posibilidad sería que el SARS-CoV-2 dañe a las células del epitelio tubular, que también expresan ACE2 y unido a la respuesta inflamatoria sistémica (citocinas proinflamatorias), causen el daño renal, que se evidencia con proteínas en la orina (Figura 4). 54

Figura 4 Mecanismos de daño renal por COVID-19. La invasión directa del SARS-CoV-2 en los podocitos y las células del epitelio tubular incrementa la inflamación local, en combinación con la respuesta inflamatoria sistémica provocan daño en el tejido renal. .54
Mecanismos de diseminación multiorgánica del SARS-CoV-2:
Luego de sustentar la presencia de SARS-CoV-2 en múltiples órganos, se genera una interrogante: ¿cómo puede este virus llegar a los diferentes sitios extrapulmonares? En este sentido, lo más atractivo es suponer que lo hace por diseminación sanguínea a través de una viremia tal como lo realizan otros virus bifásicos. 6 Sin embargo, la carga viral en la sangre de los pacientes infectados por SARS-CoV-2 es baja y es probable que, menos del 1 % de los análisis de sangre por PCR en los pacientes con COVID-19 muestren un resultado positivo, 55,56 incluso algunas pruebas no identifican su presencia. 57 Esto sugiere que la estrategia del virus para alcanzar otros órganos no implica el tráfico sanguíneo y que la viremia no es la base de la diseminación multiorgánica.
Otras posibles vías de diseminación usadas por el SARS-CoV-2 pueden ser la difusión pasiva y el transporte vesicular originado en el retículo endoplásmico. Está documentado que los coronavirus inducen la reorganización de las membranas de las células hospederas en una red usada para la replicación viral y para ocultar el ARN replicante de los mecanismos de defensa antiviral. Así, los nuevos viriones ensamblados en la red retículo vesicular y que no son liberados de la célula infectada, se acumulan en áreas determinadas, 58 que en el momento de su liberación, producen la fusión de las vesículas derivadas de la red retículo vesicular y la membrana plasmática en un proceso que parece depender de la interacción con balsas lipídicas, 59 o por proteínas autofagosómicas, como en el caso del virus de la hepatitis C. 60
Los exosomas representan otra vía de transporte extracelular del SARS-CoV-2 a través de vesículas cargadas con el virus en una estrategia denominada caballo de Troya, la cual, no solo permite la migración del SARS-CoV-2 hacia otros órganos, sino que constituye una posible explicación para la reaparición del ARN viral en los pacientes recuperados de la COVID-19, lo que sugiere que el material viral estaba oculto. 61
Diferentes tipos de virus desarrollan la capacidad para formar sincitios entre las células infectadas y células vecinas no infectadas. Durante la infección este proceso se facilita por una proteína de fusión. En SARS-CoV-2, la glicoproteína S está implicada en la formación de sincitios por medio de transfecciones transcelulares dependientes de la actividad proteolítica de la TMPRSS2. 62 Incluso, se conoce que el SARS-CoV-2 muestra una capacidad superior de fusión célula-célula in vitro comparado con el SARS-CoV. 63 Estos datos sugieren que el virus está mejor capacitado para propagarse de célula a célula. De modo que el transporte vesicular, la difusión pasiva, los exosomas, la inducción del sincitios y la diseminación célula a célula, son las posibles vías por las cuales se puede explicar la diseminación silenciosa de este nuevo virus.
Conclusiones
El SARS-CoV-2 no debe considerarse solo como un virus respiratorio de curso agudo. La COVID-19 requiere un enfoque terapéutico y manejo clínico distinto debido a las características clínicas evidenciadas en el SNC, cardiovascular, endocrino y renal, que sugiere su progresión postaguda y persistente en algunos pacientes.
Existe evidencia que propone su naturaleza bifásica en la que puede utilizar el tracto respiratorio como sitio de replicación inicial, para luego migrar a otros órganos donde en una segunda replicación continúa produciendo daño. Se debe tener en cuenta el seguimiento y la evaluación a largo plazo de los pacientes infectados con este virus a fin de detectar con antelación enfermedades que pueden complicar su recuperación














