Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med v.8 n.3 Ciudad de la Habana sep.-dic. 2003
Empresa Laboratorio Farmacéutico "Saúl Delgado"
Caracterización de los compuestos pungentes en la tintura de jengibre al 50 %
MSc. Aidelys Batista Carmona,1 Dr. Jorge Pino Alea,2 Lic. Ileana Rodríguez León,3 Lic. Armando Rodríguez Alfonso4 y Dr. Gabriel Padrón Palomar5
Resumen
Mediante cromatografía líquida de alta presión acoplada a espectrometría de masas se identificaron y cuantificaron los seis componentes pungentes mayoritarios de la tintura de jengibre al 50 % que fueron fundamentalmente cetoalcoholes y otras sustancias relacionadas: 6-gingerol, 8-gingerol, diacetato de 6-gingerol, 10-gingerol, 10-shogaol, y acetato de 6-gingerol. Los componentes mayoritarios correspondieron a los gingeroles. La comparación de los resultados, mediante análisis de cluster, para los lotes producidos entre los años 2000 y 2001 indicaron que sólo un lote se diferenció del resto en la composición de los compuestos pungentes .
DeCS: QUIMICA FARMACEUTICA; ACEITES VOLATILES; JENGIBRE; TINTURAS; CROMATROGRAFIA LIQUIDA DE ALTA PRESION; ESPECTROMETRIA DE MASA.
En la Farmacopea Americana y en otras se reconoce al jengibre (Zingiber officinale Roscoe), como droga oficinal usada como tónico general o estimulante y como estomáquico, además de presentar otros usos industriales en la preparación de bebidas estimulantes. Asimismo es conocido su efecto antiinflamatorio y analgésico usado en la terapia contra la migraña, a partir de la acción inhibitoria de los componentes pungentes sobre la ciclooxigenasa y lipoxigenasa en el metabolismo del ácido araquidónico.1
En el jengibre además de los compuestos volátiles que aportan el olor típico de este rizoma, existe un grupo de compuestos no volátiles que aportan su pungencia. Esta característica del jengibre ha sido objeto de investigación en los últimos sesenta años, pero sólo recientemente se han alcanzado conclusiones importantes sobre la naturaleza de los compuestos responsables. En la actualidad se conoce que la misma se debe a ciertos cetoalcoholes (gingeroles) relacionados con otras sustancias: shogaoles, paradoles y zingerona.2
A partir de la bondad del jengibre como planta medicinal, cuyas propiedades terapéuticas han permitido que sea parte de la producción de la industria farmacéutica cubana, los autores se propusieron profundizar en la caracterización de los compuestos pungentes con vistas a garantizar la calidad del producto denominado tintura de jengibre al 50 %.
Métodos
En el estudio se evaluaron los lotes de tintura de jengibre al 50 % producidos entre los años 2000 y 2001 que fueron obtenidos por percolación fraccionada con etanol al 90 %, según la tecnología de X. Iglesas.
Para la separación de los compuestos pungentes en el rizoma se realizó una cromatografía líquida de alta resolución (HPLC) a la muestra de tintura de jengibre con una dilución 1/100 en una mezcla de los disolventes empleados 4:1 (B:A). Se operó en una columna LiChrospher C18 (Merck, Alemania) de dimensiones 4 x 250 mm que tiene como sistema Bombas LKB 2248 (Pharmacia, Suecia), LKB 2252 (Pharmacia, Suecia) y un detector LKB 2151 (Pharmacia, Suecia). Se aplicó una velocidad de flujo de 0,8 mL/min. Los disolventes utilizados fueron A: ácido trifluoroacético (Pierce, USA) al 0,1% en agua y B: ácido trifluoroacético al 0,05 % en acetonitrilo (Chromasolv, Riedel-Haen, Alemania). El gradiente fue 0/20/80/100 y el comienzo fue isocrático (20 % B). La longitud de onda utilizada fue de 280 nm. El volumen de inyección fue 500 mL de 10/1000.
La identificación se realizó por espectrometría de masas. Los espectros de masas se adquirieron en un espectrómetro de masas híbrido con geometría ortogonal QTOF-2 (Micromass, Reino Unido) equipado con una fuente de ionización por ESI (electrospray). Los voltajes del capilar se fijaron a 3000 V para las fuentes de ESI respectivamente, mientras que el cono de entrada fue de 35 V.
El espectrómetro de masas se calibró con una mezcla de yoduro de sodio y cesio en el rango de 50-2000 Da (solución de yoduro de sodio 2 mg/mL, yoduro de cesio 0,5 mg/mL en una solución agua: isopropanol al 50 %). Las muestras se inyectaron al espectrómetro de masas mediante una bomba de jeringuilla a un flujo de 5 mL/min mediante una bomba de jeringuilla (Harvard, EE.UU). El primer cuadrupolo se fijó a una resolución de 3 a 4 Th para seleccionar el ión precursor a fragmentar. El gas de colisión fue argón y la energía de colisión empleada osciló entre 15 y 30 eV hasta lograr un espectro de masas con suficiente información estructural adecuada para su análisis. El programa para el procesamiento de los espectros de masas empleados fue el MassLinx versión 3.5 (Micromass, Reino Unido).
La cuantificación se realizó a partir de la medición de las áreas de los picos cromatográficos mediante el programa Biocrom y por el método del estándar externo, a partir de una curva patrón obtenida con soluciones patrones de eugenol (coeficiente de correlación r = 0,99 e intercepto igual a cero).
Resultados
En la figura 1 se presenta el cromatograma obtenido para uno de los lotes producidos, donde se aprecia la presencia de seis picos mayoritarios. El perfil cromatográfico respondió a una mezcla compleja con un amplio rango de hidrofobicidad, donde el pico 1 fue el más intenso.
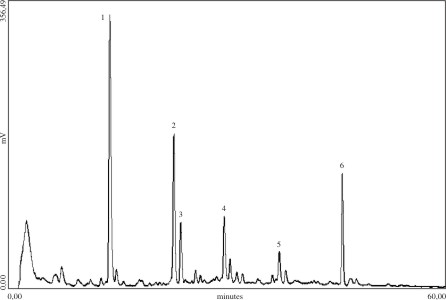
Fig. 1. Cromatograma obtenido por HPLC para la tintura de jengibre al 50 %.
En la tabla se presentan los resultados de la cuantificación de los componentes pungentes mayoritarios a partir de la identificación realizada. En la misma se aprecia que los componentes mayoritarios correspondieron a los gingeroles como era de esperar.1
Tabla . Componentes pungentes mayoritarios presentes en la tintura de jengibre
| Pico No. | Compuestos | Concentración (g/mL) | ||||
| 0001 | 1001 | 1002 | 1003 | 1004 | ||
| 1 | 6-gingerol | 1,33 | 1,19 | 1,46 | 1,45 | 0,92 |
| 2 | 8-gingerol | 0,59 | 0,71 | 0,66 | 0,68 | 0,40 |
| 3 | diacetato de 6-gingerol | 0,12 | 0,25 | 0,13 | 0,15 | 0,07 |
| 4 | 10-gingerol | 0,32 | 0,29 | 0,35 | 0,33 | 0,23 |
| 5 | 10-shogaol | 0,13 | 0,17 | 0,16 | 0,15 | 0,08 |
| 6 | acetato de 6-gingerol | 0,35 | 0,35 | 0,57 | 0,55 | 0,32 |
Resulta interesante señalar la baja concentración encontrada para los shogaoles, lo que pudiera indicar que hubo poca degradación de los gingeroles, componentes más pungentes que al perder agua durante el secado se transforman en shogaoles.
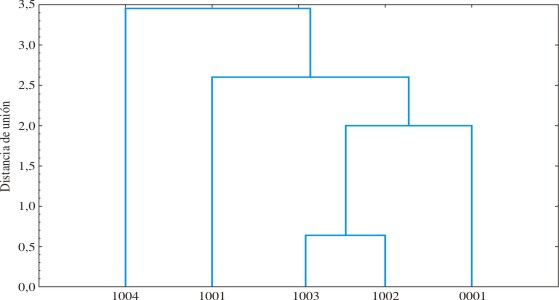
Aunque no se realizó un análisis de varianza, sólo parece haber diferencias apreciables en el lote 1004 con relación al resto de los lotes evaluados, como se demuestra por el análisis de cluster (Fig.2).
Discusión
El pico 1 del cromatograma correspondió al 6-gingerol, de acuerdo al espectro informado en la literatura.3
El pico 2 correspondió al 8-gingerol con trazas de 6-shogaol (los fragmentos 277, 299 y 315 correspondieron al M++1, M++23 y M++39 respectivamente) como se concluyó de la interpretación del espectro obtenido y de la literatura.3,4
El espectro del pico 3 no se pudo atribuir a ningún isómero del gingerol o del shogaol. Sin embargo, la presencia del fragmento m/z 137 (2-metoxi-4-metilenfenol), típico de las estructuras de estos compuestos, hizo pensar que pudo estar relacionado con ellos.
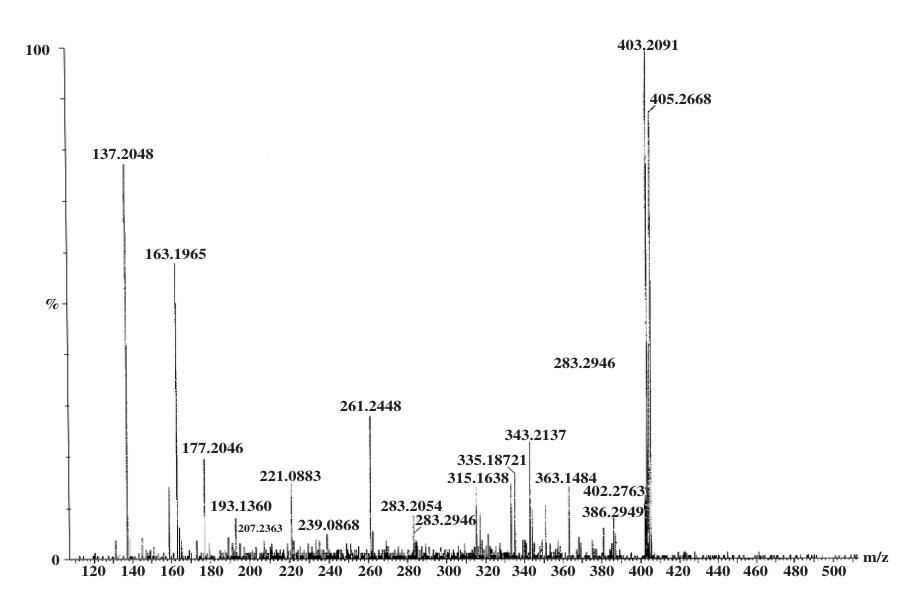
El fragmento m/z 403 se debió a la masa del 6-gingerol (294 uma) con dos grupos acetato (43 uma cada uno) unido a un ión sodio (23 uma). La fragmentación en el EM-EM de este ión, como se aprecia en al figura 3, justificó la existencia de los iones m/z 137, 261 y 343. Por otra parte, el ión m/z 338 se correspondió con el peso del 6-gingerol con un grupo acetato. Con toda esta información se llegó a la conclusión de que el pico 3 se corresponde con el diacetato del 6-gingerol, compuesto que había sido identificado anteriormente en el jengibre.1
Fig.3. Espectro EM-EM del ión 403 en el espectro del pico 3
Los picos 4 y 5 correspondieron al 10-gingerol y 10-shogaol respectivamente, de acuerdo a los espectros publicados.3,4
El espectro del pico 6 no está informado en la literatura y se hizo necesaria su interpretación. Los fragmentos del espectro parecen estar relacionados con los del espectro asignado para el diacetato de 6-gingerol (pico 3), particularmente el ión m/z 338. El fragmento m/z 363 puede atribuirse al ión anterior unido a un catión sodio. Por otra parte, el fragmento m/z 295 se correspondió con la masa molecular del 6-gingerol. Todo esto indujo a pensar que el compuesto presente es el acetato de 6-gingerol, lo que está de acuerdo con su volumen de retención posterior al del diacetato debido a su mayor polaridad por la presencia de un grupo hidroxilo libre.
De acuerdo con la literatura consultada, no existen técnicas analíticas para determinar el contenido de los compuestos pungentes en extractos hidroalcohólicos, ni aún en las farmacopeas más recientes.5,6 Solamente se tiene conocimiento de su determinación en la droga cruda y en oleorresinas mediante la técnica de cromatografía líquida de alta resolución (HPLC) en columna de RP-187 o Spherisorb CN.8 Con el uso de la primera columna se logra una mayor resolución, por lo que fue seleccionada para realizar este trabajo.
La baja concentración encontrada para los shogaoles, fue probablemente expensa de los gingeroles.9
Se identificaron y cuantificaron los seis componentes pungentes mayoritarios de la tintura de jengibre al 50 % que correspondieron al 6-gingerol, 8-gingerol, diacetato de 6-gingerol, 10-gingerol, 10-shogaol y acetato de 6-gingerol. La comparación de los resultados para los lotes producidos hasta la fecha indicó que sólo un lote se diferenció del resto de los lotes.
Summary
By high pressure liquid chromatography coupled to mass spectrometry the six main pungent components of ginger tincture 50 % that were cetoalcohols and other related susbstances: 6-gingerol, 8-gingerol, 6-gingerol diacetate, 10-gingerol, 10 shogaol, and 6-gingerol acetate, were identified and quantified. The chief components corresponded to gingerols. The comparison of the results by cluster analysis for the batches produced from 2000 to 2001 indicated that only a batch was different from the rest as regards the composition of the pungent compounds.
Subject headings: CHEMISTRY; PHARMACEUTICAL; OILS, VOLATILE; GINGER; DYES; CHROMATOGRAPHY, HIGH PRESSURE LIQUID; SPECTRUM ANALYSIS, MASS.
Referencias bibliográficas
- Mustafa T, Srivastava KC, Jensen KB. Drug Development report Pharmacology of ginger, Zingiber officinale. J Drug Dev 1993;19:25-39.
- Bisset G, Wichtl M. Herbal Drugs and Phytopharmaceuticals. 2da. ed, Boca Ratón: CRC Press; 2001. p. 537.
- Chen CC, Rosen RT, Ho CT. Chromatographic analysis of gingerol compounds of ginger (Zingiber officinale Roscoe). J Chromatogr 1986;360:163-73.
- _____. Chromatographic analysis of isomeric shogaol compounds of ginger (Zingiber officinale Roscoe). J Chromatogr 1986;360:175-84.
- US Pharmacopeia. USP 24. Rockville: USP Convention; 2000. p. 2149.
- British Pharmacopeia. Monographs: Medicinal and Pharmaceutical Substances, Ginger, 2000. p. 640.
- International Organization for Standarization (ISO). Ginger and its oleresins. Determination of the main pungent components (gingerols and shogaols). Method using high performance liquid chromatography. ISO 13 685, 1997.
- Hiserodt RD, Franzblau S G, Rosen R T. Isolation of 6-, 8- y 10 gingerol from rhizome by HPLC and preliminary evaluation of inhibition of Mycobacterium avium and Mycobacterium tuberculosis. J Agric Food Chem 1998;46:2504-8.
- Connell DW. The chemistry of the essential oil and oleoresin of ginger. Flavor Ind 1970;1:677-93.
Recibido: 19 de marzo de 2003. Aprobado: 31 de marzo de 2003.
MSc. Aidelys Batista Carmona. Empresa Laboratorio Farmacéutico "Saúl Delgado". Compostela 517, Habana Vieja, La Habana, Cuba.
1 Máster en Química Farmacéutica. Licenciada en Farmacia.
2 Doctor en Ciencias Técnicas. Licenciado en Química.
3 Licenciada en Bioquímica.
4 Licenciado en Química.
5 Doctor en Ciencias Químicas. Licenciado en Química.