Introducción
Las dislipemias o dislipidemias son trastornos frecuentes del metabolismo lipoproteico, caracterizados por presentar valores anormales en sangre de algunas de las fracciones lipídicas. Se pueden dividir en hipercolesterolemias, hipertrigliceridemias (HTG) y dislipemias mixtas o combinadas. 1
La prevalencia de las HTG alcanza el 10-30% de la población adulta y puede sobrepasar esas cifras en diferentes poblaciones, con una considerable variación regional, y se relaciona con otros componentes del síndrome metabólico. 2,3,4,5,6,7
Las HTG se clasifica según los valores de triglicéridos (TG) en ayunas, en moderada, cuando los triglicéridos (TG) están entre 1,70-11,4 mmol/L (150-1 000 mg/dL), y grave, cuando la concentración es de TG >11,4 mmol/L (> 1000 mg/dL). 8 Un grupo de pacientes puede presentar HTG muy grave, definida como una concentración de TG ≥ 22,6 mmol/L (2 000 mg/dL). 7
La HTG se acompaña frecuentemente de otros trastornos en el perfil de lípidos y en el metabolismo de lipoproteínas y se considera como un factor de riesgo independiente de la enfermedad cardiovascular aterosclerótica (ECVA), por lo que su detección temprana y tratamiento oportuno son de vital importancia para la prevención de estas enfermedades; además, los pacientes con cantidades elevadas de TG presentan riesgo de pancreatitis aguda.
El diagnóstico de HTG se basa en la determinación de TG en sangre en ayunas, aunque es recomendable determinar el colesterol total y el colesterol de lipoproteínas de alta densidad (HDL-C), que son mediciones simples de laboratorio. A partir de estos lípidos se puede calcular el colesterol de las lipoproteínas de baja densidad (LDL-C) con la fórmula de Freidewald y el colesterol no-HDL. Otros estudios incluyen apo B, apo C y apo A.
Los pacientes con HTG deben evaluarse siempre para determinar causas secundarias. 9 Entre las pruebas de laboratorio para excluir causas secundarias están: glucemia en ayunas (diabetes mellitus), creatinina sérica (enfermedad renal o síndrome nefrótico), hormona estimulante del tiroides y tiroxina (hipotiroidismo), gamma glutamil transferasa y volumen celular medio (abuso de alcohol), además de colesterol no-HDL (no-HDL-C).
En esta revisión bibliográfica se describirá la clasificación de las HTG, su relación con el riesgo cardiovascular y la conducta terapéutica.
Búsqueda de información
Se emplearon los descriptores hypertricyceridemia e hipertrigliceridemia durante el periodo de 10 de enero- 1 de febrero de 2020.
En US National Library of Medicine (https://www.nlm.nih.gov) del último año se encontraron 1 983 artículos en PMC.
En Scopus (https://www.scopus.com) se localizaron 83 documentos.
En Scientific Electrony Library Open-SciELO- (https://scielo.org/es) se hallaron 455 artículos a texto completo.
Se revisaron artículos clásicos y de la red de Infomed (www.sld.cu).
Desarrollo
Clasificación
En el pasado, las HTG se clasificaban según los fenotipos de hiperlipoproteinemias de Fredrickson. 10 Sin embargo, en la era genómica con la comprensión de sus bases genéticas, un sistema más práctico clasifica las dislipidemias en primarias o genéticas y secundarias.
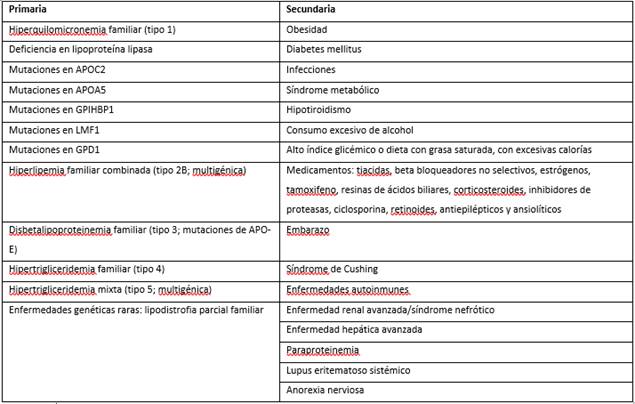
Las causas primarias y secundarias de HTG se numeran en la tabla I. La HTG primaria severa tiene determinantes monogénicos y poligénicos. 2 Entre las primarias se encuentran la hipertrigliceridemia familiar, la hipercolesterolemia combinada familiar, la disbetalipoproteinemia o el síndrome de quilomicronemia familiar. 11
Entre las causas secundarias de HTG, la obesidad, la diabetes, el síndrome metabólico, la insuficiencia renal crónica y ciertos fármacos o los trastornos tiroideos suelen ser las causas más frecuentes. 11
El síndrome de quilomicronemia familiar o quilomicronemia monogénica (FCS, antes tipo 1) es una forma de HTG autosómica recesiva, con una prevalencia de 1-10 en un millón. El solapamiento de los valores de TG séricos y los síntomas similares dificultan la diferenciación de las HTG severas más comunes del FCS, lo que constituye un desafío clínico. 12 El diagnóstico definitivo de este trastorno autosómico recesivo requiere la detección molecular de variantes raras bialélicas de 5 genes: LPL (80% de los casos), APOC2, APOA5, LMF1 y GPIHBP1.
La mayoría de los casos restantes de HTG grave son de naturaleza poligénica, lo que incluye contribuciones de variantes heterocigotas raras en los cinco genes FCS canónicos mencionados y variantes comunes acumuladas asociadas con niveles elevados de TG identificados en estudios de asociación genómica, 2 a veces denominados HTG multifactoriales (antiguo tipo 5).
La HTG de leve a moderada es usualmente poligénica, mientras que el HTG grave, especialmente en pacientes jóvenes, es más probable que se deba a causas monogénicas y está asociada con concentraciones de quilomicrones en ayunas sustancialmente mayores. 3
Metabolismo de lipoproteínas ricas en triglicéridos en enfermedades
Las lipoproteínas ricas en TG (TRL) son complejos esféricos compuestos por un núcleo de lípidos apolares (TG y ésteres de colesterol), con apoproteínas, fosfolípidos y colesterol en su superficie. Los quilomicrones formados en el intestino transportan los TG exógenos o dietéticos, mientras las lipoproteínas de muy baja densidad (VLDL) hepáticas trasladan los TG endógenos.
La secreción de quilomicrones y de VLDL, la lipolisis mediada por la lipoproteína lipasa (LPL) y la captación hepática de remanentes de lipoproteínas son determinantes en las concentraciones circulantes de TG. 2 La lipolisis mediada por la LPL de los nuevos TRL secretados es un proceso saturable, pero la lipolisis se reduce si la tasa de secreción y los valores de TG se elevan.
En general, el incremento de la síntesis de VLDL es el factor iniciador más frecuente para las HTG. Para cualquier tasa de secreción de TRL, la capacidad hereditaria de la vía LPL también modula los valores de TG.
Muchas personas con HTG también presentan resistencia a la insulina, obesidad y diabetes tipo 2 que acompañan el síndrome metabólico. Este ambiente impulsa el aumento de la secreción de VLDL, que se intensifica especialmente cuando los ácidos grasos y la insulina son excesivas.
La resistencia a la insulina con incremento de ácidos grasos circulantes también incrementa la secreción de quilomicrones. Además, la hiperglucemia estimula, mientras el péptido 1 semejante al glucagón, inhibe la secreción de quilomicrones. 2 También la apo C-III inhibe la eliminación de remanentes; por tanto, en estados con incremento de la secreción de VLDL cuando se eleva la apo C-III, la captación de partículas remanentes se reduce y se produce dislipidemia.
Riesgo cardiovascular aterosclerótico
Las TRL se relacionan con riesgo cardiovascular (CV), debido probablemente a los trastornos metabólicos acompañantes. Por ejemplo, en estudios de cohortes en Copenhague, los TG en ayunas de 6,6 vs. 0,8 mmol/L incrementaron el riesgo ajustado 5, 3 y dos veces para infarto miocárdico, trombosis isquémica y todas las causas de mortalidad, respectivamente. 2
En el Copenhagen General Population Study las personas entre 40-65 años sin ECVA y diabetes con TG >3,0 mmol/L (264 mg/dL) presentaron un riesgo similar de ECVA, comparado con personas elegibles a estatinas. 2 Esto sugiere una oportunidad para los estudios clínicos en esta población, porque el 80% de los eventos CV aparecen en personas no elegibles para la terapia profiláctica con estatinas.
Los valores de TG también predicen el riesgo CV en pacientes tratados con estatinas, después del síndrome coronario agudo, y representan una diana potencial para la prevención secundaria. 2
La relación causal entre TRL y ECVA se apoya en estudios aleatorios mendelianos y enfermedades como disbetalipoproteinemia, que aparecen en algunos pacientes homocigotos para el alelo E2 (<1% de europeos); las lipoproteínas con esta forma de apo E se unen defectuosamente a sus receptores. Sin embargo, la magnitud de esta asociación difiere. Las partículas TRL grandes de los quilomicrones nacientes son incapaces de penetrar en la pared de los vasos.
Aunque los valores circulantes de TRL predicen el riesgo de ECVA, es menos claro si los TG por sí mismos contribuyen a la aterogénesis. En contraste con el colesterol que se acumula en las células espumosas de la íntima y en las placas ateromatosas, los TG se degradan por la mayoría de las células. 2
Sin embargo, las TRL pequeñas ricas en colesterol esterificado (remanentes) promueven la aterogénesis por su infiltración en la pared de los vasos y sus acciones proinflamatorias y protrombóticas. Además, los TG elevados se asocian con frecuencia a partículas de HDL patológicas que pueden contribuir al riesgo de ECVA.
Además, se sugiere que la hidrólisis de las partículas de TRL en la superficie endotelial genera una inflamación local, lo que contribuye aún más a la formación de células espumosas a partir de los macrófagos y al proceso aterosclerótico. 3
Sin embargo, en condiciones de HTG grave, la saturación de la LPL puede impedir la hidrólisis eficiente de partículas grandes, como los quilomicrones y las VLDL, y por lo tanto las TRL pueden ser demasiado grandes para cruzar la barrera endotelial y no pueden entrar en la íntima y causar aterosclerosis, lo que sugiere que el colesterol de las lipoproteínas muy grandes puede ser menos aterogénico que el de las lipoproteínas más pequeñas. 3
La correlación de TG plasmáticos con el riesgo de ECVA en los estudios epidemiológicos se atenúa o pierde después del ajuste de no-HDL-C o apo B. 2 La mayoría del TG circulante se transporta por las VLDL y sus remanentes, que contienen apo B. Todas las partículas de TRL y de LDL tienen una molécula simple de apo B.
Se pueden estimar las lipoproteínas contenedoras de apo B con el no-HDL-C, calculado como el colesterol total menos HDL-C. Un reciente estudio encontró que todas las lipoproteínas con apo B tienen un efecto similar sobre el riesgo de ECVA. 2
Otro factor contribuyente al riesgo CV en la HTG es que en este estado, además de acompañarse de elevadas cantidades de apo B, se reduce la concentración de HDL-C. 8 Las HDL son partículas cardioprotectoras, por su papel en el transporte inverso del colesterol y sus propiedades antinflamatorias y antitrombóticas. En un estudio en pacientes tratados con estatinas con alto riesgo CV, los TG elevados son predictores significativos de insuficiencia cardíaca. 13
Algunos investigadores asocian algunos polimorfismos genéticos con la HTG, el HDL-C bajo y el riesgo CV, pero se requieren más estudios que esclarezcan las interrogantes surgidas.14
En resumen, aunque existe una asociación significativa entre la HTG y el riesgo de ECVA, la presencia de otros factores de riesgo coronarios, como diabetes mellitus, hipertensión arterial, obesidad, sedentarismo y estrés pueden introducir variables de confusión difíciles de cuantificar; además, estos factores, incluyendo la HTG, tienden a actuar durante un largo periodo, cuando comienza la aterosclerosis en las primeras etapas de la vida y llega a manifestarse clínicamente en personas adultas o adultos mayores.
Conducta terapéutica
Como con cualquier otra alteración bioquímica, antes de plantear su tratamiento, se debe siempre investigar su causa y establecer el diagnóstico diferencial.15La anamnesis, exploración física, historia familiar y los estudios complementarios básicos pueden orientar a una forma secundaria o a un trastorno primario con base genética. Para confirmar estos últimos se realizan estudios adicionales y pruebas moleculares.
Numerosas organizaciones han publicado guías de práctica clínica para la evaluación y tratamiento de la HTG, entre las cuales están: American Heart Association (AHA), National Lipid Association (NLA) y American Association of Clinical Endocrinologists (AACE)/American College of Endocrinology (ACE). (16,17,18,19
La principal indicación para el tratamiento de la dislipidemia es la prevención de la ECVA: síndromes coronarios agudos, accidente cerebrovascular, ataque isquémico transitorio o enfermedad arterial periférica, provocada por la aterosclerosis. 20 El tratamiento se indica para todos los pacientes con ECVA (prevención secundaria) y para algunos sin esta enfermedad (prevención primaria). En el caso de HTG grave, se previene la pancreatitis aguda.
La conducta terapéutica de las HTG, un desafío clínico, se basa principalmente en modificaciones de los estilos de vida no saludables y en el empleo de fármacos reductores de lípidos.
Cambios en los estilos de vida
El más importante principio para tratar las personas con HTG es el control de los estilos de vida relacionados con esta dislipidemia. Entre ellas se encuentran la obesidad y el síndrome metabólico resultantes de la inactividad física y las dietas con un alto contenido de calorías, debido al alto índice de grasa o alto índice glucémico.
El primer paso práctico en la modificación del estilo de vida se relaciona con el consumo de alcohol, que debe ser evitado por las personas con un alto nivel de TG. 2 Además, debido a los muchos efectos beneficiosos adicionales para el metabolismo y la salud, el aumento de la actividad física es otra piedra angular de las recomendaciones de estilo de vida.
La cantidad mínima de ejercicios requerida para reducir los TG posprandiales no se ha determinado, pero un periodo de 30-60 minutos de ejercicio aerobio intermitente o de fuerza parecen efectivos en la reducción plasmática de TG y de VLDL. 19 Un reciente metanálisis, que comparaba programas de ejercicios físicos aerobios, mostró efectos favorables solo en los programas de gran intensidad. 19 El mayor incremento se produjo en HDL-C y en menor medida sobre TG, colesterol total y LDL-C.
En cuanto a la dieta, el principio más importante es reducir la ingesta calórica neta, según estudios en animales 21 y humanos. En lo que respecta a las recomendaciones dietéticas específicas, los alimentos ricos en carbohidratos refinados, la sacarosa y la fructosa aumentan el TG mucho más, comparados con los alimentos ricos en fibras y de bajo índice glucémico.
Los ácidos grasos trans deben evitarse. Las dietas ricas en ácidos grasos saturados (aceites tropicales, carne grasa o procesada, dulces, crema y mantequilla) deberían sustituirse por verduras, alimentos integrales, pescado y por grasas monoinsaturadas (aceite de oliva virgen extra) y poliinsaturadas (aceites vegetales no tropicales).
Para los pacientes con HTG grave y quilomicronemia en ayunas, la grasa dietética total debe reducirse tanto como sea posible, es decir, < 30 g/día. 2 También se puede considerar la posibilidad de utilizar TG de cadena media (6 a 12 carbonos), que se transportan y metabolizan directamente en el hígado, lo que evita la formación de quilomicrones.
Algunos recomiendan la dieta mediterránea, que se asocia con una reducción del 10- 15% en el nivel de TG. 9 Esto resulta de la combinación de un aumento de los ácidos grasos omega-3, granos enteros, frutas, vegetales, legumbres y nueces. Es recomendable el consumo de pescado graso (caballa, atún, salmón, sardinas y arenque), por su alto contenido de ácidos omega-3, como se demostró en un cohorte coreano. 22
La pérdida de peso tiene efectos beneficiosos sobre el perfil lipídico. Una reducción de peso de 5-10% disminuye el 20% los TG, reduce 15% el LDL-C, de 8-10% incrementa el HDL-C. 16 Diversos ensayos clínicos han demostrado los efectos beneficiosos de las modificaciones dietéticas y los programas de ejercicios físicos en la reducción de los valores de TG séricos. 23,24
Tratamiento farmacológico
Las drogas reductoras de lípidos disponibles, como las estatinas, la ezetimiba, los inhibidores PCSK9, los fibratos, los ácidos grasos omega-3 y la niacina, afectan los TG. El efecto de estos medicamentos suele ser modesto (5-15%), mientras que los fibratos, los ácidos grasos omega-3 y la niacina tienen mayores efectos (25-45%). 2
Las estatinas son el tratamiento de elección para reducir el LDL-C, porque disminuyen las tasas de mortalidad y morbilidad CV e inhiben a la hidroximetilglutaril CoA reductasa, enzima clave en la síntesis del colesterol, lo que conduce al aumento del número de receptores para LDL y promueve la eliminación de colesterol. Estos fármacos disminuyen hasta 60% la concentración de LDL-C y generan pequeños incrementos en las concentraciones de HDL-C, con descenso moderado de la concentración de TG. 20 Por tanto, son indicados en las dislipidemias combinadas que se acompañan de HTG e hipercolesterolemia. Si el paciente solo presenta HTG, los fibratos son el fármaco de elección.
Los fibratos pueden reducir la TG hasta el 70%, aunque con una marcada variación interindividual. Como monoterapia, los fibratos probablemente reducen el riesgo de ECVA. 2 Pero cuando se usan en combinación con estatinas, no se observó ninguna otra reducción del riesgo, aunque los análisis de subgrupos indican que los pacientes con HTG y HDL-C bajo pueden beneficiarse de dicha terapia de combinación.
En la actualidad no está claro si el hecho de no mostrar beneficios se relaciona con un verdadero fracaso o con cuestiones metodológicas del diseño del estudio y los criterios de inscripción.
Altas dosis de ácidos grasos omega-3 pueden disminuir de manera variable los niveles de TG; en dosis más bajas (1 g/día), estos agentes generalmente no han mostrado una reducción de la ECVA. 2 Aunque hay resultados contradictorios, estos ácidos parecen tener efectos beneficiosos sobre la prevención primaria y secundaria de eventos cardiovasculares, según estudios moleculares y de intervención. 25
El ácido nicotínico (niacina) es el fármaco más eficaz para aumentar la concentración de HDL. 20 Su mecanismo de acción es desconocido, pero parece aumentar la síntesis de HDL y, simultáneamente, inhibir la eliminación de HDL, además de movilizar el colesterol de los macrófagos. 20,26
La niacina también disminuye la HTG y, en dosis de entre 1 500 y 2 000 mg/día, reduce la concentración de LDL-C. 20 La niacina causa sofocos, prurito y náuseas, pero la premedicación con bajas dosis de aspirina puede prevenir estos efectos adversos. Los preparados de liberación prolongada generan sofocos con menor frecuencia.
En un metanálisis, además de su efecto sobre otros lípidos, los inhibidores de PCSK9 produjeron 11,42% de reducción en los TG séricos. 27 La Food and Drug Administration (FDA) aprobó dos anticuerpos monoclonales que inactivan la proproteína convertasa subtilina-hexina tipo 9 (PCSK9), para disminuir el LDL-C. 28
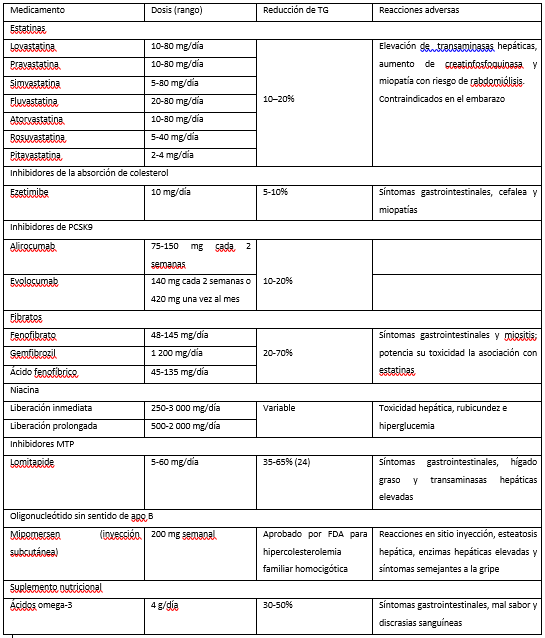
En la (tabla II) se resumen los fármacos utilizados con las dosis recomendadas. Los secuestradores de ácidos biliares están contraindicados en la HTG porque aumentan los valores de TG. 8 También deben evitarse otros medicamentos elevadores de los TG. Otras terapias se encuentran en desarrollo, como el empleo de los oligonucleótidos sin sentido y la edición genómica. 29,30,31
Conclusiones
El aumento de los TG en sangre produce HTG, debido principalmente al aumento de las concentraciones circulantes de las TRL (quilomicrones intestinales y VLDL hepáticas) y sus remanentes.
Las HTG son dislipidemias frecuentes en la práctica médica, cuya relación con la ECVA se ha subestimado. La HTG puede ser hipertrigliceridemia pura o aislada o HTG combinada (hipertrigliceridemia e hipercolesterolemia)
Las causas son primarias o genéticas y secundarias. Las HTG secundarias son más frecuentes y se observan en trastornos hormonales, dietas no saludables, consumo excesivo de alcohol, empleo de medicamentos, embarazo, enfermedades renales y hepáticas avanzadas.
La conducta terapéutica de las HTG comprende cambios en los estilos de vida, como dietas hipocalóricas ricas en fibra dietética y escasa en grasas e incremento de la actividad física. También debe disminuirse el consumo de alcohol y reducirse el peso corporal en los pacientes con obesidad.
Se dispone de fármacos reductores de lípidos eficaces para el tratamiento de las HTG, como estatinas, ezetimiba, inhibidores de PCSK9, fibratos, ácidos grasos omega-3 y niacina. Se deben controlar las enfermedades que favorecen el aumento de los TG, como la diabetes mellitus descompensada y evitar los medicamentos hiperlipemiantes.