Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Higiene y Epidemiología
versión On-line ISSN 1561-3003
Rev Cubana Hig Epidemiol vol.50 no.1 Ciudad de la Habana ene.-abr. 2012
ARTÍCULO ORIGINAL
Control de calidad de la baciloscopia de esputo BAAR en laboratorios provinciales en Cuba
Quality control of acid fast bacilli of sputum smears microscopy in tuberculosis provincial reference laboratories in Cuba
Dra. María Rosarys Martínez Romero, Téc. Grechen García León, Téc. Misleidis Sardiña Aragón, Dr. C. Ernesto Montoro Cardoso
Laboratorio Nacional de Referencia e Investigaciones en Tuberculosis y Micobacterias. Centro Colaborador OPS/OMS. Instituto de Medicina Tropical "Pedro Kourí". La Habana, Cuba.
RESUMEN
Introducción: el laboratorio es un componente crítico en el diagnóstico, tratamiento, prevención y control de la tuberculosis.
Objetivo: analizar el comportamiento del control de calidad de la baciloscopia en los laboratorios de referencia provinciales de tuberculosis de Cuba, mediante el método de rechequeo de láminas a ciegas.
Métodos: se realizó el control de calidad, por el método de rechequeo de láminas, a 5 424 láminas de esputo BAAR recibidas en el Laboratorio Nacional de Referencia de Tuberculosis y Micobacterias del Instituto de Medicina Tropical "Pedro Kourí", procedentes de los laboratorios de tuberculosis de los Centros Provinciales de Higiene, Epidemiología y Microbiología de Cuba, desde el año 2007 hasta 2009.
Resultados: se identificaron 54 errores de lectura; de ellos, 20 falsos positivos, 13 falsos negativos y 21 errores de codificación. La sensibilidad, especificidad y concordancia mostraron valores de 84,7, 99,6 y 99,4 %, respectivamente. La concordancia entre el Laboratorio Nacional de Referencia de Tuberculosis y Micobacterias del Instituto de Medicina Tropical "Pedro Kourí" y los laboratorios provinciales de tuberculosis evaluados fue de 99,4 % (índice de kappa 0,8105) y la discordancia fue de solo el 0,6 %.
Conclusiones: los resultados sugieren una adecuada calidad del personal de los laboratorios provinciales para realizar el control de calidad de la BK de esputo BAAR. Se recomienda continuar con las visitas a los laboratorios de la red para detectar las deficiencias e implementar las medidas correctivas oportunas con el fin de seguir mejorando la calidad del diagnóstico de la baciloscopia y así eliminar la tuberculosis como problema de salud en Cuba.
Palabras clave: baciloscopia, tuberculosis, control de calidad.
ABSTRACT
Introduction: the laboratory is a critical component in the diagnosis, treatment, prevention and control of tuberculosis.
Objective: to analyze the behavior of quality control of bacilloscopy in provincial reference laboratories of Cuba, by the re-checkup of blind plates.
Methods: the quality control was carried out by re-checkup method of plates at 5 424 plates of BAAR sputum received in the National Reference Laboratory of Tuberculosis and Mycobacteria of the "Pedro Kourí" Institute, originating in the laboratories of tuberculosis of Provincial Centers of Hygiene, Epidemiology and Microbiology of Cuba from 2007 to 2009.
Results: tifty four reading errors were identified; from them 20 false-positive, 13 false-negatives and 21 coding error. The sensitivity, specificity and concordance showed values of 84.7, 99.6 and 99.4 %, respectively. The concordance between the NRLTB PKI and the provincial tuberculosis laboratories assessed was of 99.4 % (Kappa rate 0.8105) and the discordance was only of 0.6 %.
Conclusions: results suggest an appropriate staff quality of the provincial laboratories staff to carry out the quality control of BAAR sputum BK. It is recommended to continue with visits to network laboratories to detect the deficiencies and to implement appropriate corrective measures to go on with the diagnosis quality of BK and so to eliminate the TB as a health problem in Cuba.
Key words: bacilloscopy, tuberculosis, quality control.
INTRODUCCIÓN
El laboratorio es un componente crítico en el diagnóstico, tratamiento, prevención y control de la tuberculosis (TB). Esta enfermedad afecta a ocho millones de personas en todo el mundo y provoca alrededor de dos millones de muertes por año.1
El examen directo de esputo continúa siendo la herramienta primaria en el diagnóstico de la TB pulmonar activa y es la prueba más utilizada a nivel internacional en la búsqueda de casos infecciosos en la comunidad.2,3 Para un control efectivo de la TB, la red de laboratorios de tuberculosis debe disponer de personal que realice la baciloscopia (BK) de forma confiable.4
Dentro de los objetivos del Plan Mundial para detener la TB de 2011 2015 se encuentra precisamente mejorar el diagnóstico de la TB por el examen directo. Se espera que al finalizar el 2015, de los 149 países considerados en el plan global, 35 deben tener al menos un laboratorio por 100 000 habitantes con un control de calidad externo efectivo y más del 90 % de los laboratorios de baciloscopía evaluados con calidad adecuada, dentro de los estándares internacionales.5
En Cuba, el programa nacional de control de la tuberculosis (PNCTB), junto con el Ministerio de Salud Pública, se encuentra trabajando arduamente con el objetivo de eliminar la TB como un problema de salud. Dentro de las tareas para lograr este propósito se encuentra el mejoramiento del sistema de vigilancia, donde el control de calidad de la BK es un aspecto de gran importancia.6
El objetivo de este estudio fue realizar y analizar el comportamiento del control de calidad de la BK en los laboratorios de referencia provinciales de TB de los Centros Provinciales de Higiene, Epidemiología y Microbiología (CPHEM) de la red, con el uso de la nueva modalidad el método de rechequeo de láminas a ciegas, como una nueva y útil herramienta para mejorar la calidad del diagnóstico por BK en Cuba.
MÉTODOS
Se realizó el control de calidad de la BK de esputo BAAR, utilizando la nueva modalidad de rechequeo de láminas a ciegas, a 5 424 láminas recibidas en el Laboratorio Nacional de Referencia de Tuberculosis y Micobacterias del Instituto "Pedro Kourí" (LNRTB IPK), procedentes de los laboratorios de TB de los 14 CPHEM de Cuba, desde 2007 hasta 2009.
Los laboratorios de TB de los CPHEM evaluados, enviaron de forma mensual el 10 % láminas de esputo negativas y el 100 % de láminas positivas al LNRTB IPK. La recoloración y codificación de las láminas se realizó según lo establecido en el PNCTB.7
Posteriormente, fueron solicitados a los laboratorios que estaban siendo evaluados los resultados del control de calidad correspondiente, y se compararon con los obtenidos en el LNRTB - IPK. En el caso donde fueron identificadas discordancias, las láminas fueron recoloreadas y evaluadas nuevamente por un segundo observador, antes de emitir el resultado final.
Para la evaluación de la calidad de las lecturas, se clasificaron los errores de la forma siguiente:
- Falso positivo (FP): láminas evaluadas como positivas por el laboratorio evaluado y resultaron negativas por el LNRTB IPK.
- Falso negativo (FN): láminas evaluadas como negativas por el laboratorio evaluado y resultaron positivas por el LNRTB IPK.
- Errores de codificación (EC): láminas con diferencias cuantitativas en dos o más valores de codificación entre el laboratorio evaluado y el LNRTB IPK.
El cálculo de las tasas de errores se realizó de la forma siguiente:
- Tasa de falsos negativos: Número de láminas leídas como negativas por el laboratorio evaluado y resultaron positivas por el laboratorio supervisor, divididas entre el total de láminas negativas por el laboratorio supervisor, multiplicado por el 100 %.
- Tasa de falsos positivo: Número de láminas leídas como positivas por el laboratorio evaluado y resultaron negativas por el laboratorio supervisor, divididas entre el total de láminas positivas por el laboratorio supervisor, multiplicado por el 100 %.
- Tasa de errores de codificación: Número de láminas con diferencias cuantitativas en más de dos valores entre el laboratorio evaluado y el LNRTB IPK, divididas entre el total de láminas positivas por el laboratorio supervisor, multiplicado por el 100 %.
Para la interpretación de los resultados, se consideró un desempeño adecuado del laboratorio, hasta de 5 % para el total de resultados FP, y 1 % para los FN, según lo establecido en las normas internacionales.8,9
El análisis estadístico para determinar los indicadores de calidad se realizó utilizando el Programa para Análisis Epidemiológico de Datos Tabulados EPIDAT, versión 3.1 (diciembre del 2003), con un intervalo de confianza del 95 %.
RESULTADOS
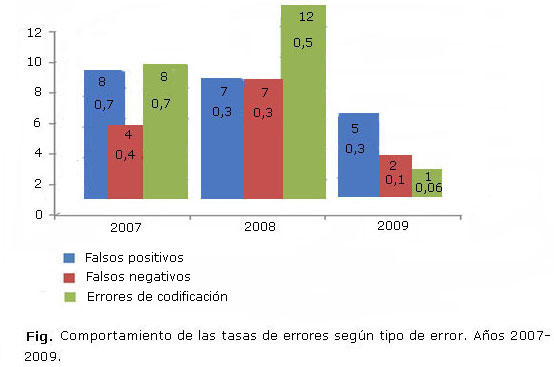
Se evaluaron un total de 5 424 láminas procedentes de los laboratorios de TB de los 14 CPHEM de Cuba. Se identificaron de forma general 54 errores de lectura, 20 (0,4 %) falsos positivos, 13 (0,2 %) falsos negativos y 21 (0,4 %) errores de codificación.
En la figura se muestra el comportamiento de las tasas de acuerdo con el tipo de error. En los años 2007 y 2008 se identificaron 20 (1,8 %) y 26 (1,02 %) errores de lectura respectivamente, donde la tasa general de errores se comportó de forma similar. En 2009 se identificaron solamente ocho errores de lectura para 0,4 %, menor a la tasa obtenida en los años anteriores. El porcentaje general de errores de lectura fue de 1 %, inferior a los valores establecidos como tolerables para un adecuado desempeño del personal del laboratorio, según la norma internacional.
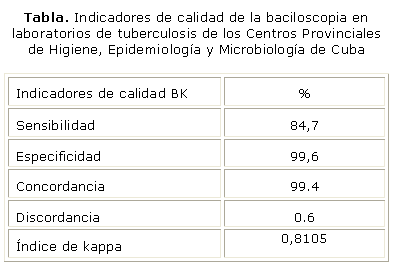
Los indicadores de calidad de la BK mostraron valores aceptables, con una sensibilidad y especificidad de 84,7 y 99,6 %, respectivamente. La concordancia obtenida entre los laboratorios evaluados y el LNRTB IPK fue elevada (99,4 %), con solamente 0,6 % de discordancia general, con un índice de kappa de 0,8105, valores muy cercanos a 1, lo que ratificó la concordancia obtenida en nuestro estudio (tabla).
DISCUSIÓN
El control de calidad externo de la BK de esputo BAAR es una excelente herramienta para mantener una buena práctica de laboratorio.10
Para obtener y mantener una alta confiabilidad en el examen directo de las muestras de esputo para el diagnóstico de la TB, es indispensable disponer de un sistema de control de calidad de la BK, debidamente implementado, que tiene la finalidad de identificar las deficiencias e implementar oportunamente medidas correctivas para mejorar la calidad del diagnóstico por esta técnica.11
A partir del año 1999, en Cuba se implementó el control de calidad de la BK de forma sistemática, donde se evaluaban mensualmente el 10 % de las láminas negativas y el 100 % de las positivas, procedentes de los laboratorios de la red hacia los laboratorios de referencia de los CPHEM de cada provincia y estos, a su vez, hacia el LNRTB IPK.5
Martínez y otros, realizaron un estudio en 2004 donde la relectura se realizó sin recolorear las láminas y con el conocimiento de los resultados. En esta investigación se identificaron 21 (0,48 %) errores de lectura; de ellos 5 (0,11 %) falsos positivos, 3 (0,07 %) falsos negativos (FN) y 21 (0,48 %) errores de codificación.12 Posteriormente, en el 2006, la misma autora realizó otro estudio donde solo se identificaron seis errores de lectura, con una tasa de FP de 1,1 %, mayor al encontrado en nuestra investigación. En esta oportunidad no se identificaron falsos negativos.13
A partir del año 2004 y hasta el 2006, se realizó en nuestro país un estudio utilizando el método de rechequeo de láminas a ciegas, modalidad que hasta la fecha no se había realizado, recomendada por expertos en el tema en el manual External Quality Assessment for AFB Smear Microscopy,14 en laboratorios seleccionados de dos provincias de Cuba: La Habana y Las Tunas, donde se realizó la relectura a ciegas y sin el conocimiento de los resultados. En esta ocasión se obtuvo una concordancia superior al 98 % y los indicadores de calidad de la BK mostraron valores aceptables, similar al obtenido en nuestro trabajo.
A partir de 2007, se implementa en el LNRTB IPK y en el resto de los laboratorios de la red de laboratorios de TB del país, la nueva modalidad con recoloración de las láminas antes de la relectura y a ciegas, como parte de un proyecto internacional del Fondo Mundial Ronda 7.
En estudios realizados, investigadores han asociado algunos errores de lectura a la exposición de alta temperatura y humedad, donde los BAAR pueden volverse invisibles en 2 a 3 semanas; además, aproximadamente cerca del 50 % de los resultados FP se han relacionado con deficiencias en la coloración. Por otro lado, un calentamiento insuficiente durante la tinción puede afectar la retención de la fucsina por el bacilo y producir resultados FN.15,16
Otras de las causas a tener en cuenta y que influyen en gran medida en la decoloración de los bacilos, es el almacenamiento inadecuado de las láminas antes de ser enviadas a los centros de referencia para el control de calidad, en sitios húmedos y con temperatura elevada. Estas condiciones influyen, a su vez, en la estabilidad de la fucsina, donde pueden producir precipitados de cristales y ocasionar resultados falsos positivos (FP).17,18
La baciloscopia, no es una técnica totalmente reproducible. El rango de reproducibilidad oscila entre 93 y 96 %.19 La concordancia obtenida en nuestro estudio podemos considerarla buena. Similares resultados obtuvieron Kusnierz y otros, en un reporte en 2004, donde la concordancia total fue de 98 %. Sin embargo, las tasas de FP y FN obtenidas en ese mismo estudio fue de 7,8 y 1,2 %, respectivamente, con una discordancia general del 2 %, mayor a la obtenida en nuestro trabajo.14 Consideramos que pueda estar relacionado con que la tasa de incidencia de TB de Argentina es elevada, por lo que son observadas mayor cantidad de frotis positivos y la probabilidad de identificar errores de lectura es mucho mayor.
Los resultados obtenidos, como en estudios anteriores realizados, sugieren la calidad del personal dedicado a realizar el control de calidad de la BK de esputo BAAR en los laboratorios provinciales, al obtenerse los indicadores con valores aceptables, para un desempeño aceptable del laboratorio. Recomendamos continuar con las visitas sistemáticas a los laboratorios de la red para detectar a tiempo las deficiencias e implementar las medidas correctivas oportunas con vista a continuar mejorando la calidad del diagnóstico de la BK y así colaborar con la eliminación de la TB como problema de salud en Cuba.
REFERENCIAS BIBLIOGRÁFICAS
1. McCarthy KD, Metchuck B, Knphukiew A, Monkongdie P, Sinthuwattanawibool C, Tasaneeyapan T, et al. Monitoring the performance of mycobacteriology laboratories: a proposal for standardized indicators. Int J Tuberc Lung Dis. 2008;12(9):1015-20.
2. Minion J, Zwerling A, Pai M. Diagnostics for tuberculosis: what knowledge did we gain through the international Journal of Tuberculosis and Lung disease in 2008. Int J Tuberc Lung Dis. 2009;13(6):691-7.
3. Steingart KR, Ng V, Henry M. Sputum processing methods to improve the sensitivity of smear microscopy for tuberculosis: a systematic review. Lancet Infect Dis. 2006;6(10):664-74.
4. Endo S, Trono M, Fujiki A, Macalalad N. Operational conditions influencing the proficiency of AFB microscopy services in The Philippines. Int J Tuberc Lung Dis. 2007;11(3):293-9.
5. The Global Plan to stop TB 20112015: transforming the fight towards elimination of tuberculosis. Geneva: WHO; 2010. p. 557.
6. González E, Armas L, Llanes MJ. Progress towards tuberculosis elimination in Cuba. Int J Tuberc Lung Dis. 2007;11(4):405-11.
7. Marrero A, Carreras L, Valdivia JA, Montoro E, González E, Torres R, et al. Programa Nacional de Control de la Tuberculosis. Manual de Normas y Procedimientos. La Habana: Ed. Ciencias Médicas; 1999.
8. Ministerio de salud Pública. Red Nacional de Laboratorios de Tuberculosis. Microscopia. Normas Técnicas [Internet]. Santa Fé, Argentina: MS/RNLT; 2000 [citado: 15 agosto 2011]. Disponible en: http://es.scribd.com/doc/6542413/Manual-de-Baciloscopia
9. Zerbini EV, Darnaud RMH, Prieto VG. Programa Nacional de Control de la Tuberculosis: Normas Técnicas; 2008. Santa Fe; Argentina: Instituto Nacional de Enfermedades Respiratorias "Dr. Emilio Coni. Anlis - Dr. Carlos G. Malbrán"; 2008.
10. Urbanczik R. Laboratory test focusing on sputum. Int J Tuberc Lung Dis. 2010;14(9):1087-93.
11. Martínez Romero MR, García León G, Sardiña Aragón M, Díaz Almaguer M, Columbié V, Pequero R, et al. Evaluación de nuevos métodos para el control de calidad de la baciloscopia de tuberculosis en Cuba. Rev Inst Nac Enf Resp Mex. 2008;21(2):99-106.
12. Martínez Romero MR, Sardiña Aragón M, García León G, Díaz Almaguer M, Llanes Cordero MJ, Montoro Cardoso E. Evaluación del control de calidad de la baciloscopia en el diagnóstico de la tuberculosis en Cuba. Rev Cubana Med Trop [Internet]. 2006 [citado: 15 agosto 2011];58(3). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0375-07602006000300004&lng=es
13. Martínez Romero MR, García G, Montoro Cardoso E. Evaluación de los indicadores de calidad de la baciloscopia de tuberculosis en los laboratorios provinciales de diagnóstico de Cuba. AVFT. 2008;27(2):110-3.
14. Aziz MA, Ba F, Becx-Bleumink M, Britzel G, Humes R, Lademarco MF, et al. External Quality Assessment for AFB smears Microscopy. Washintong, DC: Microscopy Association of Public Health Laboratories; 2002.
15. Kusnierz GF, Latini OA, Sequeira MO. Quality assessment of smears microscopy for acid fast bacilli in the Argentine tuberculosis laboratory network, 1983 2001. Int J Tuberc Lung Dis. 2004;8(10):1234-41.
16. Sarin R, Neeta S, Mukerjee S, Sharma PP. RNTCP: Quality control of sputum microscopy at sub district level. Indian J Tuberc Lung Dis. 2002;49(3):143-5.
17. De Kantor IN, Laszlo A, Vazquez L, Reneiros A, Latini O, Urbanczin R. Correspondence. More on periphery to central quality control of sputum smear microscopy and rapid fading of Zielh Neelsen staining. Int J Tuberc Lung Dis 2001;5(4):386-9.
18. Buzingo T, Sanders M, Masabo JP, Nyandwi S; Van Deun A. Systematic restaining of sputum smears for quality control is useful in Burundi. Int J Tuberc Lung Dis. 2003;7(5):439-44.
19. Van Deun A, Ronda FA, Chambugonj N, Hye A, Hossain A. Reproducibility of sputum smear examination for acid fast bacilli: practical problems met during cross checking. Int J Tuberc Lung Dis. 1999;3(9):823-9.
Recibido:8 de diciembre de 2010.
Aprobado: 12 de febrero de 2011.
Dra. María Rosarys Martínez Romero. Laboratorio Nacional de Referencia e Investigaciones en Tuberculosis y Micobacterias. Centro Colaborador OPS/OMS. Instituto de Medicina Tropical "Pedro Kourí" (IPK). La Habana, Cuba. Correo electrónico: rosarys@ipk.sld.cu