Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Fitosanidad
versión impresa ISSN 1562-3009
Fitosanidad v.15 n.1 Ciudad de la Habana ene.-mar. 2011
Control biológico
Identificación y caracterización de seis aislados pertenecientes al género Bacillus promisorios para el control de Rhizoctonia solani Künh y Sclerotium rolfsii Sacc.
Identification and Characterization of Six Isolates from Genera Bacillus with Antagonistic Capacity against Rhizoctonia solani Künh and Sclerotium rolfsii Sacc. Control
Acenet I. Sosa López,1 Victoria Pazos Álvarez-Rivera,2 Dania Torres Campos2 y Luis Casadesús Romero2
1Instituto de Investigaciones de Sanidad Vegetal. Calle 110 no. 514 e/ 5.a B y 5.a F, Playa, La Habana, C.P. 11600, asosa@inisav.cu.
2Facultad de Biología, Universidad de La Habana. Calle 25 no. 455 e/ J e I, La Habana, C.P. 10400.
RESUMEN
En la actualidad la identificación de los microorganismos se realiza por varios métodos. Existen métodos clásicos que utilizan como criterios de diferenciación los caracteres fenotípicos morfológicos y fisiológicos. Los kits miniaturizados, como los API 50CHB para Bacillusayudan a caracterizar la fisiología de las bacterias pertenecientes a este grupo, de manera fácil y rápida; además, resultan muy útiles para la identificación hasta el nivel de especie por su elevada precisión. La observación de la morfología y esporulación, la respuesta a la tinción de Gram y algunas pruebas bioquímicas permiten, en el caso de Bacillus spp., ubicarlos dentro de su género. El objetivo de esta investigación fue caracterizar morfológica, bioquímica y fisiológicamente seis aislados de suelo y rizosfera pertenecientes al género Bacillus con capacidad antagónica frente a Rhizoctonia solani y Sclerotium rolfsii (Sr.), con la utilización del API 50 CHB.Tres de los aislados resultaron pertenecer a la especie de Bacillus subtilisy otro a B. megateriumcon más del 95% de confiabilidad, además un aislado de B. licheniformis y otro de B. circulans, ambos con el 82,7%.
Palabras claves: Bacillus, identificación, antagonismo, Rhizoctonia solani, Sclerotium rolfsii.
ABSTRACT
Microorganism identification is realized by several methods, currently. Classical methods utilize phenotypic, morphologic and physiological characters as differentiation criteria. Commercial miniaturized kits as API 50CHB for Bacillus, helps to characterize physiology of this kind of bacteria in an easy and fast way; furthermore they are useful for identification until species level due to their high precision. Observation of morphology and sporulation, the answer to Gram tinction and some biochemical tests permit, in the case of Bacillus spp., put them within they genera. The objective of this investigation was to characterize morphologic, biochemical and physiologically six isolated of genera Bacillusfrom soil and rhizosphere with antagonistic capability in front of Rhizoctonia solani and Sclerotium rolfsii(Sr.), with the utilization of the API 50 CHB. Three of the isolated proved to belong to species Bacillus subtilis and another one to B. megaterium with over than 95% of reliability, also one isolated of B. licheniformis and another one of B. circulans, both with 82.7%.
Key words: Bacillus, identification, antagonism, Rhizoctonia solani, Sclerotium rolfsii.
INTRODUCCIÓN
Una nueva etapa para la taxonomía bacteriana tuvo lugar en 1980, cuando varios expertos de todo el mundo se reunieron para confeccionar la Lista de Nombres Bacterianos Aprobados [Skerman et al., 1980], donde se concibieron 38 especies de bacterias aerobias formadoras de endosporas, de las cuales 31 fueron agrupadas dentro del género Bacillus y siete dentro de otros géneros de bacterias formadoras de endosporas. Esta clasificación no se ha mantenido. La introducción de nuevas técnicas moleculares como los análisis de secuenciasha contribuido a la separación de especies del género y la creación de nuevos taxas donde ubicarlos, siendo la comparación de secuencias del gen que codifica para la subunidad 16S la base de la sistemática moderna [Stackebryt y Swidersky, 2002].
En la actualidad la identificación de los microorganismos se realiza por varios métodos. Existen métodos clásicos que utilizan como criterios de diferenciación caracteres fenotípicos como los morfológicos y fisiológicos que se describen en el Manual de Clasificación de Bergey [Claus y Berkeley, 1986].
En el caso de los Bacillus spp., la observación del fenotipo permite ubicarlo dentro del género Bacillus, pero muchas veces no resulta suficiente para una completa identificación. Por esa razón muchos investigadores acuden a técnicas más sofisticadas, como los ensayos moleculares basados en el análisis del genotipo de los microorganismos. La determinación de la composición de bases del ácido desoxirribonucleico (ADN), el estudio de la hibridación de ácidos nucleicos y la secuenciación de ácidos nucleicos son tipos de análisis que se pueden realizar sobre ácidos nucleicos aislados y que proporcionan información acerca del genotipo [Reinoso et al., 2006; Fritze, 2004].
Los kits de API 50CHB para Bacillus, introducidos en el mercado mundial en los últimos tiempos, se utilizan mucho porque ayudan a caracterizar la fisiología de estos microorganismos de una manera fácil y rápida, además de permitir caracterizar el catabolismo de los aislados, y en la mayoría de los casos la identificación hasta especie con precisiones del orden del 76-97% [Entis et al., 2001].
El objetivo de esta investigación fue caracterizar morfológica, bioquímica y fisiológicamente los aislados de suelo y rizosfera B-4, B-10, B-14, B-15, B-21 y B-42 pertenecientes al género Bacillus con capacidad antagónica frente a Rhizoctonia solani (Rs-10) y Sclerotium rolfsii (Sr.).
MATERIALES Y MÉTODOS
Se empleó la cepa de Bacillus licheniformis (Weigmann) Chester (RI-75) perteneciente al Centro de Estudios Aplicados al Desarrollo de la Energía Nuclear (CEADEN) como cepa de referencia, y los aislados de suelos y rizosfera B-4, B-10, B-14, B-15, B-21 y B-42 del género Bacillus y con capacidad antagónica frente a Rhizoctonia solani (Rs-10) y Sclerotium rolfsii (Sr).
Los seis aislados se caracterizaron morfológica y fisiológicamente según las pruebas descritas en el Manual de Clasificación de Bergey [Claus y Berkeley, 1986]. La identificación se complementó por medio de la utilización del sistema API 50 CHB para el género Bacillus. Para la identificación de Bacillus spp. se emplearon cultivos bacterianos de 18 h y se realizaron las siguientes pruebas bioquímicas (con dos réplicas en cada caso):
Tinción de Gram. Producción de la enzima catalasa. Posición de la espora (terminal, central o subterminal). Medio I (producción de ácido a partir de glucosa). Medio II (producción de gas a partir de glucosa). Medio III (producción de acetoína a partir de glucosa) (Voges-Proskauer). Hidrólisis de la gelatina. Hidrólisis del almidón. Utilización de citrato. Crecimiento en agar anaerobio. Crecimiento en NaCl al 7%. Reducción de nitratos a nitritos. Prueba de la lecitinasa. Crecimiento a 45°C y finalmente crecimiento a 55°C.
Se empleó el sistema de API 50 CHB concebido para caracterizar el metabolismo de los carbohidratos de Bacillus. La identificación de los aislados se realizó mediante la utilización de la base de datos APILAB, empleada en estos ensayos.
RESULTADOS Y DISCUSIÓN
Identificación de los aislamientos
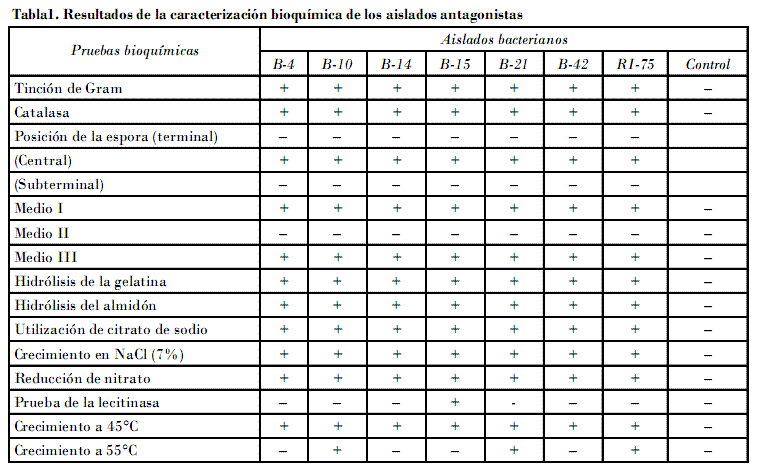
De acuerdo con las pruebas bioquímicas realizadas, los aislamientos de Bacillus B-4, B-10, B-14, B-15, B-21 y B-42 presentaron tinción de Gram positiva, endospora de posición central y forma elipsoidal, crecimiento anaerobio facultativo, utilización de citratos, hidrólisis del almidón positiva, Voges Proskauer positivo, crecimiento en NaCl al 7% y a 45°C (Tabla 1).
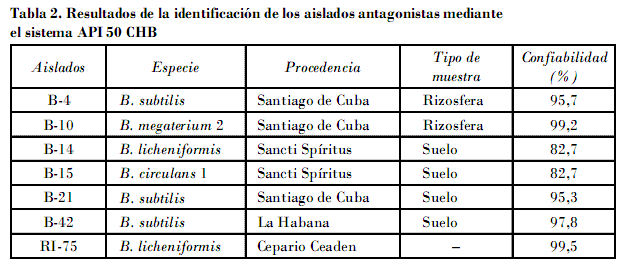
Los análisis de perfil bioquímico aportados por la base de datos APILAB del test API 50 CHB para Bacillus permitieron identificar, de una manera rápida y sencilla, los aislados seleccionados hasta especie. Tres de los aislados (B-4, B-21 y B-42) fueron identificados como Bacillus subtilis Cohn, y los aislados B-10, B-14 y B-15 como B. megaterium 2 de Bary, B. licheniformis Weigmann y B. circulans 1 Jordan, respectivamente (Tabla 2).
Guinebretiere et al. (2001) realizaron un estudio en el que identificaron 119 aislados de Bacillus mediante el sistema API 50 CHB/20 E y técnicas moleculares, basadas en la amplificación y secuenciación de su material genético, lo que les permitió comparar los resultados en ambos casos. Estos autores concluyeron que para el caso de las especies pertenecientes al grupo B. subtilis el grado de discriminación entre B. subtilis, B. licheniformis y B. amyloquefaciens puede ser bajo si se usa el sistema API 50 CHB/20 E. De igual forma, cepas pertenecientes al género Paenibacillus fueron identificadas como B. circulans grupo 2, y otras pertenecientes a este ultimo taxón se ubicaron dentro del grupo 1.
Al analizar los aislados identificados como B. subtilis se observó que crecieron en condiciones de anaerobiosis, lo cual puede deberse a que los miembros de esta especie pueden crecer en medios que contengan nitrato [Garrity et al., 2003; Todar, 2005; Calvo y Zúñiga, 2010], y en este caso el medio para la realización de esa prueba fue agar nutriente, el cual contiene peptona bacteriológica.
En el aislado B-21, identificado también como B. subtilis, se detectó crecimiento a 55°C. Esto puede ser un dato importante al seleccionar las cepas más promisorias, ya que parece ser que es una variedad diferente dentro de las especies determinadas como B. subtilis que no crecieron a esta temperatura. Claus y Berkeley (1986) plantean que la capacidad de crecimiento a 50°C es variable entre cepas de la misma especie; los rangos de temperatura de crecimiento altos son muy sensibles, tanto que a una variación de un grado puede influenciar en el crecimiento vegetativo de la bacteria. El hecho de que esta cepa haya crecido a este valor de temperatura puede ser consecuencia de la selección natural y además de la presencia de endosporas, que le han permitido a este género bacteriano una mejor adaptación a las condiciones adversas del medioambiente, tales como temperatura, pH, calor, humedad, desecación, radiaciones y sustancias químicas, condiciones a las que están expuestos con frecuencia estos microorganismos [Sosa et al., 2006]. Esta ventaja adaptativa puede estar relacionada además con las altas temperaturas que comúnmente se registran en la región oriental del país, específicamente en la provincia de Santiago de Cuba, de donde proviene esa cepa.
B. subtilis es la especie tipo del género Bacillus, y sus esporas están ampliamente distribuidas en ambientes naturales. Puede degradar pectina y polisacáridos en los tejidos vegetales. Produce una gran gama de antibióticos pertenecientes a la familia de las Iturinas [Wulff et al., 2002]. Se ha reportado como un eficiente antagonista de fitopátogenos. Esta especie se encuentra entre los microorganismos promotores del crecimiento vegetal debido a que produce sustancias semejantes a las fitohormonas, y además contribuye al mejoramiento de la absorción de agua y nutrientes en la raíz. Se le atribuye también la inducción de resistencia mediante la activación de genes defensivos de la planta [Guillén et al., 2006].
El aislado B-14, identificado como B. licheniformis, presentó resultados similares a los de la cepa RI-75, utilizada como cepa patrón, excepto que la primera no creció a 55°C; pero de acuerdo con lo planteado por el Manual de bacteriología y sistemática [Claus y Berkeley, 1986], en el caso en que los resultados sean positivos, debe tenerse en cuenta que más del 90% de las cepas son positivas y da margen a un porcentaje de variación, lo cual se corrobora al complementar la pruebas bioquímicas efectuadas y el API 50CH/B, con una confiabilidad del 82,7%. B. licheniformis produce el antibiótico bacitracina de acción frente a bacterias Gram + y de gran uso en el campo de la medicina a escala industrial con fines clínicos [Todar, 2005]; sin embargo, no se encontraron reportes de los posibles efectos antifúngicos de esta sustancia. Se utiliza además como productor de proteasas y amilasas. Esta especie fue reportada por Lee et al. (2006) como biofungicida contra el moho gris del tomate causado por Botrytis cinerea. Se encuentra clasificada dentro del grupo ecofisiológico de las bacterias desnitrificantes, por lo que muchas veces su presencia en los cultivos causa pérdidas económicas, pues volatiliza (NH3, N2O y N2) el nitrato propio del suelo, o adicionado por medio de los fertilizantes puede o no producir pigmentos rojos [Todar, 2005]. Es por ello que se recomienda la caracterización genotípica de estos aislados.
El aislado B-15, identificado como B. circulans 1, es una de las especies de Bacillus productoras de antibióticos, entre los que se encuentra la circulina, y algunas cepas presentan actividad celulolítica. Se haaislado de infecciones humanas, por lo que se recomienda probar su patogenicidad frente a animales antes de considerarlo como posible biocontrolador [Todar, 2005]. A pesar de que el 90% o más de las especies responden de forma negativa a la prueba de la lecitinasa según Claus y Berkeley (1986), esta cepa respondió positivamente, lo que demuestra que es un biovar diferente. Esta prueba mide la capacidad de producir la enzima que degrada la lecitina presente en la yema de huevo. Las cuatro especies principales de lecitinasa positiva son Bacillus anthracis, Bacillus mycoides, Bacillus cereus y Bacillus thuringiensis Berliner. Las tres primeras especies se caracterizan por ser patógenas humanas, lo cual es importante al seleccionar una cepa con fines de aplicación, ya que se puede correr el riesgo de que sean patogénicas [Claus y Berkeley, 1986; Calvo y Zúñiga, 2010].
El aislado B-10, identificado como B. megaterium 2, presenta esporas de gran tamaño y se ubica dentro de las especies psicrófilas del género. Puede causar perjuicio a animales y humanos. Sus esporas son frecuentes en el suelo [Todar, 2005].
CONCLUSIONES
• Los aislados B-4, B-21 y B-42 fueron identificados y caracterizados bioquímica y fisiológicamente como Bacillus subtilis, y ahora se nombran Bs-4, Bs-21 y Bs-42; el aislado B-10 como B. megaterium 2 (Bm-10); el aislado 14 como B. licheniformis (Bl-14) y el 15 como B. circulans 1 (Bc-15), todos con un porcentaje de confiabilidad superior al 80%.
REFERENCIAS
Calvo, P.; D. Zúñiga: «Caracterización fisiológica de cepas de Bacillus spp., aisladas de la rizosfera de papa (Solanum tuberosum)», Departamento Académico de Biología, Universidad Nacional Agraria La Molina, Lima, Perú, Ecología Aplicada 9(1):31-39, 2010,
http://redalyc.uaemex.mx/src/inicio/ArtPdfRed.jsp?iCve=34115156004 (consultado en enero de 2010).
Claus, D.; R. C. Berkeley: «Genus Bacillus Cohn 1872», Bergey's Manual of Systematic Bacteriology, Williams y Wilkins Edit., Baltimore, EE. UU., 1986, pp. 1105-1139.
Entis, P.; D. Y. Fung; M. W. Griffiths; L. McIntre; S. Russell; A. N. Sharpe; M. L. Tortorello: «Rapid Methods for Detection, Identification and Enumeration», Compendium of Methods for the Microbial Examination of Foods, 4.ª ed., Ed. American Public Health Association, Washington, 2001, pp. 89-126.
Fritze, D.: «Taxonomy of the Genus Bacillus and Related Genera: The Aerobic Endospore Forming Bacteria», Phytopathology, vol. 94, 2004, pp. 1245-1248.
Garrity, G. M.; J. A. Bell; T. G. Lilburn: «Taxonomic Outline of the Prokaryotes», Bergey's Manual of Systematic Bacteriology, Springer- Verlag, Nueva York, 2003, http://dx.doi.org/10.1007/bergeysoutline.
Guillén, R.; F. Hernández; G. Gallegos; R. Rodríguez; C. Aguilar; E. Padrón; M. Reyes: «Bacillus spp. como biocontrol en un suelo infestado con Fusarium spp., Rhizoctonia solani Kûhn y Phytophthora capsici Leonian y su efecto en el desarrollo y rendimiento del cultivo de Chile», Revista Mexicana de Fitopatología 24(2):105-114, México, 2006, http://redalyc.uaemex.mx/redalyc/pdf/612/61224204.pdf
Guinebretiere, M. E.; O. Berge; P. Normand; C. Morris; F. Carlin; C. Nguyen-The: «Identification of Bacteria in Pasteurized Zucchini Purees Stored at Different Temperatures and Comparison with Those Found in Other Pasteurized Vegetable Purées», Appl. Enviromental Microbiology 67(10):4520-4530, EE. UU., 2001.
Lee, J. P.; S. W. Lee; C. Kim; J. H. Son; J. H. Song; K. Y. Lee; H. J. Kim; S. J. Jung; B. J. Moon: «Evaluation of Formulations of Bacillus licheniformis for the Biological Control of Tomato Gray Mold Caused by Botrytis cinerea», Biological Control 37(3):329-337, Holanda, 2006.
Reinoso, Y.; V. Pazos; L. Casadesús: «Aislamiento, selección e identificación de bacterias de los géneros Bacillus, Brevibacillus y Paenibacillus con potencialidades para el control biológico de bacterias y hongos fitopatógenos del cultivo de la papa», tesis de Maestría en Microbiología General, Universidad de La Habana, 2006.
Skerman, V. B. D.; V. McGowan; P. H. A. Sneath: Approved Lists of Bacterial Names, American Society for Microbiology, Washington, 1980.
Sosa, A.; V. Pazos; M. González: «Nuevos aislados de Bacillus spp. antagonistas a Sclerotium rolfsii, Rhizoctonia solani y Pythium aphanidermatum», Fitosanidad 10(1):73-74, La Habana, 2006.
Stackebryt, E.; J. Swidersky: From phylogeny to systematics. Applications and Systematics of Bacillus and Relatives, Blackwell Publishing, Oxford, 2002, pp. 8-22.
Todar, K.: «Todar's Online Textbook of Bacteriology», University of Wisconsin-Madison Departament of Bacteriology, EE. UU., 2005, http://www.textbookofbacteriology.net/.
Wulff, E.; C. Mguni; K. Mansfeld-Giese; J. Fels; M. Lübeck; H. Hockenhull: «Biochemical and Molecular Characterization of Bacillus amyloliquefaciens, B. subtilis and B. pumilis Isolates with Distinct Antagonistic Potencial Against Xanthomonas campestris pv. Campestris», European Journal of Plant Pathology 51:574-584, Holanda, 2002.
Recibido: 28/1/11
Aceptado: 24/2/11