Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Médica Electrónica
versión On-line ISSN 1684-1824
Rev. Med. Electrón. vol.35 no.5 Matanzas sep.-oct. 2013
PRESENTACIÓN DE CASO
Seudotumor pulmonar inflamatorio. Presentación de caso
Inflammatory pulmonary pseudo tumor. Presentation of a case
Dr. Eloy Calcines Sánchez, Dra. Dulvis Primelles Cruz, Dra. Isis Sotelo Suarez, Dr. Ernesto Lima Guerra, Dr. Jorge Molina Pérez, Dra. Ana Gloria Montenegro Bello
Hospital Provincial Clínico Quirúrgico Docente José R. López Tabrane. Matanzas, Cuba.
RESUMEN
El seudotumor inflamatorio es un proceso no neoplásico poco frecuente, caracterizado por un crecimiento irregular de células inflamatorias. Puede originarse en cualquier lugar del organismo y, en la mayoría de los casos, presenta un asentamiento local único y de características benignas. Se presentó el caso de un varón de 51 años, en el que se manifestó el seudotumor inflamatorio de forma nodular en el pulmón derecho, con evolución a un empiema pleural.
Palabras clave: seudomotor inflamatorio, empiema pleural, pulmón.
ABSTRACT
The inflammatory pseudo tumor is a few frequent non neoplastic process, characterized by an irregular increase of inflammatory cells. It can be originated in any place of the organism, and in most of the cases it has only one local settlement with benign characteristics. We presented the case of a male patient, aged 51 years who had the inflammatory pseudo tumor of nodular form in the right lung, with evolution to a pleural empyema.
Key words: inflammatory pseudo tumor, pleural empyema, lung.
INTRODUCCIÓN
El seudotumor inflamatorio fue descrito por primera vez por Brunn en 1939, y también se le ha denominado histiocitoma, granuloma de células plasmáticas, xantoma, etc. Se asienta con mayor frecuencia en el pulmón, y el diagnóstico se basa en el estudio anatomopatológico. Histológicamente, se describe como un tumor de características benignas, que en escasas ocasiones infiltra estructuras vecinas o presenta desarrollo multifocal.(1,2) Está considerado como un proceso no neoplásico constituido por la proliferación de células irregulares plasmáticas maduras, acompañadas o no de linfocitos, distribuidas en el seno de un tejido fibroso estromal.(1,2)
Los tumores seudoinflamatorios son una rara entidad que en ocasiones afecta, al parénquima pulmonar. Su diagnóstico clínico es variado, siendo un hallazgo casual en casi la mitad de los casos. Entraña una difícil decisión en cuanto a la mejor opción terapéutica, ya que el diagnóstico de certeza se establece tras el estudio de la pieza quirúrgica. Es una patología relativamente poco frecuente de etiología incierta, generalmente considerada de origen reactivo. Puede observarse en diferentes localizaciones como masas únicas o múltiples. La intrapulmonar es una de sus posibles formas de presentación. A pesar de su baja frecuencia, esta patología debe tenerse en cuenta a la hora de realizar el diagnóstico diferencial de nódulos pulmonares. De otro modo, los resultados histológicos y de las pruebas de imagen pueden llegar a ser confusos. Además, presenta una baja malignidad con buena respuesta al tratamiento quirúrgico y en menor medida al farmacológico.(3,5)
Algunos autores postulan que el seudotumor inflamatorio es un proceso no neoplásico, resultado de la proliferación descontrolada de células inflamatorias. La causa de esta desregulación es desconocida, pero ciertas publicaciones concluyen que se trata de una respuesta inmunitaria secundaria a infección, traumatismo o cirugía previa. De hecho, hay antecedentes recientes de neumonía o infección del aparato respiratorio inferior en aproximadamente un 20-30 % de los pacientes; asociación que encontramos en nuestro caso.(6,7)
Se considera que las neumonías micoplásmicas constituyen alrededor del 20% de todos los casos en la población general. La incidencia y las características clínicas de la neumonía atípica por Micoplasma pneumoniae en atención primaria son poco conocidas —tanto en niños como adultos—, ya que la mayoría de los estudios son revisiones de los pacientes con neumonías que requieren hospitalización, donde el principal microorganismo es el neumococo.(9,10)
Esta neumonía no presenta ningún síntoma, signo o patrón radiológico que enfoque claramente la etiología, cuya confirmación exige la realización de pruebas serológicas específicas. Sin embargo, por su frecuencia, debe ser el primer diagnóstico de sospecha del síndrome neumónico en la edad escolar y adolescencia que no tenga otros datos que apoyen etiologías distintas. Se precisan más estudios en neumonías extrahospitalarias que evalúen correctamente la incidencia de M. pneumoniae, así como la eficacia real de los macrólidos en la evolución de la enfermedad.(10,11)
El agente etiológico de la neumonía por micoplasmas es M. pneumoniae, estableciéndose usualmente en orofaringe, bronquios y otras partes del tracto respiratorio superior durante la infección aguda. El microorganismo también ha sido aislado a partir de pulmón y fluido pleural durante una enfermedad respiratoria aguda, y del fluido bronquioalveolar de pacientes inmunodeprimidos con neumonía, incluyendo aquellos con síndrome de la inmunodeficiencia adquirida. M. pneumoniae se cultiva frecuentemente a partir de muestras de garganta en pacientes convalecientes durante las ocho semanas siguientes a su recuperación clínica. La localización extrapulmonar del microorganismo frecuentemente involucra la diseminación al tejido sinovial posterior a una infección respiratoria o asociado a una artritis séptica con hipogamaglobulinemia.(12)
Se presenta un caso ingresado por esta patología en el Hospital Provincial Clínico Quirúrgico Docente José Ramón López Tabrane. El paciente comenzó con un cuadro respiratorio inespecífico y nódulo pulmonar en pruebas de imagen, sospechoso de proceso neoplásico. Tras su estudio exhaustivo se llegó al diagnóstico de seudotumor inflamatorio pulmonar asociado a micoplasma pneumoniae, con excelente respuesta al tratamiento usado en el caso.
PRESENTACIÓN DEL CASO
Varón de 62 años de edad, albañil de profesión, con antecedentes de tabaquismo (40 paquetes/año), quien ingresó en el hospital por tos frecuente, dolor toráxico y fiebre, además de decaimiento. La exploración física en el momento de su ingreso evidenciaba palidez mucocutánea, y en la auscultación pulmonar había disminución del murmullo vesicular en hemitorax derecho.
El hemograma mostraba: leucocitos 12,3 x 109l (neutrófilos 84,8 %, linfocitos 8,2 %, monocitos 1,7 %, eosinófilos 1 %, basófilos 1,3 %), hemoglobina 11g/dl, hematocrito 34,1 %, VCM 76,2 fl, CHCM 22,6 g/dl y plaquetas 312,000/mm3.
La coagulación era normal. Glicemia: 4,6mmol/l, creatinina 98 mmol/, TGO 12U/I, TGP 22U/L, GGT54U/L.
En la gasometría arterial basal (GAB) se objetivaba: pH 7,39, PaCO2 32,9 mmHg, PaO2 70,5 mmHg y bicarbonato 21 mmol/l.
La radiografía de tórax demostraba imagen tumoral en 1/3 medio del pulmón derecho. (Fig. 1)
Ante estos hallazgos, se comienza tratamiento antibiótico y se indica tomografía axial computarizada de pulmón (fig. 2), que demostró la existencia de una masa en la región inferior derecha del corte imagenológico, de aproximadamente 7 x 5 cm, con áreas de menor densidad en su interior y con bordes mal definidos. Adicionalmente, se objetivaron pequeñas adenopatías (< 1 cm) en la ventana aortopulmonar. Se realiza también una fibrobroncoscopia para confirmación de diagnóstico. En dicha exploración no se apreciaron lesiones endobronquiales, puntos sangrantes ni restos hemáticos. Se encontraron secreciones purulentas en los bronquios del lóbulo inferior derecho, y se obtuvieron muestras en esa zona mediante catéter telescopado y aspirado bronquial. Las tinciones y los cultivos de las mismas fueron negativas. En la citología del aspirado bronquial se observaron histiocitos cargados de pigmento antracótico, células bronquiales y abundantes polimorfonucleares, signos sugestivos de inflamación aguda, y no se evidenciaron células atípicas.
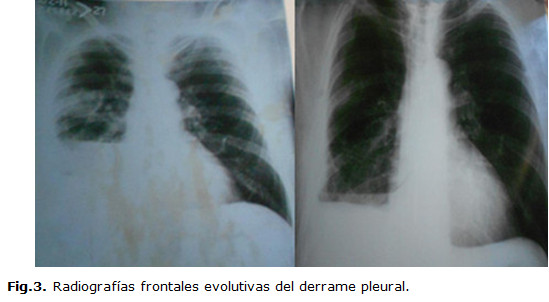
Durante su evolución, el paciente refirió dolor pleurítico nocturno con cambios de las características de la tumoración y aparición de derrame pleural derecho comprobado radiológicamente (fig. 3), lo cual requiere punción evacuadora por signos de insuficiencia respiratoria en el paciente. Discutiendo la posibilidad de una neoplasia de pulmón abscedada o absceso de pulmón, aunque radiológicamente no impresionaba dicho diagnóstico. Por otra parte, se le practicaron al enfermo pruebas de función respiratoria, que mostraron: FVC 3,97 l (89 %), FEV1 3,25 l (86 %), FEV1/FVC 100 % y MEF25-75 2,65 l (68 %).
Ante la sospecha de un posible tumor pulmonar, el enfermo fue sometido a una toracovideoendoscopia. La superficie pleural, violácea, aparecía engrosada. El parénquima pulmonar se mostraba condensado, y al corte presentaba una lesión mal delimitada, cavitada, de aspecto necrótico, con engrosamiento fibroso de su margen, que afectaba a los segmentos basales. También se observaba una marcada fibrosis con depósito de colágeno en las zonas adyacentes a la inflamación, particularmente en relación con septos vasculares y en la zona subpleural. Asimismo, se identificaba una proliferación vascular marcada relacionada con las zonas inflamatorias. No se observaron formaciones granulomatosas, ni datos de tumor. Posteriormente, se realizó una punción-aspiración con aguja fina pulmonar percutánea, y se obtuvo material que fue enviado para estudio anatomopatológico al Instituto de Medicina Tropical Pedro Kourí. Microscópicamente se apreciaron abundantes histiocitos, algunos con pigmento antracótico, entremezclados con células bronquiales y células inflamatorias, aislándose un M. pneumoniae.
Un año después de la intervención, el paciente se encuentra asintomático desde el punto de vista respiratorio. La radiografía de tórax de ese momento muestra cambios postquirúrgicos en el hemitórax derecho, sin otros hallazgos de interés.
DISCUSIÓN
La etiopatogenia del seudotumor inflamatorio es una incógnita, y existen diversas hipótesis que proponen un origen autoinmunitario o infeccioso como causa desencadenante. Su verdadera prevalencia es desconocida, y puede originarse en cualquier órgano o tejido, aunque la localización pulmonar es la más frecuente; la clínica varía en función del lugar de origen, aunque en la mayoría de las ocasiones no presenta síntomas.(1-4)
El pseudotumor inflamatorio supone una causa excepcional de lesión pulmonar benigna con aspecto de nódulo o masa en los estudios de imagen. Por su capacidad para mimetizar el carcinoma broncogénico tanto en sus manifestaciones clínicas como radiológicas debe incluirse en el diagnóstico diferencial de toda masa pulmonar, especialmente cuando los estudios microbiológicos y de anatomía patológica resultan negativos.(5,6) Aunque de naturaleza benigna, puede ser localmente invasivo, recurrente o multifocal, siendo el pulmón el órgano más frecuentemente afectado. Su diagnóstico es difícil, precisándose biopsia quirúrgica en todos los pacientes.(7)
La importancia de la determinación de la etiología de un cuadro de neumonía y, sobre todo, en casos de presentación no habitual como la pseudotumoral, se deriva de la variedad de agentes causales que pudieran estar implicados en cuadros de neumonía extra-hospitalaria, y de la notable diferencia en cuanto a su frecuencia de aparición y sus patrones de sensibilidad a antibacterianos. La aplicación de tratamiento empírico puede llevar a una falla terapéutica y coloca en riesgo la vida del paciente, además de realizar una mayor presión selectiva sobre los microorganismos resistentes, favoreciendo su multiplicación, e incrementando el riesgo de surgimiento de cepas resistentes.(8)
El papel de los micoplasmas como agentes patógenos ha sido estudiado especialmente en el aparato respiratorio, siendo la causa de aproximadamente el 20 % de las neumonías adquiridas en la comunidad en la población general, y más del 50 % de las neumonías en personas en hacinamiento. En los adultos se pueden producir casos de bronquitis y neumonía. El diagnóstico de una infección respiratoria causada por M. pneumoniae basado únicamente en la clínica del paciente es difícil, porque muchos procesos neumónicos pueden presentarse en una forma similar, en particular los causados por virus. Es por esto que se hace necesario realizar una identificación certera del agente causal que permita confirmar el diagnóstico clínico y ofrecer un tratamiento específico; además de conocer su importancia relativa entre las neumonías atípicas y su impacto epidemiológico. Es muy importante destacar que M. pneumoniae puede persistir en el tracto respiratorio por varios meses luego de la infección inicial y algunas veces por años en pacientes hipogammaglobulinémicos a pesar de un tratamiento adecuado.(9,10)
Desde el punto de vista radiológico, este tipo de tumores suele presentarse como una lesión bien delimitada. En el caso del M. pneumoniae se trataría de un patrón intersticial retículo-nodular parcheado (unilateral o bilateral), y el adenovirus presentaría hiperinsuflacion pulmonar, engrosamiento de la pared bronquial, bronconeumonía difusa y colapso lobar. Sin embargo, en la actualidad existe evidencia que sostiene que estas infecciones pueden adoptar cualquier patrón radiológico Solo en el 14 % de los casos existe confirmación diagnóstica mediante la histología (con el material obtenido mediante fibrobroncoscopia, PAAF o previa a la cirugía, y en la mayoría de las ocasiones es necesario el estudio anatomopatológico de la pieza quirúrgica y diagnostico microbiológico.(11,12)
El tratamiento de elección es la escisión radical completa con márgenes adecuados, en los pocos casos en que se produzca recurrencia, volver a resecar sigue siendo el tratamiento. El pronóstico es excelente cuando se lleva a cabo la exéresis completa del tumor, ya que es raro que infiltre estructuras vecinas o haya metástasis. El comportamiento más agresivo en estos tumores parece estar en relación con ciertas características anatomopatológicas, como un incremento de la celularidad, pleomorfismo nuclear, actividad mitótica, necrosis focal e invasión vascular.(13,14)
En los casos en que no está indicada la intervención quirúrgica, el tratamiento médico y el tratamiento sintomático de las posibles complicaciones parecen constituir la opción más adecuada. En determinados casos, la utilización de corticoides y antibióticos específicos según el germen aislado, se ha acompañado de una buena respuesta, con buenos resultados a corto y medio plazo, como es el caso de nuestro paciente.(15,16)
REFERENCIAS BIBLIOGRÁFICAS
1. Paya Llorens C, Galbis Carvajal JM, Mafé Madueño JJ, Baschwitz Gómez B, Rodríguez Paniagua JM, Alenda González C. Seudotumor inflamatorio pulmonar de localización intraparenquimatosa. Arch Bronconeumol [Internet]. 2003 [citado 12 Abr 2013];39(11):527-30. Disponible en: http://www.archbronconeumol.org/es/seudotumor-inflamatorio-pulmonar-localizacion-intraparenquimatosa/articulo/13053218/
2. Medina Archirica C, Gutiérrez de la Peña C, Gómez Menchero J. Seudotumor inflamatorio multicéntrico. Cir Esp. 2007; 81(83):150-2.
3. Vallee M, Al Rumien L, Rodríguez S, Hernández G, Figueroa L. Pseudotumor inflamatorio de pulmón en preescolar femenina: a propósito de un caso. Rev Venez Oncol [Internet]. 2006 [citado 12 Abr 2013];18(4):242-9. Disponible en: http://www.imbiomed.com.mx/1/1/articulos.php?method=showDetail&id_articulo=41446&id_seccion=1547&id_ejemplar=4242&id_revista=100
4. Rodríguez Conesa A, Castro Rodríguez E. Pseudotumor inflamatorio: una masa poco frecuente pulmonar. An Med Inter [Internet]. 2003 [citado 12 Abr 2013]; 20(1):10-4. Disponible en: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S0212-71992003000100019
5. Vergara Hidalgo M, Hernández Castellón V, Lagomasino Vergara EJ. Tumor seudoinflamatorio del pulmón. Acta Méd Centro [Internet]. 2009 [citado 12 Abr 2013];3(1). Disponible en: http://www.actamedica.sld.cu/r1_09/tumor.htm
6. Saldías F, Díaz O, Dreyse J, Gaggero A, Sandoval C, Lisboa C. Etiología y biomarcadores de inflamación sistémica en las exacerbaciones leves a moderadas de la enfermedad pulmonar obstructiva crónica. Rev Méd Chile [Internet]. 2012 [citado 12 Abr 2013];140(1). Disponible en: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0034-98872012000100002
7. González A, Baudagna G, Cremaschi M, Serrano R, Cabral G, Monteverde A. Características de la neumonía adquirida en la comunidad por neumococo y micoplasma. Rev Am Med Respir. 2010 10(4):154-9.
8. Butt S, Swiatlo E. Treatment of community-acquired pneumonia in an ambulatory setting. Am J Med. 2011 Apr;124(4):297-300. Citado en PubMed; PMID: 21435417.
9. Gómez MGA, Durán GJR, Berny CDA, Salcedo RMI. Neumonía por Mycoplasma pneumoniae: presentación de un caso y breve revisión bibliográfica. Med Int Mex [Internet]. 2012 [citado 12 Abr 2013];28(1). Disponible en: http://new.medigraphic.com/cgi-bin/resumen.cgi?IDREVISTA=83&IDARTICULO=33114&IDPUBLICACION=3574
10. Pérez I, Gómez M, González Rico S. El diagnóstico convencional de Mycoplasma pneumoniae como agente causal de Neumonías Adquiridas en la Comunidad (NAC). Rev Soc Venez Microbiol. 2011;27(2):73-8.
11. Zhai SB, Cao DB, Xu H, Li XX, Yang SR. Multiple organ dysfunction syndrome associated with Mycoplasma pneumoniae infection. Braz J Microbiol [Internet]. 2012 [citado 12 Abr 2013];43(1). Disponible en: http://www.scielo.br/scielo.php?pid=S1517-83822012000100025&script=sci_arttext
12. Tuesta Chow-Quan AD, Bruscas Alijarde MJ, Ruiz Ribó MD, Saiz García F. Neumonía por Mycoplasma pneumoniae y tromboembolia pulmonar. Med Clin (Barc). 2005;124(15):597-8. Citado en PubMed; PMID: 15860180.
13. Grimberg A, Shigueoka DC, Atallah AN, Ajzen S, Iared W. Diagnostic accuracy of sonography for pleural effusion: systematic review. Sao Paulo Med J. 2010; 128(2):90-5. Citado en PubMed; PMID: 20676576.
14. Rahman NM, Singanayagam A, Davies HE, Wrightson JM, Mishra EK, Lee YC, et al. Diagnostic accuracy, safety and utilisation of respiratory physician-delivered thoracic ultrasound. Thorax. 2010 May;65(5):449-53. Citado en PubMed; PMID: 20435870.
15. Maurya V, Gupta UA, Dewan RK, Jain S, Shah A. Resolución espontánea de un seudotumor inflamatorio del pulmón como consecuencia de una biopsia en cuña. Arch Bronconeumol [Internet]. 2013 [citado 12 Abr 2013];49(1):31-4. Disponible en: http://www.archbronconeumol.org/es/resolucion-espontanea-un-seudotumor-inflamatorio/articulo/90181175/
16. Leiva Salinas C, Domingo ML, Flors L. Tumor miofibroblástico inflamatorio pulmonar: un diagnóstico confuso. Arch Bronconeumol [Internet]. 2010 [citado 12 Abr 2013]; 46(2):106-7. Disponible en: http://www.archbronconeumol.org/es/tumor-miofibroblastico-inflamatorio-pulmonar-un/articulo/13146940/
Recibido: 15 de junio de 2013.
Aprobado: 20 de julio de 2013.
Eloy Calcines Sánchez. Hospital Provincial Docente Clínico-Quirúrgico José R. López Tabrane. Santa Rita % Santa Cecilia y San Isidro. Versalles. Matanzas, Cuba. Correo electrónico: eloycalcines.mtz@infomed.sld.cu
CÓMO CITAR ESTE ARTÍCULO
Calcines Sánchez E, Primelles Cruz D, Sotelo Suarez I, Lima Guerra E, Molina Pérez J, Montenegro Bello AG. Seudotumor pulmonar inflamatorio. Presentación de caso. Rev Méd Electrón [Internet]. 2013 Sep-Oct [citado: fecha de acceso];35(5). Disponible en: http://www.revmatanzas.sld.cu/revista%20medica/ano%202013/vol5%202013/tema07.htm