INTRODUCCIÓN
Existen dos tendencias epidemiológicas en el orbe: el envejecimiento y la obesidad. Estos dos factores afectan drásticamente a la composición corporal, la morbilidad y la mortalidad. El envejecimiento se asocia con la disminución de la masa muscular y la fuerza, y el aumento de la masa grasa corporal, lo que conduce a la fragilidad, las caídas, la discapacidad, el aislamiento social y la hospitalización.
La palabra “sarcopenia” proviene del griego y se refiere a la pérdida de masa muscular relacionada con la edad. Aunque el impacto de la sarcopenia ha sido bien demostrado, el efecto de la obesidad sobre ella emerge como un nuevo problema de salud pública.1 Por lo tanto, no es sorprendente que la obesidad se asocie con más de doscientas complicaciones médicas y con un mayor riesgo de morbilidad y mortalidad, representando la quinta causa de muerte en todo el mundo.
Asimismo, la sarcopenia, es muy común entre los adultos mayores con obesidad, lo que se conoce como obesidad sarcopénica (OS), y está estrechamente asociada con la fragilidad, una condición de deterioro de la reserva homeostática y la tolerancia al estrés, lo que resulta en una mayor vulnerabilidad para la salud. Por lo tanto, la OS está fuertemente relacionada no solo con disfunciones cardiometabólicas, sino también con discapacidad física.2
Con el envejecimiento, la pérdida de masa muscular y fuerza se produce de forma natural, y se define como sarcopenia primaria. Por su parte, la sarcopenia secundaria puede desarrollarse debido a la inactividad física, la desnutrición y enfermedades, como las neurodegenerativas, endocrinas o neoplasias malignas.3
También el tracto intestinal está habitado por 500 a 1000 billones de microbios intestinales de 100 a 1000 billones de especies, que colectivamente forman la flora intestinal. Se ha informado que los cambios en el microbiota intestinal, denominados disbiosis, están asociados con el síndrome metabólico, como la obesidad, la diabetes y la hipertensión.4
Tomando en cuenta esto, se llega a la convergencia del envejecimiento y la obesidad, lo cual da lugar a una patología única denominada OS, en la que las complicaciones de ambos estados se combinan sinérgicamente para causar pérdida de músculo y fuerza, aumento de la adiposidad e incapacidad para hacer ejercicio. Desafortunadamente, la OS es difícil de detallar como una patología distinta; es un síndrome multidimensional que se describe vagamente como un estado en el que un paciente se presenta simultáneamente con debilidad muscular y aumento de la adiposidad. Por lo tanto, la conjunción de dos enfermedades (obesidad y sarcopenia) denominadas OS ha creado un campo exigente que merece una mayor exploración y discusión.5
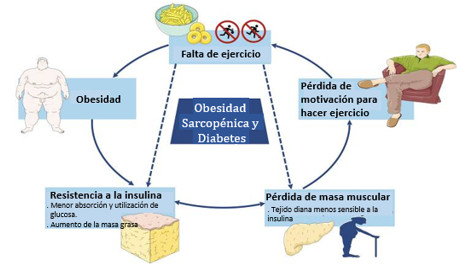
El objetivo de esta revisión es exponer los problemas que aparecen con el envejecimiento y la OS, su diagnóstico y el plan de tratamiento de este mal, enfocado en detener el círculo vicioso de un estilo de vida poco saludable y aumentar la calidad de vida del adulto mayor (figura 1).1 A la vez, consolida y discute las investigaciones más recientes en patogenia, diagnóstico y tratamiento de la diabetes y la OS.
MÉTODOS
La presente es una investigación de revisión sobre el envejecimiento y la OS, que se ha realizado en las bases de datos PubMed, Cochrane y Crossref, cuyas informaciones son las más fidedignas. Se buscó información de los últimos cinco años sobre los datos investigados. Se seleccionó lo más reciente sobre el envejecimiento y la OS. Se encontraron 33 publicaciones potencialmente relevantes y vigentes.
DISCUSIÓN
El envejecimiento se caracteriza por un deterioro progresivo de la integridad fisiológica, lo que conduce a un deterioro de la capacidad funcional y, en última instancia, a una mayor susceptibilidad a la muerte. Es un factor de riesgo importante para las enfermedades crónicas humanas, incluidas las enfermedades cardiovasculares, la diabetes, la degeneración neurológica y el cáncer.6 En la embriogénesis y la remodelación tisular, las células senescentes son necesarias para el correcto desarrollo del embrión y la reparación de los tejidos. En el cáncer, la senescencia funciona como una potente barrera para prevenir la tumorigénesis.7
La morfología del cerebro evoluciona con la edad y, con mayor frecuencia, sufre una atrofia significativa, es decir, una pérdida de volumen del tejido cerebral.8 Estos cambios van acompañados de déficits cognitivos que incluyen la pérdida de memoria, reducción del rendimiento motor y el comportamiento. Debido a los extensos esfuerzos realizados en estudios de imágenes médicas de grandes poblaciones, como la Iniciativa de Neuroimagen de la Enfermedad de Alzheimer o el Estudio de Rotterdam, se han identificado características estructurales del envejecimiento cerebral saludable y acelerado.9
Los procesos que impulsan la disminución progresiva del rendimiento funcional durante el envejecimiento aún no se comprenden del todo. En consecuencia, el término “envejecimiento” se interpreta de manera ambivalente en el campo, y los efectores del envejecimiento siguen siendo un tema muy debatido.
Además, todavía existe controversia sobre la interrelación entre el envejecimiento y la enfermedad, y si este refleja un estado de enfermedad o no. Generalmente aceptada es la opinión de que el envejecimiento subsume un fenómeno del organismo que implica una mayor probabilidad de morir y/o una disminución de la funcionalidad con el tiempo. Aunque la misma definición es aplicable a nivel de órganos y tejidos, definir el envejecimiento a nivel celular y molecular ha sido un desafío.10
La mayoría de las publicaciones sobre análisis de envejecimiento y senescencia de una sola célula se publicaron en los últimos dos años. Un primer tipo de estudio se basa en datos in vivo e investiga los efectos del envejecimiento principalmente en ratones y humanos, para un tejido específico y, a veces, para un conjunto de tejidos (multitejido). En estos estudios, los datos pueden inspeccionarse específicamente en busca de marcadores de senescencia celular como p16 (CDKN2A) o p21 (CDKN1A). Un segundo tipo de estudio, investiga colecciones de células senescentes in vitro, identificando o inspeccionando mecanismos biológicos específicos.11
También está el estudio de la sangre,12 que gracias a su fácil acceso se halla a nivel de todos los tejidos en forma unicelular. Igualmente, el páncreas,13 es un foco sorprendente de muchos estudios unicelulares y, al mismo tiempo, la senescencia celular está implicada en muchos aspectos del desarrollo y la terapia del cáncer de páncreas (específicamente adenocarcinoma ductal pancreático) y la diabetes (tanto tipo 1 como 2); el cerebro,14 ya que este complejo órgano contiene una multitud de tipos celulares que son difíciles de separar. Sin embargo, las ómicas cerebrales de los tejidos humanos son casi siempre y necesariamente post mortem, lo que puede plantear problemas causados por patrones de artefactos; y el pulmón,15 que se ha convertido en un tejido clave de las recientes investigaciones unicelulares, debido a la pandemia de COVID-19. Por ejemplo, recientemente se describieron un conjunto de datos de una sola célula que investiga el microambiente inmunológico pulmonar basado en el líquido de lavado broncoalveolar de pacientes con COVID-19.16
Además, la piel,17 que aporta una fuente de estudios que investiga el proceso de envejecimiento utilizándola. Dichas investigaciones tienen que realizarse con especial cuidado, ya que el fotoenvejecimiento, debido a la exposición de los humanos a la luz solar, puede influir fuertemente en los procesos relacionados con el envejecimiento, actuando como un factor de confusión importante. Se han recolectado células de la región de la piel inguinoilíaca protegida por el sol de donantes humanos masculinos.
Asimismo, el músculo,18 que se atribuye a las células madre musculares fueron seleccionadas específicamente como el sujeto del estudio, también motivadas por su supuesta quiescencia profunda; se utilizó un transgén para clasificar estas células basándose en el marcador Pax7. Además, teniendo en consideración la correlación por pares de la expresión génica de las células, tanto dentro como entre ratones individuales, los autores encontraron una mayor variabilidad a nivel del transcriptoma en comparación con ratones jóvenes y viejos. Se realizó cierta inmunotinción y también se observó un aumento de la heterogeneidad a nivel proteico.
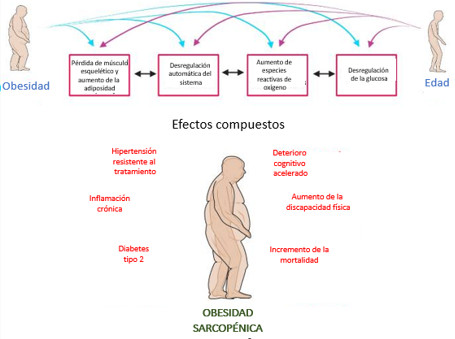
La definición de OS es una condición que ha recibido una atención considerable en los últimos años, porque se relaciona con varios resultados clínicos negativos; y no ha sido establecida universalmente. Existen varios criterios diagnósticos para la sarcopenia y la obesidad; antes se ha concluido que las diferentes definiciones de sarcopenia resultaron en un impacto diferencial sobre los factores de riesgo cardiometabólico (figura 2).5,19
En este sentido, la prevalencia de la sarcopenia y la OS depende de los criterios diagnósticos utilizados para describir estas afecciones, con un rango del 10 al 27 % para la sarcopenia y del 10 al 23 % para la OS. Hay múltiples factores que causan la OS, como el envejecimiento, la falta de actividad física, la desnutrición, la inflamación de bajo grado, la resistencia a la insulina y los cambios hormonales, lo que conlleva cambios en la composición corporal (disminución de la masa muscular y la fuerza, y aumento de la masa grasa). Además, cada factor tiene un impacto independiente en la calidad y cantidad de músculo y grasa, mientras que las conversaciones cruzadas de ellos tienen influencias más fuertes.20
La OS es el punto de partida de la mayoría de las enfermedades metabólicas, como la diabetes, la hipertensión, el síndrome metabólico, la apnea del sueño y, finalmente, las enfermedades cardiovasculares. Por lo tanto, es razonable especular que cuando el daño muscular y la obesidad coexisten, actúan sinérgicamente sobre el riesgo de mortalidad, los trastornos metabólicos y la calidad de vida.21
Actualmente, no existe un diagnóstico consistente de OS; sin embargo, se debe incluir el diagnóstico individual de obesidad y sarcopenia. Según los criterios de la Organización Mundial de la Salud, el IMC ≥ de 30 kg/m2 o la circunferencia de la muñeca en hombres ≥ 102 cm y en mujeres ≥ 88 cm, se considera obesidad. Sin embargo, se ha cuestionado si estos criterios son apropiados para cada individuo. Alternativamente, los puntos de corte del porcentaje de grasa corporal u otros índices de adiposidad, se han estimado como una medida útil de los resultados de la obesidad. El Grupo de Trabajo Europeo sobre Sarcopenia en Personas de Edad Avanzada ha propuesto que la baja masa muscular, la baja fuerza muscular y el bajo rendimiento físico, son los tres parámetros importantes para definir la sarcopenia. Surgen diversas técnicas para evaluar la masa muscular, entre las cuales, la tomografía computarizada y la resonancia magnética se consideran el estándar de oro para distinguir la grasa de otros tejidos blandos, estimando así eficazmente la masa grasa y la masa muscular.22
Los estilos para una vida sana, como son la restricción calórica y el ejercicio físico, se consideran la piedra angular de la terapia de la OS. Con respecto a la nutrición, aún no se ha establecido un enfoque ideal. De hecho, la pérdida de peso en personas obesas mayores sigue siendo controvertida, ya que es una estrategia de doble filo, que ejerce un impacto beneficioso con la disminución de las complicaciones relacionadas con la obesidad y los posibles efectos negativos. Actualmente, se debe evitar una ingesta calórica muy baja en personas mayores con OS, ya que esta estrategia puede comprometer la salud general al inducir deficiencias de micronutrientes y electrolitos, tener un impacto perjudicial en la masa muscular esquelética, así como reducir la densidad mineral ósea.23
Un estilo de vida reforzado en calcio y vitamina D es otro beneficio potencial importante en el tratamiento de la OS. Con respecto a la fisiopatología, la vitamina D representa un enfoque atractivo, ya que la unión del receptor de vitamina D a su ligando 1,25 (OH)2D3 desencadena la transcripción de genes asociados con la función muscular.24
Muchas terapias farmacológicas, incluida la administración de testosterona, son candidatas emergentes para el tratamiento de la OS en los hombres. Aunque la suplementación con testosterona presenta una clara justificación fisiológica, particularmente para aumentar la fuerza y la función muscular, los datos disponibles sobre el impacto de la administración de testosterona en la función y la masa muscular siguen siendo limitados y contradictorios. En la actualidad, diversas sociedades científicas como The Obesity Society o la American Association of Clinical Endocrinology, no recomiendan la administración de testosterona en el manejo de la obesidad y/o sarcopenia.25
La terapia con el complejo de ginseng silvestre, puede ser un nuevo tratamiento alternativo para la OS relacionada con la edad, pero se requieren más estudios que utilicen muestras más grandes para respaldar esto.26
El uso de moduladores selectivos de los receptores de andrógenos (SARM) tiene la ventaja de activar selectivamente los receptores de andrógenos en los huesos y músculos, sin inducción androgénica en el resto del cuerpo. Cuando se usa esta terapia, parece ser más beneficiosa que la mejora de la fuerza para las personas que requieren ganancia de masa muscular, y se espera que en un futuro próximo se disponga de un SARM transdérmico eficaz.27
Los tratamientos de pérdida de peso, como los que utilizan agonistas del receptor (AR) de GLP-1 han demostrado ser beneficiosas para la OS; sin embargo, los datos se producen principalmente en estudios preclínicos y se requieren parámetros específicos adecuados para esta patología, y más si son evaluados antes y después de la introducción de la AR de GLP-1. Es así, cuando se usa la cirugía bariátrica, que induce la pérdida de peso por un mecanismo restrictivo con un efecto consistente sobre la masa de tejido adiposo, pero su beneficio para el músculo esquelético aún no se ha determinado.28
Cuando se usa un tratamiento de vibración de todo el cuerpo, se estimula la contracción muscular, haciendo que la función muscular esté a un nivel similar al del entrenamiento de resistencia clásico, pero con la ventaja de ser más cómodo y seguro. Asimismo, el uso de células madre mesenquimales, representan una terapia potencial para la OS, debido a sus cualidades inmunomoduladoras y su naturaleza multipotente, aunque los datos actuales que respaldan sus beneficios siguen siendo limitados, y se requieren estudios clínicos futuros para comprender adecuadamente su mecanismo de acción en el contexto específico de la OS.29
La incidencia de la OS tiene un rápido crecimiento en todo el mundo, debido a los cambios en el estilo de vida y a la mayor esperanza de vida. De hecho, comparten muchos factores de riesgo comunes, especialmente en el envejecimiento y la obesidad. Aunque el mecanismo subyacente de la asociación sigue sin estar claro, los autores de este estudio especulan sobre una interacción bidireccional en la obesidad, la inflamación de bajo grado, la resistencia a la insulina y la sarcopenia. El OS combina sarcopenia y obesidad, y la inflamación de bajo grado juega un papel crucial en la patogénesis de la diabetes.30
Los individuos jóvenes con un buen control metabólico son capaces de realizar la mayoría de las actividades, pero se recomienda a los individuos de mediana edad y mayores, o a los pacientes con otras complicaciones, que consulten con el médico para evitar lesiones por el ejercicio intensivo; sin embargo, Wei et al.23 refieren que en un estudio que comprendía un total de 692 056 individuos con una edad media de 68,5 años, la prevalencia de sarcopenia oscilaba entre el 10 y el 27 %. En los ancianos, la OS aumenta el riesgo de discapacidad, caídas, osteoporosis, fracturas, cambios metabólicos, rigidez arterial, enfermedad del hígado graso no alcohólico, complicaciones por cáncer, peor rendimiento cognitivo y aumento de la mortalidad.19
En general, el mejor enfoque terapéutico para la OS es la modificación del estilo de vida, que incluyen ejercicios aeróbicos y de resistencia combinado regular, con modificaciones en la dieta, que debe incluir la restricción calórica, con el fin de reducir la masa grasa y aumentar la masa muscular y la función para mejorar la calidad de vida, así como reducir la mortalidad. La sarcopenia da como resultado una disminución de la tasa metabólica, baja actividad física y deficiencia de mioquinas, lo que colectivamente conduce al efecto proinflamatorio y exacerba la obesidad.21
Se han considerado diversas moléculas farmacológicas; sin embargo, aún no se recomiendan debido a la falta de pruebas sólidas. Los estudios más largos que evalúen los efectos de un enfoque multimodal contra la OS, los eventos cardiovasculares y la mortalidad, serán de gran interés. La definición clínica de la OS no se ha unificado y cada conjunto de criterios diagnósticos tiene implicaciones clínicas diferentes. Sin embargo, los fenómenos definitorios incluyen la disminución de la masa muscular y la reducción de la fuerza del músculo, independientemente del tamaño, y el aumento de la adiposidad.
Al analizar la evidencia que aportan investigaciones anteriores, se concluye que esta revisión identificó la posible patogénesis de la OS, como la desnutrición, la resistencia a la insulina, la inflamación de bajo grado y los cambios hormonales. La incidencia de la OS está aumentando, principalmente debido al envejecimiento cada vez mayor de la población mundial. Es un trastorno grave asociado a fragilidad, riesgo de caídas, fracturas óseas, enfermedades cardiovasculares, reducción de la independencia, elevada morbilidad y aumento de las tasas de hospitalización y mortalidad. La OS se asocia con un mayor riesgo de eventos cardiovasculares que los asociados con la sarcopenia o la obesidad, individualmente.
Como sugerencia final para la prevención y el tratamiento de la OS, se recomienda la intervención dietética y los ejercicios regulares, junto con los medicamentos específicos prescritos a estas personas.