Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
MediSur
versión On-line ISSN 1727-897X
Medisur vol.9 no.4 Cienfuegos jul.-ago. 2011
REVISIÓN BIBLIOGRÁFICA
Infertilidad
Infertility
Práxedes Rojas Quintana , Dulce María Medina Tío , Lidia Torres Ajá
Hospital General Universitario "Dr. Gustavo Aldereguía Lima", Cienfuegos, Cienfuegos, Cuba, CP: 55100
RESUMEN
Revisión bibliográfica sobre los principales temas referidos a la infertilidad de las parejas. Incluye concepto y clasificación, fisiología de la ovulación, causas en la mujer y en el hombre, exámenes complementarios básicos que se les realiza, evolución y pronóstico, así como acciones de salud para la orientación correcta de la pareja infértil. Tiene como objetivo crear un material de apoyo a la docencia, para estudiantes de la carrera de Medicina y de Enfermería, así como para residentes y especialistas en Medicina General Integral y Ginecoobstetricia.
Palabras clave: infertilidad femenina, infertilidad masculina, ovulación, pronóstico.
ABSTRACT
Literature review on the main issues related to infertile couples. It includes concept and classification, physiology of ovulation, causes in women and men, basic tests that are commonly performed evolution and prognosis, and health actions to provide appropriate orientation to the infertile couple. It is aimed at creating a teaching complementary material for Medicine and Nursing students, as well as for residents and specialists in general medicine and gynecology.
Key words: infertility, female, infertility, male, ovulation, prognosis.
INTRODUCCIÓN Se define como infertilidad a la falta de embarazo luego de 12 meses de relaciones sexuales regulares sin protección anticonceptiva. Aunque en muchos casos no es posible evidenciar algún tipo de enfermedad o patología que la cause, el sufrimiento, angustia y desesperación que aquejan a las parejas imposibilitadas de concebir son situaciones reales que han llegado a considerarse un verdadero y frecuente problema a enfrentar por los profesionales de la salud. (1,2) La esterilidad puede ser primaria, si la pareja nunca ha logrado un embarazo, o secundaria, si tras haber tenido un hijo o aborto, no logra volver a concebir; también puede ser de causa femenina si es la mujer la que padece la causa de la infertilidad o masculina si es el hombre el que la padece, o de la pareja pues ambos pueden tener dificultades que impidan lograr su objetivo. (2-4) Aun cuando las estimaciones sobre su incidencia no son muy precisas y varían según la región geográfica, aproximadamente entre el 8,0 % y el 12,0 % de las parejas experimentan algún problema de este tipo durante su vida fértil, lo cual, extrapolado a la población mundial, representa entre 50 y 80 millones de personas. (2) Incluso publicaciones más recientes citan cifras aun mayores y reconocen una tendencia general a la elevación de la incidencia de la infertilidad, que puede llegar al 20 %. (5-7) Entre el 15,0 y el 20,0 % de los adultos saludables tienen problemas de fertilidad. Muchos de estos problemas, con ayuda, pueden ser solucionados. (2, 5, 7) La infección genital es la principal causa de esterilidad en el mundo, no sólo en las afecciones tubáricas, sino que afecta también cada una de las diversas partes de la anatomía genital, tanto masculina como femenina. (4, 8 - 15) Las causas de infertilidad incluyen en un gran por ciento factores psicológicos y emocionales. (16,17) Aproximadamente del 30,0 al 40,0 % de toda la infertilidad es de factor masculino, debido a eyaculación retrógrada, varicocele, impotencia, deficiencias hormonales, trastornos en el conteo de espermatozoides , ITS, uso de drogas, fumadores inveterados, alcoholismo, prescripciones de medicamentos como la cimetidina, espironolactona, y nitrofurantoina, etc. (2, 10 - 18) También la edad materna es uno de los factores más importantes para la posibilidad de lograr buenos resultados, puesto que mucho antes de la menopausia la reserva ovárica, determinada por la cantidad y calidad de ovocitos disponibles en el ovario, comienza a decrecer a ritmo acelerado, (1,7,19) siendo el tiempo empleado para la investigación de la pareja un factor decisivo. Es por eso que al revisar la bibliografía relacionada con el tema se apreció que a nivel internacional se han diseñado protocolos ágiles de estudio, de forma tal que se pueda llegar a conclusiones diagnósticas y se decida el tratamiento adecuado para cada pareja en el tiempo más breve posible, a la vez que se racionalicen aquellos métodos invasivos y costosos que no sean absolutamente necesarios. (19,21,22) Esta tendencia tiene, además de un evidente objetivo económico, el de evitar el envejecimiento de la mujer hasta edades con fertilidad disminuida y por lo tanto con menos posibilidades de lograr el éxito deseado. Por otra parte, no se debe olvidar que la sociedad ha culpado y estigmatizado tradicionalmente a la mujer frente a la imposibilidad de la procreación, donde este "incumplimiento de la norma", genera y auto genera frustraciones que, a su vez, se traducen en presiones para que cualquier proceder médico en este sentido resulte satisfactorio y las expectativas de la pareja ante el recibimiento de un tratamiento se vinculan con la recuperación de un óptimo estado de la fertilidad que, a su vez, les permita tener una descendencia bajo el procedimiento normal, a través de las relaciones coitales entre ambos miembros de la pareja. En Cienfuegos existe desde hace años una consulta especializada para esta entidad y desde el año 2003 hasta la actualidad se han atendido 2 769 parejas, con un promedio de 692 al año, lo que significa un número considerable. Actualmente se cuenta con un Centro Territorial para la Atención a la Pareja Infértil, con equipamiento adecuado para las técnicas de reproducción asistida de baja tecnología, de reciente comienzo, y resulta importante destacar que las exigencias actuales para el tratamiento médico de las pacientes con infertilidad requieren contar con un profesional altamente preparado, que posea los conocimientos, las habilidades y los valores en el sentido de proporcionar una atención de salud sin riesgos, innovadora e integral. La siguiente revisión bibliográfica está encaminada a proporcionar un material de estudio para estudiantes, médicos tanto de APS como de ASS, y especialmente a ginecoobstetras para contribuir a elevar la calidad de la atención médica brindada a la pareja infértil. DESARROLLO EPIDEMIOLOGÍA DE LA INFERTILIDAD EN CUBA Es importante que cada país conozca la epidemiología de la infertilidad en su territorio pues el sistema de salud requiere estimados más exactos para poder calcular la demanda real y potencial de servicios donde se evalúen adecuadamente estos trastornos reproductivos. (22) En Cuba se plantea que existe un estimado de 300 000 parejas susceptibles de atención, que 80 000 tienen factor masculino puro, 70 000 tienen factor combinado de masculino y femenino y 22 000 mujeres tienen 1 o más causas de infertilidad tratable. (1, 7, 21) Se plantea que el 85 % de la infertilidad femenina puede ser resuelta a nivel de servicios municipales y provinciales no complejos. En Cuba los datos más recientes son los que reportan los resultados de un estudio realizado por el profesor Dr. Rubén Padrón en 1996, en el que se encuestaron 952 parejas de diversos municipios y diferentes provincias, y que arroja que existe entre un 12,0 a un 14,0 % de parejas infértiles, de las cuales entre el 42,0 y el 43,0 % desea el embarazo. (20, 21) Según los datos obtenidos en el Censo de Población y Viviendas del año 2002, (6) la población femenina cubana en edad fértil, alcanzó la cifra de 2 999 898 y esa misma fuente reportó que 1 934 204 de ellas, mantenían una relación estable de pareja. Al relacionar estos datos con los resultados de la investigación del profesor Padrón antes mencionada, se puede deducir que en Cuba 270 788 parejas presentan trastornos de la fertilidad, y de ellas poco menos de la mitad desean alcanzar la procreación (43,0 %), por lo cual se infiere que 116 439 son susceptibles de atención en consultas especializadas por problemas de infertilidad y aproximadamente 23 287 (el 20,0 %) serían tributarias de métodos de reproducción asistida (RAAT). (6, 7, 19, 21, 23) Pero en realidad en el momento actual en Cuba, aunque se han trazado estrategias nuevas para dar solución al problema de la pareja infértil, la carencia de recursos y tecnologías ha obstaculizado por muchos años el proceso, actualmente se cuenta con un programa que establece las funciones necesarias para lograrlo, en cada nivel de atención; no obstante no se ha implementado totalmente su uso, por cuanto requiere de una capacitación del personal médico, especialistas en Ginecoobstetricia que lo aplicarán en cada nivel de atención de salud. La atención primaria de salud (APS), (19) base fundamental del sistema, no cuenta con posibilidad alguna para enfrentar la problemática, solo con vías de remisión establecidas oficialmente para estos casos y las instituciones del segundo nivel que realizan procederes de reproducción asistida de baja tecnología (RABT), son sólo 3 centros a nivel de todo el país, lo que no cubre todas las necesidades crecientes. En todo este proceso se producen demoras excesivas, tanto en la búsqueda de la posibilidad de recibir el servicio como en el tiempo empleado para alcanzar un diagnóstico y en los intentos de tratamiento de las parejas y por último, los casos que requieren de procedimientos de alta tecnología como las técnicas de reproducción asistida (RAAT) se realizan en el único centro con que cuenta el país, radicado en el Hospital "Hermanos Almeijeiras", hasta la fecha sólo ha podido trabajar en forma experimental por las mencionadas dificultades económicas que ha enfrentado el país; pero, aun trabajando a plena capacidad, no tendría posibilidades, por sí solo, de dar verdadera cobertura social al problema nacional. Por otra parte, la población cubana se ha caracterizado por presentar una dinámica demográfica lenta dentro del contexto de los países latinoamericanos. Esto se debe a la influencia de la fecundidad, la cual desde inicios del pasado siglo ha sido relativamente baja. Tuvo un aumento en el primer lustro de la etapa revolucionaria, para luego caer por debajo del nivel de reemplazo demográfico desde 1978. (5, 21) El caso es que, actualmente, el país atraviesa por una avanzada transición demográfica que se caracteriza por una muy baja tasa de fecundidad y un aumento importante de la supervivencia, lo que conlleva a un envejecimiento poblacional importante que sin duda hará sentir sus efectos en los escenarios nacionales futuros, dada la interrelación existente entre los procesos demográficos, económicos y sociales. Aunque Cuba es un país subdesarrollado económicamente, desde el punto de vista demográfico presenta estos indicadores semejantes a los de los países desarrollados. (20) INFERTILIDAD. CONCEPTO Y CLASIFICACIÓN La esterilidad es la incapacidad para la reproducción tanto en el hombre como en la mujer y puede ser: absoluta o permanente, cuando no tiene posibilidad de tratamiento y tampoco de regresión o curación espontanea y que impide totalmente la fecundidad; o la relativa o temporal cuando puede desaparecer espontáneamente o no determina una imposibilidad completa de fecundar. La infertilidad es la incapacidad para quedar embarazada después de 12 meses de relaciones sexuales (coito) sin protección. (2-5) La infertilidad primaria es el término utilizado para describir a una pareja que nunca ha podido lograr un embarazo después de intentarlo durante al menos un año con relaciones sexuales sin precauciones. (3) La infertilidad secundaria es aquella en que la mujer tiene una historia previa de al menos un embarazo confirmado, aborto, parto y no es capaz de concebir después de un año de relaciones sexuales no protegidas. Existen autores que definen la infertilidad como el aborto habitual y/ o muerte habitual del feto o del recién nacido. (24) Se denomina aborto habitual a la aparición de tres abortos espontáneos consecutivos o más en la misma mujer. La infertilidad sin causa aparente comprende al grupo de pacientes en las que sin lograr identificar la causa, el embarazo no se logra. (7) FISIOLOGÍA DE LA OVULACION Para que se produzca un embarazo es necesario que ocurra una ovulación. La ovulación, por definición, es la ruptura de un folículo maduro con expulsión de líquido folicular y el cúmulo oóforo (o disco prolígero). Depende del crecimiento y del desarrollo, regulado con precisión, de un folículo preovulatorio y es la acumulación de una serie compleja de eventos fisiológicos iniciados por el surgimiento de la hormona luteinizante. (25) El reclutamiento de una cohorte de folículos dentro del reservorio de folículos en desarrollo, la selección fisiológica del folículo destinado a ovular, el crecimiento preferencial del mismo y la adquisición oportuna folicular óptima son necesarios para una ovulación y una fase luteal normal. El desarrollo del folículo preovulatorio y del ovocito ocurre en concordancia, de manera que este se encuentre en el grado correcto de maduración para que se produzca la fertilización. La ovulación ocurre aproximadamente en el día 14 de un ciclo menstrual de 28 días, sin embargo la misma puede ocurrir en cualquier momento del ciclo. La duración promedio del proceso de la ovulación es de 10 minutos, variando entre 1 y 20 minutos. (25) Al parecer, disturbios menores en la continuidad de la foliculogénesis, ovulación y lúteo génesis, parecen ser responsables del fallo de la concepción. El desarrollo folicular comienza en la vida embrionaria, deteniéndose el desarrollo de los folículos primordiales en la etapa de diploteno de la primera profase meiótica. En todo momento, incluido el embarazo, hay un continuo proceso y atresia folicular. (25) En cada ciclo menstrual, bajo la influencia de hormonas endocrinas, autocrinas, y paracrinas, así como de péptidos es reclutada una cohorte de folículos. En el día 5-7 del ciclo un folículo se vuelve dominante, continuando su crecimiento y desarrollo hasta la ovulación. Los folículos restantes se atresian, proceso denominado apoptosis. En los ciclos normales existe correlación entre el diámetro del folículo dominante y los niveles de estradiol. Esto apoya la creencia de que el 90-95 % del estradiol medible en un ciclo normal es producido por el folículo dominante. (25) Los niveles de estradiol alcanzan su valor máximo 24-36 horas antes de la ovulación, lo que da lugar al surgimiento de la LH, (34-36 horas antes de la ovulación), lo que resulta en una reanudación de la meiosis, y luteinización de las células de la granulosa, con la subsecuente producción de progesterona. (25) La LH es también responsable de la síntesis de prostaglandinas, y otros eicosanoides necesarios para la digestión de la pared folicular y de la liberación del ovocito. La ovulación se produce a 10- 17 horas después del pico de LH. Es necesario que el estradiol sea 200 pg/ ml durante unas 50 horas y debe estar presente hasta después de que se produzca la oleada de LH. El feed- back positivo del estradiol sobre la hipófisis, que hace que se produzca la oleada de LH, se ve favorecido por los bajos niveles de progesterona. El pico de progesterona se produce 8 días después de la oleada de LH, interviene en la maduración del endometrio secretor y suprime un nuevo crecimiento folicular. (25) El mecanismo por el cual se produce la ovulación no se conoce con exactitud Se defienden tres teorías para explicar el mecanismo íntimo de la producción de la ovulación: a) aumento de la presión intrafolicular, b) necrobiosis de la pared del folículo por modificaciones del flujo vascular, y c) digestión local del tejido por acción enzimática. (25) CAUSAS DE LA INFERTILIDAD I.-Causas más frecuentes de infertilidad en la mujer En relación con la obstrucción tubárica, la esterilidad se relaciona con el transporte de los ovocitos. Estos se desplazan desde los ovarios a través de las trompas de Falopio para llegar al útero (matriz).(56, 57) Si hay un bloqueo es posible que la mujer no conciba, las infecciones por chlamydia y gonococo no tratadas podrían llevar a una enfermedad inflamatoria pélvica, con daño a nivel de las trompas, e infertilidad de causa tubárica.(57 - 67) Por su parte, el síndrome de ovario poliquístico (SOPQ) como causa de esterilidad, se caracteriza por anovulación, hiperandrogenismo y resistencia a la insulina y obesidad. (26-40, 67-70) Se sabe que la hiperinsulinemia se asocia con un aumento del riesgo cardiovascular y la aparición de diabetes mellitus. Aproximadamente el 15,0 % de las pacientes con SOPQ no ovulan, presentan trastornos menstruales, ovarios con múltiples quistes y síndrome metabólico. En la poliquistosis ovárica, hay muchos folículos con un desarrollo insuficiente. Los óvulos en estos folículos no maduran y, por lo tanto, no pueden ser liberados desde los ovarios. En lugar de esto, forman quistes allí. (26–40, 67 -70) Esto puede conducir a infertilidad. La falta de maduración folicular y la incapacidad para liberar un óvulo (ovular) probablemente son ocasionadas por bajos niveles de la hormona folículo estimulante (FSH, por sus siglas en inglés) y por niveles más altos de lo normal de hormonas masculinas (andrógenos), producidas en el ovario. (26 - 40) A las mujeres usualmente se les hace el diagnóstico a los 20 o 30 años y quienes padecen este trastorno con frecuencia tienen una madre o hermana con síntomas similares de poliquistosis ovárica. (26 - 40) En relación con el fibroma uterino como causa de trastorno de fertilidad, esta se relaciona con los fibromiomas uterinos, tumores benignos más frecuentes del aparato reproductor femenino. La edad máxima de incidencia es entre los 30 y 50 años, aunque en la actualidad se diagnostican más temprano por el uso tan difundido de la ultrasonografía. Se señala una mayor frecuencia en mujeres negras, mestizas y nulíparas, obesas y perimenopáusicas. Se desconoce su etiopatogenia, aunque tanto los estrógenos como la progesterona aumentan su tamaño. Se reportan mutaciones en dos genes, HMGI(c) y HMGI (y) que parecen ser importantes en el desarrollo de algunos fibromas. Los genes cruciales en el desarrollo del fibroma aún no se han identificado. Tienden a involucionar durante la menopausia. (41-44) La presencia de estos tumores puede producir alteraciones del ciclo menstrual y puede estar asociado con subfertilidad.(45) Otra de las causas es la endometriosis. Esta es la presencia de glándulas endometriales o estroma en otros sitios que no son la cavidad uterina. Las localizaciones más frecuentes de endometriosis extrauterina son: el ovario uni o bilateralmente, la trompa de Falopio y el peritoneo pélvico sobre todo. La afectación extrapélvica no es rara, se reportan habitualmente a nivel de cicatrices quirúrgicas, generalmente laparotomías por cesáreas o histerectomías, y con menor frecuencia en la región umbilical. Esta enfermedad afecta entre el 15,0 % y el 17,0 % de las mujeres en edad fértil, entre las cuales el 44,0 % permanecen asintomáticas. (44- 46) La infertilidad sin causa aparente muchas veces se asocia a endometriosis. Los síntomas que la caracterizan son dolor pélvico crónico, dismenorrea adquirida progresiva, dispareunia profunda, pujos, tenesmos, diarreas, y defecación dolorosa, disuria y urgencia al orinar, trastornos menstruales, sobre todo sangramiento post menstrual escaso y oscuro. Las causas de infertilidad en la endometriosis son por disfunción ovárica, afecciones tubáricas, limitación de la captación ovular por adherencias, que fijan la trompa, líquido peritoneal excesivo y anormal, entre otras. (46-52) La galactorrea, síntoma frecuente como expresión de hiperprolactinemia, que es la elevación de la hormona prolactina circulante en sangre, por encima de 20-25 ng/ ml ó 888-1100 pmol/ l, producida por una alteración hipotálamo hipofisaria, es la más frecuente, se acompaña en la mujer de trastornos menstruales como amenorrea, oligomenorrea, ciclos anovulatorios, fase lútea insuficiente e infertilidad. (53-55) Otro de los temas a abordar es la problemática del aborto, que tantas secuelas deja en el aparato reproductor. El aborto se institucionalizó en Cuba a fines de la década de los 60. Desde entonces hasta hoy mucho se ha hablado a favor y en contra de esta decisión; como todo problema que se estudia en medicina, tiene aspectos positivos y negativos. Lo ideal sería brindar una educación sexual. Estudios estadísticos, tomando en cuenta datos indirectos, consideran que en Latinoamérica hay cada año alrededor de 1 000 000 de abortos en mujeres menores de 20 años. (56) La morbilidad y mortalidad relacionadas tienen consecuencias mayormente en la salud materna, así como en los recursos destinados al cuidado de la salud, sobre todo en los países en desarrollo. Las opciones más efectivas para la disminución de la morbilidad y mortalidad están dadas por la prevención de los embarazos no deseados, que se logra a través del desarrollo del acceso a la información y servicios de planificación familiar, así como por la disponibilidad de servicios donde se practique el aborto en las mejores condiciones y con poco tiempo de embarazo. (56,57) En un estudio realizado en el año 1979 en el Hospital "América Arias", se analizaron los resultados de 405 abortos practicados a mujeres menores de 18 años. La complicación más frecuente fue la enfermedad inflamatoria pélvica, que afectó a 20 pacientes, para 4,8 %; pero se debe resaltar que hubo en dos casos perforaciones uterinas, en uno de las cuales fue necesaria la realización de una histerectomía total en el primer embarazo de la joven, lo que evidencia el alto riesgo del aborto, incluso cuando se practica en las mejores condiciones. (56) El aborto, en cualquiera de sus formas clínicas, deja secuelas importantes que conducen a trastornos de la fertilidad. La infertilidad genera un importante aumento en los niveles de estrés y ansiedad los cuales pueden ser variables en cada uno de los miembros de la pareja. Estudios realizados en diversas partes del mundo coinciden al referir que las mujeres vivencian mayores niveles de estrés psicológico y ansiedades – antes, durante y después de la realización del estudio y las técnicas de reproducción, que los experimentados y registrados por varones. Sin embargo, sería justo señalar que estos niveles de estrés y ansiedades, en cuanto a la infertilidad se refiere, están íntimamente ligados a diferentes factores, los cuales no deben ser analizados a espalda de un profundo análisis que tome en consideración a la perspectiva de género. La mujer se somete a la mayoría de los procederes y técnicas, por lo que la exposición a factores condicionantes de los niveles de ansiedad y estrés sobrepasa al varón, quien solo estuvo expuesto físicamente en relación con el proceder de toma de muestra del esperma. (20, 21) II.- Causas más frecuentes de infertilidad en el hombre
La esterilidad ha aumentado a nivel mundial, esto se debe al incremento de las infecciones de transmisión sexual (ITS), de las enfermedades inflamatorias pélvicas (EIPA) que dejan como secuelas obstrucción a nivel de las trompas uterinas, lo que ha incrementado la incidencia de embarazos ectópicos, los que dejan también secuelas importantes. El incremento cada vez mayor de las ITS provoca también en el hombre obstrucciones de las vías seminales, epididimitis que causan infertilidad en este sexo. (4, 8 - 14)
Cuando la pareja no logra en un tiempo determinado su objetivo muchos abandonan la consulta y casi siempre se debe a la disolución definitiva del vínculo matrimonial o consensual, en la esperanza de lograr el hijo anhelado con otra compañera/o. (16, 17,19, 20)
Las causas más frecuentes de infertilidad en la mujer son: las obstrucciones tubáricas, (7, 8, 10, 12) el síndrome de ovario poliquístico (26 - 40) la anovulación, (41-43) la hiperprolactinemia, estenosis cervical, la fibromatosis uterina, (42, 44,45) endometriosis, (46 -48) las malformaciones en el aparato genital, (49) etc. y otras que pueden no ser identificadas. (50-55)
Las causas masculinas capaces de producir esterilidad o infertilidad son muy numerosas. A continuación se enumeran las más importantes:
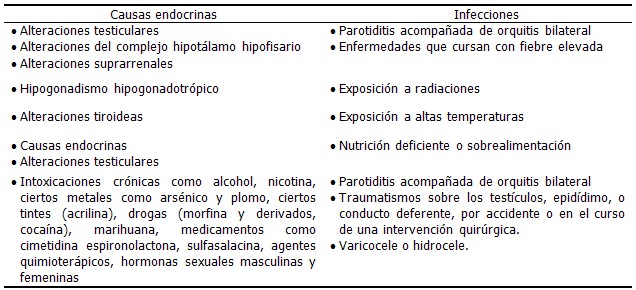
Las infecciones genitourinarias (IGU) en el hombre representan un por ciento importante en la etiología de la infertilidad, y aunque no están claros los mecanismos patogénicos implicados a nivel celular, de alguna forma alteran la calidad espermática y afectan principalmente la cantidad y movilidad de los espermatozoides (pre-requisito esencial para la fertilización). Las infecciones del tracto genital, causadas por ITS provocan inflamación de las glándulas sexuales accesorias y del epidídimo. (58, 59)
Las infecciones seminales en el hombre, con frecuencia, son de poca sintomatología, por lo que permanecen largo tiempo sin ser identificadas y generan secuelas que pueden conducir a la infertilidad. La asociación entre leucocitospermia y defectos morfológicos en los espermatozoides compromete no solo los eventos de fertilización de estos individuos, sino la implantación, e incluso, embarazo futuro, por lo que es necesario realizar estudios más profundos de morfología espermática. (58-61)
Las actuales técnicas microbiológicas de diagnóstico facilitan la detección de un gran número de gérmenes que afectan la calidad del semen y conducen a la infertilidad masculina, entre ellos, parásitos y hongos. (62) Aunque no está claro el papel de la Cándida albicans en la infertilidad, como consecuencia de la infección por este microorganismo, se describe la pérdida de la fertilización, el incremento de fragmentación del DNA espermático y la disminución de la movilidad del espermatozoide en pacientes infértiles. La Trichomona vaginalis, que causa inflamación de la uretra, también afecta la calidad del semen y la fertilidad de los individuos, y se reporta oligospermia severa como consecuencia de esta infección. (62, 63)
Los micoplasmas genitales son considerados patógenos humanos de relevante importancia, como agentes de transmisión sexual. Están implicados en una gran variedad de infecciones en el hombre, tales como uretritis, prostatitis y otros procesos inflamatorios que conducen a la infertilidad. (62-64)
La infección causada por la bacteria Chlamydia trachomatis tiene una elevada incidencia en la infertilidad masculina. La población masculina es el reservorio natural de esta bacteria, pero pocas veces provoca síntomas en ellos, de aquí el término infección "silente", que si no es tratada, puede avanzar y causar graves problemas reproductivos y de salud, con consecuencias a corto y largo plazo. La infección por esta bacteria afecta a 1 de cada 10 hombres sexualmente activos, y afecta la concentración de los espermatozoides, su movilidad y genera cambios en su morfología. Esta bacteria puede causar inflamación en los testículos y el escroto, lo cual incide en la calidad del semen, especialmente en la movilidad de los espermatozoides. (65)
Dentro de las ITS, los virus, como los virus del herpes simple tipo 1 (VHS-1) y herpes simple tipo 2 (VHS-2); aunque el VHS-1, responsable del herpes labial, se transmite a través de secreciones orales, también puede producir herpes genital a través del sexo oral, por lo que ambas cepas de virus pueden transmitirse sexualmente. Las investigaciones epidemiológicas y clínicas han enfatizado en el papel de los hombres en la transmisión viral. (66)
La infección por el Citomegalovirus humano (CMVH) como posible causa de enfermedad del sistema genital masculino, afecta la fertilidad de los hombres, y se ha publicado también su transmisión sexual a través del semen de hombres infértiles. Este virus es la causa más común de transmisión congénita, que conduce a enfermedades fetales y neonatales serias. Los virus de la hepatitis, virus del papiloma humano (VPH), específicamente el tipo 16, que puede transmitirse sexualmente, así como el virus de VIH Sida. (67,68)
Las ITS tienen en la actualidad una gran relevancia debido a la pandemia del SIDA. Tienen gran importancia en salud pública, no sólo por las infecciones agudas, sino por la gravedad de sus complicaciones y secuelas. Es un problema de salud pública. (68, 69)
Otra causa de infertilidad masculina es el varicocele o hidrocele que consiste en un aumento de la tortuosidad y dilatación de las venas del plexo pampiniforme del cordón espermático. El 25-45 % aproximadamente de los varones estériles padecen varicocele en la vena espermática interna izquierda. (57)
EXÁMENES COMPLEMENTARIOS BÁSICOS QUE SE DEBEN REALIZAR A PAREJAS INFÉRTILES
Para iniciar el estudio de la pareja infértil es necesario indicar exámenes complementarios a ambos miembros, que garanticen la salud de los mismos, tales como hemograma completo, eritrosedimentación, glucemia, exudado vaginal simple y con cultivo, test para diagnóstico de chlamydia, serología, VIH, así como dosificaciones hormonales cuando se sospeche alteraciones de las mismas, tanto en el hombre como en la mujer, y el espermatograma al varón. (1)
I.-Pruebas diagnósticas
Estudio del moco cervical
Constituye un método práctico y rápido para evaluar el factor cervical, e indirectamente el estado hormonal de la mujer. Debe obtenerse en la mitad del ciclo, es decir, cuando la producción de estradiol es máxima y coincidiendo, más o menos, con el pico de secreción de LH, en este momento es máxima la estimulación de las glándulas del endocérvix por los estrógenos. El moco se recoge con una jeringa, y se valorarán los siguientes parámetros: volumen, consistencia, viscosidad, elasticidad, celularidad, y arborización. (1, 24, 57)
- Volumen: superior a 0,1 ml
- Debe ser claro, de aspecto fluido y acuoso.
- La filancia o elasticidad debe ser de 8-10 cm.
- Celularidad por debajo de 5 x campo de gran aumento.
- Arborización cristalizar con tallos terciarios y cuaternarios.
El moco cervical puede ser anormal por las siguientes causas:
- Pobre estimulación estrogénica
- Células endocervicales que funcionan bioquímicamente mal.
- Células endocervicales inadecuadas.
Curva de temperatura basal (CTB)
El desplazamiento térmico que produce la progesterona, al activar los centros térmicos, causa elevación de la temperatura corporal mayor de 0,5 ºC. Al revisar la curva de temperatura basal de tres ciclos menstruales consecutivos se tiene una muestra simple de la ovulación, y de las alteraciones del mismo. Puede ser monofásica o bifásica. Puede afectarse por diferentes causas. (1, 24, 57)
Test postcoital
Se realiza para evaluar la interacción muco- espermática (Sims- Huhner). Proporciona evidencias de una adecuada estimulación estrogénica y de la capacidad de penetración del moco cervical por espermatozoides sanos y activos.
Debe ser realizada entre los días 11 y 13 del ciclo; y entre las 2 y 18 horas posteriores al coito. En esta prueba se valora número, motilidad, velocidad de progresión rectilínea, indicada en una escala de 0-4. (1, 24, 57)

Histerosalpingografía
Examen radiológico del tracto genital femenino que incluye cérvix, cuerpo uterino, trompas y estado general de la pelvis. Debe realizarse al octavo día del ciclo. Constituye un excelente medio diagnóstico para investigar las alteraciones de la trompa y su permeabilidad. (1)
Esta prueba también puede realizarse bajo visión con fluoroscopia, examen radiológico que tiene como contraindicación para su realización la infección pélvica, el embarazo y la alergia al yodo.
Biopsia endometrial
La biopsia de endometrio, obtenida por aspiración, es un método de gran valor y exactitud para conocer la existencia de ovulación y el funcionamiento del cuerpo lúteo. Se recomienda por algunos autores entre los días 22 y 24 del ciclo y otros el día 26 del ciclo, donde la maduración final del endometrio puede ser confirmada fácilmente. La biopsia debe tomarse de la cara anterior del útero (capas superficiales del endometrio) para disminuir la posibilidad remota de interrumpir una gestación temprana. (1, 24)
Espermatograma
El estudio de calidad del semen es el examen de laboratorio más importante en la fertilidad masculina, y es una de las prácticas que se efectúan en los servicios de atención a parejas infértiles, lo cual incluye movilidad, concentración, viabilidad, morfología y pH, siguiendo las normas recomendadas por la OMS, desde 1999, se establecieron como valores normales del semen:
- Volumen > 2ml
- Concentración > 20 millones /ml
- Movilidad > 50 %
- Morfología > 30 % normales
- Células blancas < 1 millón /ml
Para su correcta interpretación es necesario que en la recogida del semen se tenga en cuenta, que exista una abstinencia sexual previa de 2-3 días. La forma más adecuada de recoger el material es mediante masturbación, en un frasco de cristal limpio y seco. El enjuiciamiento de la movilidad de los espermatozoides debe hacerse antes de las 2 horas de obtenido el material.
El volumen normal del eyaculado oscila entre 2 y 5 ml. Cantidades inferiores a 2 ml deben considerarse anormales. El pH normal del esperma oscila entre 7,2 y 7, 8; mientras que el de la secreción prostática es de 6,3-6,5.
A pesar de esto, muchas veces los resultados satisfactorios de estos parámetros seminales convencionales no se corresponden con los resultados que desde el punto de vista de fertilidad tienen estos individuos, por lo que clínicamente no son siempre suficientes para demostrar la función espermática y fertilidad masculina. El hecho de no encontrar alteraciones en los parámetros seminales no indica que la capacidad funcional de los espermatozoides no se encuentra comprometida, ya que tanto las bacterias, como sus productos y el incremento de la peroxidación de la infección, podrían ocasionar cambios bioquímicos y moleculares en la membrana espermática, que afectan la reacción acrosómica y su capacidad de fusión con el ovocito, así como daños en el ADN espermático. (1, 57)
Laparoscopia
Constituye un procedimiento endoscópico que permite la evaluación de los genitales internos y de la pelvis, con la finalidad de diagnosticar posibles causas mecánicas de infertilidad, así como la presencia de endometriosis u otra patología orgánica de dichos órganos. (70)
Ultrasonografía
La ultrasonografía es un medio de diagnóstico esencial en el estudio de la mujer infértil, y muy especialmente en las modernas unidades de reproducción asistida. Facilita el seguimiento del desarrollo folicular y endometrial, y proporciona un apoyo imprescindible para la captación de ovocitos por punción transvaginal, en la fecundación in vitro. (71)
DIAGNÓSTICO PRECOZ Y TRATAMIENTO OPORTUNO: UN ASPECTO DE VALOR EN EL ÉXITO DEL TRATAMIENTO A LA MUJER INFÉRTIL
Como parte de la práctica médica integral y dispensarizada que el médico de la familia brinda a la mujer en las diferentes etapas de su ciclo, la ginecología en la APS ha permitido desarrollar aspectos médicos de tipo epidemiológico y preventivo relacionados con la salud ginecológica, conjuntamente con la presencia tutoral e interactiva del especialista de ginecología del grupo básico de trabajo (GBT). La especialidad se implementa en la APS, con un enfoque integral, en el que relacionan sus actividades con la calidad de vida de la mujer, su pareja y familia. En este sentido se tienen en cuenta los factores psicológicos y sociales y el enfoque de género, además de la sostenibilidad del medio ambiente, que pueden influir sobre su salud en general y, en especial, sobre la salud sexual y reproductiva. (3, 72)
Desde el surgimiento de la medicina familiar, las afecciones y necesidades ginecológicas son evaluadas y tratadas a nivel del consultorio médico, e interconsultadas con el especialista en ginecoobstetricia del GBT. Entre las enfermedades más frecuentes se encuentran las leucorreas, dolor pélvico, infecciones e inflamaciones del tracto genitourinario, trastornos menstruales, afecciones en edades extremas como la infanto juvenil, y el climaterio y menopausia, entre otras, incluyendo el riesgo reproductivo preconcepcional y la planificación familiar. (56, 72-74)
Se conoce como riesgo preconcepcional a la probabilidad que tiene una mujer no gestante de sufrir daño (ella o su producto) durante el proceso de la reproducción. Esto está condicionado por una serie de factores, enfermedades o circunstancias únicas o asociadas que pueden repercutir desfavorablemente en el binomio, durante el embarazo, parto o puerperio. (72)
Por lo antes expuesto, el riesgo puede ser de carácter biológico, psicológico y social, y no es valorado por igual en cada caso; es decir, que la misma condición de riesgo no repercute de forma igual en cada mujer o pareja, por lo que se debe hacer un enfoque y análisis individualizado en cada caso. (72)
El especialista en ginecoobstetricia del GBT durante sus evaluaciones concurrentes, debe medir la calidad de la atención médica, a través de la competencia y del desempeño del médico de familia en formación, y remitirá a nivel secundario los casos que no tengan en su área posibilidad de resolución del problema. En tal sentido en todo este proceso se producen demoras excesivas, tanto en la búsqueda de la posibilidad de recibir el servicio como en el tiempo empleado para alcanzar un diagnóstico y en los intentos de tratamiento de las parejas y, por último, los casos que requieren de procedimientos de alta tecnología pierden posibilidades de diagnóstico y tratamiento precoz de sus causas de esterilidad. La gran variedad de posibles factores causales del fenómeno de la infertilidad trae como consecuencia la necesidad de utilizar muchos recursos para la investigación de estos casos y para su tratamiento posterior. (1, 72-74)
Es, por tanto, importante que el procedimiento investigativo vaya de forma consecuente y escalonada, de lo simple a lo más complejo, de acuerdo con las posibilidades del nivel de atención, y del lugar donde se realiza la investigación, pero de manera ágil, dinámica, sin pérdida de tiempo innecesaria en los diferentes niveles, para poder brindar una atención de calidad a la pareja infértil. (72)
REFERENCIAS BIBLIOGRÁFICAS
1. Cuba. Ministerio de Salud Pública. Comisión Nacional. Programa Nacional de Atención a la Pareja Infértil. Ciudad de La Habana: MINSAP; 2007
2. Berer M. Population and family planning policies: Women-cantered perspectives. Reproductive Health Matters. 1993;1:4-12
3. Herrera V, Oliva J, Domínguez F. Riesgo reproductivo. En: Rigol . Obstetricia y Ginecología. Ciudad de La Habana: Editorial Ciencias Médicas; 2004: p. 113-120
4. Valencia MI. Reproducción Humana e Infertilidad. Quito: CEMEFES; 2002
5. World Health Organization. Report of a meeting on Medical, Ethical and Social Aspects of Assisted Reproduction. Headquarters: WHO; 2001
6. Cuba. Comité Estatal de Estadística. Censo de Población y Viviendas. La Habana: Comité Estatal de Estadística; 2002
7. Veranes A. Evaluación de la pareja infértil. En: Rigol O. Obstetricia y Ginecología [Internet]. La Habana: Editorial Ciencias Médicas; 2004 [citado 20 Mar 2008]. Disponible en: http://bvs.sld.cu/libros_texto/libro_de_ginecologia_y_obstetricia/cap35.pdf
8. Cutié E. Infecciones de transmisión sexual. En: Rigol O. Obstetricia y Ginecología [Internet]. Ciudad de La Habana: Editorial Ciencias Médicas; 2004 [citado 20 Mar 2008]. Disponible en: http://bvs.sld.cu/libros_texto/libro_de_ginecologia_y_obstetricia/cap37.pdf
9. Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines 2002. MMWR. 2002;51(RR-6):23-40
10. Rojas P, Bernia A, Bernia S, Montalvo Y, Oliva T, Fang R. Enfermedad inflamatoria pélvica. Medisur [revista en Internet]. 2007 [citado 18 Abr 2008];5(3):[aprox. 10p]. Disponible en: http://www.medisur.sld.cu/index.php/medisur
11. Álvarez Sánchez AZ, Rivero Llonch L, Martínez Murquía J, Álvarez Ponce V. La infección en el factor cervical y su relación con la infertilidad. Rev Cubana Obstet Ginecol [revista en Internet]. 2004 [citado 18 Abr 2008];30(2):[aprox. 7p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138-600X2004000200007&lng=es&nrm=iso&tlng=es
12. Askienazy EM. Male genital tract infection: the point of view of the bacteriologist. Gynecol Obstet Fertil. 2005;33:691-7
13. Brady M. Preventing sexually transmitted infections and unintended pregnancy, and safeguarding fertility: triple protection needs of young women. Reproductive Health Matters. 2003;11(22):134-41
14. Rodríguez BV, Santana F. Infecciones de transmisión sexual, calidad del semen e infertilidad. Rev Cub Endocrinol [revista en Internet]. 2008 [citado 3 Feb 2009];19(3):[aprox. 12p]. Disponible en: http://bvs.sld.cu/revistas/end/vol19_3_08/end07308.htm
15. Galvin SR, Cohen MS. The role of sexually transmitted diseases in HIV transmission. Nat Rev Microbiol. 2004;2:33-42
16. Calero JL, Magallanes M, Rechkemmer A, García M. Infertilidad o paternidad frustrada. Significados de este fenómeno desde la perspectiva masculina peruana. Rev Cubana Salud Púb. 2003;29 Suppl 1:48
17. Calero JL, Santana F. La infertilidad como evento de frustración personal. Reflexiones de un grupo de varones de parejas infértiles. Rev Cubana Endocrinol [revista en Internet]. 2006 [citado 18 Abr 2008];17(1):[aprox. 8p]. Disponible en: http://bvs.sld.cu/revistas/end/vol17_1_06/end02106r.htm
18. Escudero A. La infertilidad y el varicocele a través de la historia. Arch Esp Urol. 2004;57(9):876-882
19. González I, Millar E. Infertilidad y sexualidad. Rev Cub Med Gen Integr. 2001;17(3):291-5
20. Padrón RS, Hernández AJ, Más J, Valdés F, Seuc A. Causas de descontinuación del seguimiento de las parejas infértiles y su relación con el diagnóstico y el estado de la fertilidad. Rev Cubana Endocrinol. 1997;8(3):208-16
21. Padrón RS. Epidemiología de la infertilidad en Cuba. REVCOG. 1996;6(3):80-4
22. Terapias de fertilidad podrían detener crisis poblacional en Europa [Internet]. Ciudad de La Habana: SOCBIO; 2010 [citado 18 Abr 2011]. Disponible en: http://portalinfomed.sld.cu/socbio/infonews_render_full/15923
23. Schutt-A, Maddaleno M. Salud sexual y desarrollo de adolescentes y jóvenes en las Américas: Implicaciones de programas y políticas. Washington: OPS; 2002
24. Botella J, Clavero JA. Esterilidad e Infertilidad. En: Tratado de Ginecología. 14 ed. Madrid: Díaz de Santos; 2008: p. 987-99
25. González Merlo J, González Bosquet J, González Bosquet E. Ciclo ovárico (ovulación). Ciclo endometrial (menstruación). En: Ginecología I. La Habana: Editorial Ciencias Médicas; 2007: p. 39-54
26. Ovies Carballo G, Domínguez Alonso E, Verdeja Varela O L, Zamora Recinos H. Frecuencia y características clínicas, hormonales y ultrasonográficas sugestivas de síndrome de ovarios poliquísticos en un grupo de mujeres con síndrome metabólico. Rev Cubana Endocrinol [revista en Internet]. 2008 [citado 3 Feb 2009];19(1):[aprox. 14p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1561-29532008000100004&lng=es&nrm=iso&tlng=es
27. Lord JM, Flight IHK, Norman RJ. Fármacos sensibilizadores a la insulina (metformina, roglitazona, rosiglitazona, pioglitazona, d-chiro-inositol) para el síndrome de ovario poliquístico anovulatorio [Internet]. Oxford: La Biblioteca Cochrane Plus; 2007 [citado 18 May 2008]. Disponible en: http://www.fisterra.com/guias2/cochrane/AB003053-ES.htm
28. Pazos F, Rodríguez A. Síndrome de ovario poliquístico. Nuevas perspectivas. Endocrinol Nutr. 2004;51(9):506-11
29. Farquhar C, Lilford RJ, Marjoribanks J, Vandekerckhove P. Laparoscopic drilling by diathermy or laser for ovulation induction in anovulatory polycystic ovary syndrome. Cochrane Database Syst Rev. CD001122. 2007; (3)
30. Mafaldo Soares EM. Prevalence of metabolic syndrome, microalbuminuria and cardiovascular risk in women with polycystic ovary syndrome. Rev Bras Ginecol Obstet [revista en Internet]. 2007 [citado 3 Feb 2009];29(8):[aprox. 10p]. Disponible en: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0100-72032007000800010&lng=en doi: 10.1590/S0100-72032007000800010
31. Bregieiro Fernández LO, Oliveira Riveiro D, Oliveira M. Prevalence of the metabolic syndrome in women with polycystic ovary syndrome. Rev Bras Ginecol Obstet [revista en Internet]. 2007 [citado 3 Feb 2009];29(1):[aprox. 8p]. Disponible en: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0100-72032007000100003&lng=en
32. Legro RS, Barnhart HX, Schlaff WD, Carr BR, Diamond MP, Carson SA, et al. Cooperative Multicenter Reproductive Medicine Network. Clomiphene, metformin, or both for infertility in the polycystic ovary syndrome. N Engl J Med. 2007;356(6):551-66
33. Trivax B, Azziz R. Diagnosis of polycystic ovary syndrome. Clin Obstet Gynecol. 2007;50(1):168-77
34. Azziz R, Carmina E, Dewailly D, Diamanti-Kandarakis E, Escobar-Morreale HF, Futterweit W, et al. Positions statement: criteria for defining polycystic ovary syndrome as apredominantly hyperandrogenic syndrome: an Androgen Excess Society guideline. J Clin Endocrinol Metab. 2006;91(11):4237-45
35. Nugent D, Vandekerckhove P, Hughes E, Arnot M, Lilford R. Tratamiento con gonadotrofina para la inducción de la ovulación en la subfertilidad asociada con el síndrome de ovario poliquístico [Internet]. Oxford: La Biblioteca Cochrane Plus; 2007 [citado 18 May 2008]. Disponible en: http://www.update-software.com/BCP/BCPGetDocument.asp?DocumentID=CD000410
36. Bayram N, Van Wely M, Van der Veen F. Pulsatile gonadotrophin releasing hormone for ovulation induction in subfertility associated with polycystic ovary syndrome. Cochrane Database Syst Rev. CD000412. 2004; (1)
37. Maciel GA, Soares JM, Alves da Motta EL, Abi Haidar M, de Lima GR, Baracat EC. Nonobese women with polycystic ovary syndrome respond better than obese women to treatment with metformin. Fertil Steril. 2004;81(2):355-60
38. Teixeira Filho FL, Baracat EC, Lee TH, Suh CS, Matsui M, Chang RJ, et al. Aberrant expression of growth differentiation factor-9 in oocytes of women with polycystic ovary syndrome. J Clin Endocrinol Metab. 2002;87(3):1337-44
39. Legro RS, Castracane VD, Kauffman RP. Detecting insulin resistance in polycystic ovary syndrome: purposes and pitfalls. Obstet Gynecol Surv. 2004;59(2):141-54
40. Beck JI, Boothroyd C, Proctor M, Farquhar C, Hughes E. Oral anti-oestrogens and medical adjuncts for subfertility associated with anovulation. Cochrane Database Syst Rev. CD002249. 2005; (1)
41. Hughes E, Collins J, Vandekerckhove P. Clomiphene citrate for unexplained subfertility in women. Cochrane Database Syst Rev. CD000057. 2000; (3)
42. Athaullah N, Proctor M, Johnson NP. Oral versus injectable ovulation induction agents for unexplained subfertility. Cochrane Database Syst Rev. CD003052. 2002; (3)
43. Camus A. Reserva ovárica. Formas de medición y predicción de la respuesta ovárica a la estimulación. Reproducción Humana [revista en Internet]. 2002 [citado 18 Abr 2008];31(3):[aprox. 10p]. Disponible en: http://www.flasef.org/textos/revista/2002/3/31_39.pdf
44. Gupta JP, Sinha AS, Lumsden MA, Hickey M. Uterine artery embolization for symptomatic uterine fibroids. Cochrane Database Syst Rev. CD005073. 2006; (1)
45. Rigol O. Afecciones benignas de útero. En: Obstetricia y Ginecología. Ciudad de La Habana: Editorial Ciencias Médicas; 2004: p. 293-95
46. Rodríguez N. Endometriosis. En: Rigol O. Obstetricia y Ginecología. La Habana: Editorial Ciencias Médicas; 2006: p. 375-89
47. Jacobson TZ, Barlow DH, Koninckx PR, Olive D, Farquhar C. Laparoscopic surgery for subfertility associated with endometriosis. Cochrane Database Syst Rev. CD001398. 2002; (4)
48. Sagsveen M, Farmer JE, Prentice A, Breeze A. Gonadotrophin-releasing hormone analogues for endometriosis: bone mineral density. Cochrane Database Syst Rev. CD001297. 2003; (4)
49. Braun P, Vercher F, Pamies J. Las malformaciones uterinas congénitas como causa importante de esterilidad e infertilidad. Papel de la histerosalpingografía en su diagnóstico. Radiología. 2005;47(3):129-132
50. López O, Almaguer J, Granado O. Cirugía de mínimo acceso en el tratamiento del factor tubo peritoneal. Rev Cub Obstet Ginecol [revista en Internet]. 2005 [citado 2 Abr 2008];31(3):[aprox. 9p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138-600X2005000300001&lng=es&nrm=iso
51. Marana R. GnRH analogy´s versus expectant management in minimal and mild endometriosis-associated infertility. Acta Eur Fértil. 2002;25:37
52. Lugones M. Dismenorrea. Rev 16 de Abril [revista en Internet]. 2008 [citado 25 Feb 2008];8(2):[aprox. 10p]. Disponible en: http://www.16deabril.sld.cu/rev/211/lugones.html
53. Goyal N, Gore MA, Shankar R. Galactorrhea and amenorrhea in burn patients. Burns. 2008;34(6):825-8
54. Eftekhari N, Mirzaei F, Karimi M. The prevalence of hyperprolactinemia and galactorrhea in patients with abnormal uterine bleeding. Gynecol Endocrinol. 2008;24(5):289-9
55. Schlechte JA. Long-term management of prolactinomas. J Clin Endocrinol Metab. 2007;92(8):2861-5
56. Peláez J. Ginecología infanto juvenil. En: Rigol O. Obstetricia y Ginecología. Ciudad de La Habana: Editorial Ciencias Médicas; 2004
57. González Merlo J, González Bosquet J, González Bosquet E. Esterilidad e Infertilidad. En: Ginecología I. Ciudad de La Habana: Editorial Ciencias Médicas; 2007: p. 167-190
58. Bamberger E, Madeb R, Steinberg J, Paz A, Satinger I, Kra-Oz Z, et al. Detection of sexually transmitted pathogens in patients with hematospermia. Isr Med Assoc J. 2005;7:224-7
59. Moretti E, Federico MG, Giannerini V, Collodel G. Sperm ultrastructure and meiotic segregation in a group of patients with chronic hepatitis B and C. Andrologia. 2008;40:173-8
60. Bohbot JM. Las infecciones genitales por Chlamydia trachomatis. Aspectos clínicos. Análisis Clínicos. 2001;26(3):1-13
61. Díaz García FJ, Herrera Mendoza AP, Giono Cerezo S, Guerra Infante FM. Mycoplasma hominis attacks to and locates intracellular in human spermatozoa. Human Reprod. 2006;21(6):1591-8
62. Kranjcic Zee I, Dzamic A. The role of parasites and fungi in secondary infertility. Med Preg. 2004;57:30-2
63. Sanocka MD, Ciupinska M, Kurpisz M. Bacterial infection and semen quality. J Reprod Immunol. 2005;67:51-6
64. Fernández C, Zamora Y, Rodríguez N, Rodríguez I, Berdasquera D, Ortega LM. Diagnóstico de Mycoplasma hominis, Ureaplasma parvum y Ureaplasma urealyticum en pacientes con vaginosis bacteriana. Rev Cubana Med Trop [revista en Internet]. 2007 [citado 28 Ene 2008];59(2):[aprox. 8p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0375-07602007000200006&lng=es&nrm=iso
65. Peterson EA. Infecciones por Chlamydia y Gonococo entre adultos y jóvenes [Internet]. California: Keck Hospital of USC; 2004 [citado 20 May 2008]. Disponible en: http://www.keckhospitalofusc.org/condition/document/127148
66. Looker K, Garnett G, Schmid G. An estimate of the global prevalence and incident of herpes simplex virus type 2 infection. Bull World Health Organ. 2008;86(10):805-12
67. Reartes D. La experiencia de varones infectados por el virus del papiloma humano (VPH). Medicina. 2007;67:127
68. Leruez VM, Galimand J, Ghosn J, Briat A, Delaugerre C, Chaix ML. Male genital tract infection: the point of view of the virologist. Gynecol Obstet Fertil. 2005;33:684-90
69. Organización Mundial de la Salud. Estrategias de salud reproductiva. Headquarters: OMS; 2004
70. Saavedra J. Papel de la laparoscopia diagnóstica en la evaluación de la infertilidad femenina. Rev Colombiana Obstet Ginecol. 2004;55(1):71-80
71. Galera F, Mayoral M, Huertas MA, Frutos A, Romo A, Bajo JM. Seguimiento ultrasonográfico del ciclo endometrial. En: Bajo Arenas JM. Ultrasonografía Ginecológica. Madrid: Marban; 2007
72. Creus Ferré M. Orientación de la paciente con problemas de reproducción en atención primaria. Rev Cub Med Gen Integr. 2002;18(5):362-365
73. Prado C, Canto M, Donoso C, Arechiga J, Monsalvez T, Carmenate M, et al. Ciclo reproductor y antropología en grupos de mujeres sometidas a diferentes presiones ambientales. Rev Cubana Salud Pública [revista en Internet]. 2005 [citado 7 Abr 2008];31(2):[aprox. 10p]. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864- 200004&lng=es&nrm=iso
74. Peláez J, Salomón N, Machado H, Rodríguez O, Vanegas R. Salud sexual y reproductiva. En: Ministerio de Salud Pública. Manual de prácticas clínicas para la atención integral a la salud en la adolescencia. Ciudad de La Habana: MINSAP; 2002
Recibido: 06 de julio de 2011.
Aprobado: 06 de julio de 2011.
Práxedes Rojas Quintana. Especialista de II Grado en Ginecología y Obstetricia. Profesora Auxiliar. Investigador Agregado. Hospital General Universitario "Dr. Gustavo Aldereguía Lima". Cienfuegos. Correo electrónico: praxedes.rojas@gal.cfg.sld.cu














