INTRODUCCIÓN
La esclerosis múltiple (EM) es una enfermedad inflamatoria y desmielinizante del sistema nervioso central (SNC) que, después de presentar brotes, se transforma en crónica, progresiva y neurodegenerativa. Se caracteriza por la presencia de desmielinización del SNC debido a una respuesta inmune atípica equivocada dentro del organismo. Lo más característico en la enfermedad es el trastorno neurológico, que afecta únicamente al SNC. (1
Aunque la EM es una enfermedad incurable y de curso progresivo, existen alternativas de tratamiento para su manejo, los cuales pueden clasificarse en cuatro grandes grupos: fármacos modificadores de la enfermedad, tratamiento de las recaídas o brotes, tratamientos sintomáticos y tratamientos rehabilitadores. Los fármacos modificadores de la enfermedad (FME) tienen la finalidad de reducir la frecuencia de recaídas, retardar la progresión de la discapacidad, así como la aparición de nuevas lesiones en el SNC. 2
Los FME, como el interferón beta-1a (IFNb-1a) son el tratamiento estándar de primera línea de los pacientes con esclerosis múltiple remitente-recurrente (EMRR), puesto que han demostrado su capacidad para reducir la frecuencia de los brotes y enlentecer el progreso de la enfermedad. Los interferones requieren de la administración continua durante seis meses para ser efectivos; sin embargo, la respuesta al IFNb-1a en pacientes con EMRR es muy heterogénea y una proporción significativa de los pacientes presenta una respuesta insuficiente. 3
Los objetivos del tratamiento son: disminuir la frecuencia y número de brotes, reducir el volumen lesional cerebral (número de lesiones y volumen de las mismas) y de esta manera retrasar la progresión de la enfermedad y disminuir el acúmulo de discapacidad. Esto es lo que se conoce como no evidence of disease activity (NEDA, por sus siglas en inglés). El tratamiento precoz con interferones y acetato de glatirámero, ha demostrado que retrasa la progresión a una EM clínicamente definida; el tratamiento con teriflunomida de manera temprana ha demostrado reducir el número de brotes y lesiones objetivadas por resonancia magnética nuclear (RMN). (4
La EM es una enfermedad que en la actualidad no tiene cura y debido a que afecta tanto al SNC como al sistema inmunológico, dos sistemas encargados de la vigilancia y regulación del organismo, se dificulta su manejo y abordaje terapéutico. El tratamiento tiene como meta el control y la disminución de la actividad inflamatoria, evitando así la aparición de recaídas y la discapacidad asociada a la patología. (5 Por esto, es importante el inicio temprano del tratamiento, ya que logra prevenir la producción de lesiones irreversibles del SNC. (6)
En la actualidad todavía no se dispone de biomarcadores que puedan predecir qué pacientes presentarán una buena respuesta al tratamiento inmunomudulador; la detección precoz del fracaso terapéutico es fundamental para seleccionar a los candidatos a recibir un tratamiento alternativo. Dada la parcial eficacia del tratamiento con IFNb-1a y la disponibilidad de tratamientos más efectivos, identificar precozmente a los pacientes que no responden adecuadamente al tratamiento tiene que ser una de nuestras principales prioridades. Con este resultado, por primera vez, se describen en Villa Clara los marcadores clínicos y de resonancia magnética asociados tras el primer año de tratamiento con IFNb-1a que permitan estimar el riesgo de actividad de la enfermedad durante los siguientes dos años.
Por ello, esta investigación busca determinar los indicadores precoces de respuesta al tratamiento con IFNb-1a para disponer de herramientas sencillas, que ayuden a valorar la respuesta al tratamiento de forma precoz, lo que debe repercutir de forma positiva en la evolución de la enfermedad e identificar a aquellos pacientes con una respuesta parcial o insuficiente.
El objetivo de la investigación fue determinar los indicadores precoces de respuesta al tratamiento con IFNb-1ª.
MÉTODOS
Se realizó un estudio observacional, analítico de cohorte prospectiva longitudinal en los pacientes con diagnóstico de esclerosis múltiple. Se conformaron dos cohortes, una incluyó los pacientes con EMRR y tratamiento con FME: IFNb-1ª y la otra cohorte con aquellos pacientes con diagnóstico de EMRR que no tienen ni han tenido tratamiento con FME de la enfermedad y forman parte, al igual que el primer grupo, de la “Estrategia para el seguimiento multidisciplinario de los pacientes con esclerosis múltiple” del Hospital Universitario Clínico Quirúrgico Arnaldo Milián Castro de Santa Clara, 7 en el período comprendido de enero del 2014 a diciembre del 2020.
Criterios de inclusión para la cohorte de pacientes con EMRR y tratamiento con interferón, se consideraron los siguientes:
Pacientes con diagnóstico de esclerosis múltiple remitente-recurrente. (Criterios Diagnósticos McDonald 20178
Iniciar o haber iniciado tratamiento con IFNb-1ª subcutáneo a dosis de 44 𝜇g administrado a razón de tres dosis semanal, completar o haber completado 12 meses de tratamiento con buena adherencia al mismo y disponer de un seguimiento mínimo de tres años.
Pacientes que, previo consentimiento informado, estuvieran dispuestos a participar en el estudio.
Pacientes mayores de 18 años.
Criterios de inclusión para la cohorte de pacientes con EMRR que no tienen tratamiento con interferón, se consideraron los siguientes:
Pacientes con diagnóstico de esclerosis múltiple remitente-recurrente. (Criterios Diagnósticos McDonald 20178
Pacientes que, previo consentimiento informado, estuvieron dispuestos a participar en el estudio.
Pacientes mayores de 18 años.
Pacientes con EMRR que no tienen ni han tenido tratamiento con interferón, pero sí tratamiento sintomático, rehabilitador, que fueron atendidos en la consulta de esclerosis múltiple, durante el período de estudio y forman parte, al igual que el primer grupo, de la “Estrategia para el seguimiento multidisciplinario de los pacientes con esclerosis múltiple” del Hospital Universitario Clínico Quirúrgico Arnaldo Milián Castro de Santa Clara. 7
Criterios de exclusión para ambas cohortes:
Pacientes afectados de formas secundarias progresivas, así como pacientes con síndrome clínicamente aislado.
Criterios de salida:
Pacientes que manifestaran su deseo de abandonar el estudio.
Pacientes que no completaran todas las sesiones de evaluación.
Muestra:
Grupo 1: Cohorte de pacientes con EMRR y tratamiento con interferón: 39 pacientes.
Grupo 2: Cohorte de pacientes con EMRR que no tienen tratamiento con interferón: 39 pacientes.
Se utilizaron como instrumento de evaluación los Criterios de Rio Score (RS), 9) este es un sistema que puntúa a los pacientes de 0 a 3 basándose en la presencia de brotes, el incremento de al menos un punto en la escala ampliada del estado de discapacidad (Expanded Disability Status Scale, EDSS, por sus siglas en inglés) o la presencia de lesiones activas en la RMN durante el primer año de tratamiento con IFNb-1ª.
Procedimiento: cada paciente realizó la evaluación inicial o línea base (se midió la EDSS basal, RMN basal y la tasa anulizada de brotes), a los 12 meses de tratamiento (se midió el EDSS, RMN y los brotes), y en el período de seguimiento a los 24 meses y a los 36 meses (se medió el EDSS y los brotes).
La recogida del dato primario de la investigación se realizó mediante un formulario de recolección de datos. La información se obtuvo a través de la revisión de las historias clínicas y la entrevista médica.
En los métodos estadísticos se presencia una variable que se tomó en consideración más de dos veces con evaluación en el tiempo y exigió una utilización de un estudio de pruebas repetidas, variante de ANOVA que permitió contrastar con rigor la forma de darse el efecto en el tiempo y en el grupo de los casos. Para las pruebas de dos momentos se utilizó el concepto de ANOVA de un factor y además se trabajó buscando la exactitud de los resultados cuando las condiciones de las frecuencias exigieron del test exacto de Fisher, junto al cual se trabajó, para pruebas de dos por dos el odds ratio (OR) o razón de ventajas.
Consideraciones éticas:
El estudio cumplió con los requisitos éticos de valor, validez científica y confidencialidad. Desde el inicio de la recolección de los datos hasta el momento en que culminó el informe final, se mantuvieron en el anonimato los datos personales de los pacientes en estudio, se cumplió así con los principios éticos de respecto a las personas, beneficencia, no maleficencia y justicia. El estudio fue autorizado por el Consejo Científico y el Comité de Ética del Hospital Provincial Clínico- Quirúrgico Arnaldo Milián Castro.
RESULTADOS
Los resultados relacionados con los indicadores precoces de respuesta al tratamiento con IFNb-1ª, permitieron valorar la efectividad de la intervención de acuerdo a las progresiones por EDSS y el número de brotes. Se observó una alta significación asintótica tanto para el efecto del tiempo como para la relación de los grupos en el tiempo.
La media y desviación estándar del EDSS en la línea base y a los 36 meses fue de 1.76 ± 1.29 y 2.37 ± 1.86 respectivamente en el grupo estudio y en el control de 2.05 ± 1.54 y 3.15 ± 2.1 8 respectivamente. La media de los brotes en la línea base y a los 36 meses fue de 1.13 ± .52 y .13 ± .33 respectivamente en el grupo estudio y en el grupo control de .92 ± .48 y .41 ± .59 respectivamente. (Tabla 1).
Tabla 1 Respuesta al tratamiento con IFNb-1ª de acuerdo a EDSS y número de brotes

Leyenda: Media ± DE: Media aritmética con desviación típica.
* Efecto tiempo: F = 57,59; p < 0,001 Efecto grupo tiempo: F = 5,30; p = 0,018
** Efecto tiempo: F= 50,58; p < 0,001 Efecto grupo tiempo: F = 4,82; p = 0,003
Fuente: Formulario de recolección de datos
A través de un modelo lineal general y mediante una prueba de medidas repetidas asociadas a este se pudo valorar la efectividad de la intervención de acuerdo a las progresiones por EDSS y el número de brotes donde se ofrece una alta significación asintótica tanto para el efecto del tiempo como para la relación de los grupos en el tiempo.
La media y desviación estándar de lesiones que mostraban realce tras administrar gadolinio tras los 12 primeros meses de tratamiento era 0.36 ± .66 para el grupo estudio y 0.51 ± .50 para el grupo control. Las lesiones nuevas en T2 fue de 0.90 ± 1.16 para el grupo estudio y para el control de 1 ± 1.10. La efectividad de la intervención valorada desde las lesiones con contraste y nuevas en T2 muestran valores altamente significativos para las lesiones en T2 y significativas para las obtenidas con contraste al relacionarse mediante una prueba t. (Tabla 2).
Tabla 2 Respuesta al tratamiento con IFNb-1ª de acuerdo a lesiones con contraste y lesiones en T2
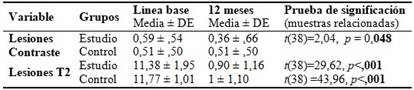
Fuente: Formulario de recolección de datos.
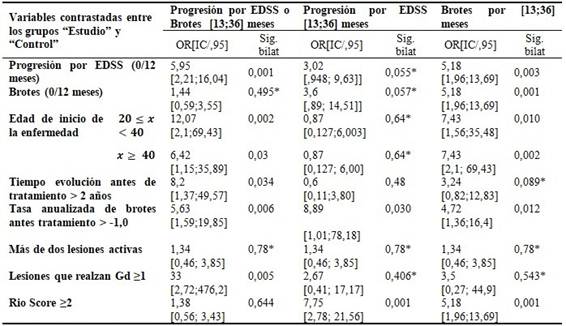
Se evaluó el riesgo de actividad clínica durante el seguimiento en cuanto al nivel de discapacidad valorado por la escala EDSS, así como de la presencia de brotes en función de la evolución durante el primer año de tratamiento para ambos grupos. La progresión por EDSS durante los 12 primeros, la tasa anualizada de brotes antes del tratamiento, la edad de inicio de la enfermedad, tiempo de evolución de la enfermedad y lesiones que realzan gadolinio se asoció de forma significativa con la razón de ventaja de mayor probabilidad de no progresión para el grupo estudio con respecto al grupo control por la variable combinada progresión por EDSS y brotes. La variable medida durante los primeros 12 meses, progresión por EDSS, los brotes, la edad de inicio de la enfermedad, la tasa anualizada de brotes antes del tratamiento y el Rio Score se asoció de forma significativa con la razón de ventaja de no brotes para el grupo estudio con respecto a los controles en los siguientes 13 a 36 meses.
La tasa anualizada de brotes antes del tratamiento y un Rio Score 2 se asoció de forma significativa con la razón de ventaja de no progresión por EDSS para el grupo estudio con respecto a los controles en los siguientes 13 a 36 meses.
Sobre la evaluación del riesgo de actividad clínica durante el seguimiento en función de la evaluación durante el primer año de tratamiento para ambos grupos, al resumir los datos obtenidos tras el tratamiento para las variables predictoras “Progresión por EDSS”, “Brotes” y “Progresión por EDSS o Brotes” y contrastarlas con los resultados de estas, en el periodo de 0 a 12 meses del estudio integrado, se concibió utilizar para estos contrastes el valor de odds ratio (OR) que posibilitó medir la razón de ventajas entre el grupo estudio y el grupo control en todos los casos del proceso efectuado y agregaba el intervalo de confianza del 95 % en el que se hallaba el mismo, así como el valor de significación bilateral asociada a dicha prueba, considerada significativa para valores menores que 0,05. (Tabla 3).
DISCUSIÓN
La identificación precoz de los pacientes que presentan una respuesta subóptima al tratamiento con IFNb-1ª es fundamental para optimizar el tratamiento y poder utilizar otras terapias más eficaces en estos pacientes. En un futuro próximo existirán nuevas terapias. Diversos estudios han tratado de hallar diferentes factores clínicos o radiológicos que predigan discapacidad a largo plazo en pacientes que reciben fármacos inmunomuduladores, pero no existe actualmente un consenso al respecto. (9
Se ha demostrado que la actividad por RMN junto con la actividad clínica durante el primer año de tratamiento con IFNb-1ª puede ayudar a predecir la respuesta al fármaco. El RS, basado en la combinación de parámetros clínicos y de RM en los primeros 12 meses de tratamiento, ha demostrado ser capaz de identificar a los pacientes con mala respuesta al IFNb-1ª tras dos años de seguimiento. (10
En este estudio, el RS se ha analizado de forma prospectiva, con el objeto de evaluar su utilidad en la práctica clínica diaria. Los resultados ratifican los hallazgos previos y demuestran que el RS en pacientes con EM tratados con IFN-β identifica a los pacientes con mayor riesgo de desarrollar recaídas o progresión de la discapacidad en los dos años siguientes. Este hecho es importante porque permite plantear una terapia alternativa a los pacientes que, tras el primer año de tratamiento, presentan un RS de riesgo.
Aunque la RM ha demostrado su valor en el diagnóstico y su utilidad para pronóstico, su relevancia en la evaluación de la respuesta al tratamiento individual en los pacientes con EM en condiciones de práctica clínica diaria no se ha demostrado. Estudios recientes sugieren que la aparición de lesiones activas después de 12 o 24 meses de tratamiento puede identificar a los pacientes con una mala respuesta y un mayor aumento de la discapacidad. 11
Los resultados muestran que la presencia aislada de actividad en la RM sin brotes clínicos concomitantes o progresión de la discapacidad no predice de forma significativa la presencia de brotes en los años posteriores, aunque sí predice un incremento de la discapacidad. En consecuencia, el uso exclusivo de criterios radiológicos es probable que sea útil para identificar a los pacientes con un alto riesgo de una mala respuesta a IFNb-1ª. Sin embargo, la utilización simultánea de medidas clínicas y radiológicas mejora la correcta identificación de los pacientes no respondedores. 12
Esto, referido anteriormente, coincide con los resultados de este estudio donde la combinación de variables clínicas como los brotes y el nivel de discapacidad medido por el EDSS, así como las variables imagenológicas de lesiones que captan gadolinio y lesiones nuevas permiten evaluar la respuesta al tratamiento con IFNb-1ª en pacientes con EMRR.
Investigaciones recomiendan el uso de tratamiento con IFNb-1ª, con buenos resultados globales. Así como la importancia de la RMN como marcador de respuesta al tratamiento. El concepto de respuesta IFNb-1ª no está bien establecido en la literatura y difiere en dependencia de las variables de respuesta seleccionadas. Si se considera una definición de respondedor muy estricta, gran número de pacientes serían considerados como no respondedores. Sin embargo, si se elige una definición muy conservadora solo un pequeño número de pacientes se considerarían como no respondedores. Atendiendo a los distintos criterios usados, se observa en la literatura una fluctuación en el número de pacientes considerados como respondedores (13 %-50 %). 13,14
Se ha demostrado que la administración temprana de tratamientos modificadores de la enfermedad es importante para reducir el riesgo de progresión de esta. El elevado número de terapias existentes hoy día requiere de una terapia individualizada atendiendo al curso de la enfermedad, a la eficacia del fármaco y a su seguridad, así como a las preferencias del paciente. (15
Una de las limitaciones importantes de este estudio es su naturaleza observacional, que condiciona una falta de aleatorización. Sin embargo, los estudios observacionales analizan grandes cohortes de pacientes durante largos períodos de seguimiento en condiciones de práctica clínica real. A pesar de estas limitaciones, el estudio ha demostrado que, en condiciones de práctica clínica diaria, la utilización del RS, la RMN, los brotes y el nivel de discapacidad ayuda a predecir la actividad clínica futura.
Se concluye que las variables clínicas nivel de discapacidad y brotes, así como las variables imagenológicas lesiones que captan gadolinio y lesiones nuevas constituyen indicadores precoces de respuesta de los pacientes al tratamiento con interferón β. Por lo que se identifican indicadores precoces de respuesta al tratamiento con IFNb-1ª; que ayudan a valorar la respuesta al tratamiento de forma precoz, lo que repercute de forma positiva en la evolución de la enfermedad.