Introducción
Los implantes dentales en el sector anterior son una de las opciones más solicitadas para la rehabilitación de pacientes edéntulos. El éxito de los implantes dentales en sectores con demanda estética, no solo radica en la integración del implante al hueso, llamado fenómeno de osteointegración; sino también en el correcto comportamiento de los tejidos blandos alrededor del implante.1) Los implantes con demanda estética suelen ser colocados cercanos al momento de la extracción. Según el consenso del International Team of Implantology (ITI) de 2003 y 2008,2,3 se pueden clasificar como: inmediatos, cuando se coloca el implante inmediatamente después de la extracción o tempranos,4 cuando han transcurrido entre 4 y 8 semanas desde la cicatrización del tejido blando. En menos casos, los implantes en zonas estéticas son colocados cuando el proceso de cicatrización ósea ha avanzado.
La diferencia principal entre colocar el implante de forma inmediata o temprana es que los tejidos blandos en la colocación temprana se encuentran cicatrizados y asegura el cierre por primera intención al momento de colocar el implante.3,4
Muchos estudios han demostrado que los implantes inmediatos pueden generar un riesgo estético importante, sobre todo asociados a recesiones vestibulares de la mucosa,5,6,7 por lo que muchas veces es justificable esperar la cicatrización de tejidos blandos para disminuir la posibilidad de aparición de complicaciones.
Es por esto que antes de iniciar el tratamiento, el paciente debe ser informado de posibles procedimientos adicionales que puedan corregir estas posibles complicaciones. Dentro de las posibilidades para tratarlas, se tiene la opción de colocar biomateriales que preserven y/o estimulen la producción de nuevo tejido. Estos materiales de acuerdo con su procedencia, podemos clasificarlos como biomateriales xenogénicos, provenientes de otras especies, por lo general de origen bovino, materiales autogénicos, provenientes del propio individuo y aloplásticos, materiales inertes o sintéticos.
Por lo general, suelen utilizarse biomateriales autógenos, debido a su compatibilidad y disponibilidad, entre los que tenemos al tejido conectivo sub epitelial, injerto gingival libre y actualmente para el tratamiento de recesiones de tejido blando al plasma rico en fibrina.8 La evaluación para la posible colocación de un biomaterial que prevenga o trate una complicación relacionada con el tejido blando, deberá realizarse en la etapa de planificación previa al tratamiento.
La justificación del uso de procedimientos regenerativos óseos es impedir la remodelación ósea natural que ocurre después de las extracciones. A la vez, los procedimientos regenerativos tisulares impiden recesiones gingivales y, por consiguiente, la exposición de las roscas de los implantes y pilares, en especial, cuando el biotipo gingival es delgado.9 En el caso de los implantes inmediatos, es discutido si los procedimientos regenerativos a través de los concentrados plaquetarios presentan o no ventajas en cuanto al proceso de oseointegración;10 sí se han reportado ventajas en cuanto a favorecer la cicatrización de los tejidos blandos;11 sin embargo, aún es controversial su eficacia clínica a largo plazo y si estos procedimientos se favorecen cuando se combinan o no con injertos de tejido blando.
De esta forma, el objetivo de esta presentación de caso es describir la rehabilitación de un incisivo central superior fracturado a través del uso de plasma rico en fibrina e injerto conectivo para el manejo de los tejidos blandos y la instalación de un implante dental.
Presentación del caso
Se presenta el caso de un paciente masculino, de 40 años de edad, quien acudió a la Clínica de Cirugía Periodontal de Post Grado de la Facultad de Odontología de la Universidad Nacional Mayor de San Marcos, en marzo de 2018 (Lima, Perú). El motivo de la consulta fue que el paciente quería recuperar la estética en un diente anterior. Tenía buena salud general, no presentaba antecedentes de enfermedades sistémicas, no fumaba, pero tenía antecedente de trauma facial moderado en 2003. Debido al trauma facial, tuvo una fractura del incisivo central superior derecho, al cual le realizaron el tratamiento de conductos y corona cerámica ese año. Al poco tiempo, se fracturó la pieza a nivel cervical.
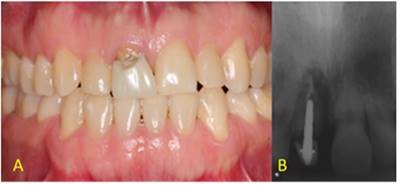
Al examen clínico, se evidenció una corona de porcelana fracturada a nivel cervical vestibular, pérdida de la estructura coronaria del incisivo central superior derecho, discromía de la pieza dentaria aparentemente por una lesión cariosa a nivel cervical. A nivel gingival, se comprobó una secreción purulenta en proceso de cicatrización, contorno gingival alterado (Figura 1A). El incisivo central superior derecho tenía contacto protusivo muy marcado con el diente antagonista debido a la fractura. La higiene oral era aceptable, el paciente refirió usar cepillos interproximales. No se observaron facetas de desgaste en los dientes anteriores ni posteriores.
Se hicieron radiografías periapicales al inicio del tratamiento. Estas se realizaron perpendicularmente al eje largo del implante con una técnica paralela a lo largo del cono. Se demostró una lesión periapical en dientes incisivos centrales superiores e incisivo lateral superior izquierdo. El incisivo central derecho superior presentaba una imagen radiolúcida por mesial en tercio apical radicular, compatible aparentemente con reabsorción radicular y una imagen radiopaca compatible con tratamientos de conductos. (Figura 1B). Se emitió una orden para realizar una tomografía computarizada de haz cónico y la planificación del software digital. Se evaluó el nivel de la cresta ósea y las características del hueso vestibular.
Se le dieron a conocer al paciente varias opciones de tratamiento de acuerdo con su necesidad de una prótesis fija. La primera, fue seguir preservando el diente con un alargamiento de corona, seguido del retratamiento endodóntico y la restauración definitiva del diente. La segunda opción fue la extracción del diente seguido de la restauración del diente retenida por los dientes; y la última opción fue la restauración soportada por un implante inmediato.
El paciente eligió la tercera opción. Se le explicó cada fase del procedimiento:
Primero, se le indicó la extracción del incisivo central superior derecho, debido a la gravedad de la lesión periapical, el ancho del espigo corto y la proporción corono-radicular desfavorable, según el examen radiográfico. Una vez extraída la pieza, se dejaría cicatrizar los tejidos blandos por 6 semanas y asegurar la estabilidad de los tejidos blandos con un cierre por primera intención. Posteriormente a la colocación del implante, se esperaron 3 ó 4 meses a que ocurriera el proceso de oseointegración para colocar una corona sobre dicho implante.
El paciente firmó su consentimiento informado por escrito para la colocación inmediata del implante. Dentro de la planificación, se contempló realizar: la fase I periodontal tres semanas antes de la cirugía, que consistió en el raspaje y pulido de los dientes usando curetas y raspadores (Hu Friedy); y se realizó en dos sesiones, cada semana. Luego se procedió a la extracción del diente incisivo central superior derecho con colocación de plasma rico en fibrina.
Se prescribió medicación preoperatoria una hora antes del procedimiento: 1g de Amoxicilina como profilaxis antibiótica, 4mg de Dexametasona y 400mg de Ibuprofeno. La zona a operar (zona anterior del maxilar superior, incisivo central superior derecho) se anestesió localmente con lidocaína a 2 % con epinefrina 1:80000. Se realizó la exodoncia atraumática con periótomos para preservar la pared ósea vestibular, sin elevación del colgajo mucoperióstico. Se eliminó todo el tejido de granulación del alveolo y los restos de ligamento periodontal y se irrigó con suero fisiológico. (Figura 2A, 2B).
Para acelerar la cicatrización de los tejidos blandos, se colocó PRF con el protocolo planteado por Choukroun.12) (Figura 2C). La fibrina se obtuvo extrayendo sangre de la vena del paciente, se centrifugó y se esperó que la sangre se coagulara, luego se separó el coágulo de fibrina que se forma en la parte media alta del tubo del coágulo de eritrocitos en la parte inferior del tubo; cuidadosamente se realizó un raspado del coágulo para eliminar los eritrocitos y quedó la fibrina utilizada para rellenar el alveolo.
Se realizó la sutura con seda negra 4/0 con puntos simples y se confeccionó una corona provisional fijada con alambre ortodóntico y resina a los dientes adyacentes.

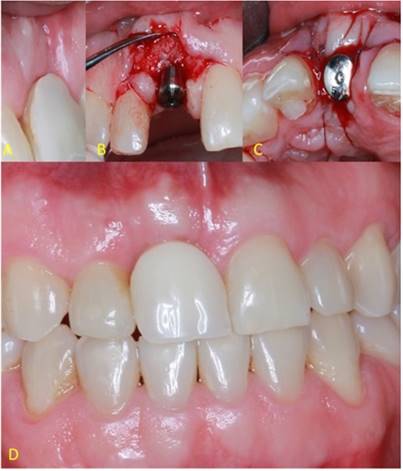
Fig. 2 A: Remanente radicular. B: Alveolo postextracción, con tejido blando y duro intacto. C: Colocación de PRF dentro del alveolo. D: Levantamiento del colgajo para colocación del implante. E: Radiografía de control inmediatamente colocado el implante.
A los 7 días se realizó un control y se mostró una cicatrización favorable de los tejidos blandos, así como una estética aceptable de la corona provisional. Una vez pasadas las 6 semanas, se procedió a la colocación del implante. Se anestesió la zona con Lidocaína, la misma usada el día de la extracción. Se realizó una incisión supracrestal hacia palatino a espesor total con hoja de bisturí N° 15, con dos liberantes preservando las papilas. Posteriormente se realizó el decolado a espesor total y deflexión total con una legra P24G (Figura 2D). Una vez elevado el colgajo en su totalidad, se procedió con el fresado progresivo convencional siguiendo las paredes óseas palatales y se utilizaron las dimensiones de la raíz del diente extraído para confirmar el largo y el diámetro del implante. Se inició a 1 200 rpm y disminuyendo a 1 000 rpm y con 35 Ncm de torque. Se procedió a colocar el pin de paralelismo (Figura 2E) para después insertar el implante seleccionado en el hueso con una inicial de 40 Ncm. El asiento final se completó con una llave de mano. El implante seleccionado fue de la marca Neobiotech ISII, de 4 mm de diámetro por 13 mm de longitud a un torque de ingreso de 40 Ncm. Se hizo una radiografía de control en la cual se apreció el implante colocado en una adecuada posición. Se hizo la sutura con ácido poliglicólico 4/0 con puntos simples y se procedió a colocar el provisional nuevamente para manejar correctamente los tejidos blandos.
Seguimiento y resultados
Se evaluaron los siguientes parámetros clínicos al cabo de 2 meses de control: placa bacteriana, índice de sangrado en cuatro superficies alrededor del implante, supuración y dolor. Los valores de los parámetros fueron negativos. Radiográficamente se evidenció una correcta integración del implante al hueso, con imagen radio opaca y continua alrededor del implante.
Después de 4 meses del proceso de oseointegración, se observó una depresión en el tejido blando vestibular (Figura 3A), por lo que se procedió a realizar un injerto de tejido conectivo subepitelial con el fin de aumentar el volumen del tejido para mejorar la estética de esa zona (Figura 3B) y al mismo tiempo colocar el pilar de cicatrización (Figura 3C) de 5 mm de diámetro y 3 mm de cuff. El sitio donante del injerto fue el paladar, la incisión fue a 90° con hoja de bisturí N°15 y luego se decoló a espesor parcial con otra hoja de bisturí N°15. Para el decolado se usó a la vez la legra p24 y cuidadosamente se manipuló el tejido donante. La cavidad del sitio donante se cerró con sutura de ácido poliglicólico 4/0. El injerto se desepitelializó y solo quedó tejido conectivo, el cual se colocó en el sitio receptor.
En el sitio receptor se realizó una incisión paracrestal y sulcular para conservar las papilas a bisel interno y deflexión total. Se colocó el injerto de tejido conectivo suavemente a la altura de la cresta alveolar y del pilar de cicatrización. Se suturó sin presión con sutura de ácido poliglicólico 4/0 para impedir la contracción de la herida y se esperaron 2 semanas.
Después de retirar los puntos a los 14 días, se evidenció un aumento del tejido blando vestibular y es en este punto donde se empezó a acondicionar el tejido blando con coronas provisionales sobre implantes. A los 2 meses de acondicionar el tejido blando para lograr un perfil de emergencia estético, se colocó la corona metal cerámica definitiva. Pasados 6 meses del tratamiento desde la extracción dental, se evidenció una mejora notable en los aspectos clínicos y radiográficos. En el aspecto clínico, se evidenció una correcta conformación de tejidos blandos, tanto de las papilas interdentarias, así como el grosor o biotipo gingival. La colocación de PRF, permitió la cicatrización adecuada de los tejidos blandos, y el cierre por primera intención al momento de colocar el implante dental. El tratamiento de engrosamiento gingival con tejido conectivo subepitelial mostró un aumento significativo del biotipo gingival vestibular, y se aseguró un correcto perfil de emergencia y como mecanismo de protección ante recesiones gingivales. (Figura 3D).
Discusión
La colocación temprana de implantes es defendida por muchos autores como un protocolo alternativo al protocolo convencional de implantes. 13 Este procedimiento requiere muchos factores, como la cicatrización rápida del tejido duro y blando, la estabilidad del implante, la estética alrededor del implante y la rehabilitación de este. El objetivo de un implante temprano es preservar la arquitectura del tejido blando y evitar la reabsorción ósea producida por las extracciones.
En el presente caso, se realizó un implante temprano postextracción de un incisivo central superior con fractura cervical; con un seguimiento de más de 8 meses se logró la carga del implante con una restauración definitiva de porcelana, considerando la estética como elemento fundamental en estos tratamientos, para lo cual se colocó un injerto de tejido conectivo y corona provisional para conformar un buen perfil de emergencia.
El uso de injertos de tejido blando y rellenos óseos se indican para favorecer el proceso regenerativo de implantes dentales o para evitar la presencia de defectos periimplantarios a futuro.14) Los injertos conectivos y los injertos de tejido queratinizado son opciones seguras pues presentan tasas de infección bajas y no son rechazados por el tejido receptor.15 Sin embargo, estas técnicas requieren una considerable experiencia e implican un aumento quirúrgico de la morbilidad, ya que necesitan un sitio donante.
Se podrían utilizar membranas aloplásticas para cubrir la zona a regenerar, pero también se pueden usar las membranas a base de PRF, pues es un producto económico y material autógeno de fácil obtención. Ya se ha demostrado que de la membrana PRF se liberan lentamente cantidades significativas de factores de crecimiento (TGF ß1, PDGF-AB, VEGF) y trombospondina- 1 (TSP-1) durante, al menos, 7 días.16 Además, se han utilizado para reemplazar el tejido conectivo en cirugía periodontal. La membrana PRF es un material autógeno con propiedades que benefician a los tejidos regeneración, que hace más fácil su manipulación alrededor de pilares protésicos durante el montaje. Puede usarse como una barrera protectora para material aloplástico.17
La colocación de implantes dentales está directamente relacionada con el volumen del hueso alveolar restante. Esto depende del cierre primario de la herida y la condición del hueso adyacente. Además de que exista un buen flujo de sangre, factores de crecimiento y promotores necesarios para la cascada de biomineralización osteogénica. Es aquí donde los derivados plaquetarios ayudan a la angiogénesis. El uso del PRF en los procedimientos de aumento alveolar es beneficioso para un mejor cierre de la herida y una recuperación más rápida de los tejidos blandos.18 En el presente caso, no se evidenciaron complicaciones, probablemente porque el implante se cargó después de 4 meses, lo cual otorgó un tiempo suficiente para la oseointegración del implante, y, a la vez, porque este logró una estabilidad primaria al inicio. Estos dos factores favorecen el éxito en el tratamiento de implantes inmediatos y tempranos.
Es recomendable que antes de una colocación de implante temprano o de cualquier cirugía se debe dar una medicación preoperatoria que consista de antibióticos, antiinflamatorios, analgésicos y corticoides. Otra recomendación antes de colocar un implante temprano es usar terapias alternativas para la cicatrización del alveolo después de una extracción; este es el caso de los factores de crecimiento derivados de plaquetas (PDGF-BB) que tienen un papel importante en la regulación de las actividades de las células mesenquimáticas y, a la vez, logran que las células del ligamento periodontal proliferen más rápidamente.18 Una última recomendación es observar si la zona de la extracción es o no de tejido infectado; mucho se ha dicho que colocar un implante inmediato en sitios infectados está contraindicado, pero hay estudios que disienten de esta hipótesis. En este caso, el diente a extraer presentaba una patología periapical, la cual fue removida por completo al momento de la extracción; después de 4 meses de insertado el implante no se detectaron complicaciones o cambios en el hueso o tejido blando debido a la patología.
Conclusiones
En el presente caso, se presentó la opción de un implante inmediato en una zona con infección periapical que requirió la combinación de plasma rico en fibrina e injerto conectivo en el lecho quirúrgico. La combinación favoreció la cicatrización estética del tejido blando periimplantario sin evidenciarse complicaciones durante el posoperatorio.