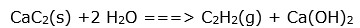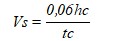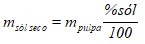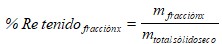INTRODUCCIÓN
Los hidróxidos son compuestos ternarios formados por la disolución de un óxido metálico en agua, poseen propiedades para aplicaciones industriales y tecnológicas, ya sea en la biomedicina (Kum et al., 2013), los dispositivos electrónicos (Irimia-Vladu, 2014), en energía solar (Lewis et al., 2014), la detección de gases (Henderson et al. 2014). Los hidróxidos se forman por la unión mediante enlaces iónicos entre un catión metálico y un anión. Al unirse el anión OH- se combina con el catión calcio (Ca2+) forma el Ca(OH)2 también conocido como cal apagada, un polvo blanco que presenta baja solubilidad en agua (1,2 g/L a 25 °C) e insolubilidad en alcohol. Es obtenido al hidratar el óxido de calcio convirtiéndose en Ca(OH)2 (Fava y Saunders, 1999).
En Cuba, muchas industrias para obtener un producto específico tienen que desechar residuos que son transportados hacia vertederos, incrementando la contaminación ambiental. Muchos de esos residuos pudieran destinarse para otros usos, en dependencia de sus características. Una de estas industrias es la fábrica de gases industriales, que genera acetileno, como resultado de la interacción entre el carburo de calcio y el agua; este no es el único producto de tal reacción química, ya que viene acompañado por el hidróxido de calcio. Sin embargo, debido a que el hidróxido se encuentra como pasta no puede ser comercializado y es desechado, derivando problemas ambientales.
Refieren Poggi et al. (2016) que el carburo de calcio, fuente para la producción de acetileno, se produce por la reducción de caliza de alta calidad mediante coque seleccionado y sometido a elevadas temperaturas en hornos eléctricos. La producción tiene lugar en equipos generadores, donde la reacción del carburo con agua genera el acetileno, obteniéndose el hidróxido de calcio.
De acuerdo con Álvarez (2014) por cada tonelada de carburo de calcio (CaC2) que se utiliza en la producción de acetileno se obtiene una de hidróxido de calcio Ca(OH)2. El lodo proveniente de la producción del acetileno (conocido indistintamente por fangos de carburo, lodos de cal, cieno de cal, cal de acetileno, lodo de acetileno o desecho de la producción del acetileno) es un hidrato de cal, masilla de cal o lechada de cal que se genera durante la producción del acetileno, a partir del carburo de calcio, según la reacción (1):
Carburo de calcio agua acetileno hidróxido de calcio
Este producto se puede encontrar de las tres formas señaladas anteriormente, ya que del reactor sale en concentraciones muy bajas, durante la decantación o sedimentación va perdiendo el agua y se convierte en una pasta o masilla y, por último, en un polvo, o sea un hidrato de cal que con el tiempo, expuesto a la intemperie, llega a carbonatarse convirtiéndose nuevamente en un carbonato de calcio para cerrar el ciclo de la cal.
Han planteado Giorgi et al. (2010) y Baglioni et al. (2014) que el Ca(OH)2 posee propiedades que ayudan a la conservación de pinturas y obras de arte. Tras la carbonatación, las partículas forman una capa de revestimiento homogénea que consolida y fortalece la superficie debilitada, disminuyendo el envejecimiento y evitando la oclusión de los poros superficiales. Las propiedades estéticas, como el color, se ven mínimamente afectadas.
El objetivo de este estudio es caracterizar química, física, granulométrica y mineralógicamente el residuo industrial hidróxido de calcio generado en el proceso de fabricación de acetileno, con la finalidad de elaborar yeso para aplicación industrial y médica.
DESARROLLO EXPERIMENTAL
Procesamiento de las muestras de hidróxido de calcio
Para la preparación de las muestras a caracterizar para el estudio granulométrico, de velocidad de sedimentación y de neutralización del carburo con ácido sulfúrico se utilizaron materiales y utensilios de laboratorio. Se empleó ácido sulfúrico con una pureza del 98 % y una densidad de 1,83 kg/L.
Equipamiento utilizado
Agitador eléctrico IKA RW 20 DZM para mezclas: líquido-sólidas y líquido-líquido
pH metro Hl 9126 para la determinación del grado de acidez en líquidos y pulpas.
Campana de extracción de gases MRC-FH-15 para la extracción de los gases generados en los experimentos.
Bomba de vacío Vacuubrand MZ 2C NT para la separación líquido-sólido.
EstufaDyanmica para el secado de las muestras sólidas.
Balanza digital ADWAG-WLC 10/A2 para el pesaje de muestras sólidas y líquidas.
Espectrofotómetro de Absorción Atómica ContrAA 300 Analytikjena para la determinación de concentraciones en soluciones.
Difractómetro X'PERT3 de PANalytical para la determinación de las fases mineralógicas presentes en un sólido.
Preparación de las muestras
Las muestras de carburo fueron filtradas, secadas y trituradas antes de someterse a la caracterización química y mineralógica. Las otras muestras del producto fueron sometidas a la misma preparación incluyéndole el lavado en el momento del filtrado. Para la determinación de la velocidad de sedimentación se realizó el procedimiento siguiente según la Norma Cubana NC-186 (2002):
Homogenización de la pulpa.
Se tomaron tres muestras de 50 mL para determinar humedad (pesar y filtrar, anotar y secar a 80 oC hasta peso constante, anotar).
Medición y pesaje de 1 L de pulpa, agitar y comenzar a leer la altura de la interfase en intervalos de tiempo conocidos, hacer esta operación en tres probetas en paralelo.
Dejar la pulpa en reposo 24 horas y leer la densificación.
Para calcular la velocidad de sedimentación, se consideró como altura crítica aquella donde se mantuvo sin variación la lectura, siendo el tiempo transcurrido donde se observó dicho fenómeno el tiempo crítico. Esta velocidad se calculó como (2):
Donde:
Vs: velocidad de sedimentación; m/h
hc: altura correspondiente a la lectura donde comienza a hacerse constante la altura de la interfase, mm
tc: tiempo correspondiente a la altura hc
0,06: factor de conversion.
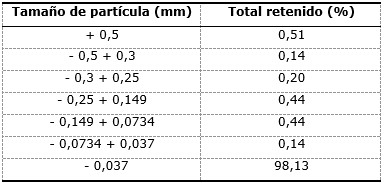
Para la granulometría se escogieron seis tamices con diferentes tamaños de abertura (0,5; 0,3; 0,25; 0,149; 0,074 y 0,037 mm) (Norma Cubana 178, 2002). Se partió de 500 mL de pulpa de carburo y de 500 g del producto obtenido seco. En el caso del carburo la pulpa fue pesada para, conociendo el porcentaje de sólido, calcular la masa de sólido base seca como (3):
El tamizado se realizó por vía húmeda, cada fracción fue secada a 80 oC hasta lograr un peso constante. Para el cálculo del porcentaje que representa cada retenido del total de muestra se utilizó la ecuación (4).
Para realizar la neutralización de las muestras de hidróxido de calcio se procedió a:
Homogenizar la pulpa de carburo,
Tomar muestra para análisis de laboratorio,
Tomar la muestra de pulpa para el ensayo a realizar (se anotó peso y volumen),
Se midió el pH,
Se mezcló con ácido sulfúrico con un flujo de 10 mL/min (se anotó hora de inicio),
Medición del pH cada 15 minutos (se anotó el valor y la hora),
Al alcanzar pH de 7 parar la alimentación de ácido y se agitó por 120 min (si se mantiene el pH parar el proceso, se encuentra por encima, repetir pasos del 5 al 8).
Al culminar la prueba se medió: pH, volumen, masa, se toma muestra para análisis granulométrico y de laboratorio.
Anotar volumen final del ácido y hora de terminación.
A través de la radiación monocromática se realizó la caracterización de los residuales mediante la aplicación de difracción de rayos X (DRX). Se analizó en el difractómetro una muestra de residual sin tratar, otra calentada a 500 oC y una tercera a 900 oC sin ácido sulfúrico; otras dos con el mismo procedimiento, pero con ácido sulfúrico. Para identificar las fases, los patrones de difracción fueron obtenidos usando fuente de radiación de cobre (CuKα, λ = 1,5418 Å), operado a 40 kV y 30 m, en un rango de 2θ = 10 ° - 50 °.
RESULTADOS Y DISCUSIÓN
Análisis de la composición química
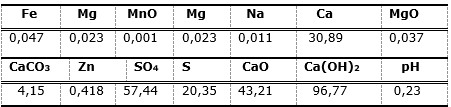
La composición química del residuo de acetileno se muestra en la Tabla 1. De acuerdo con lo establecido en la Norma Cubana 54-286 (1984), el resultado de composición del residual analizado cumple con las especificaciones del CaO y el MgO aprovechable, que es un parámetro que garantiza la pureza de este residual. La Tabla 2 muestra las características físicas del hidróxido de calcio; a menor tamaño y mayor porosidad se produce la hidratación de forma más rápida. El residual presenta la distribución granulométrica que se muestra en la Tabla 3.
En correspondencia con estas propiedades físicas, este residual cuenta con versatilidad que le proporciona diferentes características a partir del agregado de sustancias, con el fin de obtener una gama de productos para diferentes aplicaciones, como en humedad en forma de morteros, o en condiciones secas, en forma de láminas o placas, de acuerdo con lo establecido por la Norma Cubana NC 186 (2002).
Mineralógicamente, la obtención del Ca(OH)2 no sería posible sin el carbonato de calcio (CaCO3). La Tabla 4 muestra la caracterización mineralógica, en la cual se identificó en el residual alto contenido de carbonato de calcio e hidróxido de calcio, con impurezas de un compuesto de sulfato-fosfato de calcio hidratado. Esta propiedad en conjunto con la química debe estar equilibrada, con el objetivo de que, tras la cocción, el producto presente la dilatación y la resistencia mecánica exigidas.
Caracterización por rayos X (DRX)
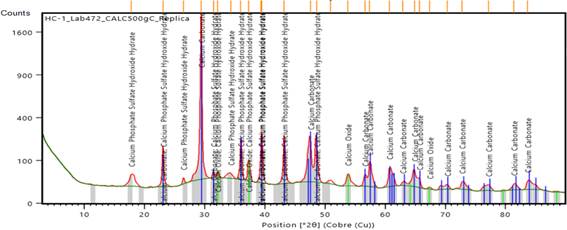
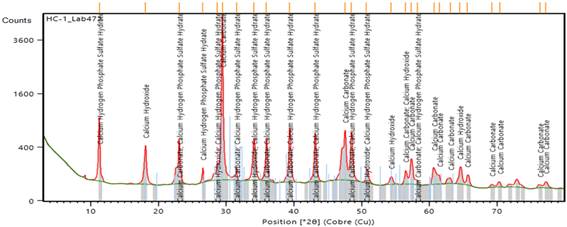
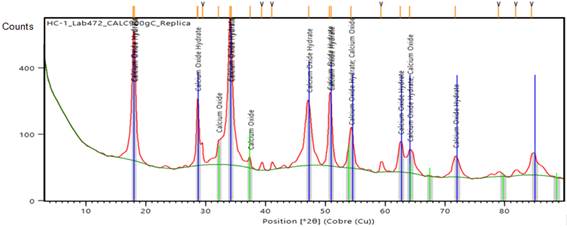
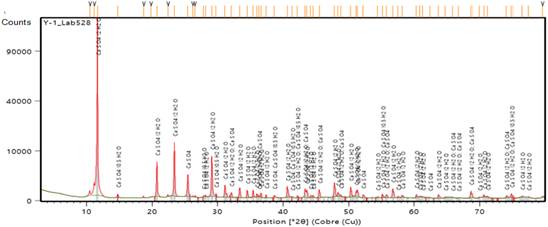
En la Figura 1 se muestra el difractograma con las fases obtenidas para la muestra de residual sin tratar con ácido sulfúrico. El difractograma de la Figura 2 es de la muestra calentada a 500 oC y el de la Figura 3 corresponde a la muestra calentada a 900 oC.
Los resultados de DRX indican que, en este residual existe una combinación de hidróxido de calcio y de hidrato de sulfato de fosfato de hidrógeno de calcio carbonato de calcio. La difracción del pico más alto se corresponde con la fase CaCO3, a 29,4° correspondiente con el plano (104), indicando el crecimiento de cristales de calcita. El patrón DRX muestra el reflejo de la calcita romboédrica con el espaciamiento d: 3,85; 3,03; 2,84; 2,49; 2,28; 2,09; correspondiente a hkl: 012, 104, 006, 110, 113, respectivamente.
Cuando el material es calentado a 500 oC, se produce la transformación del hidróxido de calcio en el óxido de hidrato de calcio y permanecen las demás fases sin alteración, sin embargo, a la temperatura de 900 oC, la transformación del residual transcurre con la pérdida de carbonato y agua para formar el óxido de calcio (CaO) en su forma tanto anhidra como hidratada; además, permanecen algunas impurezas formadas a partir de otros componentes minoritarios que contiene el material inicial.
Caracterización por rayos X de muestras tratadas con ácido sulfúrico
Para la caracterización del residual se realizaron tres experimentos de neutralización con ácido sulfúrico. Debido a esta reacción se obtuvo un producto con las características físicas siguiente: densidad del sólido de 1,90 kg/L y granulado de color blanco grisáceo, con una distribución granulométrica como se muestra en la Tabla 5. En la Tabla 6 se muestra la composición química.
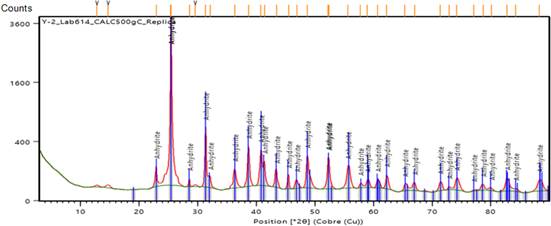
En las diferentes caracterizaciones del residual de acetileno se observa que existen modificaciones al ser neutralizado con el ácido sulfúrico. Por una parte, en la Figura 4 se muestra el difractograma obtenido de esta reacción. Mientras que en la Figura 5 se presenta el difractograma del residual neutralizado con ácido sulfúrico.
Según el difractograma de la Figura 4, el producto obtenido de la reacción del residual con el ácido sulfúrico está formado fundamentalmente por sulfato de calcio en diferentes formas estructurales. En el pico más intenso, que ha difractado a 11,3o se ha obtenido el sulfato de hidrato de calcio (CaSO4.2H2O), precedido por la formación del carbonato de calcio (CaCO3), el sulfato de calcio (CaSO4) y en otra fase el sulfato de hidrato de calcio (CaSO4.O.67H2O). En el de la Figura 5, luego de ser calentado el residual a 500 oC, pierde el agua de hidratación y ocurre una transformación total a la fase anhydrita con fórmula CaSO4.
Mediante la neutralización del carburo utilizando ácido sulfúrico se obtiene un producto con partículas finas, más del 97 % inferiores a 0,037 mm. Teniendo en cuenta las características químicas, físicas y mineralógicas se presupone se trata de yeso. La Tabla 7 muestra la comparación entre ambos materiales.
Al comparar las características del yeso con las del residual de acetileno neutralizado con ácido sulfúrico se puede plantear que la similitud entre ambos sugiere que el residual neutralizado es yeso, por lo que pudiera usarse como sustituto de este en sus distintas aplicaciones.
CONCLUSIONES
Al caracterizar el residual de acetileno se determina que la presencia del CaO y el MgO aprovechable permiten garantizar la pureza del material en función de obtener otros productos para ser empleados en la industria de la construcción, medicina y agricultura.
La caracterización del residual por difracción por rayos X, luego de calentado a 500 oC y 900 oC evidencia que independientemente de estar expuesto a estas temperaturas hay presencia de hidróxido de calcio, que permite mantener la basicidad del residual.
Los procesos de tratamiento del residual de acetileno, neutralizado con el ácido sulfúrico, permiten obtener un material con características similares a las del yeso.