INTRODUCCIÓN
La irrigación sanguínea del corazón se realiza a través de las arterias coronarias, las cuales tienen generalmente un trayecto epicárdico en sus ramos principales, de manera que recorren la superficie del miocardio. En algunos pacientes, pequeños segmentos de estas arterias se introducen en el espesor del músculo y tienen distancias variables de trayecto intramiocárdico, lo que produce una estrechez súbita de dicho segmento en cada sístole (efecto de compresión extrínseca o milking) -como consecuencia de la presión externa que realizan las fibras miocárdicas sobre la arteria-, que puede ser confundida con una estenosis ateromatosa o un espasmo coronario durante la coronariografía1.
La observación durante la diástole de una arteria de calibre normal o casi normal descarta dichos diagnósticos y confirma la presencia de esta peculiaridad anatómica, considerada una anomalía congénita, la cual se describió por primera vez por Reyman en 1737, y fue Polacek en 1961 quien le dio el nombre de «puente miocárdico» (PM) con el que se conoce en la actualidad1.
Se trata de una variante anatómica relativamente común en la población general, habitualmente benigna, que aqueja principalmente a pacientes con bajo riesgo para enfermedad arterial coronaria. No obstante, cuando es sintomática, se manifiesta en forma de angina estable o inestable, arritmias cardíacas (taquicardia ventricular y taquicardia supraventricular), infarto agudo de miocardio y muerte súbita, estos dos últimos de rara aparición2.
Su incidencia en numerosas series angiográficas es de 0,82 a 4%, mientras que en estudios autópsicos dirigidos es de 23 a 55%. La diferencia encontrada está en función, por una parte, de que no todos los puentes miocárdicos producen compresión sistólica, al menos detectable; y, por otra parte, de la oblicuidad, profundidad, o ambas, de las fibras. Pueden ser únicos o múltiples y aparecer aislados o coexistentes con otras lesiones coronarias3, y su localización más frecuente es en los segmentos medio y distal de la arteria descendente anterior (DA)4.
Esta variante anatómica está aún subdiagnosticada, en virtud de la poca cantidad de pacientes que presentan síntomas, de la falta de disponibilidad de métodos diagnósticos de mayor precisión y, consiguientemente, de su uso restringido, todo lo cual hace que sus mecanismos fisiopatológicos (más allá de la compresión extrínseca) y su tratamiento no hayan sido aun completamente esclarecidos3.
CASO CLÍNICO
Se presenta el caso de un hombre de 45 años de edad, mestizo, con antecedentes de ser fumador desde hace más de 30 años. Refiere que desde hace más o menos 1 mes, previo a la consulta, viene presentando dolor precordial opresivo que ha aumentado su frecuencia, intensidad y duración sobre todo, relacionado con el esfuerzo físico e irradiado a brazo izquierdo, cuello y mandíbula, por lo que acudió al cuerpo de guardia.
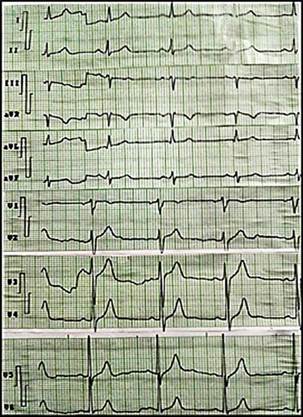
Al examen físico no hubo ningún dato positivo, la frecuencia cardíaca y la presión arterial fueron de 72 latidos por minuto y 120/80 mmHg, respectivamente. El electrocardiograma mostró ondas T altas y simétricas de V2-V6 (Figura 1), sin presentar cambios en los electrocardiogramas seriados que se le realizaron. Con este cuadro clínico y los hallazgos electrocardiográficos encontrados, se interpretó como un síndrome coronario agudo sin elevación del segmento ST y se decidió su ingreso en la Sala de Cardiología para estudio y tratamiento.
Los exámenes de laboratorio mostraron: troponinas, creatin-fosfoquinasa total y su fracción MB negativas. El resto de la analítica sanguínea resultó estar también dentro de los límites normales con glucemia en 5,4 mmol/L, creatinina 108 µmol/L, colesterol 3,4 mmol/L y triglicéridos 1,12 mmol/L.
Al tener en cuenta el resultado negativo de los biomarcadores de necrosis miocárdica, se definió que el paciente presentaba una angina inestable. Se le realizó ecocardiograma transtorácico que resultó ser normal, sin trastornos de contractilidad global y segmentaria del ventrículo izquierdo en reposo, con fracción de eyección de 64% y dimensiones de las cámaras cardíacas y los grandes vasos normales.
El paciente presentó recurrencia del dolor a pesar del tratamiento antiisquémico impuesto, por lo que se decidió realizar coronariografía la cual informó que las arterias coronarias epicárdicas (tronco coronario izquierdo, DA, circunfleja y coronaria derecha) y sus principales ramas no presentaban lesiones significativas. Además informa que la DA es un vaso de buen desarrollo con presencia de un PM de aproximadamente 30 mm que ocupa parte de los segmentos medio y distal del vaso (Figura 2).

Figura 2 Coronariografía izquierda en vista anteroposterior. A. Arteria descendente anterior de aspecto normal durante la diástole ventricular.B. Compresión extrínseca (milking) de 31,75 mm en segmento medio-distal durante la sístole.
Con este diagnóstico angiográfico se reajustó el tratamiento y se añadió atenolol 25 mg/día y amlodipino 10 mg/día, con lo que se logró la mejoría de los síntomas y el egreso del paciente, quien ha mantenido seguimiento por la especialidad, en consulta externa, durante lo cual la evolución ha sido favorable.
COMENTARIOS
La controversia sobre la capacidad del PM para ocasionar isquemia miocárdica depende del grupo de pacientes analizados5.Su expresividad clínica es variable y deriva del grado de afectación del flujo coronario6. Cuando la compresión sistólica de la luz del vaso supera el 50%, y especialmente el 70%, la reserva coronaria se halla siempre reducida5. La mayoría de los casos cursan de forma asintomática y cuando hay expresión clínica el principal síntoma es el dolor torácico, tanto de esfuerzo como de reposo, y el espectro puede variar desde angina a infarto agudo de miocardio o muerte súbita6.
El caso clínico que se describe presenta un PM largo con reducción sistólica significativa del calibre del vaso y una presentación clínica como síndrome coronario agudo sin elevación del segmento ST, definido como angina inestable.
La fisiopatología del PM deriva de las diferentes fuerzas biomecánicas que se generan en su seno y que repercuten en los segmentos adyacentes. Así, las manifestaciones histopatológicas encontradas difieren entre el segmento tunelizado y aquellos que se sitúan proximal y distal a este. En el segmento proximal existe una propensión al desarrollo de arteriosclerosis que se atribuye principalmente a alteraciones en la dinámica de fluidos como es la baja tensión de cizallamiento que genera el PM a este nivel. También podría influir el estrés mecánico proximal generado por la compresión arterial dentro del PM y la angulación con la que el vaso se introduce en el miocardio. En el segmento tunelizado, es habitual observar un remodelado vascular constrictivo, pero sin enfermedad ateromatosa asociada. En cuanto a la obstrucción dinámica, se ha documentado que la isquemia miocárdica no se relaciona exclusivamente con la compresión vascular sistólica, sino que esta persiste en meso-telediástole7, porque no se produce una relajación adecuada de esta, lo que puede producir una alteración del flujo diastólico6.
El método de referencia para el diagnóstico es la coronariografía. El comportamiento del PM en la angiografía y su impacto hemodinámico depende del grosor, la profundidad y la longitud del trayecto, así como de la orientación de la arteria y las fibras musculares, y de la naturaleza del tejido existente entre ambas. El hallazgo angiográfico es una estenosis sistólica que desaparece durante la diástole, de manera que la observación durante esta fase del ciclo cardíaco, de una arteria de calibre normal, confirma el denominado PM6.
La longitud del puente miocárdico suele estar comprendida entre 4 y 25 mm, y la arteria más frecuentemente afectada es la DA en su tercio medio y distal; y, con menos frecuencia, las ramas diagonales y marginales1. En el caso clínico que se presenta también es la DA la arteria afectada en los segmentos mencionados, aunque con la peculiaridad de que la longitud del trayecto es bien largo, de aproximadamente 30 mm, lo que se supone que contribuye a la afectación de la reserva coronaria y su consiguiente expresión clínica.
El aumento de la frecuencia cardíaca, la contractibilidad y la velocidad de flujo, el tiempo de perfusión diastólico corto y el espasmo coronario inducido por el ejercicio pueden causar angina en pacientes con PM. Al tener en cuenta esto, el tratamiento de primera línea consiste en aumentar la dosis de fármacos como los betabloqueantes, debido a su efecto inotrópico y cronotrópico negativo6. Una buena alternativa son los antagonistas del calcio, que añaden además propiedades vasodilatadoras7. De manera general, en estos pacientes se debe evitar el uso de vasodilatadores puros como los nitratos, debido que aumentan el grado de estrechamiento sistólico de los vasos y disminuyen el umbral isquémico, lo que pudiera agravar los síntomas6,7.
El paciente presentado tuvo buena respuesta al ajuste terapéutico (betabloqueadores y antagonistas del calcio), pues mejoró su sintomatología tras la introducción de estos medicamentos en su tratamiento de base.
Conocer esta variante anatómica favorece la aplicación de un tratamiento específico o bien optimizar el previo, lo cual es muy importante porque puede condicionar su pronóstico.
CONCLUSIONES
A pesar de que en muchos pacientes el puente miocárdico puede cursar de forma asintomática o presentar síntomas leves, en algunos casos -como el que se presenta en este artículo-, puede causar un síndrome coronario agudo relacionado con factores desencadenantes, y requerir hospitalización y reajuste del tratamiento.