INTRODUCCIÓN
Las enfermedades cardiovasculares son un problema sanitario global. La Organización Mundial de la Salud informa que en el año 2016 fallecieron en el mundo 17,8 millones de personas por esta causa y el 52,8% fue atribuida a la cardiopatía isquémica1. El riesgo de muerte y complicaciones tras un infarto agudo de miocardio con elevación del segmento ST (IAMCEST) es elevado, a pesar de los avances en el diagnóstico y tratamiento. Según informes de la American Heart Association, cada 40 segundos un norteamericano sufre un infarto agudo de miocardio (IAM)2. En Europa la mortalidad intrahospitalaria de los registros nacionales en los países pertenecientes a la Sociedad Europea de Cardiología está entre 4-12%, mientras que la mortalidad al año es de un 10% aproximadamente3.
El 80% de las muertes por infarto de miocardio se producen en los países de ingresos medios y bajos4. En Cuba el IAM constituye un importante problema de salud ya que la tasa de mortalidad por enfermedades del corazón en el 2018 alcanzó la cifra de 228,6 por cada 100000 habitantes y el 63,3% de estas muertes correspondieron a la cardiopatía isquémica. En relación al IAM, la tasa de mortalidad fue de 65,3 por cada 100000 habitantes, lo cual representa un 45,2% de las muertes por esta causa5.
El pronóstico de los pacientes con IAMCEST se relaciona con la probabilidad de desarrollar complicaciones a corto o largo plazo, y depende en mayor medida de las condiciones al ingreso que de los factores de riesgo coronario previos2,4. Según las guías internacionales de tratamiento del IAM, las condiciones asociadas con una peor evolución son: edad avanzada, desarrollo de algún grado de insuficiencia cardíaca, función ventricular izquierda disminuida, diabetes mellitus, estrategia de tratamiento utilizada y tipo de hospital en que es atendido el paciente2,4,6.
Los avances en el tratamiento del IAM en las últimas décadas permiten ofrecer a los pacientes múltiples opciones terapéuticas en función de la gravedad de la enfermedad y su pronóstico. Determinar este, con la mayor exactitud posible, sigue siendo un objetivo importante. Dadas las limitaciones de los algoritmos actuales se hace necesario continuar la investigación en este campo y concentrar así los esfuerzos y gastos en los pacientes con mayor riesgo, de tal manera que puedan mejorarse los índices riesgo-beneficio y costo-efectividad7,8.
PUNTUACIONES O ESCALAS (SCORES) DE RIESGO
Los estudios encaminados a desarrollar una fórmula que permita cuantificar el riesgo de muerte o complicaciones de un paciente con IAM, mediante una puntuación o score, se remontan a inicios de la década de 19509. Con la aparición de las primeras unidades coronarias se incrementaron los esfuerzos en este sentido10.
En los últimos años se han desarrollado modelos o algoritmos de predicción que integran variables clínicas, electrocardiográficas, angiográficas y biomarcadores, en un intento por hacer más exacta la evaluación del riesgo11-13. A pesar de la gran variedad de modelos que se han propuesto y de la sencillez de algunos de ellos, su utilización está muy limitada en la práctica clínica, ya que depende en gran medida de las características de la población en base a la cual se diseñó.
La conducta inicial ante un IAM está estandarizada en el mundo según las guías internacionales de tratamiento y los países de altos ingresos se ajustan a ellas2,4. A pesar de esto, en los países de medianos y bajos ingresos es menos probable que estas guías2,4 puedan ser aplicadas; lo cual ha sido demostrado por Shimony, et al.14, quienes encontraron que los pacientes de países con ingresos medianos y bajos tienen menor probabilidad de ser tratados con intervencionismo coronario percutáneo (ICP) que los de altos ingresos (4,9 vs. 45,6%; odds ratio [OR]=0,06; intervalo de confianza [IC] al 95%: 0,02-0,16). La terapia trombolítica, por el contrario, fue mayoritariamente empleada en países de medianos y bajos ingresos (72,5 vs. 38,9%; OR=4,2; IC 95%: 2,4-7,1). Estas disparidades en el tratamiento del IAMCEST a nivel mundial se evidencian en la mortalidad, que es superior en estos países en relación con los de altos ingresos4.
Un estudio que evaluó las diferencias regionales de mortalidad por IAM a los dos años, mostró que las mayores tasas se encuentran en América Latina (7,4%) y las inferiores, en el norte de Europa (2,5%)15. Las diferencias en cuanto a las opciones terapéuticas para este tipo de pacientes obligan a los países de medianos y bajos ingresos a buscar alternativas de estimación de riesgo que les permitan optimizar los recursos existentes en aras de disminuir la mortalidad.
La estratificación de riesgo se define como un proceso estadístico para determinar las características detectables relacionadas con un riesgo incrementado de eventos no deseados16. Todos los scores de riesgo diseñados tienen sus fortalezas y debilidades, y son aplicables a las poblaciones de las que se derivan. El Global Registry of Acute Coronary Events (GRACE)17) es el mejor estudiado y validado18 en el mundo, pero contiene elementos no disponibles en muchos países de medianos y bajos ingresos como las troponinas. Por otra parte, incluye variables cuantitativas y requiere de un ordenador para su cálculo, pues su aplicación en un nomograma en papel no es adecuada19. El Thrombolysis in Myocardial Infarction (TIMI) Risk Score20 es un modelo fácil de aplicar, pero fue diseñado en el curso de ensayos clínicos por lo que su utilidad en el mundo real ha sido cuestionada21. Asimismo, D'Ascenzo et al.18 muestran, en un metaanálisis, que el TIMI y el GRACE son los únicos scores que se han validado ampliamente; no obstante, el TIMI mantiene menor capacidad predictiva (C=0,77) en comparación con el GRACE (C=0,82).
Evolución de la atención al síndrome coronario agudo
En los últimos 30 años el número de muertes por IAM ha tenido un descenso progresivo que se ha estabilizado en la última década2,6. Las mejoras en el tratamiento del IAM han tenido lugar en varias etapas22. En la primera mitad del siglo XX se llevó a cabo la fase de observación de la asistencia coronaria que incluyó el registro de datos clínicos y de laboratorio, con poca intervención terapéutica23. Posteriormente, a mediados de los años 60, comenzaron las unidades de asistencia coronaria; cuyo objetivo fue la detección de arritmias cardíacas mediante la monitorización electrocardiográfica continua y su tratamiento de cardioversión o desfibrilación, con lo que se logró una reducción importante de la mortalidad. La fase de tecnología avanzada se inició con el catéter de flotación de Swan y Ganz para la arteria pulmonar, lo que dio lugar a la monitorización invasiva. Con posterioridad le sucede la etapa de la fibrinólisis y el ICP10. Todas estas mejoras en el tratamiento permitieron una mayor supervivencia en pacientes con síndrome coronario agudo, por lo que se hizo necesaria una adecuada estratificación de riesgo para la aplicación de los diferentes recursos terapéuticos existentes23.
Los primeros estudios sobre esta estrategia en la década de 19509 incluían variables clínicas muy sencillas y no fue hasta los años 1980 cuando comienzan a incluirse en la estratificación pronóstica variables como la fracción de eyección del ventrículo izquierdo (FEVI) y la gravedad de la enfermedad arterial coronaria7. En la actualidad la asistencia a los pacientes con IAMCEST ha entrado en la etapa de la medicina basada en la evidencia24, donde cada vez influyen más las guías internacionales en la conducta a seguir con estos pacientes. Desafortunadamente, todos los recursos sugeridos en estas guías2,4 no siempre están disponibles en los países de medianos y bajos ingresos; ni son accesibles para todos los pacientes.
Pathologic Index Rating9
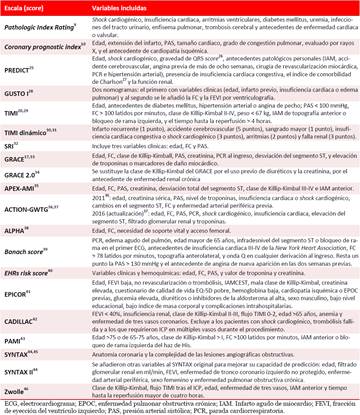
Es una de las primeras escalas que aparecen en la literatura, en el año 1953. Las variables incluidas en esta9 y en las demás escalas10,17,20,25-46 se muestran en la tabla. Pathologic Index Rating muy pronto fue superada con el advenimiento de la monitorización cardíaca y la aparición de las primeras unidades coronarias7.
Coronary prognostic index10
Fue publicado en 1969, tras la aparición de esas primeras unidades coronarias. Las variables incluidas se muestran en la tabla. Con el advenimiento de las nuevas tecnologías esta escala quedó en desuso.
PREDICT (Predicting Risk of Death in Cardiac Disease Tool)25
Esta escala fue publicada en el año 1999. Se diseñó en pacientes del Minnesota Heart Survey, entre los años 1985 y 1990. Predice la mortalidad a los treinta días, y a los dos y seis años. Sus variables predictoras25-27 se incluyen en la tabla. El área bajo la curva (ABC) en el diseño del PREDICT fue de 0,79 para mortalidad a los 30 días. Este score, que se aplica en un nomograma en papel, fue rápidamente sustituido ya que tiene un diseño antiguo y muy complejo, e incluye el cálculo de otras dos escalas.
GUSTO I (Global Utilization of Streptokinase and TPA [alteplase] for Occluded Coronary Arteries)28
Fue publicado en el año 2000. Se llevó a cabo en 15 hospitales de Estados Unidos, Europa, Israel, Australia y Nueva Zelanda. No incluyó países de ingresos bajos y medianos ni de Latinoamérica. Se obtuvieron dos nomogramas, con las variables que se muestran en la tabla, para predecir mortalidad a los 30 días y al año. Es un score difícil de aplicar por el uso de la ventriculografía y fue sustituido por el TIMI20. Por otra parte, el GUSTO-I no predice la mortalidad intrahospitalaria, pues solamente puede ser aplicado para los 30 días, y hay que recalcularlo para predecir la mortalidad al año en los pacientes que sobreviven a esos primeros 30 días después del IAM28.
TIMI (Thrombolysis in Myocardial Infarction)20
El TIMI es una de las escalas más aplicadas. Fue originalmente diseñado en 14114 pacientes del ensayo The Intravenous nPA (lanoteplase) for Treatment of Infarcting Myocardium Early II (InTIME II) Trial que incluyó 855 hospitales de Alemania, Argentina, Austria, Bélgica, Brasil, Canadá, Chile, Dinamarca, Eslovaquia, Eslovenia, España, Estados Unidos, Finlandia, Francia, Holanda, Hungría, Irlanda, Letonia, Lituania, México, Noruega, Polonia, Portugal, Reino Unido, República Checa, Rumanía, Rusia, Sudáfrica, Suecia, Suiza y Uruguay. De América Latina solo se incluyeron 407 pacientes (2,8%). El TIMI excluye en su diseño pacientes con presión arterial sistólica (PAS) > 180 mmHg y diastólica >110 mmHg, con shock cardiogénico, pacientes con riesgo aumentado de sangrado e incluyó solo pacientes elegibles para terapia fibrinolítica con nPA (Lanoteplase). Los autores reconocen en las limitaciones que los pacientes excluidos son los de mayor probabilidad de complicaciones. Las variables predictoras incluidas en el TIMI se muestran en la tabla. De igual forma, se ha descrito que infraestima el riesgo de muerte en pacientes que no reciben terapia de reperfusión (ABC 0,65)29. El TIMI se ha ajustado para riesgo de mortalidad intrahospitalaria, a los treinta días, a los seis meses y al año. Este score ha sido ampliamente validado internacionalmente18) y muy empleado, por ser de fácil aplicación a la cabecera del paciente. A pesar de ello, es una escala diseñada fundamentalmente en pacientes que recibieron tratamiento fibrinolítico con fármacos específicos de fibrina, no disponibles en Cuba, y su capacidad de predicción es inferior a otras escalas.
TIMI dinámico30
El TIMI dinámico es una modificación realizada al TIMI original20 que se basa en el incremento del riesgo de muerte que pueden aportar las complicaciones intrahospitalarias desarrolladas. Las variables añadidas se muestran en la tabla. El score se desarrolló en la base de datos del Enoxaparin and Thrombolysis Reperfusion for Acute Myocardial Infarction Treatment (ExTRACT-TIMI 25) que incluyó 20506 pacientes de 674 hospitales en 48 países. La validación se realizó en 1829 pacientes de los 3534 con IAMCEST del Trial to Assess Improvement in Therapeutic Outcomes by Optimizing Platelet Inhibition with Prasugrel (TRITON)-TIMI 38. Este TIMI dinámico predice la mortalidad al año y mejora la estratificación de riesgo al egreso, ya que tiene en cuenta las complicaciones intrahospitalarias30. A pesar de lo atractivo de su simplicidad y la habilidad de incluir las mencionadas complicaciones, ha sido poco validado en la literatura y, principalmente, en pacientes incluidos en ensayos clínicos; por lo tanto, minuciosamente seleccionados y de bajo riesgo31.
SRI (Simple Risk Index)32
Es una herramienta sencilla que incluye tres variables clínicas (edad, frecuencia cardíaca [FC] y PAS) y se utiliza para predecir mortalidad a los 30 días, pero también puede ser útil para las 24 horas. Se diseñó y validó en la misma población que el TIMI (InTIME II) trial. Las variables se combinan mediante el uso de la fórmula FC × [edad/10]2/PAS. Además de la dificultad en el cálculo, el SRI mostró poca capacidad predictiva en pacientes mayores de 65 años.
GRACE (Global Registry of Acute Coronary Events)17
GRACE es la escala de riesgo mejor validada internacionalmente18 y la que sugieren las guías de tratamiento del IAM2. Originalmente se desarrolló en 94 hospitales de 14 países (Alemania, Argentina, Australia, Austria, Bélgica, Brasil, Canadá, España, Estados Unidos, Francia, Italia, Nueva Zelanda, Polonia y Reino Unido). Los pacientes incluidos mayormente utilizaron terapia fibrinolítica y un 45%, ICP. Las variables incluidas se muestran en la tabla. El GRACE fue diseñado para predecir mortalidad intrahospitalaria y a los seis meses17. Posteriormente fue validado en la predicción de eventos adversos a largo plazo33.
GRACE 2.034
El GRACE 2.0 es una reciente actualización del GRACE17 que lo hace más fácil de aplicar en la emergencia, al sustituir la clase de Killip-Kimbal por el uso previo de diuréticos y la creatinina, por el antecedente de enfermedad renal crónica. Este score se derivó de 2959 pacientes del registro francés de síndrome coronario agudo con y sin elevación del segmento ST, con un ABC de 0,82. A pesar de las mejoras realizadas para la mayor aplicabilidad del GRACE, se mantiene el uso de las troponinas, que no siempre están disponibles en países de medianos y bajos ingresos, y la necesidad de un ordenador para su cálculo, al tratarse de una escala cuantitativa34.
APEX-AMI (Assessment of Pexelizumab in Acute Myocardial Infarction)35
El APEX-AMI fue diseñado en 5745 pacientes para predecir mortalidad a los 90 días. El estudio excluyó a los pacientes con elevación del segmento ST en cara inferior sin infradesnivel en cara anterior, y a los que recibieron terapia fibrinolítica. Se desarrolló en 17 países con altos ingresos (Alemania, Australia, Austria, Bélgica, Canadá, Dinamarca, España, Estados Unidos, Francia, Italia, Nueva Zelanda, Países Bajos, Polonia, Portugal, República Checa, Suecia y Suiza) e incluyó 296 hospitales. Las variables incluidas se muestran en la tabla. Su cálculo puede realizarse por un nomograma en papel.
ACTION (Acute Coronary Treatment and Intervention Outcomes Network) -GWTG (Get With The Guidelines)36,37
El ACTION-GWTG es un registro contemporáneo de pacientes con IAMCEST y sin elevación del segmento ST en hospitales de Estados Unidos. En el 2011 se publicó su primera versión que se desarrolló en 248 hospitales. Este registro ha sido usado para ajustar el riesgo de mortalidad según el tipo de hospital. El ACTION-GWTG en 2011 incluyó un total de 8 variables36 que se muestran en la tabla. En 2016 se llevó a cabo una actualización que se desarrolló en 665 hospitales de Estados Unidos y se obtuvieron las siguientes variables predictoras: edad, FC, PAS, parada cardiorrespiratoria, shock cardiogénico, insuficiencia cardíaca, elevación del segmento ST, filtrado glomerular renal y troponinas37. Ambos scores se diseñaron para mortalidad intrahospitalaria y pueden ser calculados en un nomograma en papel. Su aplicabilidad en países de medianos y bajos ingresos está limitada ya que incluye los valores de troponinas y es un registro contemporáneo de pacientes en un país de ingresos altos, con estrategias terapéuticas acordes a las guías internacionales2,4.
ALPHA (Age, Life support, Pressure, Heart rate, Access site)38
Es una escala clínica para IAM con y sin elevación del segmento ST, desarrollada en Hungría para predecir mortalidad a los 30 días en pacientes con realización de ICP. Las variables incluidas se muestran en la tabla. Los autores plantean en las limitaciones del estudio que no es útil para poblaciones de otras regiones geográficas con diferentes perfiles basales de riesgo.
Banach score39
Es una escala clínica para IAM con y sin elevación del segmento ST desarrollada en Varsovia, Polonia, para predecir mortalidad al año. Se nombró así en honor a un famoso matemático polaco. Incluye las variables que se muestran en la tabla. El modelo tuvo una buena discriminación con un ABC de 0,84; pero no es adecuado para mortalidad a corto plazo y fue diseñado en pacientes que, en su mayoría (87,7%), recibieron ICP.
EHRs risk score (Electronic health records)40
Es una escala para el IAM con y sin elevación del segmento ST, basada en el registro electrónico del Medicare y Medicaid en Estados Unidos. Incluye variables clínicas y hemoquímicas (Tabla) para predecir mortalidad a los 30 días. Incluyó en su diseño a 20540 pacientes y alcanzó una adecuada discriminación (ABC 0,78). Pero este diseño se basa en una historia clínica electrónica e incluye valores de troponinas, no siempre disponibles en países de ingresos medianos y bajos.
EPICOR (long-tErm follow uP of antithrombotic management patterns In acute CORonary syndrome patients)41
Es una escala pronóstica diseñada para predecir mortalidad a largo plazo en pacientes con IAM con y sin elevación del segmento ST que analiza 15 variables (Tabla). En el estudio se incluyeron hospitales de 28 países de Europa, América Latina y Asia. Esta escala no puede ser aplicada en la emergencia ya que el EQ-5D requiere cooperación del paciente.
CADILLAC (Controlled Abciximab and Device Investigation to Lower Late Angioplasty Complications)42
El CADILLAC fue obtenido de 2082 pacientes con IAMCEST e ICP primario. La escala evalúa parámetros clínicos y hemoquímicos para predecir la mortalidad al año. En su validación, realizada con 900 pacientes del ensayo clínico Stent-Primary Angioplasty in Myocardial Infarction, se evidenció su utilidad para predecir mortalidad a los 30 días. Las variables que incluye se muestran en la tabla. Para su aplicación se deben valorar algunas variables angiográficas y, a los pacientes incluidos, se les implantaron stents convencionales (bare metal stents), por lo que podría sobrestimar la mortalidad en países donde se aplican las guías actuales de tratamiento que sugieren el empleo de stents farmacoactivos (drug-eluting stents)2.
PAMI (Primary Angioplasty in Myocardial Infarction)43
Fue diseñado con pacientes de varios ensayos clínicos PAMI: PAMI-1 (195 pacientes), PAMI-2 (1100 pacientes), No-Surgery On Standby (No-SOS) con 499 pacientes y Stent PAMI (Stent Primary Angioplasty in MI con 1458 pacientes. Su principal objetivo es predecir mortalidad a los seis meses, pero los datos también fueron calculados para mortalidad intrahospitalaria, al mes y al año. Las variables incluidas se muestran en la tabla. Al igual que el CADILLAC, fue diseñado con stents convencionales e incluyó pacientes de ensayos clínicos; por lo tanto, de bajo riesgo.
SYNTAX (Synergy Between PCI With Taxus and Cardiac Surgery)44
Fue diseñado como una herramienta basada en la anatomía coronaria y la complejidad de las lesiones angiográficas obstructivas, para facilitar la elección del tipo de revascularización mecánica a emplear (ICP o cirugía de revascularización miocárdica). Con posterioridad se añadieron otras variables al SYNTAX original para mejorar su capacidad de predicción (edad, filtrado glomerular renal en ml/min, FEVI, enfermedad de tronco coronario izquierdo no protegido, enfermedad arterial periférica, sexo femenino y enfermedad pulmonar obstructiva crónica) al que se denominó SYNTAX II. Este score permite individualizar el riesgo de mortalidad a largo plazo en pacientes con enfermedad multivaso, ya sean tratados con ICP o cirugía44. Aunque en el diseño original el SYNTAX se empleó para definir el tipo de revascularización a utilizar, actualmente ha sido validado en la estratificación pronóstica del SCACEST45.
Zwolle46
Fue diseñado en Países Bajos para identificar pacientes de bajo riesgo que pudieran ser egresados precozmente. La escala incluye variables clínicas y angiográficas (Tabla) y mostró buena capacidad predictiva de complicaciones graves y mortalidad a los 30 días y al año46. Su utilidad para el alta precoz ha sido bien validada47,48. Los autores del Zwolle muestran que una estrategia de alta precoz salva una vida por cada 1097 pacientes y ahorra 194933,33 euros46.
ESTRATIFICACIÓN DE RIESGO EN CUBA
Los estudios publicados sobre la estratificación de riesgo tras un IAM en Cuba49-54 son escasos, ya que se carece de escalas pronósticas ajustadas a la población cubana. Cordero Sandoval et al.52 publicaron un artículo donde evaluaron varias de ellas en una población con IAMCEST en la provincia Villa Clara. La puntuación Índice Pronóstico mostró una pobre capacidad predictiva con un ABC de 0,67 para la predicción de complicaciones y 0,65 para la mortalidad. La escala ICR (Instituto Cardiovascular de Rosario) obtuvo un ABC de 0,45 para complicaciones graves y 0,41 para mortalidad intrahospitalaria, ambos con muy mala capacidad predictiva. En cambio el GRACE17 en este estudio52 mostró muy buena capacidad predictiva con un ABC de 0,87 para mortalidad y de 0,90 para complicaciones graves. Esta misma escala (GRACE17) también fue validada, por Santos Medina et al.53, en una población similar de Las Tunas, con una aceptable discriminación de 0,771. Ambos estudios utilizaron la escala como un nomograma en papel, que no es el método más adecuado19 y se asumió que las troponinas se encontraban elevadas por tratarse de pacientes con IAMCEST, pues este tipo de determinaciones de laboratorio no está disponible en los hospitales provinciales en Cuba.
Otro estudio publicado en esta misma revista evaluó la capacidad predictiva de la escala TIMI en pacientes con IAMCEST de La Habana54 y mostró una buena discriminación, con un ABC de 0,76; pero solo incluyó 115 pacientes con un seguimiento en las primeras 48 a 72 horas, que es la estadía en la unidad de cuidados intensivos, por lo que puede infraestimar el riesgo de muerte a largo plazo.
Por último, en este número de CorSalud se publica un artículo de Santos Medina et al.55, donde evalúan la capacidad de discriminación de varias escalas para la mortalidad hospitalaria. La investigación incluyó a 430 pacientes ingresados en las primeras 24 horas del IAM y sus resultados muestran claramente la pobre capacidad predictiva de las escalas GRACE (ABC 0,662), InTIME (ABC 0,681) e ICR (ABC 0,683). Los autores, además, plantean que la capacidad de predicción del TIMI Risk Score para la mortalidad hospitalaria fue fallida, al obtener un ABC de 0,598.
EPÍLOGO
Las diferencias en la aplicabilidad de estas escalas de estratificación de riesgo existentes, a la población cubana, derivan del hecho de haber sido desarrolladas en países de ingresos altos, generalmente Estados Unidos y Europa, por lo cual su extrapolación es cuestionable. Existen diferencias poblacionales sociodemográficas, étnicas, genéticas e idiosincráticas, que pueden ser la causa de que los resultados predichos en los estudios originales, la mayoría llevados a cabo en países de altos ingresos, no sean reproducibles con exactitud en poblaciones diferentes.