Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Finlay
versión On-line ISSN 2221-2434
Rev. Finlay vol.6 no.1 Cienfuegos ene.-mar. 2016
PRESENTACIÓN DE CASO
Acidosis tubular renal distal y parálisis hipopotasémica. Presentación de un caso y revisión de la literatura
Distal Renal Tubular Acidosis and Hypokalemic Paralysis. A Case Report and Literature Review
Miguel Ángel Serra Valdés , Dinorah Oliva Venereo , Alain Landrián Davis , Jorge Luis Valdés Fúster
Hospital General Docente Enrique Cabrera, La Habana, La Habana, Cuba, CP: 10800
RESUMEN
La acidosis tubular renal distal o tipo 1 es una entidad muy poco frecuente. Cursa con parálisis hipopotasémica. Puede ser autosómica dominante o recesiva. La autosómica dominante es menos severa y aparece en la adolescencia o en la etapa adulta. Se presenta el caso de una paciente de 42 años que comenzó con debilidad en las piernas, después en los brazos, horas después ya no podía mover las piernas y tenía sensación de falta de aire sin otro síntoma. El examen físico, neurológico, gasometría, ionograma, orina y la recuperación en 24 horas con aporte de potasio y corrección de la acidosis metabólica permitieron hacer el diagnóstico, de acidosis tubular renal distal. Este es un trastorno muy poco frecuente en la práctica clínica y también en la nefrológica.
Palabras clave: acidosis tubular renal, parálisis periódica hipopotasémica, diagnóstico clínico, adulto, debilidad muscular.
ABSTRACT
Distal renal tubular acidosis, or type 1 renal tubular acidosis, is a rare condition that presents with hypokalemic paralysis. It can show an autosomal dominant or autosomal recessive pattern. The autosomal dominant form is less severe and appears during adolescence or adulthood. We present the case of a 42-year-old woman that began suffering from with weakness of the legs that spread to the arms and could no longer move her legs hours later. She also felt shortness of breath without other symptoms. Physical and neurological examination, blood gas analysis, electrolyte panel, urine test and recovery in 24 hours with potassium intake and correction of metabolic acidosis led to the diagnosis of distal renal tubular acidosis. It is a disorder rarely seen in clinical practice and nephrology services.
Key words: acidosis renal tubular, hypokalemic periodic paralysis, clinical diagnosis, adult, muscle weakness.
INTRODUCCIÓN
La parálisis hipopotasémica por acidosis tubular renal (ATR) distal (ARTD) o tipo 1 es una entidad muy poco frecuente en la práctica clínica y en la nefrológica, y se define como un síndrome clínico caracterizado por debilidad muscular generalizada aguda y valores bajos de potasio plasmático menores de 3,5 mEq/L. Por tales motivos la prevalencia se desconoce. En general se manifiesta clínicamente con síntomas neuromusculares, a pesar de que otros sistemas como el cardiovascular y el gastrointestinal pueden estar afectados. A pesar de las múltiples causas de hipopotasemia, son muy pocas las entidades con las cuales hay que hacer diagnóstico diferencial cuando esta entidad se asocia a debilidad muscular extrema. La hipopotasemia debida a la ingestión insuficiente de potasio resulta excepcional, ya que el riñón normal tiene capacidad para ahorrar dicho potasio. Muchos desórdenes renales se han reportado asociados con parálisis hipopotasémica, sin embargo, la mayoría de los casos se deben a ATR.1-4 La parálisis hipopotasémica provoca acidosis en el plasma con hipercloremia, hipopotasemia e hipercalciuria que puede llegar a producir cálculos renales y nefrocalcinosis. Este desorden se puede heredar como un desorden primario o puede ser expresión de una enfermedad sistémica. Los investigadores han hallado los genes anormales responsables para las formas heredadas.5-7 El riñón mantiene y controla el equilibrio ácido-base de la sangre a través de tres mecanismos: la filtración y la reabsorción del bicarbonato, la excreción de los ácidos (o de álcalis), y la síntesis de amonio y de bicarbonato. En el riñón se llevan a cabo dos procesos bioquímicos acoplados: la reabsorción del bicarbonato y la síntesis, secreción, reciclaje y excreción urinaria del amonio. La presencia de múltiples sistemas de transporte en los diferentes segmentos de los túbulos de la nefrona hace posible recuperar todo el bicarbonato (HCO3-) filtrado (4320 mmol/día) en el glomérulo. En los primeros segmentos tubulares de la nefrona, los túbulos proximales reabsorben cerca del 80 % del bicarbonato. En este segmento tubular la reabsorción del bicarbonato ocurre a través del cotransportador Na+/HCO3- (NBCe1), esta absorción está acoplada a la secreción de ácido en la orina por el intercambiador Na+/H+ (NHE3). En los túbulos proximales se reabsorbe la glutamina circulante a partir de la cual se sintetizan simultáneamente amonio y bicarbonato. La reabsorción del 15 % del bicarbonato ocurre en el asa gruesa ascendente de Henle y solo cerca del 5 % del bicarbonato se recupera en los túbulos distales de la nefrona. Por último, el riñón elimina la carga ácida en la orina: el fosfato diácido H2PO4 - (ácido titulable) y el sulfato de amonio.8-9 Se realiza la presentación de caso por lo muy poco frecuente de la entidad, y por haber tenido la oportunidad de diagnosticarlo y tratarlo en nuestro Centro Hospitalario sin tener la paciente, antecedentes, ni poder demostrarse en ella una enfermedad sistémica. Tiene también propósitos docentes para el personal de postgrado de la especialidad en formación y para los diplomantes y maestrantes de cuidados intensivos y emergentes.
PRESENTACIÓN DEL CASO
Se presenta el caso de una paciente de 42 años que acudió al Servicio de Urgencias del Hospital General Docente Enrique Cabrera por haber comenzado con debilidad en los miembros inferiores y posteriormente en los superiores, horas después ya no podía mover las piernas y sostenerse de pie además de tener sensación de falta de aire, sin otro síntoma. La paciente refirió posteriormente una vez recuperada del episodio, que hacía unos 5 meses se cansaba a la hora de realizar las actividades físicas y sentía debilidad en las piernas; pero nunca antes se había sentido como hasta ese momento. Lo atribuyó a ejercicios desacostumbrados al inicio. Notaba también que ante actividades físicas rutinarias en su trabajo y en el hogar se cansaba y le faltaban las fuerzas en los brazos y piernas para continuar sus labores. Antecedentes patológicos familiares: una prima, más joven que ella, padece de estas crisis y desconoce si tiene diagnóstico. Antecedentes patológicos personales: ninguno. Examen físico (datos de interés): Paciente bien nutrida, con temperatura normal, algo obnubilada. Con tensión arterial (TA) 100/60. Frecuencia cardiaca en 68 x min. Frecuencia respiratoria 23 x min. Examen cardiorespiratorio: sin alteraciones. Abdomen: sin alteraciones. Examen neurológico: paraparesia flácida 4/5. Disminución de la fuerza muscular en miembros superiores de 3/5. Hiporreflexia osteotendinosa generalizada. Sin trastornos sensitivos, ni signos meníngeos. De inicio se pensó en la posibilidad de un Síndrome de Guillain Barré, pero no existía un cuadro infeccioso previo, de ningún tipo. Exámenes complementarios: Tomografía axial computarizada (TAC) sin alteraciones craneoencefálicas. Hematocrito (Hto): 037. Hemoglobina (Hb): 120 gr/l. Leucograma: 12,0 x 109/l. Gasometría arterial: pH 7,21; pCO2 23; pO2 97; HCO3- 11,0; EB -14,0; compatible con una acidosis metabólica. Ionograma: Potasio en 1,48 mmol/l. Cloro: 128 mmol/l. Sodio: 140 mmol/l. Calcio: 0,93. Orina: pH 8, densidad 1005, resto de los elementos: normales. Glucemia: 6,0 mmol/l. Creatinina: 106 mmol/l. La paciente fue ingresada las primeras 24 horas hasta su mejoría en la Unidad de Cuidados Intensivos (UCI) y posteriormente, a las 48 horas fue trasladada a sala de clínica con potasio en 3,8 mmol/l y gasometría arterial normal para completar estudio y continuar tratamiento. Se planteó como diagnóstico una acidosis metabólica que por los complementarios iniciales se sospechó una acidosis tubular renal, aunque es una afección rara o poco frecuente. La acidosis metabólica hiperclorémica con hipopotasemia y un pH urinario mayor de 6 en presencia de acidosis metabólica sistémica, constituye de por sí un diagnóstico de acidosis tubular distal1, ya que pone en evidencia la incapacidad del túbulo distal para secretar hidrogeniones en presencia del fuerte estímulo que para ello representa la acidosis sistémica. Quedaron descartadas pues otras causas de acidosis metabólica en ausencia de antecedentes y del cuadro clínico. Resto de exámenes realizados en sala: Analítica de laboratorio: La aspartato aminotransferasa (AST/TGO) y la alanino aminotransferasa (ALT/TGP) fueron normales. Colesterol y triglicéridos: normales. Amilasa: normal. Bilirrubinas: normales. La gammaglutamiltranspeptidasa (GGT) y fosfatasa alcalina: normales. Velocidad de sedimentación globular (VSG) 30 mm x h. Ecografía abdominal: Riñones: micro litiasis bilateral. Riñones de tamaño normal con buena delimitación corticomedular. Aumento de la ecogenicidad. Sistema excretor no dilatado. Hígado y vías biliares sin alteraciones. Bazo y páncreas sin alteraciones. Radiología del tórax: sin alteraciones pleuropulmonares. Electrocardiograma: signos de hipopotasemia, sin otras alteraciones en el trazado. Ionogramas evolutivos: potasio. 3,8, 3,9, 4,2, 4,9 mmol/l. Electrolitos en orina de 24 horas: no pudo dosificarse por dificultades técnicas en el laboratorio. Conducta asumida: se inició tratamiento en la UCI con aportes de potasio en soluciones y pequeñas dosis repetidas de bicarbonato. La paciente recuperó la actividad motora y se sintió totalmente bien a las 24 horas. A las 48 horas fue trasladada a sala de clínica con un examen neurológico totalmente negativo. Luego de 15 días de ingreso se le dio de alta totalmente recuperada, asintomática, con un potasio en 4,9 mmol/l y una gasometría arterial normal. Se continuó terapia con sales de potasio por vía oral con jarabe 3 veces al día. Se expidió un resumen de historia clínica y se remitió a consulta de clasificación al Instituto de Nefrología para completar estudio y continuar seguimiento posterior. Extremadamente importante fue recomendarle a la paciente asegurar una alimentación balanceada, ya que el consumo excesivo de proteínas (precursoras de ácidos) y la ingestión deficiente de frutas y hortalizas (precursoras de bases) podrían hacer reaparecer episodios de acidosis metabólica. La conclusión diagnóstica final se correspondió con una acidosis tubular renal distal (ATRD) o tipo 1.
DISCUSIÓN
Muchos desórdenes renales se han reportado asociados con parálisis hipopotasémica, sin embargo, la mayoría de los casos se deben a ATR. La ATRD puede ser autosómica dominante o recesiva. La ATRD autosómica recesiva se manifiesta en los primeros meses de vida, cursa con nefrocalcinosis y sordera temprana o tardía. La ATRD autosómica dominante es menos severa y aparece en la adolescencia o en la etapa adulta, y puede o no presentar nefrocalcinosis. Más a menudo, la ATRD distal ocurre secundaria a enfermedades que afecten muchos sistemas de órgano como las autoinmunes y otros trastornos.10 (Cuadro 1). La acidosis tubular renal es un síndrome clínico caracterizado por acidosis metabólica hiperclorémica producida por disfunción tubular para la secreción de iones hidrógeno con una función glomerular normal. Se clasifica en dos grandes grupos: acidosis tubular proximal o tipo 2 y acidosis tubular distal o tipo I. En la acidosis tubular proximal existe disminución en la reabsorción proximal de bicarbonato, que causa bicarbonaturia y disminución del bicarbonato sérico. En la acidosis tubular distal disminuye la secreción de iones H +. Existen dos variantes de la forma distal; una se acompaña de pérdidas importantes de bicarbonato por la orina, (tipo 3), la otra, de hiperkalemia (tipo 4). Ambas pueden ser primarias o secundarias a distintas enfermedades.1,3 (Cuadro 2).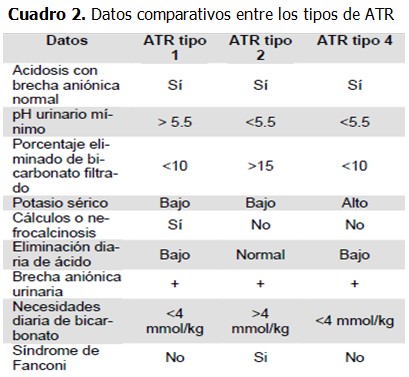
La ATRD pertenece al grupo de enfermedades renales de baja incidencia. En la ATRD se pierde la capacidad para acidificar la orina por un defecto en la excreción de la carga ácida (iones H+ y amonio) en las células intercaladas alfa del túbulo colector. La acumulación de la carga ácida en la nefrona distal tiene como consecuencia el consumo y disminución del amortiguador bicarbonato/CO2 en la sangre.1-4
El retraso del crecimiento es un rasgo característico en niños con ATRD, al que contribuye la acidosis, per se, y sus efectos sobre el metabolismo del calcio, del colágeno y del eje hormona de crecimiento (HC)/factor de crecimiento (IGF-I). La existencia de una correlación significativa entre la secreción diaria de hormona de crecimiento y los niveles séricos de IGF-I con el pH plasmático y las concentraciones de bicarbonato en niños con ATR sugiere una acción directa de la acidosis sobre la secreción de HC. En las células intercaladas alfa de los túbulos colectores se lleva a cabo la excreción urinaria de la carga ácida: los ácidos titulables (fosfatos) y el amonio. La ATRD autosómica recesiva se asocia con mutaciones en los genes ATP6V1B1, ATP6V0A4 y SLC4A1, los cuales codifican las subunidades a4 y B1 de la V-ATPasa y el intercambiador de bicarbonato/cloruro AE1, respectivamente. En contraste, la ATRD autosómica dominante se relaciona con mutaciones solo en AE1.1, 6,7
Una vez diagnosticada la acidosis metabólica hiperclorémica, pero con hipopotasemia significativa y los síntomas clínicos, se deben realizar pruebas diagnósticas que permitan diferenciar la acidosis tubular distal de la proximal. Para poder diagnosticar la ATRD en la clínica es necesario determinar la creatinina plasmática y las excreciones fraccionales de sodio, potasio y cloro, la calciuria y la citraturia. Generalmente se observa acidosis en la sangre (pH < 7,35) y una disminución pronunciada de la concentración del bicarbonato y del CO2 (< 15 mEq/l). En la ATRD el pH de la orina es mayor de 6 en presencia de acidosis metabólica sistémica. Para los casos cuyo diagnóstico está en duda, como en la ATRD incompleta, es recomendable aplicar pruebas de acidificación. Estas pruebas consisten en la administración de NH4Cl, determinándose a continuación: el pH, la acidez titulable y la excreción urinaria de amonio. Exámenes que no se pueden realizar en el Enrique Cabrera, así como la hipercalciuria e hipocitraturia que tampoco se pudieron demostrar por limitaciones técnicas del laboratorio. Los pacientes con ATRD cursan con una brecha aniónica (anión restante) urinaria positiva y una brecha aniónica del plasma normal ([Na+] + [K+] - [Cl-]), que la distingue de otro tipo de acidosis. El potasio es muy importante para la transmisión nerviosa y la contractura muscular, incluyendo el funcionamiento cardiaco. Por tales motivos niveles bajos pueden causar debilidad extrema que puede llegar a la parálisis, latidos cardiacos irregulares y la muerte. El nivel cae porque los riñones excretan demasiado potasio en la orina en lugar de retornarlo a la sangre. Las pruebas de sobrecarga de bicarbonato, la medida de la diferencia de pCO2 entre orina y sangre y la excreción neta de ácidos después de una sobrecarga de amonio son pruebas más complejas, que se requieren en algunos casos, para el diagnóstico definitivo del tipo de acidosis tubular.3, 5, 10,11
El tratamiento de la ATRD incluye la administración de potasio y la corrección de la acidosis con suplementos de bicarbonato. Los requerimientos diarios de potasio en la ATRD son de 1 a 2 mEq/kg/día. La terapia alcalina usualmente es combinada con reemplazo de potasio para evitar la hipopotasemia severa. La hipopotasemia debería ser corregida primero, debido a que la terapia alcalina puede empeorar la hipopotasemia con consecuencias peligrosas. El tratamiento temprano mejora la nefrocalcinosis, previene la recurrencia de cálculos renales y la aparición de insuficiencia renal. Afortunadamente, la ATRD tiene un buen pronóstico si se diagnostica tempranamente y se sigue el tratamiento alcalino, el cual consiste en dosis periódicas de bicarbonato de sodio y/o de citrato de potasio durante el día. La dieta sin excesos de proteína y aportes de frutas y vegetales es importante.1
En este caso fue posible identificar el trastorno de la paciente porque que acudió con una acidosis metabólica franca, por gasometría con hipercloremia e hipopotasemia, responsables del cuadro de debilidad extrema con parálisis de ambos miembros inferiores y marcada debilidad muscular con disminución de la fuerza en los miembros superiores, que hizo pensar en otras posibilidades diagnósticas como pudo haber sido el Síndrome de Guillain Barré. La gasometría, el ionograma, el pH urinario, otra causa que no justificara una acidosis metabólica y la administración de potasio y bicarbonato con una recuperación en 24 horas indujo al diagnóstico. A pesar de ello, las referencias revisadas coinciden que los elementos básicos para el diagnóstico están en el caso.1, 3, 4, 5,10, 11 Basta con ello para hacer el diagnóstico. La paciente no tenía antecedentes de patología alguna y el resto de los exámenes no ofrecían indicios de otro trastorno que pudiera haberla llevado a una acidosis metabólica. El dato recogido en el interrogatorio que desde agosto comenzó a presentar debilidad muscular frecuente con cansancio, lo que atribuía primero a unas vacaciones en la playa donde manejaba bicicletas acuáticas fue un elemento importante para la sospecha diagnóstica. Otro dato de interés referido por la paciente se relaciona con que una prima, también padecía de estas crisis de debilidad muscular extrema; pero ella desconocía si se le había dado un diagnóstico. Una vez que fue dada de alta se remitió al Instituto de Nefrología para completar su seguimiento.
La ATRD es un trastorno muy poco frecuente en la práctica clínica y según referencias bibliográficas revisadas también en nefrología. Saber interpretar los resultados de la gasometría, el ionograma y elementos importantes en el análisis de la orina son suficientes para sugerir el diagnóstico y descartar otras causas de acidosis metabólica. La administración de potasio y varias dosis bajas de bicarbonato posteriormente producen una recuperación que confirman el diagnóstico. La ATRD tiene un buen pronóstico si se diagnostica tempranamente y se sigue el tratamiento adecuado.
REFERENCIAS BIBLIOGRÁFICAS
1. Escobar L, Mejía N, Gil H, Santos F. La acidosis tubular renal distal: una enfermedad hereditaria en la que no se pueden eliminar los hidrogeniones. Nefrología. 2013;33(3):289-96
2. Enfermedades raras renales. Acidosis tubular renal distal. Orphanet [Internet]. 2014 [citado 28 Ene 2015]; . Disponible en: http://www.orpha.net/consor/cgi-bin/Disease_Classif.php?lng=ES&data_id=188&PatId=260&search=Disease_Classif_Simple&new=1
3. Sharma S, Gupta A, Saxena S. Comprehensive clinical approach to renal tubular acidosis. Clin Exp Nephrol. 2015;19(4):556-61
4. Zhang C, Ren H, Shen P, Xu Y, Zhang W, Wang W, et al. Clinical evaluation of Chinese patients with primary distal renal tubular acidosis. Intern Med. 2015;54(7):725-30
5. Carrisoza R, Rangel C, Saldaña R, Salvador C, Escalona C, Satlin LM, et al. Acidosis tubular renal. Kidney International. 2011;80(8):832-40
6. Mohebbi N, Vargas R, Hegemann SC, Schuknecht B, Kistler A, Wüthrich R, et al. Homozygous and compound heterozygous mutations in the ATP6V1B1 gene in patients with renal tubular acidosis and sensorineural hearing loss. Clin Genet. 2013;83(3):274-8
7. Chu C, Woods N, Sawasdee N, Guizouarn H, Pellissier B, Borgese F, et al. Band 3 Edmonton I, a novel mutant of the anion exchanger 1 causing spherocytosis and distal renal tubular acidosis. Biochem J. 2010;426(3):379-88
8. Gumz ML, Lynch IJ, Greenlee MM, Cain BD, Wingo CS. The renal H+-K+-ATPases: physiology, regulation, and structure. Am J Physiol Renal Physiol. 2010;298(1):12-21
9. Kraut JA, Madias NE. Metabolic acidosis: pathophysiology, diagnosis and management. Nat Rev Nephrol. 2010;6(5):274-85
10. Carrisoza R, Salvador C, Satlin LM, Liu W, Zavilowitz B, Bobadilla NA, et al. A novel K+ secretory renal channel. Kidney International. 2010;78(11):229-30
11. López M. Acidosis tubular renal. Diagnóstico y tratamiento médico. Centro Médico Docente La Trinidad [Internet]. 2014 [citado 23 Mar 2015]; . Disponible en: http://www.slan.org.ve/descargas/Acidosis tubular renal. Diagnóstico y tratamiento médico.pdf
Recibido: 21 de enero de 2016.
Aprobado: 25 de enero de 2016.
Miguel Ángel Serra Valdés. Especialista de II Grado en Medicina Interna. MSc. en Enfermedades Infecciosas. Profesor Auxiliar.Hospital General Docente Enrique Cabrera. La Habana. Correo electrónico: maserra@infomed.sld.cu















