INTRODUCCION
El OLEOZON® Oral es un medicamento desarrollado y producido por el CNIC y registrado en Cuba para el tratamiento de la giardiasis intestinal (Díaz et al. (2006). Es bien conocido que los Órganos Reguladores de Medicamentos exigen a los fabricantes de productos farmacéuticos evidencias de que estos son producidos de forma consistente, garantizando el cumplimiento de las especificaciones de calidad predefinidas (Suárez, (2013). El control es la forma más tradicional de gestionar la calidad resultante de los procesos. Asegurar la calidad en los procesos supone una calidad elevada, a un costo admisible, que consiste en la recolección, análisis e interpretación de datos, establecimiento de calidades, comparación de desempeños, verificación de desvíos, para su utilización en las actividades de mejoría y control de calidad de productos (Hernández et al. (2016).
El objetivo del trabajo fue demostrar la consistencia del proceso de fabricación del OLEOZON® Oral a través de los controles de proceso, que es uno de los aspectos evaluados a demostrar en la Revisión de la Calidad del Producto.
MATERIALES Y MÉTODOS
A partir de los datos primarios reflejados en los informes de análisis del producto terminado, fueron seleccionados 221 lotes del OLEOZON® Oral, producidos durante el período 2019-2020, estos fueron comparados con resultados de lotes producidos en el año 2018. Se realizaron diferentes ensayos físico-químicos para verificar la calidad de los lotes: Índice de peróxido(IP), Índice de acidez(IA) y Concentración de aldehídos(CA). En la Tabla I se resumen los ensayos monitoreados en el control de calidad y los límites correspondientes a cada uno de ellos. Para el análisis del comportamiento de estos lotes se utilizaron los informes de análisis del producto terminado en cada caso. En la selección de los lotes de OLEOZON® Oral se utilizaron los resultados obtenidos en el control de calidad, estos debían cumplir los siguientes requisitos:
Ser lotes producidos de forma consecutiva durante la etapa comprendida entre 2019 - 2020.
Ser lotes liberados según certificados de análisis emitidos por el Departamento de Aseguramiento de Calidad de la entidad.
Prueba de distribución normal
Se utilizó el programa Statgraphics Plus 5.1 (Statistical Graphics Corp., EE.UU.) con el objetivo de verificar si los datos analizados se ajustaban a la distribución normal. La normalidad se valoró a partir de las medidas descriptivas de las muestras: media, mediana, curtosis y asimetría, y mediante la aplicación de la prueba de bondad de ajuste Kolmogorov-Smirnov. En estas pruebas de contrastes se consideró un nivel de significación (α) del 5,0 %.
Criterios de aceptación: la media y la mediana de las muestras deben ser similares. Los coeficientes estandarizados de asimetría y curtosis, para determinar si la muestra procede de una distribución normal, deben estar dentro del intervalo de -2 a +2 (De Muth, 1999). En los ensayos de bondad de ajuste la p (significación) debe ser mayor de 0,05.
Control estadístico
Los datos anteriores se procesaron con el programa MINITAB 15 (EE.UU.) para determinar los resultados correspondientes a la línea central, los límites de control superior e inferior (LCS y LCI), respectivamente, así como el valor de ( (nivel de significación o probabilidad de error). En caso necesario se eliminaron los puntos fuera de los límites de control (LC) o las rachas que describían tendencias ascendentes o descendentes (causas asignables) (Mosquera et al. (2014)).
RESULTADOS Y DISCUSIÓN
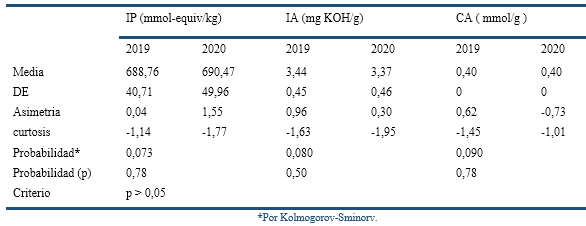
Los resultados de índice de peróxido se encontraron dentro de los límites establecidos (500 - 800 mmol-equiv/kg), así como el índice de acidez (0 - 15 mg KOH/g) y la concentración de aldehídos (0 - 0,9 mmol/g) (Tabla 2).
Adicionalmente, los valores estandarizados de curtosis y coeficientes de asimetría estuvieron dentro de los intervalos esperados (-2 a +2) para los datos de una distribución normal, elementos que corroboran el comportamiento mesocúrtico y simétrico de los datos (De Muth, 1999).
Los resultados demostraron un alto grado de conformidad en las propiedades de los lotes analizados, los resultados de índice de peróxido, aunque cumplieron el límite establecido, presentaron mayor variación, a partir de los resultados de desviación estándar. Los valores de probabilidad, en todos los casos, resultaron mayores que el criterio establecido (p > 0,05) (0,073; 0,080; y 0,090), por lo que no existen diferencias significativas entre los dos años evaluados.
Control estadístico de los procesos
El cumplimiento de los parámetros, con la demostración de la normalidad, constituye un paso indispensable para la comprobación de los parámetros de calidad del OLEOZON® Oral, desde el punto de vista estadístico. Los gráficos de control para los lotes de OLEOZON® elaborados industrialmente se reflejan en la Figura 1, donde se presentan los parámetros de calidad en una serie cronológica.
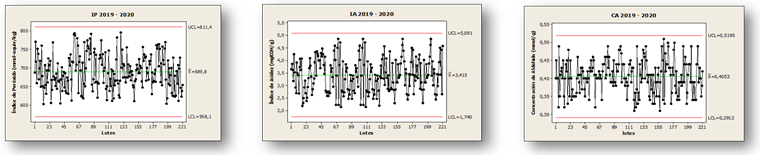
Fig. 1 Gráficos de control para los parámetros IP, IA y CA de lotes industriales de OLEOZON® Oral producidos entre 2019 -2020.
Los resultados reflejados en los gráficos de control alcanzaron una media igual a 689,80 mmol-equiv/kg de índice de peróxido; 3,41 mg KOH/g de índice de acidez y 0,40 mmol/g de concentración de aldehídos. Todos los puntos fluctuaron dentro de los límites de control, por lo que el proceso, a partir de los análisis de los controles de calidad, está en un estado de control para un nivel de confianza del 95,0 %. Todos los lotes evaluados cumplieron satisfactoriamente las especificaciones de calidad.
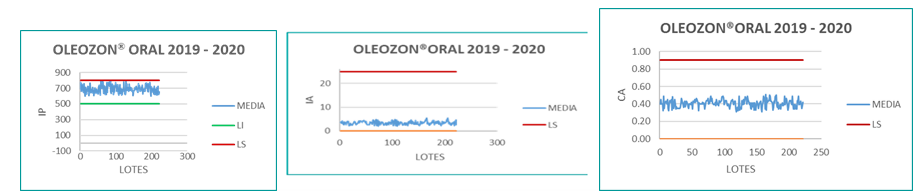
A pesar de la variabilidad mostrada para el índice de peróxido, se puede afirmar que el proceso se encuentra en estado de control desde el punto de vista estadístico. Se evidenció el cumplimiento de las especificaciones de calidad (Figura 2), como una de las utilidades de los gráficos de control. Se lograron patrones gráficos que demuestran la influencia sobre el proceso solo de causas aleatorias, por lo que pueden considerarse gráficos patrones, cuyos límites de control sirven para el monitoreo continuo de estos parámetros en producciones posteriores. De igual forma, hay correspondencia con los estudios previamente publicados por (Hernández et al. (2016).
Según los gráficos de tendencia realizados a los tres parámetros evaluados en el producto durante el periodo analizado, se puede concluir que estos se mantienen dentro de los límites establecidos.
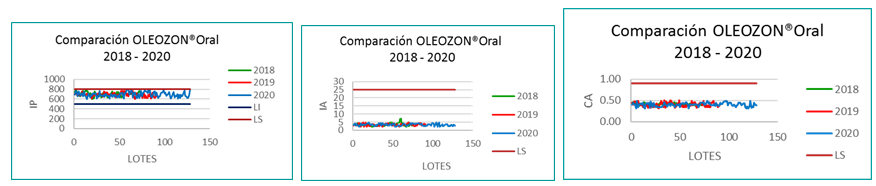
Se evaluó la consistencia, mediante la comparación estadística del comportamiento de IP, IA y CA entre los años 2018, 2019 y 2020. Los resultados obtenidos reflejaron valores de probabilidad, en todos los casos, mayores que el criterio establecido (p > 0,05) (0,08 para IP; 0,49 para IA; 0,33 para CA), por lo que no existen diferencias significativas entre en los tres años analizados (Figura 3).
CONCLUSIONES
Los lotes industriales de Oleozón® Oral cumplieron satisfactoriamente con las especificaciones de calidad del producto terminado, demostrando consistencia y reproducibilidad en los controles de calidad.El Oleozón® Oral se encuentra bajo control estadístico, en conformidad con las especificaciones de calidad establecidas para el índice de peróxido, índice de acidez y concentración de aldehídos, demostrándose, a través de los controles de proceso, la consistencia de su proceso de fabricación.