INTRODUCCIÓN
En Cuba, el tomate es la principal hortaliza que se cultiva, tanto por sus volúmenes de producción, como por su amplio y variado consumo por la población; además, asegura la mayor parte de la materia prima para la industria conservera y es un producto adecuado para la exportación, según reportes de (Anuario Estadístico de Cuba, 2018).
En la provincia de Pinar del Río se encuentra la Fábrica de Conservas “La Conchita”, la cual tiene entre sus líneas de producción la elaboración de pastas concentradas de tomate. Como resultado de esta producción se generan anualmente alrededor de 83,27 t de residuos sólidos, volúmenes importantes que pueden tener prominentes aplicaciones energéticas y medioambientales y que son destinados para la alimentación animal, especialmente para bovino y ovino.
Debido a la no existencia de una valoración energética, a través del proceso de pirólisis de los residuos sólidos de tomate (RST), en el trabajo se efectúa un estudio termogravimétrico de la pirólisis, a escala de laboratorio, que tiene como objetivo determinar la conversión final de la biomasa así como la influencia de la velocidad de calentamiento y masa de la muestra en la misma, además de la energía de activación y el factor de frecuencia, con lo cual se obtiene un criterio energético para definir el intervalo de temperatura que se puede explotar.
MATERIALES Y MÉTODOS
2.1. Sistema experimental
Para la realización del estudio termogravimétrico se utilizó una termobalanza de la marca CAHN, modelo TG-131. El control de temperaturas del sistema, así como la toma de datos, se realizó desde una computadora compatible mediante un software.
2.2. Materiales empleados
La materia prima seleccionada son los RST, consistentes en la mezcla de cáscaras y semillas resultantes del proceso de extracción de la pulpa de tomate. Para el trabajo la materia prima se secó, hasta obtener una humedad entre el (8 - 9) %.
2.2.1. Análisis de la composición química de la muestra de biomasaEcuación (1):
El análisis inmediato de la muestra original se realizó en el Laboratorio de Química Orgánica de la Universidad de Pinar del Río, según las normas analíticas (ASTM E 871-82, 1998), (ASTM E 1755-01, 2001) y (ASTM E 872-82, 1982). Los resultados (en porcientos en peso) se muestran en la tabla 1. A partir de los mismos se predice el análisis elemental de la muestra, según lo planteado por (Parikh et al., 2007), los resultados (en porcientos en peso) se recogen en la tabla 2.
Tabla 1 Análisis inmediato de los residuos sólidos de tomate
| Cenizas (%) | ASTM E 1755-01 | 3,65 |
| Volátiles (%) | ASTM E 872-82 | 86,63 |
| Carbono Fijo (%) | Por diferencia | 9,72 |
Donde:
MV |
% de materia volátil contenido en la biomasa. |
CF |
% de carbono fijo contenido en la biomasa. |
C |
% de carbono elemental contenido en la biomasa. |
H |
% de hidrógeno contenido en la biomasa. |
O |
% de oxígeno contenido en la biomasa. |
N |
% de nitrógeno contenido en la biomasa. |
Los valores calculados en la tabla 2 se utilizan para el cálculo del poder calórico superior de la biomasa, según la ecuación de Dulong (Braz y Crnkovic, 2014).
Donde:
2.3. Procedimiento experimental.
Para el análisis de los resultados alcanzados en el estudio termogravimétrico, se utilizó el software Design-Expert® Versión 7, con el que se obtuvo un estudio factorial de análisis de varianza (Anova), utilizando un grado de significación del 95 % (α=0,05), de acuerdo con (Manyà et al., 2006). Para la toma de decisión de las condiciones en que se deben efectuar los procesos en la región estudiada, nos basamos en el criterio: maximizar el resultado, minimizarlo, no tenerlo en cuenta o que se mantenga en el rango alcanzado y en la importancia que se le brinda a cada respuesta alcanzada.
El diseño de experimentos se basó en un diseño factorial completo de 2k (k-número de factores o variables que intervienen en el proceso). Se seleccionaron como variables de estudio las siguientes:
Masa de la muestra (mg): Pm = 10, 15 y 20 mg.
Velocidad de calentamiento (ºC/min): Vc = 5, 10 y 15 ºC/min.
En el diseño se obtuvo un modelo de 22 = 4 experimentos y se realizaron tres réplicas en el punto central, por lo que el número final de experimentos a realizar es de siete. Para evitar que el orden de realización de los experimentos sea un factor más que influya en el proceso, éstos se llevaron a cabo de forma aleatoria. En la tabla 3 se muestra la matriz con los experimentos a realizar.
Tabla 3 Matriz con los experimentos
| 2 | 1 | 15 | 10 |
| 1 | 2 | 5 | 10 |
| 3 | 3 | 5 | 20 |
| 7 | 4 | 10 | 15 |
| 5 | 5 | 10 | 15 |
| 6 | 6 | 10 | 15 |
| 4 | 7 | 15 | 20 |
En la termobalanza se realizaron los experimentos dinámicos. En los mismos el programa de calentamiento utilizado comienza a 40 ºC y llega hasta 900 ºC a una velocidad de calentamiento determinada para cada experimento y un caudal constante de gas nitrógeno de 100 cm3/min. Cuando el sistema alcanza los 900 ºC se elimina la corriente de gas nitrógeno y se introduce el mismo caudal de aire, registrando datos de tiempo, temperatura y masa durante el calentamiento.
En el proceso de descomposición térmica se analizaron las siguientes respuestas:
2.3.1. Variación de la conversión final alcanzada: X en (%)Ecuación (3): Ecuación (4): Ecuación (5): Ecuación (6): Ecuación (7):
Donde:
X |
- conversión final (%): varía de un valor inicial cero e idealmente puede llegar a uno, si la masa final es cero, pero en pirólisis nunca se obtiene este valor porque m ∞ > 0. |
m o |
- masa inicial de la biomasa (mg). |
m i |
- masa de la biomasa en un instante (mg). |
Se define la máxima conversión como (As) y se determina por la expresión:
Representando m ∞ la masa de la biomasa en un tiempo infinito (mg).
Además se trabajó también con las definiciones de conversión como la fracción de pérdida de masa respecto a la masa inicial (f), variando de la unidad a un valor final definida como la fracción final de pérdida de masa y la conversión α, que varía de cero a uno.
Donde:
Al sustituir la ecuación 2, 3 en la expresión general − 𝑑𝑚 𝑚 0 ∗𝑑𝑡 =𝑘∗ 𝑚− 𝑚 ∞ 𝑚 0 𝑛 , (Gonzalo, 2004), se obtiene la expresión general de la cinética de la descomposición térmica del material analizado.
Donde “n” es el orden de la reacción y “k” es la constante de velocidad o cinética, siguiendo la ecuación de Arrhenius se expresa de la siguiente forma:
Definiendo a:
2.3.2. La energía de activación Ea y factor de frecuencia ZEcuación (8): Ecuación (9): Ecuación (10):
Para determinar los valores de la energía de activación y el factor de frecuencia nos basamos en el método de isoconversiones, como proponen (Hu et al., 2007; Gonzalo, 2004), para valores fijos de “α” y en modelos de un sólo paso, la relación entre la energía de activación, la temperatura y la velocidad de calentamiento está dada por:
Donde C es una constante relacionada con el factor de frecuencia y la energía de activación y coincide con la ordenada en el origen y el valor de la energía de activación se obtiene de la pendiente al representar la curva de variación de ln (Vc) vs. 1/T.
Para determinar el valor del factor de frecuencia, se considera que α=1 a la temperatura de 900 ºC y g(α)=1 en este valor como propone (Gonzalo, 2004), obteniendo la expresión:
RESULTADOS Y DISCUSIÓN
Los resultados de conversión (X) utilizando la ecuación 2, al variar las variables velocidad de calentamiento (Vc) y masa de la materia prima (Pm), alcanzados en la descomposición termogravimétrica en termobalanza, se muestran en la tabla 4.
Tabla 4 Conversión alcanzada en la descomposición termogravimétrica
| 2 | 1 | 15 | 10 | 74,23 |
| 1 | 2 | 5 | 10 | 81,39 |
| 3 | 3 | 5 | 20 | 80,59 |
| 7 | 4 | 10 | 15 | 79,51 |
| 5 | 5 | 10 | 15 | 80,92 |
| 6 | 6 | 10 | 15 | 78,22 |
| 4 | 7 | 15 | 20 | 81,03 |
En la (Fig. 1) se muestran las gráficas de los experimentos dinámicos referidas a la conversión que se obtiene al variar los parámetros velocidad de calentamiento y masa de la muestra. Como se observa en la misma, del (70 - 80) % de la descomposición ocurren entre los 250 ºC y 500 ºC, mientras que el rango de temperatura a la cual ocurre la tasa máxima de pérdida de peso en la pirólisis es entre 310 ºC y 350 ºC, para todas las condiciones en que se desarrollaron los experimentos (Fisher et al., 2002; Sumon et al., 2019; Alvarez et al., 2019).
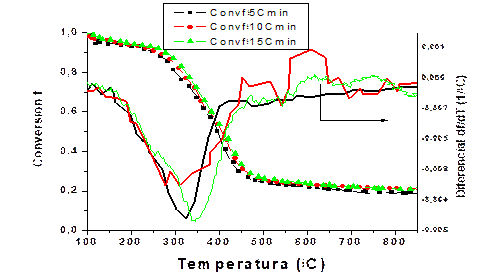
Fig. 1 Conversión, representada por la fracción pérdida de masa (f), y el diferencial df/dT frente a la temperatura
El proceso de pirólisis de RST se lleva a cabo en tres etapas. La primera, hasta aproximadamente 250 ºC, en la que se descomponen las pectinas y xilanos obteniendo una pérdida del 10 % al 15 % de la masa. La segunda de (250 - 500) ºC en la que se desprenden la mayor parte de los volátiles, que representan cerca del 80 % de pérdida de masa y la tercera que al alcanzar los 900 ºC se ha perdido aproximadamente el 90 % de la masa en la materia prima, resultados similares son obtenidos por (Fisher et al., 2002; Sumon et al., 2019; Alvarez et al., 2019). La pérdida de agua y algún volátil ligero ocurre en la primera etapa. La pérdida del mayor volumen de los volátiles y otros compuestos presentes en el residuo sólido de tomate tiene lugar en la segunda y tercera etapa. La pérdida de masa en la muestra de RST después de sobrepasar los 450 ºC es pequeña, debido a su composición química (Fisher et al., 2002).
3.1. Influencia de los factores velocidad de calentamiento y masa de la muestra, en la conversión final de la materia prima.
Al analizar los resultados obtenidos se demuestra que sobre la conversión, no ejercen influencia significativa ninguno de los factores estudiados y su interacción, producto que en el análisis de varianza la distribución “F” de Fischer-Snedecor (Fcada factor < Ftabulada) y a partir del nivel de significación fijado la (Pvalorcada factor > 0,05), por lo que se puede tomar constante, con un valor medio de X = 79,31 %.
Según (Rincón et al., 2009) la composición química de las biomasas vegetales presenta altos contenidos de polisacáridos, muy bajos contenidos de lignina y la presencia de otras sustancias orgánicas como azúcares simples, grasas, vitaminas y pectinas, lo que apunta a diferencias en el comportamiento térmico si se compara con materiales lignocelulósicos que poseen en general hasta 30 % de lignina. Lo que justifica que el aumento de la velocidad de calentamiento no favorezca la conversión, a diferencia de lo que ocurre con otras biomasas, según (Encinar et al., 2000; Püttün et al., 2007).
Otro de los resultados obtenidos en el análisis de varianza realizado, son las condiciones de trabajo para las cuales la conversión va a ser máxima. Manteniendo la velocidad de calentamiento y la masa de la muestra en el rango y maximizando la conversión, obtenemos que la conversión a carbón de los RST es máxima para Vc=5 ºC/min y Pm=10 mg. Lo que se justifica porque a bajas velocidades de calentamiento reduce la formación de volátiles producto que no se favorecen las descomposiciones endotérmicas de la biomasa, aumentando el tiempo requerido para que ocurran reacciones secundarias favoreciendo la formación del carbón (Verma et al., 2018).
3.2. Estudio cinético de la pirólisis de los residuos sólidos de tomate.
Al representar la curva de variación de ln(Vc) vs. 1/T, el valor de la energía de activación se determina de la pendiente de la recta para cada grado de conversión “α” alcanzado, obteniendo los resultados que se muestran en la tabla 5.
Como se puede apreciar, la energía de activación alcanza los mayores valores en la zona de los 250 ºC a los 450 ºC, coincidiendo con el intervalo donde ocurre la mayor descomposición de la biomasa, (Mishra y Mohanty, 2018).
Para determinar el factor de frecuencia, a partir de la ecuación 10, se trabaja con un valor medio de la energía de activación, Ea = 236,62 kJ/mol, obteniendo los resultados que se muestran en la tabla 6.
Como se aprecia, existe un aumento del factor de frecuencia a medida que aumenta la velocidad de calentamiento. Lo cual se explica por la ecuación de Arrhenius, en la que al aumentar la velocidad de calentamiento, la temperatura aumenta más rápido, elevándose la energía potencial y por tanto aumenta la interacción molecular.
Tabla 5 Variación de la energía de activación frente al grado de conversión “α” alcanzado
| 51,05 | 0,1 | 200 - 234 |
| 115,81 | 0,2 | 284 - 308 |
| 118,85 | 0,3 | 311 - 336 |
| 149,35 | 0,4 | 338 - 358 |
| 269,70 | 0,5 | 369 - 382 |
| 299,09 | 0,6 | 393 - 405 |
| 286,04 | 0,7 | 408 - 423 |
| 223,07 | 0,8 | 422 - 440 |
| 389,26 | 0,9 | 463 - 476 |
CONCLUSIONES
Después de realizar los estudios de descomposición termogravimétrica de los residuos sólidos de tomate, se puede concluir que el 80 % de la descomposición térmica de los RST, en la región analizada, se produce fundamentalmente entre los 250 ºC y 450 ºC. La tasa máxima de pérdida de peso en la pirólisis ocurre entre 310 ºC y 350 ºC, para todas las condiciones en que se desarrollaron los experimentos.
La conversión final alcanzada varía entre un 74,23 % y 81,39 % según las condiciones en que se efectúan los procesos, pero debido a la influencia no significativa de los factores sobre la misma, se puede tomar un valor medio de 79,31 %.
El factor de frecuencia aumenta con el aumento de la velocidad de calentamiento con valores de 182 s-1 a 547 s-1. La energía de activación alcanza los mayores valores en las zonas de mayor descomposición de los RST, de 250 ºC a 450 ºC, con un valor medio de 236,62 kJ/mol.

























