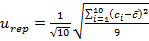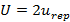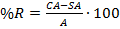Introducción
El cadmio es un metal con importantes aplicaciones. Se emplea en la elaboración de baterías recargables, como aditivo para plásticos y vidrios, en la galvanización y recubrimiento de superficies debido a su resistencia a la corrosión, y como mordiente en tinturas textiles. Sin embargo, es uno de los elementos más monitoreados en aguas naturales y residuales pues sus compuestos son tóxicos, incluso en muy bajas concentraciones, causando problemas renales, infertilidad, afectaciones nerviosas e inmunológicas, cáncer, entre otras. También es bioacumulado por peces y crustáceos, pudiendo entrar fácilmente a la cadena de alimentación humana. Por tanto, el control de los niveles de este metal es importante debido a su marcada toxicidad sobre los ecosistemas.1
Este metal se puede encontrar en las aguas residuales de laboratorio, de procesos de galvanotecnia y del procesamiento de minerales, formando diferentes tipos de compuestos: solubles, insolubles, inorgánicos, organometálicos, compuestos de coordinación, entre otros. Las concentraciones en las que se pueden encontrar en estos efluentes son variables; por ejemplo, en los efluentes de procesamientos industriales de metales las concentraciones más pequeñas del mismo pueden encontrarse entre 7 y 30 mg/L aproximadamente 2; en los procesos de galvanotecnia las concentraciones son mayores, pudiendo estar entre 1 y 3 g/L 3; e incluso, algunos autores reportan concentraciones muy elevadas, con valores cercanos a 30 g/L como óxido de cadmio.4
El cadmio ha sido determinado fundamentalmente mediante métodos espectroscópicos como la Espectroscopía de Absorción Atómica, la Espectrometría de Emisión con Plasma Acoplado Inductivamente, así como la Espectroscopía de Absorción Molecular.5-6 Sin embargo, un método económico y experimentalmente más sencillo que puede emplearse con este fin es la voltamperometría.1,7) La detección voltamperométrica se realiza a partir de la reducción del metal sobre electrodos de grafito, carbono vítreo y mercurio. Es posible emplear el método de preconcentración por redisolución anódica sobre electrodos de película de mercurio para disminuir los límites de detección.8
Una de las ventajas de los métodos electroquímicos es que han demostrado la posibilidad de usar mínima instrumentación no comercial, logrando bajos costos en las determinaciones de las diferentes sustancias. En el caso de la voltamperometría, esta se desarrolla con el circuito mínimo necesario para provocar una electrólisis a potencial controlado y registrar la corriente, con resultados similares a los obtenidos cuando se emplean instrumentos comerciales.9
Existen pocos reportes de determinación de metales pesados por métodos de redisolución empleando mínima instrumentación.1-8 Con este trabajo se presenta un método de determinación de cadmio por redisolución anódica, que permitirá disponer de un método sencillo y económicamente más factible para cuantificar este metal, al emplear equipamiento construido con materiales de fácil adquisición. Se presenta la evaluación de la linealidad y sensibilidad, límites de detección y cuantificación, precisión y exactitud de un método voltamperométrico de redisolución anódica; empleando electrodos de película de mercurio in situ y un potenciostato construido de forma manual reportado por Vilasó y col.10) La investigación es la continuidad a la validación de la determinación de cadmio empleando el mismo equipo, pero sobre electrodos de grafito.11 Con la redisolución anódica sobre película de mercurio se logra una disminución de los límites de detección y cuantificación para ajustar el método a las concentraciones reales en las cuales podría encontrarse este metal en aguas naturales y residuales.
Materiales y métodos
Muestras
Todos los reactivos descritos en este trabajo fueron de calidad Puro para Análisis (PA), de la marca UNI-CHEM. Los materiales y equipamiento empleados estuvieron certificados y calibrados. El residual líquido empleado en esta investigación se tomó del envase de vertimiento de residuos del laboratorio de Electroquímica Analítica, del Departamento de Química de la Facultad de Ciencias Naturales y Exactas de la Universidad de Oriente.
Instrumentación electroquímica y medio de electrólisis
Para el desarrollo del método voltamperométrico de determinación de cadmio en el residual líquido de laboratorio se utilizó el micropotenciostato de mínima instrumentación reportado por Vilasó y col.10 El electrodo de trabajo empleó una película de mercurio generada in situ sobre grafito a partir de una disolución de HgCl2 1 g/L, como electrodo auxiliar fue utilizada una barra de grafito también y como electrodo de referencia un alambre de plata. El electrolito soporte que se empleó fue KCl 1 mol/L.
El medio de electrólisis que se utilizó fue un buffer de ácido acético/acetato de sodio.12) El buffer fue preparado mezclando 7,3 mL de CH3COOH 1 mol/L con 5 mL de NaOH 1 mol/L para 50 mL de disolución.13
Establecimiento de las condiciones de trabajo
Para realizar los experimentos de redisolución anódica del cadmio inicialmente se realizó la preconcentración potenciostática del analito a un potencial y tiempo determinados en agitación. Posteriormente se detuvo la agitación, se esperó un tiempo de estabilización de la corriente de 10 s y luego se registraron los voltamperogramas, realizando barridos lineales de potenciales de -1200 a -10 mV, a una velocidad de generada al azar entre 2,45 y 10,90 mV/s. Se empleó una microcelda electrolítica de 5 mL. Para mayor información sobre parámetros instrumentales de este potenciostato pueden consultarse los resultados mostrados por Vilasó y col.10,11,14
El estudio del comportamiento de la corriente a un potencial fijo, se realizó mediante cronoamperometría. Esta técnica permite visualizar la variación de la corriente en el tiempo cuando se fija un potencial para detectar posibles anomalías durante la electrólisis, teniendo en cuenta que una voltamperometría es un conjunto sucesivo de electrólisis potenciostáticas.7 Además, permite fijar el tiempo de lectura de la corriente para la obtención de los voltamperogramas. La cronoamperometría se realizó sobre una muestra del residual líquido a los potenciales: -1300, -900 y -500 mV.
Finalmente se establecieron las condiciones experimentales óptimas para el método voltamperométrico de redisolución mediante un diseño de experimentos factorial 23. Los factores y niveles evaluados fueron: potencial de electrodeposición (-1300 y -1500 mV), tiempo de agitación (5 y 10 min) y pH del medio (3 y 5).
Linealidad y sensibilidad
Para obtener la curva de calibración se registraron los voltamperogramas correspondientes a las concentraciones: 6·10-5; 1·10-4; 2·10-4; 3·10-4 y 5·10-4 mol/L de CdCl2 a pH 5 ajustado con buffer acetato/ácido acético y se graficó la intensidad de corriente en función de la concentración. Las diferentes disoluciones se prepararon por dilución a partir de un patrón de CdCl2 0.1 mol/L. Se obtuvieron tres curvas de calibración mediante regresión lineal y se generó la ecuación de la curva de calibración promedio. Se realizó un Análisis de Varianza Simple (ANOVA) de la regresión.15
Límites de detección y cuantificación
Los límites de detección y cuantificación se evaluaron siguiendo la metodología descrita por la Norma Cubana.15 Se registraron 20 voltamperogramas del blanco (buffer+KCl+Hg2+ sin analito) y se determinó la corriente residual correspondiente al intervalo de potenciales donde aparece el pico de cadmio. Cada una de esas corrientes se introdujeron en la curva de calibración y se determinó la concentración correspondiente. El límite de detección se calculó como 3 veces la desviación estándar de las concentraciones de blanco, mientras que el límite de cuantificación se calculó como 10 veces la desviación estándar.15
Precisión
La precisión se evaluó en condiciones de repetibilidad y reproducibilidad del método. Para la repetibilidad se registraron 10 voltamperogramas a las concentraciones 6·10-5; 3·10-4 y 5·10-4 mol/L de CdCl2, y se calculó el coeficiente de variación para cada concentración como medida de la dispersión de los resultados.15
Para evaluar la reproducibilidad se emplearon dos analistas en dos días de análisis diferentes. Se registraron 5 voltamperogramas y se realizó una comparación de medias mediante una prueba t de Student para verificar si existían diferencias entre los resultados obtenidos por ambos analistas en días diferentes.
La incertidumbre asociada a la concentración de cadmio se estimó según la Guía para la Estimación de la Incertidumbre de Medición.16 Solo se consideró la incertidumbre de la repetibilidad del método. Se desestimaron las restantes posibles fuentes de incertidumbre, teniendo en cuenta los resultados reportados por Vilasó y col.10 donde se demuestra que los errores sistemáticos asociados a la medición de la corriente empleando el potenciostato no comercial solo contribuyen a la incertidumbre expandida en un 0,3 %, por lo que pueden considerarse insignificantes ante el aporte de la repetibilidad.
La incertidumbre asociada a la repetibilidad se calculó según la ecuación (1) para 10 determinaciones.
La incertidumbre expandida se calculó según la ecuación (2), teniendo en cuenta que la incertidumbre combinada se hace igual a la incertidumbre asociada a la repetibilidad.
El factor de cobertura igual a 2 está asociado a un 95 % de confianza. La concentración determinada según el método voltamperométrico empleando un potenciostato no comercial queda reportada finalmente como [c(Cd2+) ± U].
Exactitud
La exactitud se evaluó mediante ensayos de recuperación según la metodología descrita por la Norma Cubana.15 Se seleccionó una concentración de cadmio de 2∙10-4 mol/L. Se cuantificaron 5 muestras del patrón y posteriormente se realizaron adiciones de 0.0001 mol de cadmio a cada uno, para luego realizar nuevamente la cuantificación voltamperométrica. El porcentaje de recuperación se calculó según la ecuación (3).
donde:
%R: porcentaje de recuperación
C.A: concentración de la disolución con adición
S.A: concentración de la disolución sin adición
A: cantidad añadida
Resultados y discusión
Establecimiento de las condiciones de trabajo
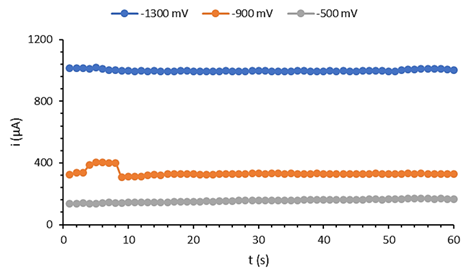
La figura 1 muestra el comportamiento cronoamperométrico modular a tres potenciales. Como puede observarse, a -1300 mV ocurre la electrodeposición del cadmio, a -900 mV aún no ha ocurrido la redisolución y a -500 mV ha ocurrido completamente el proceso.
El estudio del comportamiento cronoamperométrico a estos potenciales evidenció que a -900 mV ocurre una inestabilidad de la corriente en un rango cerca de los 8 s, lo cual puede estar asociado con la variabilidad inicial del potencial cuando se realiza la imposición del mismo. De manera general en los tres casos se observa un comportamiento estable de la corriente en el tiempo. Esto demuestra que la señal de respuesta es estable; por tanto, el tiempo de lectura puede ser fijado en cualquier momento después de imponer el potencial. En este trabajo el tiempo fijado fue de 10 s.
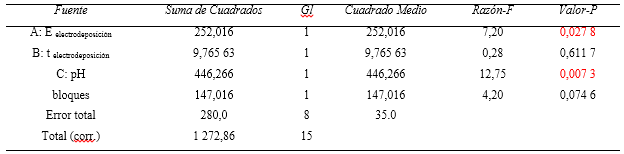
La tabla 1 muestra el análisis de varianza para el establecimiento de las condiciones experimentales para la cuantificación de cadmio empleando el método voltamperométrico. De los factores estudiados, el potencial de electrodeposición y el pH del medio tienen un valor p inferior al nivel de significación (0.05), indicando que tienen influencia estadísticamente significativa en la corriente de pico, con un nivel de confianza del 95 %; por tanto, son parámetros experimentales a tener en cuenta durante la determinación voltamperométrica de cadmio.
Tabla 1 Análisis de varianza simple de efectos principales sobre la intensidad de corriente de pico (ip).
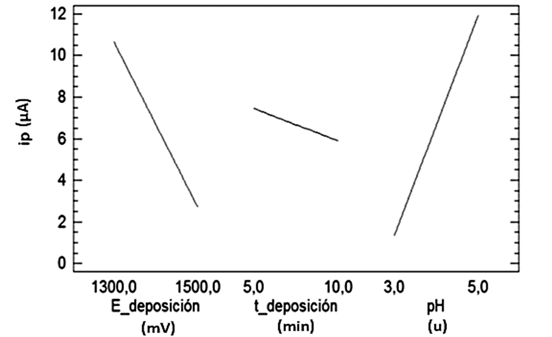
El efecto de las diferentes condiciones estudiadas sobre la corriente de pico (ip) puede observarse en la figura 2. Al aumentar modularmente el potencial de electrodeposición, se observa una significativa disminución de la corriente de pico. Esto puede estar asociado fundamentalmente al hecho de que la electrodeposición de cada metal ocurre a un potencial específico,17-19
La corriente de pico no tiene una variación significativa con el aumento del tiempo de electrodeposición de 5 a 10 min; sin embargo, este es un factor que ha sido reportado en ocasiones como importante para la electrodeposición.17,19,20 Este hecho experimental puede deberse a que a los 5 min ya se ha electrodepositado todo el cadmio en el electrodo, por lo que a tiempos de deposición mayores no se evidencia un incremento de la corriente de pico.
Al aumentar el pH de 3 a 5, la corriente de pico aumenta, esto se debe a que a valores de pH más ácidos la evolución de hidrógeno interfiere en el proceso de electrodeposición de este metal, casi siempre el cadmio se determina voltamperométricamente a pH porque es donde mejor ocurre su electrodeposición.1,21,22
Las condiciones óptimas fijadas a partir de estos resultados son: potencial de electrodeposición de -1300 mV, pH 5, tiempo de electrodeposición de 5 min en agitación, barrido lineal de potenciales de -1200 mV a -10 mV.
Voltamperogramas y curva de calibración
La figura 3 muestra los voltamperogramas de la redisolución anódica del cadmio, que fueron obtenidos bajo las condiciones de trabajo establecidas con anterioridad. Se pueden observar los picos típicos de los voltamperogramas obtenidos por redisolución. La corriente de pico aumenta con el potencial hasta alcanzar un valor máximo cerca de los -800 mV, indicando la presencia de cadmio. Se observa la variación de la corriente de pico con la concentración, lo que permite la construcción de una curva de calibración.
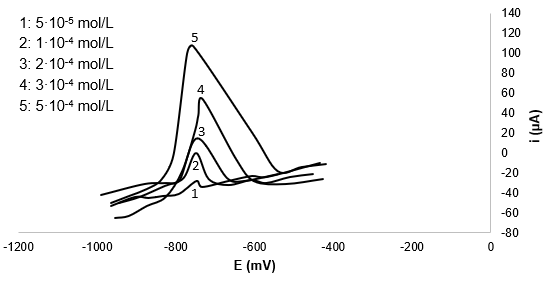
Fig. 3 Voltamperogramas de la redisolución anódica del cadmio a diferentes concentraciones en KCl 1 mol/L y medio buffer ácido acético/acetato de sodio. ET: película de mercurio sobre carbono, EA: Carbono, ER: alambre de Ag
La figura 4 muestra tres curvas de calibración y la curva promedio para el intervalo de concentraciones de 6·10-5 a 5·10-4 mol/L. Al aumentar la concentración de cadmio, la intensidad de corriente correspondiente al proceso de reoxidación aumenta linealmente. El coeficiente de correlación lineal (r) de la curva promedio es 0,996 8; lo que demuestra que existe una fuerte correlación lineal entre la corriente y la concentración. El coeficiente de determinación (R2) es 0.9936; lo que evidencia que el modelo matemático generado explica un 99.36 % de la variabilidad entre ambas variables. El coeficiente de determinación ajustado a grados de libertad (R2 aj.) es 0,993 1.
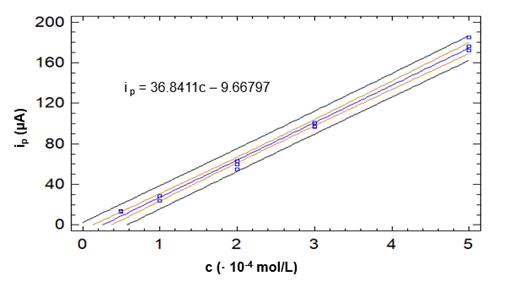
Fig. 4 Curva de calibración voltamperométrica de CdCl2 para la cuantificación de cadmio en el residual de laboratorio
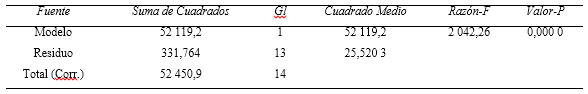
La tabla 2 muestra el ANOVA simple de la curva de calibración para la determinación de cadmio en el residual. El valor p es inferior al nivel de significación (0.05), lo que indica que existe una relación estadísticamente significativa entre la corriente de pico y la concentración para el 95 % de confianza.
Tabla 2 Análisis de varianza simple de la regresión lineal de la curva de calibración para la cuantificación de cadmio en el residual de laboratorio.
Los resultados de la regresión lineal para la curva de calibración obtenida empleando el método propuesto en este trabajo, están en correspondencia con los resultados mostrados por otros autores que emplearon la voltamperometría de redisolución para la cuantificación de cadmio en diferentes muestras. Silva y col.17 reportan una curva de calibración para cadmio con coeficiente de determinación de 0,995 y utilizan un electrodo de trabajo de película de mercurio sobre carbón vítreo. Quispe 22 emplea la voltamperometría de redisolución con una curva de calibración con coeficiente de determinación de 0.9935. Moreno y col.1 reportan la cuantificación de cadmio a pH 5 empleando una curva de calibración con coeficiente de determinación de 0,994 3.
Límites de detección y cuantificación
Para el método voltamperométrico de determinación de cadmio por redisolución anódica sobre electrodos de película de mercurio, el límite de detección (LD) fue 10-5 mol/L y el límite de cuantificación (LC) fue 5·10-5 mol/L.
Los valores obtenidos para cada uno de los límites son inferiores al valor mínimo de 10-4 mol/L reportado para la voltamperometría de barrido lineal sin preconcentración.7
Vilasó y col.11 reportan la determinación de cadmio empleando mínima instrumentación, pero sobre un electrodo de grafito, o sea, sin preconcentración. Este estudio mostró un límite de detección de 3∙10-4 mol/L, y un límite de cuantificación de 10-3 mol/L. Se observa como en el presente trabajo los límites alcanzados son mucho menores. El límite de detección se logró disminuir en un orden de magnitud, mientras que el de cuantificación se disminuyó en dos órdenes de magnitud.
Repetibilidad
Para evaluar la repetibilidad del método voltamperométrico de redisolución se estimó la concentración del analito a partir de disoluciones patrones de cadmio a las concentraciones 6·10-5; 3·10-4 y 5·10-4 mol/L, correspondientes a tres puntos de la curva de calibración. La tabla 3 muestra los resultados obtenidos.
Tabla 3 Repetibilidad del método voltamperométrico de redisolución anódica para la determinación de Cd2+.
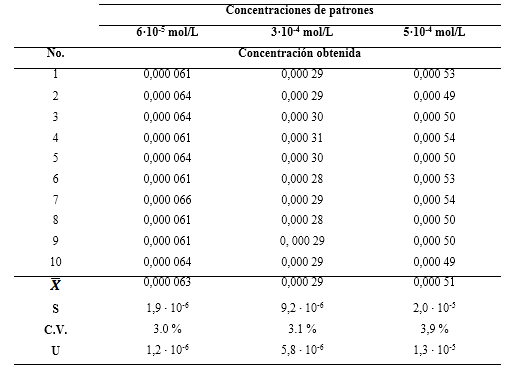
La desviación estándar es pequeña en cada caso, siendo de orden menor que la concentración del patrón correspondiente. Esto indica que existe poca dispersión de los valores. Los coeficientes de variación son aceptables, teniendo en cuenta que todos son inferiores al intervalo de 4 a 6 % reportado para el método voltamperométrico.1 Los coeficientes de variación en voltamperometría se reportan en un amplio intervalo. Valdivieso 23 muestra coeficientes de variación en el intervalo de 2 a 9 %. Quispe 22 reporta un coeficiente máximo de un 8 %. Romero y col. 24 obtienen coeficientes de variación de 6,5 y 7,5 % para diferentes concentraciones de cadmio empleando un electrodo de carbón vítreo modificado con película de bismuto.
Tomando en cuenta los resultados reportados por Vilasó y col. 10 en un estudio de incertidumbre para el método voltamperométrico, la única fuente de incertidumbre incluida en la estimación fue la repetibilidad de los resultados. La incertidumbre en todos los casos es de orden menor que el correspondiente a cada concentración de patrón, lo que está de acuerdo con lo establecido por la Guía para la Estimación de Incertidumbre de Medición.16 Esto demuestra que el método es preciso en condiciones de repetibilidad.
Reproducibilidad
La tabla 4 muestra los resultados para cinco repeticiones de la determinación de cadmio bajo condiciones de reproducibilidad interdía-interanalista, es decir, usando dos analistas en días diferentes.
Tabla 4 Reproducibilidad del método voltamperométrico de redisolución anódica para la determinación de Cd2+.
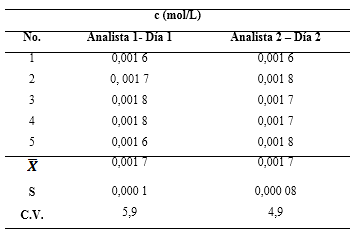
Una prueba Fisher para la comparación de las varianzas arrojó un estadístico F de 1,428 57 y un valor p de 0,738 042. Teniendo en cuenta que el valor p es mayor que el nivel de significación de la prueba (α=0,05), no existen diferencias estadísticamente significativas entre las varianzas para las determinaciones realizadas por ambos analistas en días diferentes.
Se realizó una prueba t para la comparación de los resultados obtenidos por ambos analistas partiendo de la hipótesis nula de que las medias son iguales. La prueba arrojó un estadístico t de -0,342 997 y un valor p de 0,740 439. Teniendo en cuenta que el valor p es mayor que el nivel de significación de la prueba (α=0,05), es posible afirmar que no existen diferencias estadísticamente significativas entre las concentraciones determinadas por ambos analistas en días diferentes, con un 95% de confianza.
Esto demuestra que el método voltamperométrico de redisolución anódica para la cuantificación de cadmio es reproducible.
Exactitud
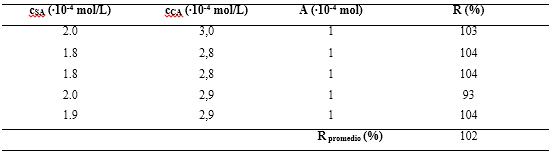
La tabla 5 muestra los valores del porcentaje de recuperación de cinco muestras de un patrón a las cuales se les realizó una adición de estándar de 0,000 1 mol de cadmio. Los porcentajes de recuperación en todos los casos son superiores al 80 % y menores que el 110 %, límites mínimo y máximo establecidos por la Norma Cubana.15 El porcentaje promedio fue de un 102 %. Esto demuestra que el método es exacto.
Análisis de muestras de un residual líquido
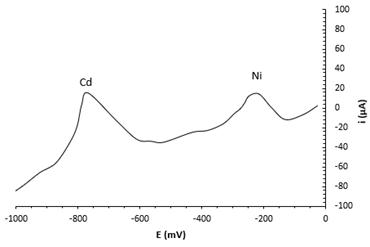
La figura 5 muestra un voltamperograma de redisolución anódica para el análisis del residual líquido del laboratorio de Electroquímica Analítica. Se observa correspondencia con la forma esperada para este tipo de voltamperometría. Aparecen dos picos de redisolución, el primero a - 750 mV y el segundo a -200 mV. El primer pico es el correspondiente al cadmio, teniendo en cuenta que el valor del potencial corresponde con el observado en los voltamperogramas de los patrones de cadmio en la figura 3. El segundo pico corresponde a la redisolución de níquel, debido a que la muestra analizada contiene también este metal.
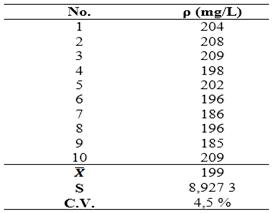
La tabla 6 muestra los resultados obtenidos del análisis de 10 muestras del residual. Se reporta además el promedio, desviación estándar y coeficiente de variación. El coeficiente de variación tuvo un valor aceptable, estando en el intervalo teórico reportado para el método voltamperométrico de un 4 a un 6 %.7,25
Conclusiones
Se desarrolló el método voltamperométrico de redisolución anódica para la determinación de cadmio en aguas residuales. Se observó un aumento de la corriente de pico a pH 5 y a un potencial de -1300 mV, mientras que los tiempos de electrodeposición estudiados no mostraron influencia significativa. El intervalo lineal del método estuvo entre 6·10-5 y 5·10-4 mol/L. El límite de detección fue 10-5 mol/L y el límite de cuantificación fue 5·10-5 mol/L. El método es preciso y reproducible, con coeficientes de variación en correspondencia con lo reportado para este tipo de Voltamperometría. Es exacto, con porcentajes de recuperación dentro de los límites establecidos en la literatura. La incertidumbre asociada a la determinación de la concentración de cadmio fue de orden menor que la concentración correspondiente. El análisis de muestras del residual líquido mostró una concentración de cadmio de 199 ± 8,9 mg/L, con un coeficiente de variación aceptable.