Introducción
Los metales son contaminantes no biodegradables y se acumulan fácilmente en los organismos vivos, causando enfermedades graves. 1 Estos elementos metálicos pueden ser tóxicos para los seres vivos cuando están presentes en sistemas ambientales, a concentraciones superiores a ciertos niveles, aunque algunos son nutrientes esenciales para las plantas y los animales. 2
El petróleo crudo está compuesto por elementos metálicos a niveles traza, dependiendo del origen del petróleo la concentración de éstos puede superar los 100 y 1000 ppm, respectivamente. 3,4 Estos metales se encuentran en los compuestos carboxilatos, porfirínicos y no porfirínicos presentes en las fracciones pesadas del petróleo, 3 las cuales son las responsables de algunos los problemas que se generan durante la extracción, el almacenamiento, el transporte y la refinación, 5,6 además, sus emisiones causan contaminación ambiental así como efectos mutagénicos y cancerígenos, por lo que sus niveles son regulados en muchos países. 7
Existen diferentes métodos para la reducción de metales pesados en la industria petrolera, ya sea del crudo o de los derivados del proceso de refinación. Algunos autores (8 plantean que la combustión de fuel oil genera cenizas volátiles y escoria con altas concentraciones de V y Ni, los cuales son altamente contaminantes y pueden ser valoradas por calcinación y lixiviación. La escoria con 8% Ni; 28 % V fue tratada con lixiviación agitada con H2SO4 lo cual permitió recuperar 22% Ni y 75% V en solución.
Algunos autores estudiaron 9) la adsorción de Ni y V de los crudos y coques venezolanos a partir de soluciones ácidas mediante ligninas, se utilizó un carbón activado comercial como referencia.
Otro autor 10) aisló los complejos metaloporfirínicos del crudo Ayacucho, que es donde se encuentran estos metales, mediante extracción Soxhlet con acetonitrilo como solvente. Se tomó una muestra de 10,221 g de dicho crudo obteniéndose 6,223 g del residuo generado posterior a la evaporación del solvente de extracción, lo que representa un 60%. Todos estos métodos resultan atractivos, pero poco viables al utilizar soluciones ácidas y materiales poco comunes.
Actualmente existen investigaciones relacionadas con la reducción de metales pesados utilizando materiales porosos como son los carbones activados y la zeolita, este último es de origen natural y nuestro país cuenta con un gran número de formaciones de este mineral distribuidas en todo el país. Por lo que sería una opción de grandes ventajas económicas y tecnológicas. 11,12
Las zeolitas son aluminosilicatos microporosos que destacan por su capacidad de hidratarse y deshidratarse reversiblemente. Son sólidos con una estructura cristalina tridimensional relativamente abierta construida a partir de los elementos aluminio, oxígeno y silicio, con metales alcalinos o alcalinotérreos (como el Na, K y Mg) más moléculas de agua atrapadas en los huecos entre ellos. 13,14
Este mineral es aplicado en la reducción de metales pesados en diferentes ámbitos, estudiándose los efectos de la tasa de flujo, el tamaño de las partículas (0,8-1,7 mm), la concentración y el enriquecimiento con Na+ de la clinoptilolita natural en la eficiencia de remoción de metales pesados en soluciones acuosas. 15 La eficiencia de remoción aumenta al disminuir el tamaño de partícula y la concentración. Con la modificación de la muestra natural se logró el aumento de la eficiencia de remoción en un 32 a un 100%. Logrando el orden de eficiencia de eliminación siguiente: Pb2+> Cr3+> Fe3+ ≥Cu2+.
También fue investigado el intercambio de algunos iones metálicos en solución acuosa sobre cuatro muestras de minerales zeolíticos, constituidas principalmente por zeolita natural clinoptilolita. Para los iones metálicos Cr (III), Pb (II), Cd (II), y Zn (II) se reportan porcentajes de remoción que varían de 3,82 a 74,5 %. Otros autores12 plantearon que la remoción de material contaminante en orden descendente es dureza (Ca+2 y Mg+2)>NH4+>material coloidal (materia orgánica).
En la industria petroquímica la zeolita se utiliza como catalizadores para el hidromejoramiento del craqueo catalítico en lecho fluido (FCC, según sus siglas en inglés) de gasolina y en la desulfuración profunda de los combustibles diésel. 16,17 De esta forma constituiría una novedad su aplicación en el crudo ligero cubano para reducir metales pesados, para de esta manera aplicarla en las aguas contaminadas con crudo.
Teniendo en cuenta la importancia de reducir los contenidos de metales pesados en el crudo ligero cubano y las propiedades de adsorción e intercambio iónico en las zeolitas se propone valorar la aplicación de la misma
Materiales y métodos
Los materiales usados en la investigación fueron zeolita del yacimiento de San Andrés del tipo clinoptilolita y crudo ligero cubano. Las muestras de zeolita fueron obtenidas de la Planta de Procesamiento de zeolitas naturales en Loma Blanca, de la Unidad Empresarial Minera (UEB) Geominera Holguín.
El petróleo crudo ligero utilizado en la experimentación proviene de uno de los yacimientos ubicados en la costa norte de La Habana y Matanzas. Fue caracterizado tanto física como químicamente en el Centro de Investigaciones del Petróleo (CEINPET), La Habana, Cuba. Para la caracterización química se utilizó el procedimiento OXFORD y para la física como los oAPI y densidad la norma ASTM-D 1298/99.
Las muestras de zeolitas naturales comprenden su caracterización desde la química y la física hasta la mineralógica y la granulométrica. En esta investigación solo fue realizada la primera en el laboratorio Elio Trincado de la Empresa Geominera Oriente, Santiago de Cuba y la última en laboratorio de Operaciones Unitarias (OPU) de Universidad de Oriente.
Las muestras de zeolita para la caracterización granulométrica se lavaron con agua destilada durante 5 repeticiones para eliminar el polvo. Luego fueron dispuestas en bandejas para eliminar la humedad y se sometieron a secado durante 3 h a temperatura constante de 110ºC. Se pesaron 460 g de zeolita con una balanza analítica Sartorius y se tamizaron de acuerdo a las diferentes clases para determinar donde se encontraba la mayor fracción en peso.
Cada muestra de zeolita fue analizada por ICP-AES (Espectrometría de Emisión Atómica con Plasma Inductivamente Acoplado) en su estado natural y una vez puesta en contacto con el crudo. Las mediciones se efectuaron en un Spectroflame Modula, secuencial de la firma alemana SPECTRO. 18
A partir de los datos obtenidos de concentración en %, se calculó el porcentaje en óxido de los elementos mayoritarios según ecuación 1: (19)
Experimentos de zeolita con crudo
Para evaluar la capacidad de la zeolita para captar metales pesados del crudo se pusieron ambos en contacto teniendo en cuenta los parámetros siguientes: granulometría y relación sólido líquido (S/L), por un tiempo de 18h.
Las granulometrías utilizadas fueron las retenidas en los tamices malla 6 y 18 que reportaron los mayores porcentajes en peso de la muestra.
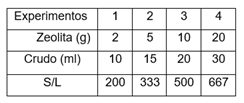
En la tabla 1 se muestran las relaciones S/L utilizadas. Fueron tomadas teniendo en cuenta que se realizará a pequeña escala y que en las referencias consultadas manejan diferentes relaciones desde 2 hasta 700, siendo una variable de influencia en los procesos de adsorción. 20
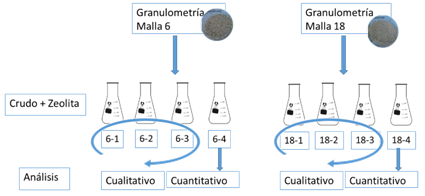
Los experimentos se realizaron según figura 1. El número de los erlenmeyers que se muestra se refiere, el primero a la granulometría (3,35 o 1 mm) y el segundo al experimento con diferentes relaciones S/L.
Los análisis cualitativos fueron analizados según la retención de crudo en el lecho de zeolita para las 2 granulometrías analizadas luego del contacto con el crudo.
Los análisis cuantitativos se le realizaron a la zeolita por la técnica de ICP-AES donde se obtuvo la concentración de metales en la zeolita como son: V, Pb, Hg, Ba, Fe.
Resultados y discusión
Análisis granulométrico
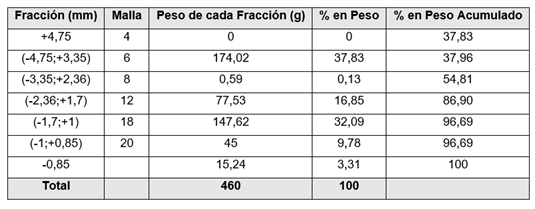
Los resultados del análisis granulométrico de la zeolita se muestran en la tabla 2. Reflejan que la mayor cantidad de la muestra original se encuentran entre las fracciones (-4,75+3,35) mm y (-1,7;+1) mm con un 37,83 % y el 32,09 % en peso de respectivamente. De esta forma los experimentos con el crudo y la zeolita se realizaron con ambas granulometrías para valorar la influencia que puede tener esta variable en la remoción de compuestos.
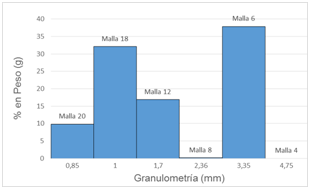
La representación del porcentaje de masa retenido por cada tamiz más utilizada es en forma de histograma, en el eje de abcisas (eje x) los intervalos de tamaño y el porcentaje de masa retenido por cada tamiz en el eje de las ordenadas (eje y).
La figura 2 muestra el comportamiento de la distribución granulométrica y confirma que el mayor porcentaje de la muestra queda retenido en los tamices mallas 6 y 18.
Composición química de la zeolita natural
Los resultados del análisis mayoritario y minoritario por ICP-AES se presentan en las tablas 3 y 4. Demuestran una correspondencia bastante cercana con los valores reportados en la literatura. (21,22
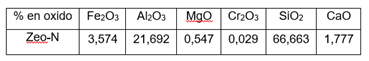
Se puede observar en la tabla 3 el porcentaje en óxido de elementos mayoritarios, siendo los de mayores valores el SiO2 y el Al2O3 propio de los aluminosilicatos, presentando una relación molar SiO2 /Al2O3 de 5,43; típico de zeolitas con un alto contenido de sílice. Este valor permite esperar una mayor estabilidad térmica, marcadamente hidrofóbicas y estables frente a soluciones ácidas lo que tiene indiscutible valor práctico. Le sigue con valores que no sobrepasan el 5% los óxidos de Fe, Ca, Mg y Cr (III).
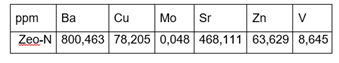
Para los elementos minoritarios presentados en la tabla 4 destaca el Ba y el Sr, seguido del cobre y el zinc y en menor concentración el vanadio y el molibdeno.
Composición física y química del crudo cubano
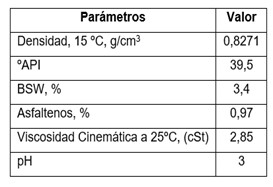
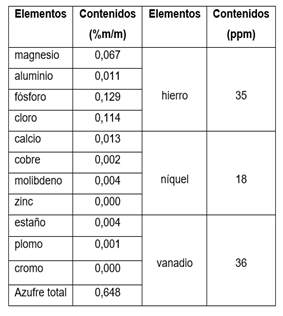
Los resultados de la composición física y química se muestran en las tablas 5 y 6. Es un crudo ligero porque tiene baja viscosidad y densidad. Es ácido porque su pH es de 3. En su composición química se destaca la presencia de azufre y no contiene Zn y Cr. La relación V/Ni se utiliza para identificar el origen y la edad del petróleo, en este caso la relación es de 2 lo que indica que es un petróleo crudo joven y en condiciones reductoras.
Análisis experimentos de zeolita con crudo
Los experimentos de crudo en contacto con la zeolita se realizaron para evaluar la capacidad de la zeolita de captar determinados elementos químicos como metales pesados de importancia medioambiental, así como evaluar la propiedad de retención del lecho.
Análisis cualitativo
El contacto de la zeolita del yacimiento de San Andrés con el crudo cubano permitió con el análisis de 2 granulometrías, demostrar una mayor retención del lecho de menor granulometría, resultado que puede ser valorado para uso industrial, como el tratamiento de residuales.
En la figura 3 se muestra el resultado del crudo luego del contacto con la zeolita, el número 6 y 18 se refiere a la granulometría del experimento y el 2 a que ambos se realizaron bajo la misma relación S/L de 333. Se observa que el experimento 18-2 tiene un menor volumen de crudo lo que evidencia mayor retención de la zeolita de menor granulometría. Esto se debe a que cuanto menor es el tamaño de las partículas, mayor es el área disponible o la superficie de contacto.
Análisis cuantitativo
Al realizar el análisis químico por ICP-AES de la zeolita en contacto con el crudo de los experimentos 6-4 y18-4 se obtuvieron los siguientes resultados.
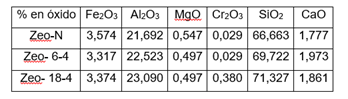
En la tabla 7 se muestran los valores de la composición química en base a óxido de la zeolita tanto natural (Zeo-N) y de las 2 granulometrías estudiadas luego del contacto con el petróleo crudo (Zeo- 6-4 y Zeo- 18-4). Se observa además que se produce una disminución del contenido de MgO, esto corrobora que el proceso de intercambio estuvo dado por los iones Mg2+ que intercambió con los iones metálicos presentes en el crudo y no por los iones Ca2+ que aumentaron su concentración. En el caso de los iones K+ y Na+ aunque no fueron determinados en estos experimentos, existe la posibilidad de que alguno esté involucrado en el proceso de intercambio iónico.
El aumento del contenido de CaO, muestra que el ion Ca2+ pasa a la zeolita quedando retenida en ella, resultado favorable porque evidencia la aplicación de la zeolita en la eliminación de la dureza del agua contaminada con crudo. El por ciento de Fe2O3 disminuyó en señal de que la zeolita cedió este metal.
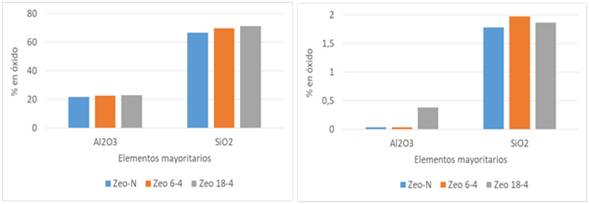
En la figura 4 se muestra el comportamiento de la granulometría en cuanto a la adsorción de los compuestos mayoritarios. Se dividieron en 2 gráficas por las diferencias de concentraciones. Se pudo corroborar lo anteriormente expuesto en el análisis cualitativo de que, a menor granulometría, mayor retención del lecho. En este caso las mayores retenciones del lecho (AlO3, Cr2O3, SiO2) están dada para las muestras de menor granulometría, excepto para el CaO en el cual la mayor retención estuvo dada por la zeolita de mayor granulometría.
Anteriormente en la caracterización química del crudo se expuso que el crudo no contiene Cr, sin embargo la zeolita captó este metal (figura 4), esto puede estar dado por la sensibilidad de las técnicas de análisis, en el caso del ICP es de mayor
precisión.
El resultado obtenido con el Cr2O3 fue expuesto por otros autores. 23 donde con tamaños de partículas de 0,85 mm, fue el adecuado para proporcionan una adecuada superficie de transferencia para la adsorción de este compuesto. Este proceso ocurre por adsorción específica polar de los iones cromato sobre la superficie externa del mineral.
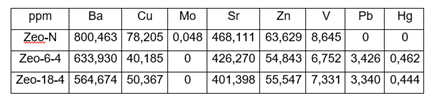
En la tabla 8 se muestran los resultados de la composición química de los elementos minoritarios de la zeolita tratada con crudo. Como se puede apreciar ocurre una disminución en la concentración de estos elementos.
El caso del Ba la zeolita cede este metal, por liberación de 236 ppm para la menor granulometría. Lo mismo ocurre para el Cu, Mo, Sr, Zn y V debido a que los 5 cationes forman parte de la composición de la zeolita, pero en menor cantidad que el Ba, estos cationes son sustituidos como cationes compensantes de la carga negativa de la estructura zeolítica por protones hidratados, dado el pH bajo del crudo. 24
En esta tabla también se muestran las composiciones de los metales que la zeolita captó pero no formaban parte de su estructura como son el caso de Pb y el Hg. Existen numerosos reportes de esta selectividad por otros autores. (25,26 En el caso del Pb la alta selectividad se debe a su radio hidratado pequeño que le permite entrar a los canales de la zeolita, factor importante para que ocurra este proceso de adsorción.
Tabla 8 Composición química de los elementos minoritarios de la zeolita de 2 granulometrías tratadas con crudo
En la figura 5 se muestra el comportamiento de la granulometría en cuanto a la adsorción de los compuestos minoritarios, como son el caso del Pb y el Hg. En este
caso, a mayor granulometría ocurrió una mayor adsorción de estos compuestos, aunque las diferencias no son tan marcadas.
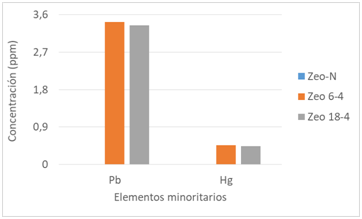
Fig. 5 Comportamiento de la adsorción de los elementos minoritarios para las 2 granulometrías estudiadas
Estos resultados son satisfactorios porque debido a la no biodegradabilidad típica de los metales pesados, su eliminación es necesaria, aunque se encuentren en niveles muy bajos (trazas), porque se acumulan y con el tiempo pueden alcanzar magnitudes perjudiciales donde son depositados.
En los resultados de ICP se puede apreciar que hay elementos metálicos de interés como el Cu, Zn y V que la muestra de zeolita ya tenía en su composición inicial. Esto puede afectar de manera negativa a la hora del intercambio de la zeolita con la disolución, ya que al tener presentes elementos en su estructura que se desean eliminar en la disolución, dicho intercambio puede ser en sentido contrario.
Conclusiones
1- El análisis granulométrico de la zeolita del yacimiento de San Andrés, mostró que el mayor porcentaje de la muestra quedó retenido en los tamices malla 6 y 18, con tamaños de partículas de 3,35 y 1 mm respectivamente, por lo que con ellas fueron realizados todos los experimentos.
2- La caracterización química de la zeolita fue realizada utilizando ICP-AES, se obtuvo una relación molar SiO2/Al2O3 de 5,43 típico de zeolitas con un alto contenido de sílice, gran estabilidad térmica, hidrofóbicas y estables frente a soluciones ácidas lo que le confieren aplicación práctica, los elementos minoritarios fueron Ba, Zn, V y Mo.
3- Los experimentos de adsorción aplicando zeolita natural con crudo mostraron la capacidad del material de adsorber metales pesado como Pb y Hg que no se encontraban en su estructura natural, en el caso del Cr la menor granulometría favoreció una adecuada superficie de transferencia para la adsorción de este compuesto, el Ca2+ fue otro ion retenido en la zeolita y a pesar de no ser un metal pesado es favorable en la eliminación de la dureza del agua contaminada con crudo.