INTRODUCCIÓN
Los pacientes con COVID-19 que transitan hacia estadios graves y críticos de la enfermedad, se caracterizan por desarrollar una inflamación sistémica exacerbada. 1) En este contexto, es vital la identificación y tratamiento de la hiperinflamación, para reducir la mortalidad en los pacientes. En el mundo se recomiendan terapias aprobadas para el tratamiento de enfermedades autoinmunes. 2 Sin embargo, estos fármacos son inmunosupresores potentes y el uso de estas terapias para tratar la COVID-19, puede conllevar al empeoramiento del estado general de los pacientes. Se ha comprobado que el virus persiste durante el transcurso de la enfermedad, y para contribuir a su eliminación eficaz, el sistema inmunológico no debe estar sometido a terapias inmunosupresoras. 3,4
Una alternativa terapéutica para el tratamiento de pacientes graves y críticos con COVID-19, es el péptido codificado como CIGB-258. En el Centro de Ingeniería Genética y Biotecnología (CIGB), se diseñó y desarrolló dicho péptido (previamente denominado APL1 y posteriormente CIGB-814) para el tratamiento de las enfermedades autoinmunes, específicamente para la artritis reumatoide (AR). Este péptido fue diseñado a través de herramientas de la bioinformática; es derivado de un epitopo de células T de la proteína de estrés celular (HSP, del inglés Heat Shock Protein) de 60 kDa (HSP60). 5,6). El epitope de células T identificado, fue modificado en un aminoácido, lo cual transformó el fenotipo TH1 (de inglés, T helper) del epitopo original en un péptido con propiedades inmunoreguladoras. 5-10
En este trabajo se describen los resultados fundamentales relacionados con el tratamiento del CIGB-258 a un grupo de pacientes graves y críticos con COVID-19, para lo cual fueron esenciales los estudios de farmacocinética y biodistribución del péptido en ratas Lewis. Además, se evalúan una serie de parámetros clínicos, radiológicos y biomarcadores inflamatorios sistémicos en estos pacientes. El presente trabajo tiene como objetivo demostrar que el CIGB-258 reduce la hiperinflamación en los pacientes con COVID-19.
MÉTODOS
Farmacocinética y biodistribución del péptido en ratas Lewis
Se estudiaron 3 niveles de dosis: 5 mg/kg, 1 mg/kg and 0,25 mg/kg. El estudio se realizó a través de 3 rutas de administración: subcutánea, intradérmica e intravenosa en ratas Lewis.
Estudios en pacientes
Estos estudios están de acuerdo con lo establecido en la declaración de Helsinki para la investigación en humanos 11) y las directrices de la Conferencia Internacional de Armonización. El Comité de Ética y el Consejo Científico del Hospital Militar Central Dr. Luis Díaz Soto y la Autoridad Reguladora de Cuba (CECMED) aprobaron el protocolo.
Este estudio fue registrado como RPCEC00000313 en el Registro Público Cubano de Ensayos Clínicos. Los pacientes fueron incluidos, entre el 31 de marzo y el 24 de abril de 2020, en el Hospital Militar Central Dr. Luis Díaz Soto. Los pacientes fueron diagnósticos con la COVID-19 y tratados según el protocolo cubano de actuación contra la COVID-19. (12) Se incluyeron 13 pacientes críticos y 9 pacientes graves.
Se registraron las características demográficas, la clasificación clínica (condición crítica o grave) y las comorbilidades. Las pruebas de laboratorio, las radiografías de tórax y los resultados clínicos se registraron de acuerdo al protocolo establecido para este estudio (RPCEC00000313). Se obtuvieron muestras de suero antes del tratamiento con CIGB-258 (T0) y después de 24 h, 48 h, 72 h y 96 h de tratamiento.
Se midieron en el suero, los niveles de las citocinas: IL-6, TNFα e IL-10 usando el panel de perlas magnéticas de células T CD8 + humanas (HCD8MAG15K17PMX, EMD Millipore, Alemania) de acuerdo con las instrucciones del fabricante. Los resultados se obtuvieron mediante el analizador Luminex® y se procesaron en el software Milliplex Analyst v 5.1.0.0 (MAGPIX® y Millipex EMD Millipore, Alemania). Los niveles de la Calprotectina se cuatificaron mediante un ELISA comercial (R and D system)
Los datos de seguridad de los pacientes, fueron recolectados de acuerdo a la Resolución 45/2007 13 de la Autoridad Reguladora de Cuba: “Requisitos para reportar eventos adversos en ensayos clínicos en curso, con base en las regulaciones de la OMS”.
Los eventos adversos, los signos vitales, las radiografías de tórax y las evidencias de efectos terapéuticos se compararon descriptivamente entre el valor inicial (T0) y los datos recopilados de los pacientes después de comenzar el tratamiento con CIGB-258.
Los parámetros de laboratorio, los niveles en suero de las citocinas se analizaron a través del paquete estadístico GraphPad Prism, versión 8.02 (GraphPadSofware, San Diego California, EE. UU.). Los datos se examinaron para determinar la normalidad y la igualdad de varianza con las pruebas de Kolmogorov-Smirnov y Bartlett, respectivamente. Los niveles de PCR (proteína C reactiva) se expresaron como medias y las diferencias se analizaron con ANOVA y la prueba de Tukey. Se utilizaron las pruebas de de Kruskal-Wallis y Dunn para los niveles séricos de citocinas. Los valores de p < 0,05 se consideraron estadísticamente significativos.
RESULTADOS
Farmacocinética y biodistribución del péptido en ratas Lewis
La concentración plasmática del péptido marcado con yodo [125I] a lo largo del tiempo estuvo de acuerdo con la administración extravascular del fármaco. La figura 1, panel A muestra los gráficos para los 3 niveles de dosis (5 mg/kg, 1 mg/kg y 0,25 mg/kg). Según el análisis de datos, la variación interindividual, expresada como desviación estándar del valor de concentración promedio en cada punto de tiempo, fue adecuada, mostrando valores más elevados en el nivel de dosis más alto (5 mg/kg). El ajuste a los modelos farmacocinéticos compartiméntales no fue homogéneo, por lo que el análisis de pK se realizó mediante análisis no compartimental. Se obtuvo una dependencia de la dosis para el AUC, en el intervalo de confianza del 95 %, para cada nivel de dosis (figura 1, panel B).
Por otro lado, la concentración máxima del péptido en la sangre de las ratas fue de 0,5 h a 1 h; y se calculó que el tiempo de vida medio estuvo de 6,3 h a 6,9 h para las 3 dosis estudiadas.

Fig. 1 Estudio farmacocinético. A) Distribución de péptido marcado con [125I] en sangre a lo largo del tiempo. El péptido se administró a razón de 5 (rombos), 1 (cuadrados) y 0,25 (triángulos) mg/kg. B) Variación interindividual, expresada como desviación estándar del valor de concentración promedio en cada momento.
El tratamiento con CIGB- 258 contribuye a la mejoría clínica y radiológica de los pacientes con COVID-19, en estado grave o crítico
Los pacientes críticos incluidos en este estudio presentaban distrés respiratorio, según los criterios de Berlín. 14 Estos pacientes presentaron mejorías clínicas, las cuales fueron corroboradas por estudios radiológicos. En la figura 2 se muestran imágenes representativas de las radiografías de tórax de un paciente.

Fig. 2 Evolución radiológica de un paciente crítico tratado con CIGB-258. A) Rx de tórax previa ventilación: Se observan radiopacidades difusas en ambos hemitórax compatibles con signos de distrés respiratorio moderado. B) Rx de tórax después de 48 h de tratamiento. Se observan lesiones inflamatorias con predominio en la base del pulmón derecho. C) Rx de tórax previa extubación: Mejoría radiológica de las lesiones previamente descritas.
El tratamiento con CIGB-258 contribuye a la mejoría de los parámetros ventilatorios y disminuye los niveles de la Proteína C Reactiva
Las mejorías clínicas y radiológicas de los pacientes ventilados, se correlacionaron con una mejoría en los parámetros ventilatorios y una disminución de los niveles de la Proteína C Reactiva (PCR). En este trabajo se realizó una cuantificación detallada de los niveles de PCR y el P/F (presión arterial parcial de oxígeno y la fracción inspirada de oxígeno: PaO2 /FiO2) en dichos pacientes. Como se muestra en la figura 3A, en correspondencia con la mejoría de los parámetros ventilatorios disminuyeron los niveles de la PCR, en los pacientes críticos. Además, hubo una correlación inversamente significativa entre el P/F y la PCR en los pacientes críticos con ventilación mecánica invasiva (P<0.040) (figura 3B).

Fig. 3 Relación entre la presión arterial parcial de oxígeno y la fracción inspirada de oxígeno (PaO2/FiO2) y la proteína C reactiva (PCR en mg/L) en 11 pacientes críticos con ventilación mecánica invasiva. +: días con ventilación. Línea de puntos: indica el inicio del tratamiento con CIGB-258. B) Correlación entre la presión arterial parcial de oxígeno y la fracción inspirada de oxígeno (PaO2/FiO2) y los niveles de la proteína C reactiva (PCR en mg/L). El análisis se realizó mediante la prueba de Spearman. *P˂0.05.
El tratamiento con CIGB-258 disminuye biomarcadores de inflamación en periferia
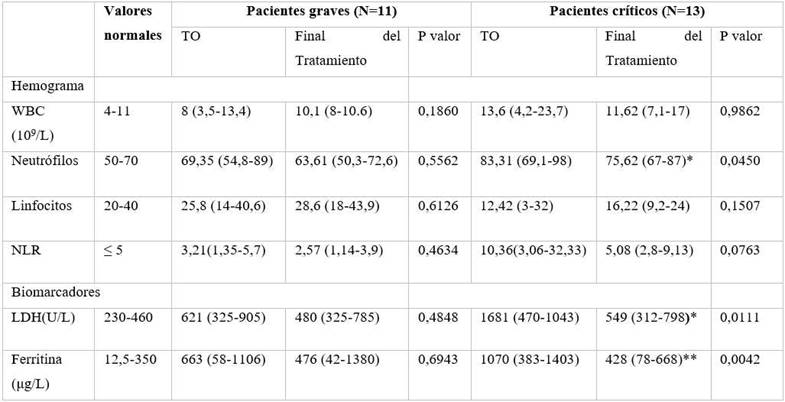
Otros biomarcadores de la inflamación como: ferritina y la lactado deshirogenasa, disminuyeron significativamente durante el tratamiento. La terapia con el CIGB-258 redujo el NLR a valores normales en la mayoría de los pacientes (tabla 1).
Por otra parte, los pacientes graves tratados con el CIGB-258 no evolucionaron hacia el estadio crítico de la enfermedad. En estos pacientes, no se observó aumento en los biomarcadores de inflamación analizados (tabla 1).
DISCUSIÓN
El mecanismo de acción del péptido CIGB-258, se ha asociado con la inhibición de la inflamación en varios modelos inflamatorios experimentales y en pacientes con AR. Este péptido regula la magnitud de la respuesta inflamatoria, pero sin causar inmunosupresión. 5-10
Los estudios de farmacocinética y biodistribución del péptido, a través de 3 vías: intravenosa, intradérmica y subcutánea, demostraron que la máxima concentración en sangre, la alcanza a la media hora y su aclaramiento ocurre en 6 h. 15) Estos resultados fueron la base para definir el tiempo de administración del péptido cada 12 h, en los pacientes con COVID-19. Estos resultados se corresponden con las propiedades farmacocinéticas del péptido observadas en los pacientes con AR. 16 No se describió ningún efecto adverso asociado al tratamiento, resultados que coinciden con las investigaciones clínicas en pacientes con AR. 9)
La mejoría clínica y radiológica de los pacientes, se asoció con una disminución de los niveles séricos de la PCR, la lactato deshidrogenasa, la creatinina, la calprotectina y las citocinas: IL-6, IL-10 y TNFα. La terapia con el CIGB-258 contribuyó a restablecer los niveles normales de neutrófilos y linfocitos en pacientes graves y críticos (17-19) Li y otros 20 describieron el perfil de proteínas de las PBMC (células mononucleares periféricas, del inglés “peripheral blood mononuclear cells”) de pacientes con la COVID-19 en estado grave. Estos autores identificaron 2 proteínas del SARS-CoV-2, que interactúan con el factor de transcripción NKRF, esta interacción produce la inducción de IL-8/IL-6, lo que conduce a la activación y migración de neutrófilos a los pulmones infectados. Estos hallazgos coinciden con resultados previos, pues el análisis del perfil de proteínas que induce el CIGB-258 en PBMC aisladas de pacientes con AR, puede interferir con la activación de neutrófilos y macrófagos alveolares, con la consiguiente reducción del biomarcador calprotectina. 19,21
Por otra parte, los pacientes de esta serie tenían linfopenia. La linfopenia se correlaciona con niveles altos de IL-6, IL-10 y TNF-α séricos. 22,23) La disminución de estas citocinas, se correlaciona con el hecho de que el CIGB-258 aumenta los niveles de Treg en modelos de AR. 5,6) Las Treg limitan la activación de las células T y reducen eficazmente los niveles de citocinas proinflamatorias, asociadas con la tormenta de citocinas en los pacientes con COVID-19. 24,25
Estos resultados preliminares son alentadores y sugieren que el CIGB-258 puede ejercer un amplio espectro de actividades biológicas, que pueden limitar la cascada inflamatoria en los pacientes con COVID-19, en fase grave y crítica.
Conclusiones
La terapia con el CIGB-258 indujo una mejoría clínica y radiológica en los pacientes graves y críticos con COVID-19, en correspondencia con su perfil de farmacocinética y biodistribución. Dicha mejoría estuvo asociada con la disminución de biomarcadores de la inflamación sistémica
La administración del CIGB-258 en los pacientes graves, evitó la progresión hacia el estadio crítico de la enfermedad. Estos resultados indican que el CIGB-258 puede limitar la cascada inflamatoria en estos pacientes
La terapia con el CIGB-258 contribuyó a restablecer los niveles normales de neutrófilos y linfocitos en pacientes graves y críticos, asociado con una disminución de los niveles de IL-6, IL-10, TNF-α. Estos resultados indican la capacidad del CIGB-258 de regular la magnitud de la respuesta inflamatoria