Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Cirugía
versión On-line ISSN 1561-2945
Rev Cubana Cir v.49 n.3 Ciudad de la Habana jul.-sep. 2010
Resección de un carcinoma renal izquierdo con extensión trombótica hacia la aurícula derecha
Resection of a left renal carcinoma with thrombotic extension to right atrium
Alejandro Villar Inclán,I Juliette Suárez López,II Nicolás Chaos González,III Adolfo García García,IV Boris Gala López,V José Copo Jorge VI
I Especialista de II Grado en Cirugía General y Cardiovascular. Profesor Auxiliar de Cirugía Cardiovascular. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
II Especialista de I Grado en Anestesia y Reanimación. Instructora de Anestesia y Reanimación. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
III Especialista de I Grado en Cirugía General y Cardiovascular. Instructor de Cirugía Cardiovascular. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
IV Especialista de I Grado en Urología. Asistente de Urología. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
V Especialista de I Grado en Cirugía General. Instructor de Cirugía General. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
VI Especialista de I Grado en Cirugía General. Asistente de Cirugía General. Hospital «Hermanos Ameijeiras». La Habana, Cuba.
RESUMEN
Se presenta el caso de un hombre de 59 años con diagnóstico de hipernefroma izquierdo y trombosis de la vena cava inferior con extensión hacia la aurícula derecha. Un equipo multidisciplinario realizó una nefrectomía radical izquierda, exposición de la vena cava inferior con técnica de piggyback, atriotomía derecha y cavotomía inferior para extracción del trombo, previo pinzamiento de la vena renal derecha y el hilio hepático. El tiempo quirúrgico total fue de 7 h 30 min. El procedimiento se realizó con anestesia general y un período mínimo de derivación cardiopulmonar. Se utilizó monitorización transoperatoria estandarizada de los parámetros vitales y además ecocardiografía transesofágica para la detección de la remoción completa del trombo y su extracción, así como posibles émbolos desprendidos. La evolución transoperatoria y posoperatoria fue satisfactoria. Se realiza una revisión de la literatura médica internacional sobre el tema y se ofrecen conclusiones.
Palabras clave: Carcinoma renal, vena cava inferior, trombosis.
ABSTRACT
This is the male case aged 59 diagnosed with left hypernephroma and thrombosis of the inferior vena cava with extension to right atrium. A multidisciplinary staff performed a left radical nephrectomy, exposition of inferior vena cava using the piggyback technique, right atriotomy and inferior cavotomy for extension of thrombus and previous clamping of right renal vein and hepatic hilus. The total surgical time was of 7 hours and 30 minutes. The procedure was performed under general anesthesia and a minimal period of cardiopulmonary shunt. Standardized transoperative monitoring of vital parameters was used and also transesophageal echocardiography to detect the total removal of thrombus and its extraction, as well as the potential detached emboli. The transoperative and postoperative course was satisfactory. A review of the international medical literature on this subject was made offering conclusions.
Key words: Renal carcinoma, inferior vena cava, thrombosis.
INTRODUCCIÓN
La trombosis de vena cava inferior (VCI) ha sido descrita en un 415 % de los pacientes con diagnóstico de carcinoma de células renales (CCR)1-3 y no necesariamente se relaciona con un peor pronóstico de la enfermedad, sobre todo cuando no está asociada a metástasis.4 Dados los diferentes niveles a los que puede llegar el trombo en la vena cava, se deben realizar todos los estudios necesarios para conocerlo y así poder definir un acceso adecuado que permita resecar todo el trombo.
La resección quirúrgica del tumor más trombectomía es el tratamiento de elección, siempre que el estado físico del paciente lo permita.5 El procedimiento es altamente riesgoso y durante su ejecución pueden aparecer importantes complicaciones, como hemorragias, embolismos y disfunción hepatorrenal, entre otras.6,7 El realizar la intervención quirúrgica constituye un gran desafío para cirujanos y anestesiólogos.
En este trabajo se presenta el caso de un paciente con diagnóstico de CCR izquierdo y trombosis de vena renal que se extendía hasta la porción supradiafragmática de la VCI, con protrusión en la aurícula derecha (AD). Se muestran las estrategias quirúrgicas y anestésicas.
PRESENTACIÓN DEL CASO
Paciente del sexo masculino, de 59 años y 74 kg de peso, con antecedentes de hipertensión arterial (HTA), sin tratamiento habitual. Fue hospitalizado para estudio por pérdida de peso y astenia. Al efectuarse una ecografía abdominal se detecta un proceso expansivo renal izquierdo, muy vascularizado, con trombo en la vena renal de ese lado que penetra en VCI.
El ecocardiograma transtorácico (ETT) reveló la existencia de una masa homogénea de 2 cm x 5,2 cm (área de 6,2 cm²) de la VCI que penetra en la AD. En la ecocardiografía transesofágica (ETE) se especifica la existencia de una masa de bordes bien definidos, homogénea y alargada, con bandas en su extremo distal, que llega hasta el tabique interauricular; no es móvil y aunque está en contacto íntimo con las paredes de la VCI no hay evidencia de que las infiltre. Dicha masa entra en la AD hasta su porción media sin obstrucción del flujo de la VCI hacia la AD. La masa medía 7,06 cm de longitud x 1,65 cm transversal (área de 7,2 cm²). Estas características permitieron clasificar la extensión cefálica del trombo en grado IV, según Neves y Zincke.8
La tomografía axial computarizada, la resonancia magnética nuclear y la cavografía mostraron que existía trombosis de la cava inferior y renal con prolongación hacia la aurícula derecha.
En la evaluación clínica no se encontraron alteraciones relevantes al examen físico ni en las pruebas complementarias, excepto la presencia de valores de creatinina en 151 mmol/L. La radiografía de tórax fue normal. En el electrocardiograma (EKG) se detectó bradicardia sinusal. La coronariografía reportó ausencia de lesiones significativas de las coronarias. El ETT mostró función normal del ventrículo izquierdo (fracción de eyección del 56 %) y ausencia de alteraciones valvulares. Los tamaños y volúmenes de las cavidades estaban dentro de valores normales.
Un equipo multidisciplinario integrado por urólogos, cirujanos cardiovasculares y generales, angiólogos, perfusionistas y anestesiólogos se reunió para evaluar la posible intervención quirúrgica con el objetivo de resecar el tumor renal y efectuar trombectomía. Después del análisis cuidadoso de riesgos y beneficios se decidió realizar la operación, previo consentimiento del paciente y la familia.
Desde la semana anterior a la intervención se indicó terapia broncodilatadora y se incentivó una fisioterapia respiratoria por los antecedentes de tabaquismo. A la llegada al quirófano se realizó monitorización no invasiva de la tensión arterial y se detectó una HTA grave (200/100 mm Hg), sin sintomatología acompañante. No hubo otros hallazgos positivos al examen físico. Se premedicó por vía parenteral intramuscular (IM) con midazolam en dosis de 3 mg y fentanil en 50 ìcg. A los 45 min el valor de las cifras tensionales era de 150/90 mm Hg. Se colocó una manta térmica para regular la temperatura durante el tiempo operatorio. Posteriormente se procedió a canular los accesos vasculares.
Antes de la inducción de la anestesia fue establecida la monitorización pautada por la ASA para este tipo de intervención: presión arterial media (PAM), presión venosa central (PVC), ritmo cardíaco (FC y EKG), saturación de oxígeno de la hemoglobina y temperatura.9 También se midió el tiempo de coagulación activado (TCA) basal (< 120 s). La profilaxis antimicrobiana se realizó con cefazolina en dosis de 1 g por vía endovenosa (EV).
Se indujo la anestesia general con fentanilo en dosis de 8 μg/kg, midazolam en 0,15 mg/kg y pavulón en 0,01 mg/kg. El mantenimiento anestésico se efectuó con isoflurane en mezcla de O2 y aire más infusión de fentanil (0,01 μg/[kg∙min]) y midazolam (0,5 μg/[kg∙min]).
Se accedió a la tráquea con un tubo orotraqueal convencional núm. 8, sin complicaciones. La ventilación mecánica se mantuvo a través de un ventilador volumétrico Ohmeda MII 7000, modalidad volumen control, FiO2 del 50 %, FR de 15 resp/min, volumen corriente entre 6-8 mL/kg ajustado para mantener pCO2 entre 30 y 45 mm Hg y presión pico inferior a 35 cm H20. Se utilizó PEEP entre 0-5 cm H20.
Se colocó una sonda urinaria para cuantificar el ritmo diurético horario y una sonda nasogástrica para evacuar el contenido estomacal. También se ubicaron termómetros en el esófago, la nasofaringe y el recto. Se administraron 8 mg de ácido epsilón amino caproico (EACA), por vía endovenosa.
En el período transoperatorio se utilizaron infusiones de esmolol (50-150 μg/[kg∙min]), de nitroglicerina (NTG) (0,08-0,15 μg/[kg∙min]) y de dopamina (2 μg/[kg∙min]). Se mantuvo también una infusión EACA (2 g/h).
La técnica quirúrgica consistió en una laparotomía por incisión subcostal bilateral con ampliación al xifoides (incisión de «Mercedes Benz»), vía por la cual inicialmente los urólogos realizaron una nefrectomía izquierda en un tiempo de 1,40 h. Posteriormente los cirujanos generales (hepatólogos) disecaron la arteria y vena renal derecha y con maniobra de piggyback expusieron la VCI y las venas suprahepáticas, en un tiempo de 2,40 h.
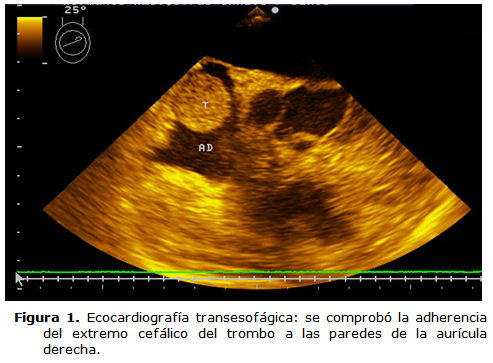
En estas circunstancias se introdujo una sonda de ETE (figura 1) para monitorizar las características del trombo (tamaño, movilidad y consistencia), así como su emergencia desde la VCI hacia la AD. Se comprobó la adherencia del extremo cefálico del trombo a las paredes de la AD, lo que exigió pasar a la siguiente etapa de la cirugía.
Se procedió a realizar una esternotomía media longitudinal para la exposición del corazón y canulación de vena cava superior (cánula núm. 32, Stockert) y raíz aórtica (cánula núm. 24, Storckert). Simultáneamente se canalizó la vena femoral izquierda (cánula núm. 28, Storckert). Se instaló el circuito de circulación extracorpórea (CEC) utilizando máquina marca JOSTRA y oxigenador de membrana DIDECO SIMPLEX III. El flujo calculado fue de 2,4 L/(min∙superficie corporal). El tiempo total utilizado para la realización de estas maniobras fue de 45 min.
Previa canulación de los grandes vasos se administró heparina sódica (3 U/kg) y se monitorizó el estado de anticoagulación por medio del TCA (> 480 s). El cebado del circuito de CEC se realizó con 20 mL de albúmina al 20 %, 500 mL de gelafusine, 800 mL de Ringer lactato, 30 g de manitol y 2500 U de heparina sódica.
Se administró tiopental (3 mg/kg) EV y dosis de rescate de pavulón y fentanilo. Manteniendo el estado de normotermia y sin parada cardíaca, se inició la CEC. Bajo visión directa los cirujanos liberaron el trombo adherido a las paredes de la AD, el cual pudo extraerse realizando también cavotomía inferior. Se pinzó la vena renal derecha y se realizó una maniobra de Pringle (pinzamiento del hilio hepático) durante 15 min.
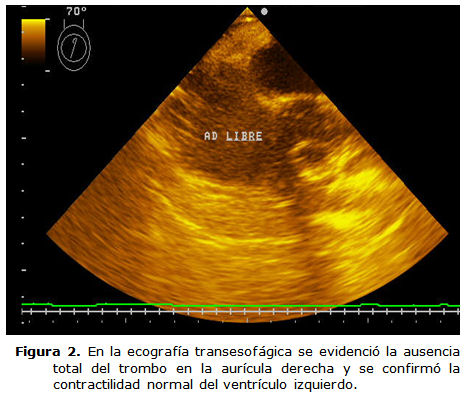
Antes de culminar la derivación cardiopulmonar el paciente presentaba ritmo sinusal. La FC y la contractilidad eran normales. El tiempo de CEC fue de 30 min. Tras el destete de CEC se evidenció por ETE la ausencia total del trombo en la AD y se confirmó la contractilidad normal del ventrículo izquierdo (VI) (figura 2).
Se revirtió heparina con sulfato de protamina (1,5 veces la dosis de heparina), sin complicaciones. El sangrado total en la cirugía fue de aproximadamente 8. Los valores límites de los bioparámetros durante el transoperatorio fueron los siguientes:
- PAM: 70-80 mm Hg,
- PVC: 3-16 mm Hg,
- FC: 56-150 lat/min,
- Temperatura esofágica: 34,8-36º,
- Ritmo diurético: 1,6 mL/(kg∙h),
- EKG: sinusal,
- Sat Hb: 99-100 %.
Antes de la salida del quirófano se comprobó: TA: 130/80, FC: 89 lat/min, PVC: 15 mm Hg, Temp: 35º, Sat Hb: 100 %, EKG: sinusal y ausencia de gradiente térmico. Se utilizó nueva dosis de EACA de 8 g EV para completar una dosis de 30 g en todo el acto quirúrgico. Se mantuvo infusión de dopamina a 2 μg/(kg∙min) y se continuó la reposición con glóbulos, plasma y plaquetas.
En estas condiciones el paciente fue trasladado a la unidad de cuidados intensivos (UCI), donde pasó el posoperatorio sin complicaciones. Presentó estadía en UCI de 2 días y se le comenzó terapia antitrombótica. Se dio de alta a los 10 días.
DISCUSIÓN
Las características histológicas de este tipo de tumor hacen que el uso de tratamientos convencionales para su control, como la quimioterapia y la radioterapia, sean inútiles. El tratamiento de elección en estos pacientes es el quirúrgico, pero la cirugía sólo podrá llevarse a cabo si en los exámenes clínicos previos no existe evidencia de metástasis.10-12
Inicialmente se pensaba que la presencia de un trombo tumoral tenía un efecto negativo en la supervivencia, pero a medida que las técnicas quirúrgicas y los cuidados posoperatorios han mejorado, la supervivencia de estos pacientes se encuentra entre un 45 a 65 % a los 5 años,2, 10, 13-15 porcentajes que se ven afectados por la presencia de afectación de la grasa perirrenal, ganglios linfáticos positivos y metástasis a distancia, entre otros elementos.13,16
Este paciente cumplía los criterios de aceptación para proceder con este tipo de cirugía. Significativos eran los antecedentes de HTA mal controlada y disfunción renal preoperatoria, dada por cifras elevadas de creatinina (aclaramiento de creatinina 48,6 mL/min).
Dado que la mejor opción terapéutica para estos pacientes era la cirugía, el diagnosticar el nivel al que llega el trombo es un factor importante para definir la estrategia terapéutica, no solo en cuanto a la vía de abordaje, sino también por la necesidad de cuidados perioperatorios especiales.
Ante un paciente con tumor renal con afectación de la vena cava inferior (VCI), el grupo que atiende al paciente debe completar el estudio de la extensión del trombo tumoral en la VCI. Para ello existen diferentes exámenes diagnósticos, tales como la resonancia magnética nuclear (RMN), la tomografía axial computarizada (TAC), la cavografía, la ecografía, entre otros estudios.
Según Parra,17 la resonancia magnética puede predecir la presencia de trombo en la vena cava inferior en el 100 % de los casos y en qué nivel se encuentra en un 88 %, mientras que la tomografía axial computarizada abdominal tiene una sensibilidad del 78 y 96 % para la detección trombo tumoral en la vena renal y la vena cava inferior. La ecografía con Doppler puede ser útil para determinar el flujo en las venas suprahepáticas y la VCI, y permite observar también la presencia de una imagen tumoral en la VCI y en la AD. La cavografía se utiliza como complemento o cuando los hallazgos en la RNM son equívocos o existe contraindicación para la realización de la RNM. A nuestro paciente se le indicó cavografía y tomografía axial computarizada.
Se ha propuesto la ecografía transesofágica para aquellos casos en los que el trombo se extiende hasta un nivel auricular, como lo fue el caso descrito por nosotros, como parte del estudio para definir la extensión proximal del trombo, aunque no aporta mucha más información que la RNM.2,13 El eco transesofágico (ETE) ha demostrado tener una elevada sensibilidad para el diagnóstico de tumores en la aurícula derecha. Schwartzbard y cols.18 evidenciaron la superioridad de la ETE sobre la ecografía transtorácica en la detección y extracción de tumores en la aurícula derecha.
La localización más o menos precisa del nivel del trombo tumoral es fundamental para decidir la técnica quirúrgica que se va a emplear. Basados en los hallazgos imaginológicos se puede definir el nivel del trombo tumoral para así poder clasificarlo. Existen varias clasificaciones; la más utilizada divide la extensión topográfica tumoral en la vena cava inferior en cuatro niveles: a) nivel I o A: extensión infrahepática, b) nivel II o B: extensión intrahepática, c) nivel III o C: compromiso suprahepático infradiafragmático y d) nivel IV o D: compromiso supradiafragmático, según la referencia recogida por Vaidya2 en su trabajo. Esta clasificación tiene como único fin el de ayudar a definir el mejor acceso quirúrgico.16
La frecuencia varía en las series publicadas: Parra y cols.17 recogen que el 53 % de las trombosis de la cava inferior en los carcinomas renales son infrahepáticas; el 24 %, suprahepáticas, y el 23 % llegan al atrio muy por encima de la media que se recoge en la bibliografía. Por otro lado, los resultados de Li y cols.19 se expresan, según su localización, en 56, 31 y 12,5 %, respectivamente. Nesbitt y cols.12 refieren en su serie que en el 49 % de sus pacientes la trombosis de la cava inferior estaba por debajo del hígado, mientras que en el 51 % de sus pacientes llegaba por encima del hígado y en el 5 % aparecía el tumor en la aurícula derecha.
En los tipos A, B y C la técnica quirúrgica recomendada es la trombectomía, junto con nefrectomía vía laparotomía media o transversa; los tipos A y B del lado derecho también se pueden tratar por vía retroperitoneal derecha. Cuando hay infiltración de la pared de la VCI es obligada la resección de un segmento de ésta con interposición de un injerto protésico de tipo PTFE.
En el tipo C se es partidario del pinzamiento de la VCI intrapericárdica si el paciente lo tolera. Por otra parte, si no presenta inestabilidad hemodinámica, se procede a la trombectomía y posteriormente se lleva la pinza a un nivel inferior. Se realiza la reconstrucción de la VCI y más tarde se practica la nefrectomía; con este procedimiento es posible evitar una cirugía mucho más agresiva con circulación extracorpórea, que presenta más morbilidad y mortalidad. Sin embargo, autores como Staehler y cols.14 y Yamashita y coautores20 han planteado que en algún que otro caso se tiene que usar la circulación extracorpórea (CEC).
Cuando el trombo llega a nivel de la aurícula, como en nuestro caso, entonces la intervención quirúrgica se realiza con CEC con hipotermia o sin ella.21 En el 2003 Vaidya y cols.2 propusieron una serie de estrategias según el nivel del trombo y, para el abordaje de los trombos de IV nivel o D, recomendaban una incisión toracoabdominal, de tipo Chevron con extensión xifoesternal o mediana abdominal con estereotomía o de «Mercedes Benz», teniendo como propósito extraer el trombo sin fragmentarlo. Generalmente, plantean que se requiere una derivación cardiopulmonar o venosa con hipotermia profunda o sin ella y paro cardiocirculatorio.
Señala, también, Vaidyan2 que para la trombectomía se pueden emplear varias técnicas: una es «ordeñar» la vena cava inferior; otra es la disección digital proximal y distal, similar a la aplicada en nuestro caso. También se podría realizar la trombectomía con una sonda de Foley, la cual se avanza desde la incisión distal en la cava inferior hasta sobrepasar el trombo, se infla el balón con posterior tracción de la sonda, realizando así la extracción del trombo.
Durante el procedimiento quirúrgico, cuando se procedió a extraer el trombo, fueron seguidos algunos principios, similares a los descritos por algunos autores:13,22,23
- Visualización y control completo de la vena cava inferior, que se pudo lograr con la movilización del hígado con la técnica de piggyback.
- Control de la vena renal contralateral.
- Isquemia menor posible del hígado y del riñón no afectado.
- Incisión combinada de la cava inferior y de la aurícula derecha, estando el paciente en circulación extracorpórea.
- Remoción y extracción del trombo.
- Verificación de la existencia o no de infiltración de la pared de la VCI, para ser reparada, lo cual no ocurrió en nuestro caso.
Conociendo que el fallo renal perioperatorio se asocia a una alta morbilidad y mortalidad en este período, la estrategia que desde el punto de vista anestésico seguimos fue proteger la función renal residual.24 Iniciamos tempranamente terapéutica con dopamina en dosis bajas por su conocido papel activador de receptores dopaminérgicos vasodilatadores de la vasculatura renal.25 Teniendo en cuenta además que todo paciente hipertenso presenta trastornos en los mecanismos de autorregulación del flujo sanguíneo renal (FSR), insistimos durante el período transoperatorio mantener un plano anestésico que permitiera garantizar cifras de PAM entre 70-80 mm Hg, con lo que se pudo optimizar el FSR lo cual se hizo evidente por el gasto urinario superior a 0,5 ml/(kg∙h). En este contexto cabe decir que los fármacos anestésicos utilizados fueron seleccionados por sus características farmacocinéticas, que no afectaran la función renal.
También, y como parte de la estrategia de protección de la función renal, se estimuló la diuresis de solutos con pequeñas dosis de diuréticos (manitol: 0,25 g/kg y furosemida 0,5 mg/kg). A pesar de que aún no existe un consenso sobre la verdadera nefroprotección que ofrecen estas estrategias, en este paciente se logró una adecuada función renal durante todo el transoperatorio, evaluado por un gasto urinario adecuado.26
Consideramos que el antifibrinolítico EACA suministrado de forma continua durante el procedimiento ayudó a amortiguar la aparición de trastornos de la coagulación secundarios a la dilución de factores.
Teniendo en cuenta las alteraciones de la permeabilidad capilar con secuestro de líquidos al intersticio y la disfunción pulmonar posoperatoria secundaria a éstas que suele ocurrir cuando se reponen grandes volúmenes de líquido, como ocurrió en nuestro caso, por la pérdida de líquidos se decidió aumentar la PEEP a 5 cm H20, lo que fue bien tolerado durante la intervención. Con esta maniobra también se hizo profilaxis de las atelectasias que pueden aparecer hasta en un 50 % de estas intervenciones y causan una disminución de la oxigenación arterial, la capacidad residual y distensibilidad pulmonar.27-29
El uso de ETE en este tipo de intervención ha permitido un mejor cuidado anestésico y aproximación quirúrgica, lo cual facilitó la remoción del trombo de la VCI.30 Treiger y cols.31 describieron en 5 pacientes la utilidad que tuvo la ETE e identificaron la extensión cefálica del tumor en forma correcta, lo cual determina la conducta del cirujano para la extracción del trombo.
El problema de esta trombosis es que en cualquier momento de su evolución puede desprenderse parcial o totalmente y causar embolia pulmonar masiva. Se ha demostrado que un tumor frágil tiene mayor riesgo de embolización que uno adherente. El riesgo aumenta durante el intraoperatorio al manipular el tumor, y es por que para muchos autores es importante contar con una ETE.32-34
Okiwaka demostró en una serie de 5 pacientes, que la ETE permitió determinar la extensión cefálica tumoral, vigilar la presencia de embolizaciones y también garantizar el manejo exitoso de la hemodinamia.35 Para Sigman36 fue muy importante a la hora de canular y para la confirmación de no masa intracardiaca en otro lugar que no fuera la cava inferior.
En nuestro caso, la ETE igualmente permitió observar en tiempo real la extensión cefálica del trombo desde la VCI hacia la AD y sus características, además de que también hizo posible vigilar la posible embolización de fragmentos tumorales; permitió canular adecuadamente, sin demostración de trombo al nivel del sitio de canulación y ayudó a optimizar el cuidado hemodinámico del paciente.
En el posoperatorio, como recomienda Vahadilla,2 el paciente se mantuvo con terapia antitrombótica.
En resumen, es posible afirmar que un abordaje multidisciplinario coordinado, asociado a una estrategia quirúrgica y anestésica basada en la coordinación quirúrgica de los grupos implicados, más la protección de la función renal, respiratoria, cerebral y cardiovascular, así como el uso de la ecocardiografía transesofágica intraoperatoria, permitió un resultado exitoso en este paciente con CCR y trombo en la VCI con extensión a la AD.
Para una estrategia quirúrgica adecuada es absolutamente necesario un estudio imaginológico completo, lo cual permite identificar plenamente el nivel del trombo, que es lo que definirá la vía de acceso.
El tratamiento quirúrgico continúa siendo la mejor alternativa para el tratamiento del cáncer renal, a pesar de la afectación tumoral de la vena cava inferior, sea cual sea el lugar donde se encuentre el trombo.
REFERENCIAS BIBLIOGRÁFICAS
1. Kaplan S, Ekici S, Dogan R, Demircini m, Ozen H, Pasaoglu I. Surgical management of renal cell carcinoma with inferior vena cava tumor thrombus. American Journal of Surgery 2002;183(3):194.
2. Vaidya A, Ciancino G, Soloway M. Surgical techniques for treating a renal neoplasm invading the inferior vena cava. J Urology 2003;169:435-44.
3. Zisman A, Wieder J, Pantuck A. Renal cell carcinoma with tumor thrombus extension: Biology, role of nephrectomy and response to immunotherapy. J Urology. 2003;169:909-16.
4. Ciancio G, Vaidya A, Savoie M, Soloway M. Management of renal cell carcinoma with level III thrombus in the inferior vena cava. J Urol. 2002;168:1374-7.
5. Ciancio G, Soloway MS. Renal cell carcinoma with tumor thrombus extending above diaphragm: avoiding cardiopulmonary bypass. Urology 2005;66:26670.
6. Cabrera MC, Murillo C, Díaz de Valdés V, Farías J, Bernier P, Luly de La Fuente EU. Ecocardiografía transesofágica intraoperatoria en el manejo de resección de hipernefroma con compromiso de vena cava y aurícula derecha. Rev Esp Anestesiol Reanim. 2005;52:48-51.
7. Sasaoka N, Kawaguchi M, Sha K. Intraoperative immediate diagnosis of acute obstruction of tricuspid valve and pulmonary embolism due to renal cell carcinoma with transesophageal echocardiography. Anesthesiology 1997;87:998-1001.
8. Neves RJ, Zincke H. Surgical treatment of renal cancer with vena cava extension. Br J Urol 1987;59:390-5.
9. Moskowitz DM, Perelman SI, Cousineau KM, Klein JJ, Shander A. Multidisciplinary management of a Jehovah's Witness patient for the removal of a renal cell carcinoma extending into the right atrium. Can J Anesth 2002;49(4):4028.
10. Tigrani VS, Reese DM, Small EJ. Potential role of nephrectomy in the treatment of metastatic renal cell carcinoma: a retrospective analysis. Urology 2000;55:3640.
11. Bromwich E, Hendry D, Aitchinson M. Cytoreductive nephrectomy: is it a realistic option in patients with renal cancer? BJU Int 2002;89:523-5.
12. Nesbitt JC, Soltero ER, Dinney CP. Surgical management of renal cell carcinoma with inferior vena cava tumor thrombus. Ann Thorac Surg 1997;63:1592-600.
13. Novick A, Campbell S. Renal tumors. En: Walsh PC, Retik AB, Vaughan ED Jr, Wein AJ. (eds): Campbell's Urology. 8va ed. Philadelphia: W.B Saunders; 2002. Pp. 2672-731.
14. Staehler G, Brkovic D. The role of radical surgery for renal cell carcinoma with extension into the cava. J Urol 2000;163:16715
15. Masatoshi J, Takehisa I, Yoshinori I, Norihide S, Kazunori K, Nobuhiko H, Makoto S. Surgical strategy for treating renal cell carcinoma with thrombus extending into the inferior vena cava. J Vasc Surg. 2004;39(4):829-35.
16. Mejean A, Oudard S, Thiounn N. Prognostic factors of renal cell carcinoma. J Urology 2003;169:821-7.
17. Parra OR, Gómez Jiménez J, Wilson PM. Experience with the of treatment renal cell carcinoma with thrombus in inferior vena cava and right atrium. Actas Urol Esp 1997;2:5507.
18. Schwartzbard AZ, Tunick PA, Rosenzweig BP, Kronzon I. The role of transesophageal echocardiography in the diagnosis and treatment of right atrial thrombi. J Am Soc Echocardiogr. 1999;12(1):64-69.
19. Li XD, Cheng S, Rui XF, Li GH, Chen YB, Yu DM. Diagnosis and surgical management of renal cell carcinoma with inferior vena cava tumor thrombus—a report of 6 cases with literature review. Ai Zhen 2005;24(11):1394-7.
20. Yamashita C, Azami T, Okada M, Toyoda Y, Wakiyama H, Yoshida M. Usefulness of cardiopulmonary bypass in reconstruction of inferior vena cava occupied by renal cell carcinoma tumor thrombus. Angiology 1999;50: 47-53.
21. Kalaycioglu S, Sinci V, Aydin H, Soncul H. Cardiopulmonary bypass technique for treatment of renal cell carcinoma extending into the vena cava. Ann Thoracic Cardiovasc Surg 1999;5:419-21.
22. Ujjwal C, Chowdhury K, Mishra A K, Seth A, Dogra P N, Honnakere JHV. Novel Techniques for tumor thrombectomy for renal cell carcinoma with intraatrial tumor thrombus. Ann Thorac Surg 2007;83:1731-6.
23. Ciancino G, Hawke C, Soloway M. The use of liver transplant technique to aid in the surgical management of urological tumors. J Urol 2000;164:665.
24. Sear JW. Kidney dysfunction in the postoperative period. Br J Anaesth 2005;95(1):20-32.
25. Lema G, Urzua J, Jalil R, Canessa R, Moran S, Sacco C. Renal protection in patients undergoing cardiopulmonary bypass with preoperative abnormal renal function. Anesth Analg. 1998;86(1):3-8.
26. Zacharias M, Gilmore IC, Herbison GP, Sivalingam P, Walker RJ. Interventions for protecting renal function in the perioperative period. Cochrane Database Syst Rev 2005;20(3):CD 003590.
27. Hedenstierna G. Alveolar collapse and closure of airways: regular effects of anaesthesia. Clin Physiol Funct Imaging 2003;23:123-9.
28. Tusman G, Bohm SH, Suarez-Sipmannf F, Turchetto E. Alveolar recruitment improves ventilatory efficiency of the lungs during anesthesia. Can J Anaesth 2004;51(7):649-53.
29. Johnson D. Lung recruitment during general anesthesia. Can J Anesth 2004;51:649-53.
30. Koide Y, Mizoguchi T, Ishii K, Okumura F. Intraoperative management for removal of tumor thrombus in the inferior vena cava or the right atrium with multiplane transesophageal echocardiography. J Cardiovascular Surg 1998;39(5):641-7.
31. Treiger B, Humphrey LS, Peterson CV Jr, Oesterling JE, Mostwin JL, Reits BA. Transesophageal echocardiography in renal cell carcinoma: an accurate diagnostic technique for intracaval neoplastic extension. J Urol 1991;145(6):1138-40.
32. O'Hara JF Jr, Sprung J, Whalley D, Lewis B, Zanettin G, Klein E. Transesophageal echocardiography in monitoring of intrapulmonary embolism during inferior vena cava tumor resection. J Cardiothorac Vasc Anesth 1999;13(1):69-71.
33. Hasnain JU, Watson RJ. Transesophageal echocardiography during resection of renal cell carcinoma involving the inferior vena cava. South Med J 1994;87(2):273-5.
34. Singh I, Jacobs LE, Kotler MN, Ioli A. The utility of transesophageal echocardiography in the management of renal cell carcinoma with intracardiac extension. J Am Soc Echocardiogr 1995;8(3):245-50.
35. Oikawa T, Shimazui T, Johraku A, Kihara S, Tsukamoto S, Miyanaga N. Intraoperative transesophageal echocardiography for inferior vena caval tumor thrombus in renal cell carcinoma. Int J Urol 2004;11(4):189-92.
36. Sigman DB, Hasnain JU, Del Pizzo JJ, Sklar GN. Real-time transesophageal echocardiography for intraoperative surveillance of patients with renal cell carcinoma and vena caval extension undergoing radical nephrectomy. J Urol 1999;161(1):36-8.
Recibido: 17 de marzo de 2009.
Aprobado: 26 de junio de 2009.
Alejandro Villar Inclán. Hospital «Hermanos Ameijeiras». Calle Padre Varela y San Lázaro, Centro Habana. La Habana, Cuba.
Correo electrónico: alejandro.villar@infomed.sld.cu