Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Cirugía
versión impresa ISSN 0034-7493
Rev Cubana Cir vol.51 no.2 Ciudad de la Habana abr.-jun. 2012
PRESENTACIÓN DE CASO
Fístula de alto gasto
High output fistula
Dr. Ricardo Almeida Varela, Dr. Oscar Suárez Echeverría, Dr. Oscar Pérez Gutiérrez, Dr. Eugenio Selman Houssein, Dr. Claudio Cordovés Sánchez, Dr. Yossuan García Ruiz
Hospital Universitario "Gral. Calixto García". La Habana, Cuba.
RESUMEN
Se presenta a un paciente de 37 años de edad que acude a nuestro Cuerpo de Guardia politraumatizado, con lesiones torácicas y abdominales, con síntomas y signos sugestivos de fracturas costales múltiples, con hemotórax derecho y hemoperitoneo, corroborado imaginológicamente y en la punción abdominal. Se realiza pleurostomía mínima intermedia y laparotomía exploratoria. Se le encuentran lesiones hepáticas de los segmentos VI, V, VIII y IV, con una profundidad mayor de 3 cm, además, deserosamientos en las asas delgadas intestinales y colon. Se realiza hepatorrafia y empaquetamiento hepático. Posteriormente van apareciendo complicaciones, por lo que tiene que ser reintervenido en más de 60 ocasiones. Entre ellas, la aparición de una fístula de alto gasto, que lo llevó a la desnutrición y a la permanencia con el abdomen expuesto durante 7 meses hasta el egreso. Se revisa la literatura correspondiente a estas entidades.
Palabras clave: politrauma, trauma hepático, empaquetamiento, abdomen expuesto, bolsa de Bogotá, fístula intestinal.
ABSTRACT
A 37 years-old multi-traumatized male patient went to our emergency service. He had many injures in the thorax and the abdomen, together with symptoms and signs suggestive of multiple costal fractures, with right hemothorax and hemoperitoneum, all of which was confirmed by imaging techniques and by abdominal puncture. Minimal intermediate pleurostomy and exploratory laparoscopy were performed. We found hepatic lesions in the 6th, 5th, 8th and 4th segments, over 3 cm deep; additionally, the loss of serosa from the intestinal ansae and from the colon. Hepatorrhaphy and hepatic packing were also performed. Later on, more complications appeared, so he had to be re-operated more than 60 times. The occurrence of a high output fistula led him to malnutrition and his abdomen remained exposed for 7 months until he was finally discharged from hospital. This paper also presented a literature review on this topic.
Key words: multitrauma, hepatic trauma, packing, exposed abdomen, Bogota's bag, intestinal fistula.
INTRODUCCIÓN
Las fístulas enterocutáneas son un problema mayor en la práctica quirúrgica. Se definen como la comunicación anormal entre el aparato gastrointestinal y la piel, con salida del contenido intestinal a través de esta por un periodo mayor de 24 h. Es una de las complicaciones más serias que enfrenta el cirujano, y a pesar de que el tratamiento sea satisfactorio, la estancia hospitalaria con frecuencia es prolongada.1-4
A pesar de los avances en el tratamiento de este padecimiento, la morbilidad y mortalidad persisten elevadas. La mortalidad se reporta entre 6 y el 25 % a nivel mundial, y en Cuba oscila entre un 20-50 %, en dependencia del segmento del tubo digestivo que afecte.5
Su etiología en el 80 al 90 % de los casos es después de una cirugía,6,7 principalmente de urgencia,8,9 secundarias a dehiscencia de anastomosis o lesiones intestinales inadvertidas al momento de realizar la primera cirugía. Otras causas de fístulas enterocutáneas son: enfermedad inflamatoria intestinal (Crohn, colitis ulcerosa), cáncer, traumas y diverticulitis.6-9
Actualmente la mayor parte de los centros que se especializan en el tratamiento de esta enfermedad reciben a los pacientes referidos de otras unidades, y la celeridad con que se envíen a estos pacientes repercute en la evolución en cuanto al cierre y pronóstico.10-13
Teniendo en cuenta los aspectos antes mencionados, revisamos esta entidad y presentamos lo ocurrido con un paciente con una fístula de alto gasto, con una evolución de 8 meses, desde agosto de 2009 hasta marzo de 2010, atendido en el Hospital Universitario "Gral. Calixto García" por los servicios de Cirugía General y las Unidades de Cuidados Intensivos e Intermedios, el cual, finalmente, tuvo solución quirúrgica.
PRESENTACIÓN DEL CASO
El paciente es del sexo masculino, blanco, tenía 37 años de edad, sin antecedentes patológicos personales de salud, ni de hábitos tóxicos, ni de operaciones anteriores. Se recibe en el Cuerpo de Guardia, del Hospital Universitario "Gral. Calixto García", en estado de shock, consciente, con estigmas de traumas torácicos y abdominales. Se realizan medidas inmediatas del tratamiento del shock, junto a la anamnesis al paciente y al personal que lo traía del lugar del accidente, para conocer su cinemática. Refieren que manejaba un auto, se quedó dormido, y se impactó frontalmente contra un árbol, por lo cual se desplazó la carrocería y el timón contra el tórax y el abdomen.
Al examen físico se diagnostican fracturas costales múltiples y hemoneumotórax derecho. Se le realiza ultrasonido, en el que se observa líquido libre en la cavidad abdominal, y en la punción abdominal se comprueba la existencia de sangre que no coagulaba. Se anuncia para tratamiento quirúrgico, y se le traslada como una emergencia al salón de operaciones. Se completan los estudios de laboratorio y radiográficos en el salón de operaciones.
Por la sonda de pleurostomía se evacuan cerca de 200 cc de sangre y se deja conectado a sello de agua. En la laparotomía exploradora se realiza una incisión media supra e infraumbilical, que posteriormente hubo que ampliar en forma de L, transversal derecha, subcostal derecha, para visualizar rápidamente la región hepática sangrante. En la cavidad peritoneal aspiramos alrededor de 3 000 cc de sangre libre, y localizamos la zona fundamental del sangrado, que estaba situada en 3 lesiones del hígado que abarcaban los 2 lóbulos, principalmente el derecho. Afectaban los segmentos VI, V, VIII y IV, con una profundidad mayor de 3 cm, en forma de Y, y 2 lesiones adicionales separadas de esta, ubicadas paralelas entre sí, en el segmento IV. Para controlar el sangrado se realizó la maniobra de Pringle, momentáneamente, se hizo hemostasia intrahepática, se suturó con catgut cromado las lesiones, y después se empaquetó con compresas el hígado para controlar el daño de forma transitoria. Además, para disminuir la presión en la vía biliar, se complementó la operación con una colecistostomía, ya que las lesiones hepáticas eran muy amplias, y la posibilidad de un daño en la vía biliar intrahepática no se podía descartar, además, ello permitió también, realizar con un arco en C, una colangiografía a través de la sonda de la colecistostomía en el transoperatorio, que permitió descartar una lesión de vías biliares principales extrahepáticas. Adicional a esto, existían alteraciones traumáticas de la serosa en el yeyuno y colon que se afrontaron con poliéster 3-0.
Se mantuvo estable hemodinámicamente en el transoperatorio y posoperatorio inmediato, seguido estrictamente por el grupo de anestesia de guardia. A las 48 h se le reintervino de forma programada para reevaluar las lesiones intrabdominales y retirar las compresas de la zona hepática, y se encontraron todavía lesiones en el lóbulo izquierdo que sangraban al retirar las compresas, las que se suturaron, y se detuvo el sangrado.
La tercera intervención se realiza al incrementarse la presión intrabdominal, salir por el drenaje abdominal escasa cantidad de líquido bilioso, y ultrasonográficamente, por existir líquido libre en el abdomen. Se encontró bilirragia escasa por una de las lesiones del lóbulo izquierdo, se reparó la zona con cromado, y se logró detener este.
A partir del quinto día comienza la salida de líquido intestinal por los drenajes abdominales, se le opera nuevamente, y se observa que uno de los traumas en la serosa del yeyuno se había perforado. Se sutura y se lava la cavidad con iodo povidona y suero fisiológico. Además, se mantenía la bilirragia escasa por la lesión antes descrita del lóbulo izquierdo. Se reinterviene de forma programada posteriormente a las 48 h, y se encuentra escape por la sutura intestinal, por lo que se hace yeyunostomía por sonda en la zona del escape y lavado amplio de la cavidad. Se mantiene escasa la bilirragia antes mencionada.
En posteriores laparotomías decidimos dejar colocada una bolsa de Bogotá, o sea, una bolsa de poliuretano sobre las asas intestinales expuestas, ya que la retracción de la pared abdominal, fundamentalmente por la aponeurosis, impedía cerrar el abdomen sin que aumentase la presión intrabdominal y provocara un síndrome compartimental, lo cual facilitaría, además, las posteriores reintervenciones hasta que se controlara la infección abdominal.
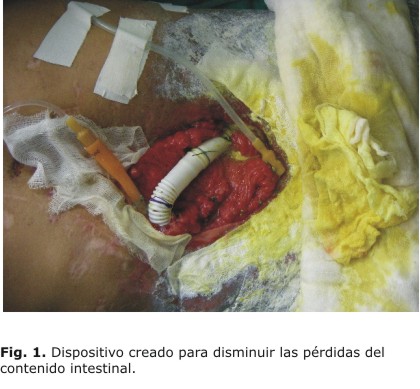
Quedaría constituido un bloque compacto entre las asas intestinales, con una fístula de alto gasto en el yeyuno, y una fístula biliar en el lóbulo izquierdo del hígado. Como se muestra en la figura 1 y en el video, se le colocó una sonda intermedia entre los cabos proximal y distal del yeyuno para reducir las pérdidas, que llegaban a ser de más de 2 000 cc en 24 h. Apoyado con una aspiración continua en el cabo proximal, se almacenaba lo aspirado, y se le reintroducía mezclado con los alimentos por la sonda de yeyunostomía colocada en el cabo distal.
La fístula biliar se logró eliminar al realizar una esfinterotomía a través de una colangiografía retrógrada endoscópica en días posteriores, y quedó entonces por resolver en el abdomen la fístula de alto gasto del yeyuno. Concomitante a los problemas del abdomen, se produjeron alteraciones en el tórax, donde persistía un derrame pleural derecho que se resolvió por mínimo acceso con abrasión de la pleura parietal para provocar sinequias (pleurodesis).
Permaneció ingresado en la Unidad de Terapia Intensiva hasta que se fueron resolviendo otras complicaciones, como la contusión pulmonar, las bronconeumonías (que se repitieron por la permanencia prolongada en cama, la entubación y la ventilación artificial que lo apoyó por un periodo prolongado). Para facilitar la ventilación se le practicó una traqueostomía al séptimo día.
Previa a la operación final de anastomosis intestinal, se hizo un estudio contrastado del intestino delgado con bario para establecer la ubicación real de la fístula, que dio como resultado que el cabo proximal estaba localizado en el yeyuno proximal, un segmento de asa yeyunal ciega en la pelvis, y la porción distal de yeyuno e íleo en forma de ovillo en el flanco derecho del abdomen. Este último segmento con un tránsito aparentemente normal.
A finales de enero del año 2010, después de una bronconeumonía que lo llevó a estar varias semanas en Terapia Intensiva, se comenzó un régimen de alimentación enteral y parenteral intensivo, apoyados por el Servicio de Terapia Intermedia, que nos permitió mejorar su estado general y nutricional, por lo que se decide la reintervención el 17 de febrero de 2010 para solucionar la fístula de alto gasto yeyunal.
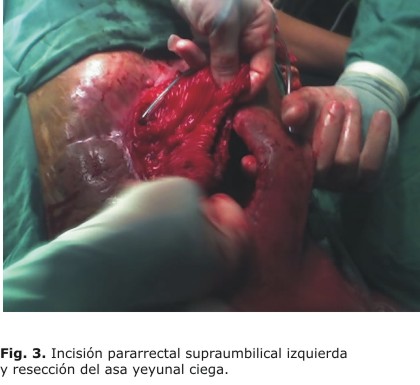
Al tener un defecto de 30 cm en la pared en el epigastrio y mesogastrio donde estaba el yeyuno evertido, con la mucosa expuesta, y la salida de contenido gástrico, biliar y pancreático (fístula de alto gasto), se hizo necesario abrir la cavidad abdominal por una zona virgen, o sea, por el flanco izquierdo, y se realizó entonces una incisión pararrectal supraumbilical izquierda (Fig. 3).
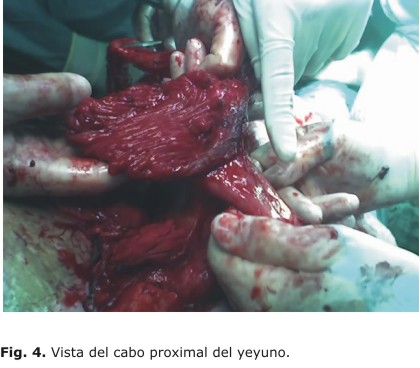
Se encontraron múltiples adherencias entre los órganos intrabdominales, y se logró identificar con una sonda intraluminal el cabo proximal, distal y el asa ciega de yeyuno. Se reseca cerca de un metro de yeyuno, y se dejan solo los cabos proximal y distal, para la anastomosis (Fig. 4 y 5). Esta se hace con una sutura de ácido poliglicólico 2-0, en un solo plano extramucoso, y se dejó colocada por debajo de la piel, intrabdominal, en la zona de la pelvis, para evitar su exposición al exterior. No se pudo dejar extraperitoneal por las alteraciones anatómicas impuestas.
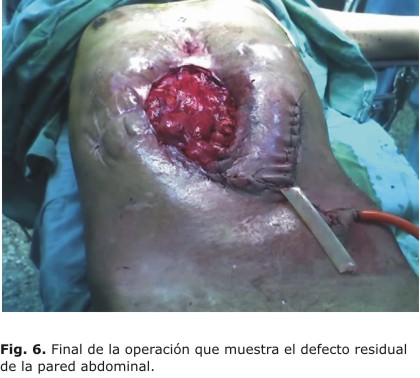
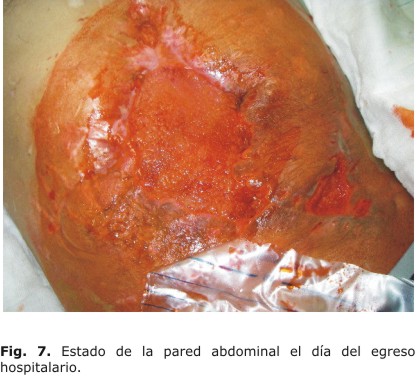
Quedaba un defecto amplio de la pared en el epigastrio y mesogastrio, que, para tratar de cubrirlo, se rota un colgajo de piel completa del flanco izquierdo al centro del defecto. Se cierra la incisión de la aponeurosis pararrectal izquierda, y se libera la piel que rodeaba esta zona para permitir la rotación del colgajo; no obstante, quedó la región epigástrica sin poderse cubrir con piel (Fig. 6). Se coloca una lámina de poliuretano sobre las asas intestinales expuestas, hasta lograr que en días posteriores se formasen adherencias entre estas que evitaron la evisceración. Se mantuvo con curas locales diarias, y se tapó la zona con una lámina de poliuretano hasta el alta hospitalaria el 10 de marzo del año 2010, 21 días después de la operación (Fig. 7).
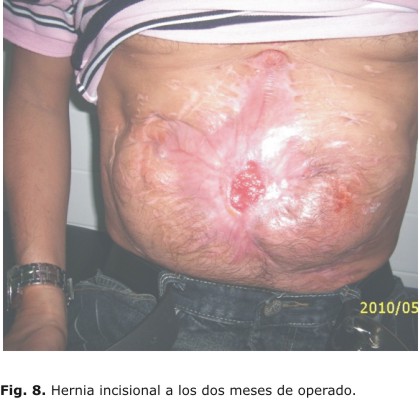
Actualmente se mantiene con una evolución satisfactoria en su casa, después de ser reintervenidos casi en 60 ocasiones, quedando con una hernia incisional en la región del mesogastrio a los 3 meses de operado (Fig. 8).
DISCUSIÓN
La estadía hospitalaria de un paciente con una fístula intestinal es muy variable, y a la vez dependiente de múltiples factores. Los avances en los conocimientos relacionados con el tratamiento a los pacientes mediante la nutrición quirúrgica, reposición de líquidos y electrólitos, así como el cuidado respiratorio, han mejorado la supervivencia. No obstante, continúa siendo un problema que precisa el ingreso hospitalario, al menos, de 2 a 3 meses.14
Chapman y Seldon15 plantean un algoritmo de trabajo, por el cual, luego de una semana de tratamiento, siguiendo 4 fases bien predeterminadas, el cirujano está en condiciones de predecir si este paciente tendrá necesidad de tratamiento médico o quirúrgico. Otros autores, como Zudiema Schakerford,16 plantean un mes para el tratamiento médico conservador y estudio del paciente. Howard17 plantea que el 90 % de los cierres espontáneos ocurren luego de este periodo, de controlada la sepsis local y mejorado el estado nutricional, pero si esto no ocurriera habría que descartar la presencia de otros factores locales y sistémicos, y valorar el tratamiento quirúrgico.
Las fístulas intestinales se pueden formar por diferentes mecanismos fisiopatológicos, con elevada frecuencia como complicaciones de intervenciones quirúrgicas abdominales. Webster y Carey,18 propusieron diferentes mecanismos de formación de las fístulas, los cuales son: alteraciones congénitas y adquiridas, entre estas últimas, los traumatismos, inflamaciones, abscesos, la irradiación, tumores y perforaciones. En el caso presentado la etiología postraumática fue la desencadenante de la enfermedad. Existen muchas clasificaciones de las fístulas intestinales, en dependencia de diferentes aspectos. Morales Díaz19 las clasifica: teniendo en cuenta la localización topográfica en el tubo digestivo hasta las mixtas, en las cuales el paciente puede tener otras fístulas concomitantes (por ejemplo, biliar), como ocurre en el nuestro; según el número (únicas o múltiples); según su origen (congénitas o adquiridas); por el gasto alto (más de 500 cc en 24 h) o bajo; y según la parte del órgano que comunica con el exterior (lateral o terminal).
La fístula intestinal externa constituye la forma más común de esta afección. Entre 35 fístulas originadas en el yeyuno y el íleon informadas por Mac Fadyen,20 el 75 % eran externas. El íleon es el sitio de origen de la mayor parte de estas fístulas. Reber,21 señaló que en 120 fístulas externas de intestino delgado, el 60 % provenían del íleon y 40 % de yeyuno. Vallés Gamboa14 informa la frecuencia de 68,5 % de localización ileal en un estudio de 10 años de trabajo, excepto Fuentes Valdés,5 que reporta la variedad anatómica yeyunal en el 52,2 % de 110 pacientes analizados, lo cual coincide con el caso presentado por nosotros. Este último resultado se debió a que las lesiones del hemiabdomen superior, secundarias al impacto en los accidentes de tránsito, afectaron más las asas yeyunales y no tanto a las distales, las del íleon, las cuales quedaban en la posición más declive.
Mughal22 afirma que, paralelamente con el incremento en el uso de las técnicas quirúrgicas en el tratamiento de las peritonitis graves, han aparecido complicaciones relacionadas, como la pérdida de líquidos por evaporación o escurrimiento, la evisceración, el desarrollo de grandes hernias incisionales, así como la aparición de fístulas gastrointestinales. La combinación de estas 2 últimas resulta un verdadero desafío para el cirujano, pues en estas condiciones la mortalidad es elevada. Motivados por esto, Stiges-Serra y otros23 proponen una nueva clasificación en 3 grupos, incluyendo en el grupo 2 a las fístulas que drenan a través de un defecto grande de la pared abdominal, las cuales puede alcanzar hasta el 60 % de mortalidad, a diferencia de las fístulas que se presentan con la pared abdominal íntegra, en las que la mortalidad está entre el 6 y el 20 %.24 Cuando esta lesión hace su aparición, la concurrencia de estas 2 complicaciones crea un cuadro clínico similar al de otras fístulas intestinales, pero el hecho de no tener una pared abdominal íntegra convierte tal situación en un reto para su solución. Generalmente el problema se inicia como consecuencia de reexploraciones programadas por una infección intrabdominal grave, seguido del desarrollo de adherencias firmes, ricamente vascularizadas que sellan la cavidad y envuelven el intestino delgado, que se encuentra edematoso, congestivo y friable como parte del proceso inflamatorio, por la lesión inicial. Esto es agravado por el trauma quirúrgico de la laparotomía, que hace la pared del intestino vulnerable al desecamiento y a la isquemia por compresión, y ocasiona necrosis y soluciones de continuidad en la pared intestinal.25 El contenido intestinal busca salida a través de estos sitios, y su producto enzimático contribuye a la lisis de los tejidos vecinos. Opinamos que en nuestro paciente estas fueron algunas de las causas determinantes del retraso de la curación.
Existen controversias entre diferentes autores en cuanto a qué flujo considerar grande y cuál pequeño, pues mientras unos26 señalan que grande es el flujo superior a 500 mL en 24 h, otros lo consideran si asciende a 200 mL o más al día.27 Nosotros adoptamos los 500 mL en 24 h. Es comúnmente aceptado que las de alto débito tienen una mayor mortalidad. Sin embargo, resulta interesante la opinión de Peix,28 entre otros autores,29 quienes plantearon que, si bien el alto flujo intestinal en los primeros enfermos estudiados por ellos fue un factor de gravedad, no ocurrió igual en los últimos, lo que explicaron al mejorar la atención médica con los adelantos en la protección cutánea, la nutrición parenteral total y la reinyección del quimo. En el trabajo presentado por Fuentes,5 el estudio multivariado demostró la alta probabilidad de morir para los pacientes con alto flujo (p< 0,05). Nuestro paciente mantuvo en todo momento un débito intestinal por encima de lo 2 000 mL diarios. Atribuimos a los cuidados médicos intensivos, la nutrición mixta y reintroducción del contenido intestinal, su desenlace feliz.
En la mayoría de los pacientes con fístulas externas del intestino delgado se presentan complicaciones críticas. Soeter30 encontró que el 27 % de estos pacientes en un período de 5 años presentaron desequilibrio electrolítico. Las alteraciones más comunes fueron la depleción volumétrica, la hipopotasemia y la acidosis metabólica. La pérdida de líquidos y electrolitos se asocia con una alta mortalidad en los pacientes portadores de fístulas. En el Hospital General de Massachussets, el 78 % de los pacientes que padecieron esta complicación, fallecieron. Mediante el monitoreo invasivo y el tratamiento intensivo esta mortalidad ha disminuido en los últimos años.6 El caso descrito en el presente trabajo, debido a la variedad anatómica de fístula y el alto gasto de contenido biliodigestivo, provocó 3 episodios de deshidratación muy graves y shock, que ocasionaron el retraso en el tratamiento definitivo.
La desnutrición es otra de las complicaciones de las fístulas enterocutáneas. Sus causas son: bajo aporte calórico (ingesta), hipercatabolismo por sepsis y pérdida de proteínas por la fístula.7,31,32 La desarrollan más de la mitad de los pacientes, y esto tiene como consecuencia la mortalidad de más del 60 % de los pacientes desnutridos. Desde 1964 se demostró que los pacientes que recibían mayor aporte nutricional tenían mejor evolución,15 hallazgos que fueron comprobados posteriormente. En un estudio realizado por Apostolos, el 31,8 % de los pacientes desnutridos fallecieron, mientras que del grupo mejor nutrido solo fue de 3,6 %.33 En nuestro paciente la desnutrición fue uno de los determinantes en la demora del tratamiento quirúrgico, ya que es conocido que la anemia y la hipoproteinemia, entre otras carencias, pueden provocar una evolución desfavorable de las suturas intestinales.
La sepsis es la complicación más temida en los pacientes con fístulas enterocutáneas, tanto la sistémica como las intrabdominales y de la pared abdominal, estas últimas, principalmente, por la presencia de tejido necrótico que se infecta por microorganismos de la flora intestinal y de la piel.7 Se presenta en poco más de la mitad de los pacientes en algún momento durante su evolución, y se localiza en cualquier región.6,34 Controlar la sepsis rápidamente es importante, porque al hacerlo se favorece una mejor nutrición, que ayuda al cierre espontáneo, evita la recurrencia posterior al cierre y disminuye la mortalidad.6,17,27 Es una de las causas más frecuentes de tratamiento quirúrgico, y la principal causa de mortalidad de los pacientes con fístulas enterocutáneas. En el caso que nos ocupa, la infección respiratoria baja (bronconeumonía) del lado afectado por el trauma, fue una de las causas del retraso del tratamiento definitivo, secundario a la contusión pulmonar al inicio, al decúbito prolongado y la manipulación de la vía aérea después, que pudo ser controlado con tratamiento antibiótico específico y fisioterapia respiratoria. A pesar de que para algunos autores el tratamiento establecido disminuye el porcentaje de pacientes que deben ser operados, entre el 39 y el 80 % de los pacientes con fístulas enterocutáneas necesitarán algún tipo de tratamiento quirúrgico durante su evolución.6,16,27,35,36
La principal indicación para el tratamiento quirúrgico es el control de la sepsis, generalmente para el drenaje de abscesos.37-39 Otras indicaciones incluyen a los factores de mal pronóstico para el cierre espontáneo: trayecto corto o epitelizado, lesión de más de un 50 % del diámetro del asa intestinal, eversión de la mucosa, entre otros. El deterioro del paciente secundario al gasto de la fístula, también es un importante indicativo para intervenir o no quirúrgicamente. También debe considerarse en el tratamiento quirúrgico el factor tiempo, o sea, la persistencia de la fístula por más de 6 semanas después del control o eliminación de la sepsis, ya que la probabilidad de cierre espontáneo es menor del 10 % en estos casos.6,16,38,39 La cirugía de elección en los pacientes con fístulas enterocutáneas persistentes, si es posible, debe ser radical y agresiva.6,16,39,40
La mayoría de los cirujanos accede a la cavidad abdominal a través de una incisión que dista 5 cm de la cicatriz quirúrgica original. Esto es para llegar a un área virgen donde las adherencias son más laxas, o no hay, y a partir de esta zona comenzar la exploración. Se debe liberar todo el intestino proximal y distal para asegurar que no esté ocluido. La resección del segmento afectado brinda mejores resultados al buscar zonas mejor vascularizadas y menos traumatizadas. Otros procedimientos incluyen la realización de ostomías de alimentación, desfuncionalización del segmento intestinal que presenta la fístula, parcial o totalmente, cierre con colocación de sondas intraluminales y cierres primarios (este último tiene una falla reportada del 40 al 80 %).6,16,40 En el presente trabajo fue posible la realización del acceso al del abdomen por la región pararrectal izquierda, lisis de bridas y anastomosis primaria con resultados satisfactorios. Dadas las malas condiciones de la pared abdominal nos fue imposible el cierre completo de todos los planos, teniendo que hacerlo la piel y el tejido celular subcutáneo por segunda intención, lo que tardó alrededor de 3 meses, que dejó una hernia incisional como secuela.
Como diagnóstico definitivo se puede plantear que nos encontramos frente a un paciente politraumatizado complejo, con lesiones toracoabdominales graves con peligro inminente para su vida, que nos llevó a realizar una intervención rápida del personal del Servicio de Anestesia y de Cirugía de guardia. Además, se produjeron múltiples complicaciones como: hemoneumotórax derecho, derrame pleural persistente, hemoperitoneo, lesiones hepáticas en los 2 lóbulos, bilirragia persistente, perforación intestinal, fístula de alto gasto en el yeyuno, desnutrición severa, bronconeumonías a repetición, abdomen expuesto y hernia incisional, que lo llevaron a numerosas intervenciones quirúrgicas.
REFERENCIAS BIBLIOGRÁFICAS
1. Halversen RC, Hogle HH, Richards RC. Gastric and small bowel fistulas. Am J Surg. 1969;118:968-72.
2. Nassos TP, Braash JW. External small bowel fistulas. Current treatment and results. Surg Clin North Am. 1971;51:687-92.
3. Hollender LF, Meyer C, Avet D, Zeyer B. Postoperative fistulas of the small intestine: therapeutic principles. Worid J Surg. 1983;7:474-80.
4. Martineau P, Schwed JA, Denis R. Is octreotide a new hope for enterocutaneous and external pancreatic fistulas closure? Am J Surg. 1996;172:386-95.
5. Fuentes Valdés E. Fístulas gastroenterocutáneas: factores que influyen en la mortalidad. Rev Cubana Cir [serie en internet]. 2000 [citado 20 de febrero de 2011];41(2). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0034-74932002000200004&lng=es&nrm=iso&tlng=es
6. Edmunds Jr LH, Williams GM, Welch CE. External fistulas arising from the gastrointestinal tract. Ann Surg. 1960;152:445-71.
7. Berry SM, Fischer JE. Classification and pathophysiologyof enterocutaneous fistulas. Surg Clin North Am. 1996;76:1027-36.
8. Prickett D, Montgomery R, Cheadie WG. External fistulas arising from the digestive tract. South Med J. 1991;84:736-9.
9. Fischer JE. The pathophysiology of enterocutaneous fistulas. World J Surg. 1983;7:446-50.
10. Arenas-Márquez H, Anaya-Prado R, Hurtado H. Consenso mexicano en el manejo integral de las fístulas del aparato digestivo. Cir Gen. 2000;22:287-9.
11. Kuvshinoff BW, Brodish RJ, McFadden DW, Fischer JE. Serum transferrin as a prognostic indicator of spontaneous closure and mortality in gastrointestinal cutaneous fistulas. Ann Surg. 1993;217(6)5:623.
12. Lévy E, Frileux P, Cugnenc PH, Honiger J, Ollivier JM, Parc R. High-output external fistulae of the small bowel: management with continuous enteral nutrition. Br J Surg. 1989;76:676-9.
13. Schein M, Decker GAG. Postoperative external alimentary tract fistulas. Am J Surg. 1991;161:435-8.
14. Vallés Gamboa M. Fístulas enterocutáneas de intestino delgado. Manejo terapéutico. Gastroenterología Integrada. 2002;3(3):162-6.
15. Chapman R, Foran R, Dunphy JE. Management of intestinal Fistulas. Am J Surg. 1964;108:157-64.
16. Zuidema G, Shakelford RT. Fístulas del intestino delgado. 3ra edición. Buenos Aires: Editorial Panamericana; 1997. p. 200-50.
17. Howard A, Reber CR. Management of External Gastrointestinal Fistulas. Ann Surg. 9 October 1978;188(4):460-83.
18. Webster NW, Carey LC. Fistulae of intestinal tract. Year Book Medical Publisher. 1976;13(6):20-30.
19. Morales Díaz I, Pinilla González R. Fístulas externas del tubo digestivo. Actualización de las normas de cirugía [homepage en Internet] La Habana, Cuba [citado 20 de febrero de 2011]. Disponible en: http://www.sld.cu/galerias/pdf/uvs/cirured/38.-_fistulas_intest._ext_2.pdf
20. MacFayden BV. Management of gastrointestinal fistulas with parenteral hyperalimentation. Ann Surg. 1973;74:100.
21. Reber HA. Management of external gastrointestinal fistulas. Annals of Surg. 1978;188:460.
22. Mughal MM, Bancewicz J, Irving HM. "Laparostomy" a technique for the management of intractable abdominal sepsis. Br J Surg. 1996;73:253-9.
23. Stiges-Serra A, Jaurrieta E, Stiges-Creus A. Management of external postoperative enterocutaneous fistula. Ann Surg. 1979;190:189-202.
24. Schein M, Decker D. Gastrointestinal fistulas associated with large abdominal wall defects: experience with 43 patients. Br J Surg. 1990;77:97-100.
25. Stone Patrick A. Trauma. Inf Crit Care. 2004;57:1082-6.
26. Schirmer CC, Gurski RR, Gugel FL, Lazzaron AR, Brentano L, Kruel CD. Alternative surgical treatment for complex enterocutaneous fistula. Int Surg. 1999;84(1):29-34.
27. Fazio W, Cooutsoftides T, Eteiger E. Factor influencing the outcome of treatment of small bowell cutaneous fistula. World J Surg. 1983;7(4):481-8.
28. Peix JL, Barth X, Baulieux J, Boulez J, Donne R, Maillet P. Etude d´une serie de soixante-six fistules postoperatoires de l´intestin grele. Ann Chir. 1982;36:18-24.
29. Halasz NA. Changing patterns in the management of small bowell fistulas. Am J Surg. 1978;136:61-6.
30. Soeter PB. Review of 404 patients with gastrointestinal fistulas: impact of parenteral nutrition. Ann Surg. 1979;190:189.
31. Foster CE, Lefor AT. General treatment of gastrointestinal fistulas. Recognition, stabilization, and correction of fluid and electrolyte imbalances. Surg Clin North Am. 1996;76:1037-52.
32. Dudrick SJ, Maharaj AR, McKeivey AA. Artificial nutrition support in patients with gastrointestinal fistulas. World J Surg. 1999;23:570-6.
33. Apostolos K, Tassiopoulos MD, Baum G, Halverson JD. Small bowell fistulas. Surg Clin N Am. 1996;76(5):1175-81.
34. Buechter KJ, Leonovicz D, Hastings PR, Fonts C. Enterocutaneous fistulas following laparotomy for trauma. Am Surg. 1991;57:354-8.
35. McIntyre PB, Ritchie JK, Hawley PR, Bartram CI, Lennard-Jones JE. Management of enterocutaneous fistulas: a review of 132 cases. Br J Surg. 1984;71:293-6.
36. Sheldon GF, Gardiner BN, Way LW, Dunphy JE. Management of gastrointestinal fistulas. Surg Gynecol Obstet. 1971;133:385-9.
37. Rose D, Yarborough MF, Canizaro PC, Lowry SF. One hundred and fourteen fistulas of the gastrointestinal tract treated with total parenteral nutrition. Surg Gynecol Obstet. 1986;163:345-50.
38. Buechter KJ, Leonovicz D, Hastings PR, Fonts C. Enterocutaneous fistulas following laparotomy for trauma. Am Surg. 1991;57:354-8.
39. Hill GL. Operative strategy in the treatment of enterocutaneous fistulas. World J Surg. 1983;7:495-501.
40. Martínez O. Fístulas enterocutáneas posoperatorias. Gaceta Médica México. 2003;139(2):30-40.
Recibido: 15 de septiembre de 2010
Aprobado: 8 de noviembre de 2010.
Ricardo Almeida Varela. Hospital Universitario "Gral. Calixto García". Ave Universidad y calle J. El Vedado, municipio Plaza. La Habana, Cuba. Correo electrónico: ralmeida@infomed.sld.cu