Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm v.35 n.2 Ciudad de la Habana Mayo-ago. 2001
Productos naturales
Instituto de Farmacia y Alimentos. Universidad de La Habana
Ácidos carboxílicos del fruto de Bromelia pinguin L. (piña de ratón) por HPLC
Juan Abreu Payrol,1 Migdalia Miranda Martínez,1 Osmaida Castillo García3 y Delfa Redondo López4
Resumen
Se realizó el estudio de un extracto acuoalcohólico del fruto de B. pinguin L. (piña de ratón) por cromatografía líquida de alta presión (HPLC), con el objetivo de detectar la presencia de ácidos carboxílicos. Se ratificó la presencia de ácido cítrico, y por primera vez se señala la existencia de ácidos glicólico, málico, láctico, succínico y aconítico. Estos compuestos se identificaron por sus tiempos de retención contra patrones.
DeCS: PLANTAS MEDICINALES; EXTRACTOS VEGETALES; ACIDOS CAROBOXILICOS/análisis; ACIDOS CARBOXILICOS/farmacología; CROMATOGRAFIA LIQUIDA DE ALTA PRESION; QUIMICA FARMACEUTICA.
La elevada frecuencia de la presencia, desde el punto de vista bioquímico, del grupo carboxilo, significa que los ácidos se encuentran en todos los organismos vivos, ellos mismos y, como derivados, en todos los grupos metabólicos mayores. Esta propiedad puede presentarse en ausencia de este grupo funcional, como en los fenoles y el ácido ascórbico (enol). Participan en el metabolismo esencial y, en este papel, se alinean desde los ácidos sencillos de la frecuencia respiratoria a los complejos ácidos desoxirribonucleicos, implicados en la conservación y transmi-sión de los caracteres hereditarios. En los ciclos metabólicos suelen funcionar asociados con coenzimas, y acumularse como sales simples, ésteres y amidas o, menos frecuentemente, en estado libre.1,2
La mayoría de los ácidos se han aislado de los frutos, aunque se supone que gran parte de ellos se sintetizan en hojas y raíces, y de aquí son translocados. Existen argumentos a favor de esta hipótesis.3 La aplicación de la técnica de cromatografía líquida de alta presión (HPLC) al estudio de los ácidos carboxílicos se realiza hoy rutinariamente. Inabarcables son los reportes que refieren su empleo en el estudio de ácidos carboxílicos de diferentes fuentes naturales, entre las que resaltan los jugos y extractos de frutas. En este último caso generalmente se emplea una columna de fase reversa (C18, ODS-2), con una fase móvil constituida por una solución acuosa de pH 2-2,5 y la utilización de un detector UV a una longitud de onda que puede variar de 206 a 215 nm.
Con estas condiciones se han separado mezclas de ácidos, entre los que se pueden citar: oxálico, tartárico, málico, acético, cítrico, succínico, ascórbico, dehidroascórbico, quínico, shiquímico, láctico, etc. Los experimentos han permitido la cuantificación de los ácidos encontrados, y se han diseñado técnicas con este fin.4-10
Métodos
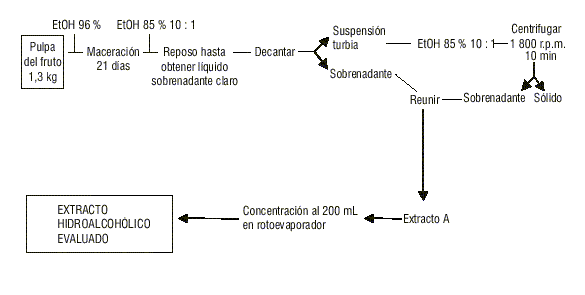
Se obtuvo el extracto estudiado mediante el procedimiento expuesto en la figura 1.
El experimento se realizó en un cromatógrafo KNAUER, con un integrador SHIMADZU. Se utilizó una columna Hypersil C18 (fase reversa) de 25 cm de longitud y d.i. 4,6 mm. La presión de trabajo fue de 7,8-8 MPa y la velocidad de flujo de 0,6 mL/min. El tiempo de corrida fue de 30 min.
Como solvente de elución se empleó buffer fosfato a pH 2,5; se utilizó un detector UV a l 210 nm.
Se inyectó una solución de la muestra, de concentración 1 m g/1 mL. Se identifica-ron los ácidos por sus tiempos de retención en comparación con patrones.
Tabla. HPLC de los ácidos de la muestra
|
Tiempo de retención (min) | Compuesto | Concentración (g.L-1) |
|
6,25 | Ácido glicólico | 0,029 |
|
7,665 | Ácido (+) - málico | 0,048 |
|
8,76 | Ácido (+) - láctico | 0,129 |
|
14,225 | Ácido cítrico | 0,366 |
|
16,245 | Ácido succínico | 0,208 |
|
24,958 | Ácido aconítico | - |
Resultados
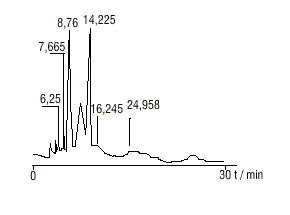
En el cromatograma del extracto (fig. 2), bajo las condiciones de estudio antes descritas, se observaron más de 20 picos. Varios de estos picos pudieron ser identificados como hidroxiácidos por sus tiempos de retención, en comparación con patrones estudiados en estas mismas condiciones (tabla).
Fig. 2. Cromatograma del HPLC de los ácidos de la muestra.
Discusión
Se pudieron identificar los ácidos glicólico, málico, láctico, cítrico, succínico y aconítico; este último en forma de trazas, teniendo en cuenta su tiempo de retención contra patrones, lo que permitió su cuantificación parcial. Se confirma la presencia de ácido cítrico, anunciada por Abreu J (Estudio químico y farmacognóstico preliminar de Bromelia pinguin L. [ piña de ratón). Tesis. Universidad de La Habana, Instituto de Farmacia y Alimentos. 1996), con el empleo de CG-EM, y se detecta la presencia de un importante grupo de hidroxiácidos por primera vez en los frutos maduros de B. pinguin L.
Se identifican por primera vez los ácidos glicólico, málico, láctico, succínico y aconítico en este fruto.
También se ratifica el hecho de la composición compleja en ácidos orgánicos del fruto de B. pinguin L. Se precisa un estudio más detallado para llegar a conocer completamente los componentes de la fracción acídica de este fruto.
Summary
The study of an aqueous-alcoholic extract from B.Pinguin L.(piña de ratón) fruit by high-performance liquid chromatography (HPLC) was conducted to detect carboxylic acids. The presence of citric acid was confirmed and for the first time, glycolic, malic, lactic, succinic and aconitic acids were detected. These compounds were identified by their holding times when compared to the patterns.
Subject headings: PLANTS, MEDICINAL; PLANT EXTRACTS; CARBOXYLIC ACIDS/analysis; CARBOXYLIC ACIDS/pharmacology; CHROMATOGRAPHY; HIGH PRESSURE LIQUID; CHEMISTRY PHAR-MACEUTICAL.
Referencias bibliográficas
- Trease GE, Evans WC. Lipids. En: Tratado de farmacognosia. 13 ed. México DF: Interamericana, McGraw-Hill, 1991:231-67.
- Claus EP, Tyler VE. Lípidos. En: Farmacognosia. La Habana: Editorial Ciencia y Técnica, 1970:177--97.
- Albornoz A. Ácidos orgánicos y carbohidratos. En: Productos naturales: estudio de las sustancias y drogas extraídas de las plantas. Caracas: Publicaciones de la Universidad Central de Venezuela, 1980:257-89.
- Shaw PE, Wilson CW. III. Organic acids in orange, grapefruit and cherry juices quantified by high-performance liquid chromatography using neutral resin or propylamine columns. J Sci Food Agric 1983;34(11):1285-8.
- Coppola ED, Starr MS. Liquid-chromatographic determination of major organic acids in apple juice and cranberry juice cocktail: collaborative study. J Assoc Off Anal Chem 1986;69(4):594-7.
- Eckert M, Baumann G, Gierschner K. Comparative high-pressure liquid-chromatographic and enzymic analysis for fruits acids in fruit juices. Fluess Obstet 1987;54(3):134-8.
- Romero Rodríguez MA, González Rodríguez MV, Lage Yusty MA, López Hernández J, Paseiro Losada P, Simal Lozano J. Identification and quantitative analysis of the major organic acids in fruits by HPLC. An Bromatol 1991;42(2):299-306.
- Nisperos Corriedo MO, Buslig BS, Shaw PE. Simultaneous detection of dehydroascorbic, ascorbic and some organic acids in fruits and vegetables by HPLC. J Agric Food Chem 1992;40(7):1127-30.
- Li JC, Shi J. Determination of fruit acid by high-performance liquid chromatography. Fenxi-Huaxue 1993;21(8):878-81.
- Elkins ER, Heuser JR. Detection of adulteration in apple juice by L-malic/total malic acid ratio: collaborative study. J AOAC Int 1994;77(2):411-5.
Recibido: 18 de diciembre del 2000. Aprobado: 26 de enero del 2001.
M.Sc. Juan Abreu Payrol. Instituto de Farmacia y Alimentos. Universidad de La Habana. Ave. 23 No. 21422 entre 214 y 222, La Coronela, municipio La Lisa, Ciudad de La Habana, Cuba.
1 Master en Ciencias. Profesor Auxiliar.
2 Doctora en Ciencias. Profesora Titular.
3 Licenciada en Ciencias Farmacéuticas.
4 Licenciada en Química. Investigadora Agregada. Instituto Cubano de Investigaciones de Derivados de la Caña de Azúcar (ICIDCA).