Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión impresa ISSN 0034-7515versión On-line ISSN 1561-2988
Rev Cubana Farm v.43 n.2 Ciudad de la Habana Mayo-ago. 2009
ARTÍCULOS ORIGINALES
Optimización de un juego de reactivo para determinar fósforo por método ultravioleta
Determination of phosphorus presence by UV method and the of a reactant kit optimization
Lisandra García BorgesI; Niurka Russeaux GuíaII; Lilliam Valdés DiezIII
IMáster en Ciencias Tecnología y Control de Medicamentos. Empresa de Productos Biológicos "Carlos J. Finlay". La Habana, Cuba.
IIMáster en Ciencias Tecnología y Control de Medicamentos. Investigadora Agregada. Empresa de Productos Biológicos "Carlos J. Finlay". La Habana, Cuba.
IIIMáster en Ciencias Bioquímicas. Investigadora Titular. Empresa de Productos Biológicos "Carlos J. Finlay". La Habana, Cuba.
RESUMEN
Cada día, en la medicina clínica, cobra mayor auge el estudio de las enfermedades relacionadas con la formación del esqueleto y el metabolismo de los minerales, de gran importancia en afecciones renales y las relacionadas con la nutrición, donde desempeña una función primordial el ion fósforo. Con vistas a ofertar a los laboratorios clínicos de Cuba un diagnosticador para determinar fósforo por un método ultravioleta, se formuló un monorreactivo listo para su uso, realizando la optimización de este, así como de la técnica de análisis diseñada para su determinación, la cual es aplicable en los laboratorios clínicos de la red de salud que cuentan con el equipamiento tecnológico para la lectura en el espectro ultravioleta. Se optimizó cada uno de los componentes del monorreactivo, así como la técnica analítica mediante diseños experimentales, y quedaron establecidos los valores óptimos de cada uno. Adicionalmente, se realizó una evaluación con el reactivo optimizado donde se obtuvo una curva lineal en el intervalo de interés clínico y un coeficiente de variación menor del 3 %.
Palabras clave: Fósforo, optimización, diagnóstico clínico, analítica.
ABSTRACT
Every day, in clinical medicine, increase the interest for the diseases study related to skeletal development and the mineral metabolism, very important in renal affections and those related to nutrition, where it has an essential role the phosphorus ion. To offer Cuban clinical laboratories with diagnosis tool to determine the presence of phosphorus by a UV method, we formulated a monoreactive component ready for use, performing its optimization, as well as of the analysis technique designed to its assessment, which is applicable in clinical laboratories of health network with the technological equipment to read in UV spectrum. Each monoreactive component was optimized, as well as the analytical technique by means of experimental designs, staying the optimal values of each. Also, we performed an assessment using optimized reactive obtaining a lineal curve in clinical interest interval, and a variation coefficient lower than 3 %.
Key words: Phosphorus, optimization, clinical diagnosis, analytical.
INTRODUCCIÓN
El ion fósforo es un elemento ampliamente distribuido en el cuerpo humano, constituye el principal anión encontrado dentro de las células y se encuentra fisiológicamente relacionado con diversas funciones metabólicas importantes. Está involucrado en el metabolismo de los carbohidratos como intermediario fundamental y sirve como donante de fosfatos de alta energía (ATP) durante la fosforilación oxidativa en la mitocondria.1 Esta fuente de energía mantiene muchas funciones fisiológicas como contractilidad muscular, funciones neurológicas y transporte de electrolitos. El fósforo, además es un componente estructural de otras sustancias fisiológicamente importantes: ácidos nucleicos, fosfolípidos, nucleótidos (NADP, NADPH), los cuales son importantes en sistemas enzimáticos. El fósforo constituye un ele mento esencial en la membrana celular fosfolípidica, en las fosfoproteínas, contribuye a mantener la concentración crítica intracelular y proporciona sustrato para la mineralización de los huesos.2
Teniendo en cuenta lo anteriormente descrito, la determinación de fósforo en la rutina del laboratorio clínico se encuentra relacionada con el diagnóstico de diversas afecciones como las enfermedades de los huesos, músculos debilitados, enfermedades renales crónicas, en pacientes con diálisis, estatus poscirugía de tiroides, enfermedades paratiroideas, pacientes con nefrolitiasis, alcoholismo crónico, deficiencias de vitamina D (síndrome de mala absorción) y en pacientes que requieren de cuidados intensivos (nutrición parenteral, ventilación mecánica).3
La determinación del fósforo inorgánico se efectúa en suero o plasma, con el empleo de diferentes métodos como son la titulación acidimétrica, procedimientos enzimáticos, la determinación fotométrica del compuesto no reducido a 340 nm, la determinación fotométrica en el espectro visible de la reacción del fósforo con diferentes compuestos cromogénicos entre ellos el ácido molibdivanadofosfórico, el compuesto formado con verde malaquita, entre otros. De los métodos mencionados, el método ultravioleta (UV) presenta mayor aceptación (modificaciones hechas al método propuesto por Daly y Ertingshausen 1972).4 Este método posee varias ventajas entre las que se incluyen mayor sensibilidad, estabilidad, simplicidad y rapidez ya que no requiere del uso de un segundo reactivo en la determinación; perfectamente automatizable lo que constituye la clave para lograr una mayor reducción de los costos y un mayor procesamiento de muestras en el diagnóstico. Aproximadamente el 80 % de los laboratorios en el mundo usan el procedimiento UV en las determinaciones de fósforo inorgánico en suero.5 El fundamento de la técnica se basa en la reacción de los molibdatos con los fosfatos para formar compuestos heteropoli como el fosfomolibdato amónico ((NH4)3[P(MO3O10]4) que presentan un máximo de absorción en la zona del espectro UV, a una longitud de onda de 340 nm.6,7 Se describen modificaciones para esta técnica basada en la composición del juego de reactivo: sales de molibdato, ácidos,6 preservos, entre otros y las condiciones en que se realiza la técnica analítica de las cuales la temperatura de reacción y el tiempo de desarrollo de reacción son las más frecuentes.4,5,8
En Cuba se desarrolla una técnica colorimétrica para la determinación de fósforo compleja que requiere del filtrado libre de proteínas. Con vistas a la introducción del método UV en los laboratorios clínicos de la red nacional de salud, que garantice mayor rapidez y confiabilidad en los resultados analíticos, el objetivo de este trabajo fue el diseño y optimización de un reactivo listo para su uso cuya técnica se basa en el método UV, que evite el paso previo de desproteinización.
MÉTODOS
Los productos químicos utilizados fueron de calidad analítica, de la firma Merck, Alemania. Las mediciones espectrofotométricas se realizaron en un equipo espectrofotómetro LAMBDA EZ 201 de la firma Seppim, Francia. Las pesadas se realizaron en balanza analítica Sartorius (d= 0,1), Alemania. Los resultados fueron procesados por el programa estadístico STATISTIC versión 5.1.
Composición del monorreactivo
Los estudios de optimización están dirigidos a los componentes críticos de la formulación: amonio molibdato, ácido sulfúrico y un agente surfactante no iónico. El fundamento de la técnica se basa en la reacción de los fosfatos con el ion molibdato en medio ácido para formar un complejo inorgánico molibdato fosfórico con un máximo de absorción a 340 nm.
En la optimización de las concentraciones de amonio molibdato y ácido sulfúrico se tuvo en cuenta la relación entre la variable dependiente (absorbancia) y las variables independientes del juego: y= f (t0;T0) donde t0= concentración de amonio molibdato; T0= concentración de ácido sulfúrico. Los puntos de las corridas son colocados simétricamente alrededor del punto inicial, transformados a los valores de las coordenadas en forma estándar con la relación:
donde:
xjm: valor de la variable xj en el centro µ del plan experimental
hj: módulo de la variable xj
La optimización se realizó a través de un plan cuadrático 32, en el cual el intervalo de concentraciones analizado (x1= amonio molibdato de 0,4 a 2,0 mmol/L y x2= ácido sulfúrico de 200 a 500 mmol/L), varía para cada formulación, lo que permite definir la combinación óptima de concentraciones. Las concentraciones estuvieron centradas en un valor inicial hasta ahora utilizado: amonio molibdato 0,8 mmol/L y ácido sulfúrico 210 mol/L. Con las 9 variantes preparadas se realizó el ensayo funcional por triplicado para cada variante, con vistas a determinar los valores de absorbancia: 2 mL de reactivo preparado por 20 µL de muestra de referencia de fósforo, con la utilización de una sustancia de referencia producida por la Empresa "Carlos J. Finlay" a una concentración de 1,64 mmol/L. Las lecturas de absorbancia se realizaron a 340 nm.
Con las concentraciones obtenidas para cada uno de los componentes durante la optimización se preparó el reactivo y se determinó la absorbancia promedio en un número de 2 corridas a 340 nm.
Las concentraciones del agente surfactante se optimizaron a través de la comparación de las curvas de calibración obtenidas a diferentes concentraciones entre 0,1 y el 0,5 % (m/v) del surfactante con un juego de soluciones de referencia de fósforo de producción nacional en un intervalo de concentraciones entre 0,83 y 4,00 mmol/L. Se realizó el análisis estadístico con el empleo del estadígrafo t de Student para 2 coeficientes de regresión en ecuaciones lineales a partir de los valores de las pendientes obtenidas, a las concentraciones 0,2 y 0,3 %.
La optimización de la técnica analítica se realizó a través de diseños factoriales independientes, como se indica a continuación:
Volúmenes de muestra y de reactivo: Se empleó el análisis estadístico a través de la prueba ANOVA de clasificación simple con diseños experimentales independientes sencillos basados en la respuesta de absorbancia de la reacción a 340 nm; se realizaron 9 réplicas para cada variante de combinación entre los volúmenes.
Temperatura de reacción: La técnica analítica se evaluó según plantea la literatura4 para el método en estudio, donde se analizaron 5 réplicas a 25, 30 y 37 ºC; se evaluó la funcionabilidad del ensayo con 20 µL de suero control por 2 mL de reactivo, y se propuso un tiempo de incubación de 1, 3 y 5 min. Los resultados fueron procesados a través del método de Anova clasificación simple y la prueba de Duncan para muestras independientes.
Tiempo de desarrollo de color: Se varió el tiempo de desarrollo de reacción hasta 120 min, y se realizaron 5 determinaciones en cada ensayo. El ensayo funcional se realizó con las condiciones de volúmenes de muestra y de reactivo anteriormente establecidas durante este estudio, a temperatura ambiente de 25 a 30 ºC. Se analizaron los resultados por la prueba de Anova clasificación simple y la prueba de Duncan para muestras independientes.
Estudio de funcionabilidad
Con la nueva formulación optimizada y la técnica analítica se estudió la linealidad, en un intervalo de 0,8 hasta 4,8 mmol/L; se compararon los resultados con la formulación empleada como punto de partida a este diseño. Se evaluaron muestras de suero control a diferentes concentraciones: 0,34, 0,56, 1,25, 2,05 y 2,23 mmol/L. Los resultados se expresaron en términos de coeficiente de variación entre los valores obtenidos para 9 réplicas, a cada concentración, teniendo en cuenta el valor de las medias aritméticas y la desviación estándar.
RESULTADOS
Composición del monorreactivo
Los resultados del plan factorial se muestran en la tabla 1. Existe un estrecho grado de concordancia entre las variables, donde a medida que aumenta el valor de las variables x1 y x2 aumenta el valor respuesta absorbancia. De los resultados experimentales se obtuvo la ecuación de regresión cuadrática siguiente:
![]()
donde:
![]()
![]()
F tabulado (05; 2; 6)= 5,10 < F experimental= 6,24
Mediante un sistema de ecuaciones del polinomio aproximado se obtuvo que las variables que constituyen experimentalmente un punto óptimo son amonio molibdato 0,505 mmol/L y ácido sulfúrico 206,5 mmol/L, con un valor de absorbancia promedio en el ensayo funcional de 0,279 ± 0,001895.
Con el agente surfactante al 0,1 % no se obtuvo señal cuantificable en niveles altos de fósforo, a partir de 2,0 mmol/L. En el reactivo preparado con 0,4 y 0,5 % de surfactante, la técnica no cumple con la funcionabilidad del reactivo. No así con la formulación al 0,3 y al 0,2 %, donde se obtuvieron los valores de pendiente m (0,3 %)= 0,396 y m (0,2 %)= 0,377 y los coeficientes de regresión y determinación r=1,000; r2= 0,999 al 0,3 % y r= 0,997, r2= 0,995 al 0,2 %, respectivamente.
Técnica analítica
Volúmenes de muestra y de reactivo: Se obtuvo un nivel de significación p= 0,300 (> 0,05) a través de la prueba de Anova para un nivel de confianza de 95 %. Con la relación de 2 mL volumen del reactivo y 20 µL volumen de muestra de suero, el valor de absorbancia: 0,325, fue mayor respecto a las restantes relaciones estudiadas.
Temperatura de reacción: Los valores resultantes en este estudio se muestran en la tabla 2.
Con la prueba de Duncan aplicada a las medias en cada tiempo, y cada temperatura, no se observaron diferencias significativas p > 0,05, como se muestra:
| Probabilidades(nivel de confianza) p 0,05 | |||
| Temperaturas (ºC) | tiempo (min) | ||
| 1 min | 0,194 | 25 ºC | 0,209 |
| 3 min | 0,464 | 30 ºC | 0,680 |
| 5 min | 0,981 | 37 ºC | 0,877 |
Tiempo del desarrollo de la reacción: El comportamiento de los valores de absorbancia obtenidos se muestran en la figura 1. Los resultados no difieren en el tiempo de estudio, Fexp= 1,0738 (tabulado(0,05;8;36)= 3,06); sin embargo, se puede observar un ligero incremento de los valores de absorbancia de la mezcla de reacción a los 90 min, con la posterior caída de los valores de absorbancia antes de culminar el tiempo de estudio (120 min).
Estudio de funcionabilidad
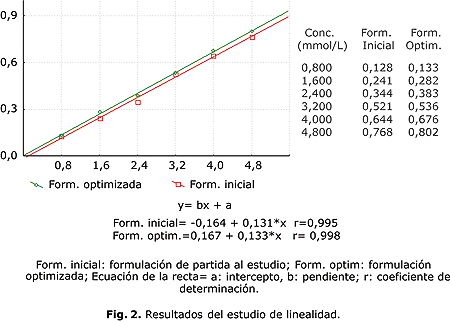
Los resultados de la evaluación de la linealidad del método entre la formulación optimizada y la formulación no optimizada, se muestran en la figura 2, mientras que los resultados del ensayo funcional aparecen en la tabla 3.
DISCUSIÓN
La optimización de un reactivo, método de análisis o procesos, refleja la manera más eficiente de obtener mejores respuestas durante la investigación con la disminución del tiempo del proceso de desarrollo. Para ello se emplean diseños experimentales que le facilitan al analista, con el menor número de experimentos, obtener una respuesta certera y confiable de la composición que debe tener un reactivo, así como de las condiciones óptimas para el desarrollo de la técnica analítica.
Para el diseño de la optimización es importante determinar los factores principales que influyen en la variable objetivo, establecer el intervalo de los valores de estos factores y admitir dónde es más probable que se encuentre el valor óptimo. En este estudio las variables independientes que influyen en la absorbancia (variable objetivo) son las concentraciones de amonio molibdato y ácido sulfúrico, las cuales estuvieron centradas en un valor inicial hasta ahora utilizado en el laboratorio: amonio molibdato 0,8 mmol/L y ácido sulfúrico 210 mol/L.
Para optimizar las concentraciones de estos componentes se seleccionó un diseño cuadrático que permitiera la combinación de estos, por la relación existente entre el amonio molibdato, que reacciona con los iones fósforo en la formación del complejo medible espectrofotométricamente a 340 nm, y el ácido sulfúrico que confiere la acidez requerida.
La combinación óptima del reactivo la constituyen experimentalmente las concentraciones de amonio molibdato 0,505 mmol/L y para el ácido sulfúrico 206,5 mmol/L. El análisis del coeficiente de determinación indica que existe estrecha relación entre las variables independientes (concentración de amonio molibdato y ácido sulfúrico) y la variable respuesta (absorbancia).
El valor del estadígrafo F experimental fue mayor que el F tabulado (0,05; 2; 6), la regresión es significativa para una probabilidad de 0,05 lo cual indica que el modelo es adecuado, y teniendo en cuenta la comparación de los valores de absorbancia para un nivel de confianza de 95 % (valor de absorbancia teórica= 0,277), donde no se aprecian diferencias significativas; se puede considerar que los valores de concentración obtenidos son óptimos para la formulación estudiada.
En la proporción en que se forma el complejo fosfomolibdato, resultado de la reacción del amonio molibdato con el ion fósforo presente en las muestras de suero, influye la precipitaco de proteínas, por lo que para descartar la necesidad de preparar un filtrado libre de proteínas, se empleó el agente surfactante no iónico, que además de solubilizar la mezcla de reacción y evitar, de esta forma, la desproteinización previa de las muestras de suero, acelera la formación de color de la reacción y le confiere estabilidad al reactivo.9
En la optimización del agente surfactante no iónico se observó que las formulaciones preparadas con el tensoactivo a las concentraciones 0,1, 0,4 y 0,5 % no ofrecen respuestas confiables en la determinación de fósforo. Al analizar la formulación preparada con el 0,2 y 0,3 % de surfactante se comprobó estadísticamente que existen diferencias significativas entre los valores de pendiente para cada concentración: t experimental= 4,355 (t tabulada (0.01;8)= 2,896). Se continuó el desarrollo de la formulación con concentración de 0,3 % del agente surfactante, con la cual como se muestra en los resultados, la curva presenta mayor valor de pendiente y los coeficientes de regresión y determinación son más cercanos al valor óptimo de una curva ideal.
De esta forma quedó diseñado un juego de reactivos para la determinación de fósforo en suero, sencillo y rápido, conformado por amonio molibdato 0,505 mmol/L, ácido sulfúrico 206,5 mmol/L, surfactante no iónico 0,3 % (m/v) y la solución de referencia de fósforo.
El diseño de la técnica analítica es un paso más en el desarrollo del diagnosticador con el objetivo de lograr flexibilidad y resultados confiables en la técnica a introducir en los laboratorios clínicos, tanto para uso manual como automatizado.
La relación entre los volúmenes de reactivo y de la muestra durante la reacción, es un aspecto importante para la aplicación de un nuevo producto, pues garantiza menor costo en el laboratorio y mayor factibilidad para la automatización de las técnicas analíticas. Con este estudio se decidió utilizar 2 mL de reactivo por 20 µL de muestra de suero, a través del análisis estadístico por el método ANOVA de clasificación simple, al no observarse diferencias significativas con un nivel de confianza del 95 % con la variable respuesta reportada para este método (p= 0,300).
La temperatura y el tiempo de desarrollo de la reacción son parámetros indispensables en el estudio de optimización y dan criterio de la flexibilidad de la técnica para su aplicación en el laboratorio de forma manual o automatizada, lo que responde a la necesidad o no de una infraestructura determinada para la implementación de los métodos de análisis.
Los resultados de estos experimentos garantizan el desarrollo de la técnica bajo diferentes condiciones de temperaturas, por no existir diferencias significativas para una probabilidad de 0,05 entre las variables analizadas en los tiempos de incubación a las temperaturas estudiadas cuando se analizaron por el método ANOVA y por la prueba de Duncan para muestras independientes, por lo que la técnica se puede realizar a temperatura entre 25 y 30 ºC. En dependencia del equipo de laboratorio, se podrá incubar la reacción a 37 ºC, sin variación de la respuesta analítica. La reacción se completa a los 3 min, los valores de absorbancia a partir de este tiempo se estabilizan hasta los 90 min, además cuando se analizaron las medias individuales a través de la prueba de Duncan se demostró que no existen diferencias significativas para una probabilidad de 0,05 a partir de que se alcanza los 3 min. Por lo que se propone realizar la lectura de absorbancia del complejo a partir de los 3 min en una técnica automatizable, y a los 5 min con la técnica manual.
Con todos los parámetros optimizados en la técnica de análisis, el desarrollo del ensayo funcional manualmente queda diseñado: 20 µL de muestra por 2 mL de reactivo, esperar 5 min a temperatura entre 25 y 30 ºC y leer a 340 nm, con flexibilidad a leer a los 3 min en equipos automatizados e incubar a temperatura 37 ºC, si así lo requiere de acuerdo con la infraestructura tecnológica del laboratorio. Con estas condiciones se evaluaron las características funcionales del diagnosticador para avalar la confiabilidad y seguridad de los resultados obtenidos durante la optimización.
En el ensayo de linealidad se comparó la formulación optimizada con la formulación punto de partida a este diseño, la cual se obtuvo a través de la estimación del valor promedio de un intervalo de valores reportados en la bibliografía consultada2,5-7 para cada componente seleccionado y diseños experimentales 22 con los que se ofrecen respuestas analíticas para esta formulación. La formulación antes de ser optimizada cumple con el criterio de aceptación r ³ 0,99; sin embargo, se observó un mayor incremento en las lecturas de absorbancia y en el valor de la pendiente, lo que indica que la formulación optimizada brinda mayor sensibilidad frente a los cambios de concentración.
Las concentraciones de fósforo en el suero se encuentran entre 0,81 y 1,45 mmol/L. La variación de estas concentraciones se relaciona con afecciones provocadas por hipofosfatemia o hiperfosfatemia, de ahí la necesidad de realizar un ensayo de precisión que demuestre la funcionabilidad del reactivo optimizado.
En el estudio de funcionabilidad, el reactivo debe ser capaz de brindar valores confiables en la respuesta analítica, lo cual es medible con la utilización del coeficiente de variación que deberá ser menor al 3 % para esta determinación. Se obtuvieron valores del coeficiente de variación entre 0,55 y 1,98 % en los niveles clínicamente significativos de mayor incidencia, lo que garantiza seguridad en las respuestas analíticas en un amplio intervalo de concentraciones de fósforo. A una concentración de fósforo de 0,3 mmol/L, el coeficiente de variación es mayor, pero se encuentra dentro del límite permisible para este estudio (3 %), lo cual no es significativo, si se tiene en cuenta que un 98 % de las determinaciones de este analito en el laboratorio se asocia con intervalos normales, patológicos altos y patológicos bajos (superiores a una concentración de 0,60 mmol/L) y el 2 % de las determinaciones restantes se encuentra presente en patologías más frecuentes a valores inferiores por debajo de 0,6 mmol/L asociados al metabolismo de fósforo, por lo que los resultados garantizan el diagnóstico de las afecciones relacionadas con el ion fósforo.
REFERENCIAS BIBLIOGRÁFICAS
1. Martindale. The Complete Drug Reference: Electrolytes. 32 ed. London: Pharmaceutical Press; 1999. p. 1147.
2. Davidsohn J, Henry JB. Diagnóstico clínico por el laboratorio. 6 ed. Vol. 1. Madrid: Jims; 1985. p. 653-66.
3. Lotear T. Clinical Laboratory Diagnostics: Use and Assessment of Clinical Laboratory Results. Frankfurt: TH-Books Verlagsgesellschaft mbH; 1998.
4. Daly J. Direct Method for determinating Inorganic Phosphate in serum with the centrifichem. Clin Chem. 1972;18(3):263-5.
5. Kauffman RA. Method and reagent for the quantitative determination of phosphorus in serum and urine. Patent Aplication 0351605. 1996.
6. Diagnostic Chemical Limited, Catalogue No 120-15-1: Inorganic Phosphorus Assay Kit. Montreal: Charlottetown, PEEI; 1987.
7. Martindale. The Complete Drug Reference: Bone Modulating Drugs. 32 ed. London: Pharmaceutical Press; 1999. p.730- 2.
8. Henry RJ, Cannon DC, Winkelman JW. Química Clínica. Bases y técnicas. 2 ed. Tomo I. Barcelona: Jims; 1980. p. 729-38.
9. Neugebauer J. A guide to the properties and uses of detergents in Biology and Biochemistry. New York: Calbiochem Corporation; 1990.
Recibido: 12 de enero de 2009.
Aprobado: 17 de febrero de 2009.
M. C. Lisandra García Borges. Empresa de Productos Biológicos "Carlos J. Finlay". Infanta No.1 162, entre Manglar y Línea de Ferrocarril, municipio Centro Habana, CP 10 300, La Habana, Cuba. Correo electrónico: lisygarcia@finlay.quimefa.cu