Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión impresa ISSN 0034-7515versión On-line ISSN 1561-2988
Rev Cubana Farm v.43 n.3 Ciudad de la Habana sep.-nov. 2009
ARTÍCULOS ORIGINALES
La técnica de Western Blot como criterio de identidad para la vacuna antimeningocócica Men B
Western Blot technique as an identity criterion for Men B antimeningococcal vaccine
R. Rosario Diéguez CastroI; Yanin Muñoz TrujilloII; Mirta Castiñeira DíazIII
I Licenciada en Química. Máster en Tecnología y Control de Medicamentos. Instituto Finlay. La Habana, Cuba.
II Lic. Química. Máster en Ciencias Químicas. Cuba Farmacia. La Habana, Cuba.
III Doctora en Ciencias Farmacéuticas. Instituto de Farmacia y Alimentos (IFAL). Universidad de La Habana. La Habana, Cuba.
RESUMEN
Se desarrolló y validó la técnica de Western Blot aplicada a la vacuna antimeningocócica Men B producida en el Instituto Finlay con el objetivo de demostrar un criterio de identidad. En el estudio de las proteínas antigénicas de la vacuna, P1.15 y P1.4 en vesícula de membrana externa,monograneles y producto final se emplearon en la identificación anticuerpos monoclonales específicos para estas proteínas. Los parámetros desarrollados en la validación de la técnica fueron: especificidad, límite de detección, repetibilidad, precisión intermedia, reproducibilidad y robustez. El método cumplió con los parámetros señalados, por lo que se consideró validado.
Palabras clave: Técnica de Western Blot, vacuna antimeningocócica Men B, identidad, validación del Western Blot.
ABSTRACT
Western Blot technique was developed and validated, applied to Men B meningococcal vaccine produced in "Carlos J, Finlay" Institute to demonstrate an identity criterion. In study of antigenic proteins of the vaccine, we used P1.15 y P1.4 in vesicle of external membrane, monogranels, and end product to identify the monoclonal antibodies specific of these proteins. Parameters developed in technique validation included: specificity, detection limit, repetition, average accuracy, reproduction, and strength. Method fulfilled with specified parameters, thus considering its validation.
Key words: Western blot technique, Men B antimeningococcal vaccine, identity, Western blot validation.
INTRODUCCIÓN
La enfermedad meningocócica constituye uno de los problemas de salud más importantes del mundo, no solo por las altas cifras de muertes, sino por las secuelas que deja fundamentalmente en niños. Sus manifestaciones clínicas pueden variar desde el portador asintomático hasta la meningococemia fulminante.1
El hecho de que estas epidemias continúen ocurriendo en el mundo y que la quimioprofilaxis con sulfadiazina y algunos antibióticos no presenten una efectividad prolongada por la resistencia del microorganismo al tratamiento, hizo pensar en la prevención de la enfermedad a través de vacunas.2,3
La vacuna Men B producida en el Instituto Finlay y obtenida a través del convenio colaborativo con la Glaxo Smith Kline posee en su composición vesícula de membrana externa (VME) del serogrupo B de Neisseria menigitidis correspondiente a la cepa cubana 385/83 y la cepa 228 de Nueva Zelanda además de hidróxido de aluminio como adyuvante y no posee tiomersal.
La importancia del criterio de identidad para la vacuna, estriba en la identificación de las principales proteínas antigénicas presentes en la VME de Neisseria meningitidis serogrupo B como componente principal de la vacuna. El empleo de anticuerpos monoclonales en la identificación específica de las bandas proteicas en la vacuna Men B, logra ubicarla en una posición preferencial por su seguridad, eficacia y tecnología.4
El Western Blot es un método más específico que el de la electroforesis en gel de poliacrilamida desde el punto de vista inmunoquímico y evidencia el reconocimiento de los antígenos por anticuerpos específicos inducidos (identidad), y se puede conocer el peso molecular de las proteínas antigénicas objeto de estudio con el empleo de adecuados patrones de peso molecular conocidos y un equipo analizador de bandas electroforéticas.4,5
MÉTODOS
Equipos e instrumentos de medición: balanza analítica, medidor de pH digital, pipeta automática 2-20 µL, pipeta automática 20-200 µL, pipeta automática 100-1 000 µL.
Muestras:
- VME lote 103-385 correspondiente a la cepa cubana (385).
- VME lote 101-228 correspondiente a la cepa Nueva Zelanda, la cual presenta realizados los controles de calidad según la especificación correspondiente.
- Vacuna monogranel Cu desabsorbido lote 102-385 correspondiente a la cepa Cu certificada con los respectivos controles de calidad según la especificación correspondiente.
- Vacuna monogranel NZ desabsorbido lote 101-228 correspondiente a la cepa NZ certificada con los respectivos controles de calidad según la especificación correspondiente.
- Vacuna Men B desabsorbida lote 129 E certificada con los respectivos controles de calidad según la especificación establecida.
Reactivos (Calidad USP): acrilamida, N',N' metilendaicrilamida (bisacrilamida), tris-(hidroximetil)-aminometano, ácido clorhídrico, hidróxido de sodio, dodecil sulfato de sodio, persulfato de amonio, glicerol, ß mercaptoetanol, glicina, 2-butanol, N,N,N',N' tetrametilendiamina (TEMED), leche descremada, metanol, fosfato dibásico de sodio, fosfato monobásico de sodio, cloruro de sodio, fosfato monobásico de potasio, cloruro de potasio, peróxido de hidrógeno, diaminobencidina, tween 20, agua, conjugado avidin-horseradish peroxidase (BioRad) para revelar el patrón de proteínas biotiniladas de diferentes pesos moleculares, conjugado anti IgG-ratón-peroxidasa (sigma), conjugado anti IgG (específico para Fc)-peroxidasa (sigma).
Técnica: la determinación inmunoquímica cualitativa se realiza a partir del método de Western Blot según los procedimientos iniciales del laboratorio.
La electroforesis se realiza en las mismas condiciones descritas en el Procedimiento Normalizado de Operación (PNO 12-114) establecido en el Laboratorio de Inmunoquímica de la Dirección de Calidad del Instituto. Se utilizó un sistema de geles discontinuos con un gel separador del 14 %. Las muestras se ajustaron a 1 mg/mL con agua purificada y tratadas posteriormente con solución de tratamiento (tris-HCl 0,1 M pH 6,8, b mercaptoetanol 1 %, SDS 2 %, glicerol 0,1 %, bromofenol azul 0,1 %) en una relación 1:1. Se calentaron a 100 °C durante 5 min. Se aplicaron 10 mL y se efectuó la corrida a 35 mA, 200 V y 60 Watt durante 1 h.
Una vez concluida la electroforesis, se continuó con los pasos establecidos para el desarrollo de la técnica del Western Blot. Las proteínas sin teñir se transfirieron a una membrana de nitrocelulosa de 0,45 µm a 350 mA durante 2 h con una solución tris 0,02 mol/L glicina 0,15 mol/L SDS 0,1 % pH 8,3.
El bloqueo se efectuó con leche descremada al 3 % en solución fosfato (fosfato sodio dibásico 0,08 mol/L, cloruro de sodio 1,37 mol/L, dihidrógeno fosfato de potasio 0,015 mol/L, cloruro de potasio 0,27 mol/L pH 7,2) diluido 10 veces, durante 1 h a 37 °C.
Luego de los lavados con el mismo buffer diluido 1/10 se incubó con los anticuerpos monoclonales (anti P1.4 y anti P1.15) diluidos en solución de leche descremada al 1,5 % en solución fosfato (1/10) tween 20 0,1 %. Se repiten los lavados y posteriormente se incubó por espacio de 2 h en una solución de leche descremada 1,5 % con el conjugado adecuado, conjugado anti IgG ratón-peroxidasa.
Se reveló con el sistema diaminobencidina (DAB)-H2O2 y el patrón de PM biotinilado se reveló con el conjugado avidin-horseradish peroxidasa.
Como factor crítico en la validación de la técnica de Western Blot para la vacuna se consideró el tiempo de bloqueo de la membrana de nitrocelulosa con leche descremada al 3 %, haciendo un estudio comparativo entre 1 h y 50 min.
Validación del método de Western Blot: se procedió a la elaboración de la documentación requerida para la validación con la confección del Protocolo de Validación del ensayo según la metodología que se establece en el Protocolo Maestro de Validación de Métodos Analíticos (PMV-002) desarrollado en el Instituto Finlay.
En nuestro caso se evaluaron los parámetros especificidad, límite de detección, precisión (repetibilidad, precisión intermedia y reproducibilidad) y robustez. En el caso de la precisión intermedia se trabajó con los mismos reactivos, equipos, condiciones de laboratorio, en días diferentes y soluciones preparadas por 2 analistas del mismo laboratorio. En la reproducibilidad los analistas de diferentes laboratorios trabajaron con soluciones, equipos, reactivos, condiciones de laboratorio diferentes y días diferentes.
Se elaboró el Protocolo de Validación según los diseños experimentales de cada parámetro estudiado.
De acuerdo con las regulaciones internacionales actuales (Normas ICH, USP 30) en el caso de la validación de una técnica de identidad, solo se requiere el estudio de especificidad, aunque en la regulación 41 del CECMED relacionado con la Validación de Métodos Analíticos se incorpora el límite de detección y la robustez. No obstante, en el Protocolo de Validación diseñado incluimos por las características de la técnica parámetros como la precisión, los cuales aportan una información mayor del desarrollo de la técnica.
RESULTADOS
Se confeccionó el Informe de Validación del estudio realizado de cada parámetro a la vesícula, monograneles y vacuna final donde se presentan los resultados obtenidos en el estudio de cada parámetro y las recomendaciones a seguir con el objetivo de mejorar la técnica.
Especificidad
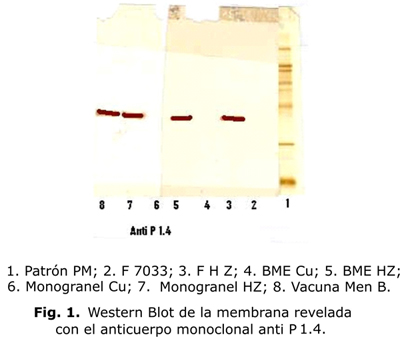
En los resultados de los Western Blot realizados a las muestras de vesículas, vacunas monogranel y vacuna final de las 2 cepas que componen la vacuna Men B, la cepa cubana Cu 385 y la cepa Nueva Zelanda NZ 228, se observó en la membrana revelada con el anticuerpo monoclonal anti P 1.4 que no manifestó la presencia de la banda de la proteína P 1.15 presente en la vesícula de la cepa cubana 385 y en el monogranel Cu (fig. 1). Sin embargo, si apareció la banda característica de la proteína perteneciente a la VME de la cepa NZ P 1.4 así como también se observó en el monogranel NZ y en la vacuna Men B final.
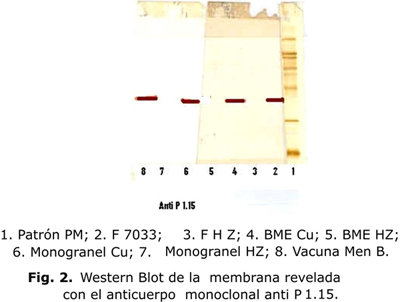
En la otra membrana revelada con el anticuerpo monoclonal anti P1.15 se mostró la banda correspondiente a la proteína de la VME de la cepa cubana 385, la P 1.15, así como también se manifestó en el monogranel Cu y en la vacuna final Men B, no apareciendo la banda de la proteína P 1.4 en el estudio (fig. 2).
Límite de detección
Teniendo en cuenta los resultados obtenidos durante la evaluación del reconocimiento de las proteínas de ambas vesículas de las cepas Cu y NZ preparadas a diferentes concentraciones (0,12, 0,5 y 5 mg) por los anticuerpos monoclonales específicos anti P1.15 y anti P1.4 respectivamente, se observó que puede aplicarse para el estudio de ambas cepas, hasta una concentración mínima de 0,12 mg de las vesículas apreciándose la presencia de las bandas características para cada tipo (fig. 3).
Precisión. Repetibilidad
Los resultados obtenidos fueron satisfactorios y consistentes en cuanto a la repetibilidad para cada réplica de muestras (10 réplicas del Western Blot) de VME de las cepas Cu y NZ, monograneles Cu y NZ y para la vacuna final Men B frente a los respectivos anticuerpos monoclonales anti P 1.15 y anti P 1.4. Se observó la presencia en todos los casos de la banda de proteína específica para cada cepa esperada en cuanto a intensidad y posición obtenida de acuerdo al anticuerpo monoclonal específico al cual se enfrentó (figs. 4 y 5).
Precisión intermedia
Al realizarse el estudio de la precisión intermedia con igual diseño que el de repetibilidad por parte de otro analista del mismo laboratorio con igual equipamiento, reactivos, condiciones ambientales de temperatura y realizado en días diferentes, se observaron iguales resultados en cuanto a la intensidad y posición de la banda de proteína característica de cada cepa, la cubana 385 revelada con el anticuerpo monoclonal anti P 1.15 y la cepa de Nueva Zelanda NZ 228 revelado con el anticuerpo monoclonal anti P1.4 (figs. 4 y 5).
Reproducibilidad
Aun cuando las condiciones de trabajo entre los analistas involucrados de diferentes laboratorios en la validación fueron diferentes en cuanto a reactivos, soluciones, equipamiento y locales de trabajo, se obtuvieron resultados reproducibles (figs. 4 y 5) en cuanto a la presencia de las bandas características de proteína para cada tipo de muestra (VME) Cu y NZ, monograneles Cu y NZ y vacuna Men B final) frente a los dos tipos de anticuerpos monoclonales anti P 1.15 y anti P 1.4.
Robustez
El análisis de los resultados obtenidos durante el revelado de las membranas de nitrocelulosa sometidas a diferentes tiempos de incubación del bloqueo con la leche descremada al 3 % (se ensayó a 1 h y a 50 min cada membrana), tanto para la vesícula como los monograneles y vacuna final, reveló no haber afectación en el patrón de las bandas características para cada muestra estudiada (fig. 6), por lo que se demostró la factibilidad de la disminución del tiempo de incubación de las membranas en el paso de bloqueo hasta 50 min, sin afectar los resultados.
DISCUSIÓN
La técnica de Western Blot diseñada para determinar criterio de identidad en el control de calidad de la vesícula y vacuna final Men B, se ajusta a las condiciones de trabajo del laboratorio y los resultados obtenidos cumplieron con los objetivos para los cuales fue diseñada: el estudio de identidad establecido en las especificaciones de calidad de dichos productos con el empleo de anticuerpos monoclonales contra las proteínas específicas P1.15 y P1.4 presentes en las vesículas Cu 385 y NZ 228 respectivamente como proteínas antigénicas que las componen así como en los monograneles y vacuna final.
Los resultados obtenidos en el estudio de la especificidad con la metodología aplicada, demostró que nuestra técnica es específica para identificar las proteínas correspondientes a cada cepa, Cu y NZ, las cuales son componentes de la vacuna Men B. Este propósito se logró con el empleo de los anticuerpos monoclonales, condición de obligatorio cumplimiento para que una técnica inmunoquímica sea utilizada en el estudio de identidad de un producto.
Aunque se comprobó en el estudio del límite de detección, que puede aplicarse hasta una concentración de 0,12 µg de muestra y lograr la presencia de las bandas de proteínas, se recomienda trabajar con una concentración de 0,5 µg por observarse una mejor definición de las bandas.
Se observó en todos los ensayos de precisión realizados: precisión intermedia, repetibilidad y reproducibilidad que a pesar de realizarse el ensayo en diferentes condiciones de laboratorio, diferentes analistas, diferentes equipamientos y reactivos, no se aprecian cambios significativos en los resultados. Es por esto que se toma como referencia las figuras 5 y 6 para reflejar los resultados por coincidir en todos los casos.
Igualmente en el estudio de la robustez se tomó la misma figura (fig. 6) por obtenerse igual resultado.
Para el caso del estudio del tiempo de bloqueo, se valoró la posibilidad de estudiar reducir el tiempo de bloqueo hasta 30 minutos así como también el tiempo de transferencia.
REFERENCIAS BIBLIOGRÁFICAS
1. Frasch CE, Gotschlich EC. An outer membrane protein of Neisseria meningitidis group B responsible for serotype specificity. J Exp Med. 1974;140:87-104.
2. Robbins JB. Vacunas para la prevención de enfermedades bacterianas encapsuladas: problemas y perspectivas futuras: Inmunoquímica. 1978;15:839-54.
3. Zollinger WD. New and Improved vaccine againts meningoccical disease. New generation vaccine. New York: Dekker Inc.; 1990. p. 325-48.
4. Estrada E. Optimización del Western Blot y aplicación en el estudio de la inmunogenicidad de las proteínas de la vacuna antimeningocócica cubana VA MENGOC BC. Trabajo de determinación de residencia en inmunología. Instituto Finlay. La Habana, 1995.
5. Puido AI, Ruisanchez R, Boqué F, Ruis X. Western Blott como método analítico de control. Analitical Chim Acta. 2002;455:267.
Recibido: 2 de marzo de 2009.
Aprobado: 7 de abril de 2009.
Lic. R. Rosario Diéguez Castro. Instituto Finlay. Centro de Investigación-Producción de Vacunas. Calle 17 No. 19 805, La Coronela, La Lisa, CP 11600, La Habana, Cuba.