Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm v.44 n.1 Ciudad de la Habana ene.-mar. 2010
ARTÍCULOS ORIGINALES
Validación de métodos analíticos de control de procesos de antitumorales inyectables
Analytical methods validation of processes control in injectable antitumor agents
Caridad Margarita García PeñaI; Edel Cunill SemanatII; Mayra Cartaya MoralesIII; Anyisela Díaz de ArmaIV; Yusleydis Curbelo FonteV
IMáster en Tecnología y Control de Medicamentos. Investigador Agregado. Centro de Investigaciones y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
IILicenciado en Bioquímica. CIDEM. La Habana, Cuba.
IIIMáster en Tecnología y Control de Medicamentos. CIDEM. La Habana, Cuba.
IVTécnico Medio en Tecnología de la Salud. CIDEM. La Habana, Cuba.
VTécnico Medio en Química. CIDEM. La Habana, Cuba.
RESUMEN
Se validaron los métodos analíticos alternativos para el control de proceso de fluorouracilo 500 mg, doxorrubicina 50 mg y metotrexato 50 mg por espectrofotometría, por ser estos métodos más sencillos, económicos, que permiten controlar la calidad de los medicamentos en el análisis de control de proceso. Las curvas de calibración del fluorouracilo, la doxorrubicina y el metotrexato, se realizaron en el intervalo de 60 al 140 %, donde fueron lineales con coeficientes de correlación iguales a 0,9998; 0,9999 y 0,9999, respectivamente; la prueba estadística para el intercepto y la pendiente se consideraron no significativas. Se obtuvieron recobrados del 99,97, 99,08 y 99,35 %, respectivamente en el intervalo de concentraciones estudiado, y las pruebas de Cochran y t de Student resultaron no significativas. Los coeficientes de variación de los estudios de la repetibilidad fueron inferiores al 3 % para las 6 réplicas ensayadas, mientras que en los análisis de la precisión intermedia las pruebas de Fischer y t de Student indicaron diferencias no significativas. Los métodos resultaron específicos, lineales, precisos y exactos en el intervalo de concentraciones estudiadas.
Palabras clave: Espectrofotometría, doxorrubicina, metotrexato, fluorouracilo, inyectable.
ABSTRACT
Alternative analytical methods were validated for the process control of 500 mg florouacil, 50 mg doxorrubicin and 50 mg methotrexate by spectrophotometry because of they are more simple and economic allowint to control the drugs quality in process anaslysis control. Calibration curves of fluorouracil, doxorrubicin and methotrexate were plotted in interval from 60 to 140 %, where there were linear with correlation coeficients similar to 0.9998, 0.9999 and 0.9999, respectively; statistical text for intercept and slope were considered as non-significant. Recoveries of 99.97, 99.98 and 99.35 % were achieved, respectively in study concentration interval and Cochran and t-Student tests were also non-significant. Methods were specific, linear, precises and exacts in interval of study concentrations.
Key words: Spectrophotometry, doxorrubicin, methotrexate, fluorouracil, injectable.
INTRODUCCIÓN
El fluorouracilo, la doxorrubicina y el metrotexato inyectable se indican para el tratamiento de diferentes variedades de cáncer entre los que se pueden citar: carcinoma colorectal, de mama, gástrico, pancreático, de vejiga, prostático, carcinoma epitelial de ovario, cervical y hepático, leucemia linfoblástica (linfocítica) aguda, leucemia mieloblástica (mielocítica) aguda, entre otros.1
La espectrofotometría es un poderoso instrumento en una variedad de problemas analíticos. Aunque en muchas ocasiones tiene el inconveniente de la falta de especificidad, debido a la interferencia con los productos de degradación, los cuales en ocasiones pueden presentar un espectro idéntico al componente sin degradar, y en otras las concentraciones a determinar son muy pequeñas y están por debajo del límite de sensibilidad del método o dentro de su error experimental.2,3
La validación es el proceso establecido para la obtención de pruebas documentadas de que el método es lo suficientemente fiable para producir el resultado esperado.4-6 Los parámetros analíticos que pueden ser considerados en la validación de un método analítico, según se expresa en la United States Pharmacopoeia (USP 31), son exactitud, precisión, especificidad, límite de detección, límite de cuantificación, linealidad, intervalo, tolerancia y robustez.
El presente trabajo tiene como objetivo validar los métodos analíticos por espectrofotometría ultravioleta visible, que se utilizan para el control de proceso de 3 formulaciones de citostáticos inyectables: fluorouracilo 500 mg/bbo, doxorrubicina 50 mg/bbo, metotrexato 50 mg/bbo.
MÉTODOS
Métodos de análisis para el control de proceso
Las sustancias de referencia química de fluorouracilo, doxorrubicina y metotrexato fueron suministradas por el grupo de sustancias de referencia del Centro de Investigación y Desarrollo de Medicamentos (CIDEM), La Habana, Cuba), las cuales fueron analizadas por el método cromatográfico establecido para realizar el control de la calidad de la materia prima con purezas de 99,6; 99,2; 99,4 %, respectivamente.
Para el análisis del fluorouracilo se preparó la sustancia de referencia química y las muestras a una concentración de 50 mg/mL, disueltas en ácido clorhídrico 0,1 N. Mientras que para la determinación de doxorrubicina en el control de proceso la sustancia de referencia química y las muestras se prepararon a una concentración de 0,02 mg/mL, disueltas en agua destilada.
Para el análisis del metotrexato se prepararon la sustancia de referencia y las muestras a una concentración de 0,05 mg/mL, disueltas en una mezcla de fosfato de sodio dibásico 0,2 M y ácido cítrico 0,1 M en proporción (63:37); ajustado a pH 6,0. Posteriormente se mezcla la solución anterior con acetonitrilo en proporción (90:10).
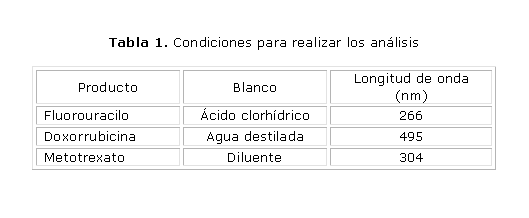
Los análisis de control de proceso de los inyectables se realizaron empleando un espectrofotómetro UV-VIS (Spectronic® GénesisTM 2PC, Japón) con las siguientes condiciones: cubetas: cuarzo; paso óptico de luz: 1 cm. En la tabla 1 se muestran las longitudes de onda y las soluciones blancos empleadas para cada uno de los productos objeto de estudio.
Validación de los métodos analíticos
Las validaciones fueron realizadas según la categoría I (USP 31); se evaluaron los parámetros que a continuación se describen.
Linealidad
Para el análisis de la linealidad se realizaron a través de modelos de 3 determinaciones individuales para 5 concentraciones diferentes que representan el 50, 80, 100, 120, y 150 % de la concentración teórica declarada. Se determinaron las ecuaciones de las rectas, los coeficientes de correlación, las pruebas de significación estadística de la pendiente Sb rel(%), los coeficiente de variación de los factores de respuesta y los ensayos de proporcionalidad.
Exactitud
El análisis de exactitud se realizó con el empleo del método de adición de concentraciones conocidas de sustancias de referencia química a los placebos; se realizaron los modelos de 3 réplicas para 3 concentraciones diferentes: 80, 100, 120 %; se determinaron los porcentajes de recuperación, las desviaciones estándar y los coeficientes de variación. Se analizaron los datos mediante la prueba de Cochran con vistas a comprobar si la variación de la concentración producía diferencias significativas en los resultados y la prueba t de Student para determinar diferencias significativas entre la recuperación media y el 100 % de recuperación.
Precisión
El estudio de la precisión se realizó mediante la evaluación de la repetibilidad y la precisión intermedia del método. La repetibilidad se analizó mediante la evaluación de 6 réplicas; de determinaron los valores medios, las desviaciones estándar y los coeficientes de variación de los 3 métodos.
De igual manera para el ensayo de la precisión intermedia se emplearon 2 analistas en 2 días diferentes. Se aplicaron las pruebas de Fisher y t de Student para determinar si existían diferencias significativas al variar las condiciones de análisis.
Especificidad
Para el estudio de especificidad se analizaron: las sustancias de referencia de fluorouracilo, metrotexato y doxorrubicina; el placebo; las muestras de producto terminado.
Criterio de aceptación: El valor de absorbancia del blanco muestra debía ser menor del 1 % con respecto a los valores de absorbancia de las muestras y las sustancias de referencia química.
RESULTADOS
Los valores de absorbancia determinados en los estudios de especificidad de los métodos por espectrofotometría, realizado para cada uno de los productos objeto de estudio, con el empleo del blanco muestra se encontraron entre 0,001 y 0,003. Se demostró que los excipientes de las formulaciones no absorben a la longitud de onda del máximo de absorción de los principios activos.
En la tabla 2 se reportan los resultados de los estudios de la linealidad del sistema, para el fluorouracilo, doxorrubicina, metotrexato; los coeficientes de regresión lineal fueron de 0,9999; 0,9998 y 0,9999, respectivamente, y los coeficientes de variación del factor de respuesta resultaron iguales a 2,38; 4,89 y 2,84 %.
Los resultados de los estudios de precisión de los métodos desarrollados aparecen reportados en la tabla 3. En los estudios de repetibilidad realizados, para el fluorouracilo, doxorrubicina, metotrexato, las medias obtenidas resultaron de 101,96; 95,4 y 98,5 %, y los coeficientes de variación fueron de 0,31; 0,39 y 0,62 %, respectivamente, mientras que los valores de F calculadas y los valores de t calculadas fueron menores que los valores tabulados, para un 95 % de confianza, para cada uno de los niveles estudiados.
En la tabla 4, aparecen reportados los resultados de los estudios de exactitud, para el fluorouracilo, doxorrubicina, metotrexato. Las recuperaciones medias fueron de 99,08; 99,97 y 99,35 %, respectivamente, y los valores de t calculadas (1,987; 2,109 y 1,857) y de G calculada (0,798; 0,733 y 0,625) resultaron menores que los valores tabulados, para un 95 % de confianza, t tabulada 2,306 y G tabulada 0,871.
DISCUSIÓN
Los valores de los estudio de especificidad de los métodos espectrofotométricos demostraron que las sustancias auxiliares a las longitudes de onda correspondientes a los máximos de absorción de los principios activos no interfieren, ya que los valores de absorbancias de los blancos muestras corresponden al 1 % en relación con los valores de los principios activos en las muestras. No se evidenció interferencia de los excipientes utilizados en ninguna de las 3 formulaciones: fluorouracilo (hidróxido de sodio, agua para inyección), doxorrubicina (cloruro de sodio, ácido clorhídrico, agua para inyección), metotrexato (cloruro de sodio, hidróxido de sodio, agua para inyección); por tanto, son adecuados para el control de proceso del producto terminado, lo que permite la toma de decisiones antes de realizar el envasado del producto terminado. Estos métodos resultan de gran utilidad en el control de proceso ya que son rápidos, sencillos y baratos, y permiten el control de la calidad del producto en proceso, resultan confiables para estos fines ya que en el proceso de elaboración de los medicamentos objeto de estudio se demostró que no se afectan, ni degradan durante el proceso de fabricación. Solo se aplicarían estos métodos para el control de proceso, porque para el control de la calidad y el estudio de estabilidad se emplean los métodos cromatográficos reportados en el literatura.4,5
Los resultados del estudio de linealidad (tabla 2) probaron que los métodos cumplen con los parámetros establecidos; los coeficientes de correlación de las rectas de regresión son mayor que 0,999, para los 3 métodos, los factores respuestas son semejantes entre sí, similares al valor de la pendiente de la recta de regresión y el coeficiente de variación de estos menores que 5 %. Al aplicarse la prueba de proporcionalidad este resultó no significativo (SBrel < 2,0 %) y el intervalo de confianza del intercepto incluye el valor cero en cada método.4,5
Los ensayos de precisión (tabla 3) indicaron que no existían diferencias significativas entre las precisiones alcanzadas por ambos analistas, en días diferentes, ni en las medias obtenidas por ellos. Los valores que se obtienen en el estudio de precisión intermedia, de las pruebas de Fischer y t de Student, para el estudio de la precisión intermedia demuestran que no existen diferencias significativas entre las precisiones y las medias alcanzadas por los analistas en diferentes días para una probabilidad de 0,05.6
El estudio de la exactitud (tabla 4) demostró que los métodos cumplen con los requisitos establecidos para este estudio. Los valores de recuperación media se encuentran dentro de los límites establecidos (98-102 %), con coeficientes de variación adecuados. Los valores de t experimental fueron menores que el tabulado para un 95 % de confianza y g.l. 8, lo que señala que los métodos son exactos, con una certeza del 95 %, para la cuantificación de los principios activos y que no existieron desviaciones por exceso o por defecto. Tampoco el factor concentración influyó en la variabilidad de los resultados pues los valores de G exp fueron menores que el tabulado para una probabilidad de 0,05, k= 3 y n= 3.6
En conclusión, los métodos analíticos espectrofotométricos validados, por espectrofotometría, para los controles de procesos de los 3 inyectables fluorouracilo, doxorrubicina, metotrexato resultaron específicos, lineales, precisos y exactos en el intervalo de concentraciones establecido y pueden establecerse como método de control de proceso de los medicamentos.
REFERENCIAS BIBLIOGRÁFICAS
1. Martindale W. The extra Pharmacopoeia 28th ed. London: Pharmaceutical Press; 1989. p. 1224-6.
2. Reactivos Merck. Folleto de cromatografía en la Química clínica. HPLC. Alemania; 1988. p. 3-16.
3. Quattrocchi OA, Laba RF. Introducción a la HPLC en Aplicación y práctica. Buenos Aires: Ed. Artes Gráficas Farro; 1992. p. 106-22, 284, 302-28.
4. Asociación Española de Farmacéuticos de la Industria. Validación de Métodos Analíticos. Sección Catalana de AEFI. Comisión de normas de buena fabricación y control de la calidad. Barcelona: AEFI; 1989. p 1-94.
5. United States Pharmacopoeial Convention. USP XXX. United States Pharmacopoeia Convention. 30 ed. Rockville: Mack Printing; 2007. p. 2883-5. Versión electrónica en CD.
6. Guidance for Industry: Analytical Procedures and Methods Validation. FDA & Center for Drugs Evaluation and Research (CDER). 2000. Disponible en: http://www.fda.gov/cber/guidelines.htm
Recibido: 18 de septiembre de 2009.
Aprobado: 21 de octubre de 2009.
M. C. Caridad Margarita García Peña. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave 26, No. 1 605 entre Boyeros y Calzada de Puentes Grandes, CP 10 600, municipio Plaza de la Revolución, La Habana, Cuba. Correo electrónico: caridadgp@infomed.sld.cu