Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm v.45 n.1 Ciudad de la Habana ene.-mar. 2011
ARTÍCULOS ORIGINALES
Compatibilidad química por calorimetría diferencial de barrido y termogravimetría del auranofin tabletas 3 mg
Chemical compatibility of 3 mg Auranofin tablets demonstrated by differential scanning calorimetry and thermogravimetry
Luis Octavio Martínez ÁlvarezI; Marlene Montes PérezII
IMáster en Ciencias Químicas Farmacéuticas. Investigador Agregado. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
IILicenciada en Ciencias Farmacéuticas. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
RESUMEN
Como parte de la pre-estabilidad de la preformulación de auranofin tabletas, se realizó un estudio de compatibilidad química, para lo cual se emplearon técnicas de análisis térmico como la calorimetría diferencial de barrido y la termogravimetría. Previo a dichos estudios se caracterizó térmicamente por calorimetría diferencial de barrido el principio activo y cada uno de los excipientes. Posteriormente se procedió a la realización del estudio de compatibilidad química, mediante la preparación de mezclas físicas binarias entre el principio activo y cada uno de los excipientes. Se detectó por ambos métodos que el principio activo tuvo una transición física de fusión, no reportada en la literatura, lo que permitió poder calcular su pureza por calorimetría diferencial de barrido. Mediante la técnica calorimétrica fue posible inferir la ausencia de incompatibilidad química entre el principio activo y los excipientes estudiados. Además, mediante el cálculo de la energía de activación se estableció el siguiente orden de estabilidad térmica: auranofin:PVP> auranofin:lactosa> auranofin:explotab> auranofin:estearato> auranofin:aerosil> auranofin:celulosa, por lo que se recomienda el uso de estos excipientes en la elaboración de la formulación farmacéutica.
Palabras clave: Calorimetría diferencial de barrido, termogravimetría, auranofin.
ABSTRACT
As part of the pre-stability study of the Auranofin tablet pre-formulation, a chemical compatibility study was conducted using thermal analysis techniques such as the differential scanning calorimetry and the thermogravimetry. Prior to these studies, the active principle and each of the excipients were thermally characterized with the aid of the differential scanning calorimetry. Then, there proceeded to carry out the chemical compatibility study by preparing binary physical mixtures between the active principle and each of the excipients. Both methods showed that the active principle had a melting physical transition, not reported in the literature, which allowed calculating its purity aided by the differential scanning calorimetry. It was possible to infer from the calorimetry technique that there was not chemical incompatibility between the active principle and the studied excipients. By means of the activation energy estimation, the following order of thermal stability was set: Auranofin:PVP> Auranofin: lactose> Auranofin:explotab> Auranofin:estearate> Auranofin:aerosil> Auranofin:celullose. The use of these excipients was recommended for the preparation of the pharmaceutical formulation.
Key words: differential scanning calorimetry, thermogravimetry, Auranofin.
INTRODUCCIÓN
La artritis reumatoide es una enfermedad sistémica de tipo inflamatorio, de causa desconocida, que afecta primariamente las articulaciones. Sus manifestaciones son variadas y producen diversos grados de molestias y limitaciones, que si no se logra controlar provoca la destrucción progresiva de las articulaciones afectadas, con deformaciones asociadas.1
Los antiinflamatorios no esteroideos son de uso habitual en el tratamiento de la artritis reumatoide, ya sea como una ayuda sintomática mientras se realiza y confirma el diagnóstico, o durante el tratamiento de mantención como coadyuvantes en el manejo del dolor y la inflamación.1
Dentro de estos agentes se incluyen los compuestos antimaláricos, sulfalazina, penicilamina, metotrexate, azatioprin, ciclofosfamida, clorambucil y los compuestos áuricos, dentro de estos últimos se encuentra el auranofin, el cual fue descubierto hace más de 15 años y es usualmente empleado en pacientes con enfermedad rápidamente progresiva que no logran alivio satisfactorio con drogas similares a la aspirina.2-4
El presente trabajo tiene como objetivo la realización del estudio de compatibilidad química, como parte de los estudios de una formulación cubana de auranofin tabletas, con el empleo de la calorimetría diferencial de barrido (DSC) y la termogravimetría (TG).5,6
MÉTODOS
Las sustancias farmacéuticas empleadas en este estudio fueron las siguientes: Aurofin, principio activo, y los siguientes excipientes: polivinilpirrolidona (PVP), lactosa monohidrato, estearato de magnesio, aerosil, celulosa microcristalina y sodio almidón glicolato (Explotab).
En la caracterización térmica de cada una de las sustancias empleadas en la preformulación estudiadas, se empleó el sistema de análisis térmico Mettler TA 3000 con unidades acopladas de calorimetría, DSC20 y termogravimetría, TG50. Con el propósito de determinar con exactitud las temperaturas de transición en DSC, se calibró5,6 la temperatura del equipo con un estándar de Indium, programándose una velocidad de calentamiento de 5 °C/min., en un rango de temperatura entre 35 y 350 °C. El peso de la muestra osciló entre 5 y 10 mg, empleándose crisoles desechables de aluminio de 40 µL.
Para la corroboración de la temperatura de fusión del auranofin detectada por DSC, paralelamente se analizó un material de referencia química (MRQ), ya que este valor no aparece reportado en la literatura7,8
En la evaluación de la pureza por DSC del auranofin, las condiciones experimentales fueron las mismas que las que se emplearon en la identificación, excepto que se programó una velocidad de calentamiento de 2 °/min.5,6
Para el estudio de compatibilidad se empleó el mismo calorímetro, solo que la velocidad de calentamiento fue de 10 °/min y se prepararon 6 mezclas físicas binarias de principio activo con cada una de las sustancias preseleccionadas en una relación de concentración de 1:1 y al mismo tiempo se le determinó a cada mezcla la energía de activación (Ea).
RESULTADOS
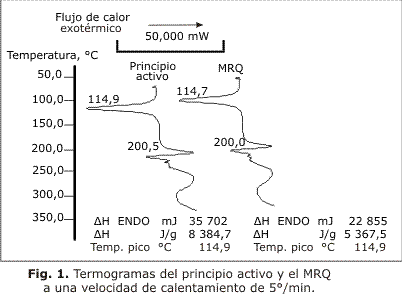
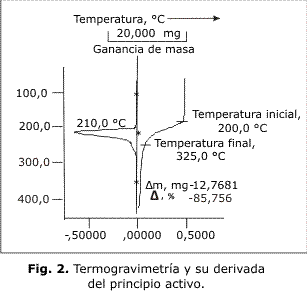
En la figura 1 se observan los termogramas obtenidos para el auranofin y el MRQ, detectándose para ambas sustancias una transición física endotérmica a una temperatura de 114,9 y 114,7 °C respectivamente. Mientras que en la figura 2 se muestran los resultados del análisis termogra-vimétrico, detectándose que en el rango entre 110 y 130 °C no hubo pérdida de masa.
Las distintas transiciones físicas detectadas para cada uno de los excipientes se presentan en la tabla 1, lo cual coincide tales transiciones con las reportadas.9
Por otro lado, en la tabla 2 se muestran los resultados obtenidos en la determinación de pureza por DSC, para un valor promedio de 99,4 % y una desviación estándar de 0,10.
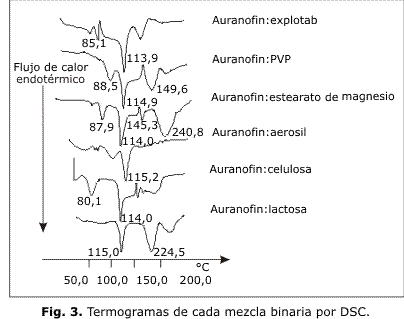
El estudio de compatibilidad química mostró la existencia de un pico endotérmico a 114,9 °C característico del principio activo en estudio; no se observó aparición de ninguna otra transición física o química (fig. 3).
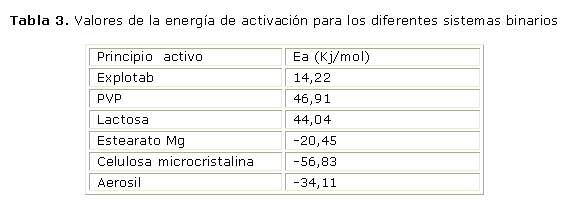
En la tabla 3 se presentan las distintas Ea obtenidas para cada mezcla binaria; se observa el siguiente orden de estabilidad térmica: auranofin:PVP> auranofin:lactosa> auranofin:explotab> auranofin: estearato> auranofin:aerosil> auranofin:celulosa.
DISCUSIÓN
La calorimetría, como método absoluto de determinación de pureza en sustancias sólidas con puntos de fusión definidos, permitió evaluar con toda certeza la pureza del principio activo mediante su fusión, la cual no se vio afectada por la ausencia de impurezas que no llevaron a la depresión de la temperatura de fusión detectada ni a la aparición de otras nuevas transiciones. La TG por su parte, aseveró que realmente la transición detectada por DSC si era una auténtica transición física de fusión.
En los estudios de compatibilidad química dicha transición se detectó en todas las corridas efectuadas para las distintas mezclas binarias. La no aparición de nuevas transiciones así como la no desaparición de la transición física de fusión del principio activo indujo a afirmar la no existencia de interacción química entre el auranofin con cada uno de los excipientes estudiados, por lo que el empleo de estas para la elaboración de la formulación de la tableta es ampliamente recomendado, sin obviar el orden establecido de para la estabilidad térmica.
REFERENCIAS BIBLIOGRÁFICAS
1. Ministerio de Salud. Guía Clínica Artritis Reumatoide. Santiago: MINSAL; 2007.
2. Anonymous. Drug for rheumatoid arthritis. Med Lett. Drugs Ther. 1991;3:65-70.
3. Furst DE. Rational use of disease-modifying antirheumatic drugs. Drugs. 1990;39:19-37.
4. Hart.LE, Tugwell P. The use of disease-modifying antirheumatic drugs in the management of rheumatoid arthritis. Postgrad Med J. 1989;65:905-12.
5 Ford JL, Timmis P. Pharmaceutical Thermal Analysis, Techniques and applications. New York: John Wiley Sons; 1988.
6 Venkataram S, Khohlokwane M, Wallis SH. Differential scanning calorimetry as a quick scanning technique for solid state stability studies. Drug Dev Industrial Pharm. 1995; 21(7):847-55.
7 Budavari S. The Merck Index. 11 ed. New York: Merck; 1989. p. 898.
8 Gennaro AR. Remington: The Science and Practice of Pharmacy, 19th ed. Easton: Mack Publishing; 1995.
9 American Pharmaceutical Association and Pharmaceutical Press. Handbook of Pharmaceutical Excipients. CD-ROM. Washington: Pharmaceutical Press; 2000.
Recibido: 5 de octubre de 2010.
Aprobado: 13 de noviembre de 2010.
MSc. Luis Octavio Martínez Álvarez. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 26 No. 1 605 entre Boyeros y Puentes Grandes. CP 10 600. Plaza de la Revolución, La Habana, Cuba.