My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Farmacia
Print version ISSN 0034-7515
Rev Cubana Farm vol.45 no.3 Ciudad de la Habana July-Sept. 2011
Determinación cuantitativa por electroforesis capilar de zona de mangiferina en tabletas VIMANG® 300 mg
Quantitative determination through capillary zone electrophoresis of mangiferin in 300 mg VIMANG® tablets
Harold Curiel HernándezI, Hermán Vélez CastroII, Janet Lora GarcíaIII
I Maestro en Química. Instructor. Investigador Agregado. Centro de Química Biomolecular. La Habana, Cuba.
II Doctor en Ciencias Químicas. Investigador Titular. Centro de Química Biomolecular. La Habana, Cuba.
III Maestra en Química Farmacéutica. Investigadora Agregada. Instructora. Centro de Química Biomolecular. La Habana, Cuba.
RESUMEN
La mangiferina se seleccionó como marcador en el control de calidad del ingrediente farmacéutico activo VIMANG® y sus formulaciones, que se han empleado como suplemento nutricional, cosmético y fitomedicamento. El trabajo tuvo como objetivo la validación del método electroforesis capilar para la determinación cuantitativa de mangiferina en la formulación farmacéutica tabletas VIMANG® 300 mg. Se evaluaron la especificidad, linealidad, exactitud y precisión. Los resultados obtenidos demostraron que el método fue específico, al no existir interferencias de los excipientes o sus productos de degradación. La linealidad mostró un coeficiente de correlación de 0,9979 en el intervalo de concentraciones estudiado. Los coeficientes de variación para la repetibilidad y la precisión intermedia fueron menores de 2 %. La exactitud mostró un recobrado del 100,20 % que no difiere significativamente de 100 %. En conclusión, el método validado es específico, lineal, preciso y exacto, y constituye una alternativa ventajosa al método cromatografía líquida de alta resolución establecido con anterioridad en el laboratorio.
Palabras clave: mangiferina, VIMANG®, electroforesis capilar, detección ultravioleta, electroforesis capilar de zona.
ABSTRACT
Mangiferin was selected as marker in the quality control of active principle VIMANG® and its formulations, which have been used as nutritional supplement, cosmetic, and phytomedication. This paper was aimed at validating the capillary electrophoresis method for the quantitative analysis of mangiferin in the pharmaceutical formulation 300 mg VIMANG® tablets. The specificity, linearity, accuracy and precision were assessed. The results showed the method specificity owing to lack of interference by the excipients or their degradation products. Linearity showed a correlation coefficient of 0.9979 in the studied concentration range. The variation coefficients for repeatability and intermediate precision were less than 2 %. Accuracy reached a recovery rate of 100.20 % that is not statistically different from 100 %. It may be concluded that the validated method is specific, linear, precise and accurate and could be an advantageous alternative to the high resolution liquid chromatography method used at the lab setting.
Key words: mangiferin, VIMANG®, capillary electrophoresis, UV detection, control zone electrophoresis.
INTRODUCCIÓN
El ingrediente farmacéutico activo (IFA) VIMANG® es un polvo que se obtiene a partir de la decocción acuosa de la corteza del árbol de mango (Mangifera indica L.). Este producto natural ha sido desarrollado en Cuba a escala industrial para emplearse como suplemento nutricional, cosmético y fitomedicamento. Estudios químicos realizados han permitido el aislamiento e identificación de ácidos fenólicos (ácido gálico, ácido 3,4-dihidroxibenzóico, ácido benzoico), ésteres fenólicos (éster metílico del ácido gálico, éster propílico del ácido gálico, éster propílico del ácido benzoico), flavon-3-oles (catequina y epicatequina) y la xantona mangiferina, que constituye el componente mayoritario de la fracción polifenólica de este extracto (aproximadamente 10 %). El IFA VIMANG® también contiene ácidos grasos como el mirístico, el palmítico, el esteárico y el eicosatrienóico.1
Se ha reportado el efecto analgésico y antiinflamatorio del IFA VIMANG® 2 y un amplio rango de actividades farmacológicas incluyendo las acciones antioxidante,3 antitumoral y antiviral,4 especialmente para la mangiferina. Por su mayor concentración, la mangiferina se seleccionó como el marcador en el control de calidad del IFA VIMANG® y sus formulaciones.
Entre los métodos empleados para el análisis de mangiferina se encuentran la cromatografía líquida de alta resolución (CLAR),5,6 la cromatografía de capa delgada (CCD)7 y, más recientemente, la electroforesis capilar (EC).8-10 El desarrollo y mejora en los últimos años de la EC la hacen un método atractivo para el estudio de productos naturales, debido a su elevada eficiencia de separación, corto tiempo de análisis, bajo consumo de muestra y disolventes, bajo costo, fácil limpieza y regeneración de las columnas capilares.
Un método por EC con detección electroquímica y electrolito de separación borax (50 mmol/L y pH 9,2) se aplicó para detectar la presencia de mangiferina y otras sustancias activas en crudos de 2 plantas.8 En este método se utilizó la inyección electrocinética aplicando 14 kV durante 10 s para la introducción de la muestra en el capilar.8 Otro método por EC se empleó para el análisis de mangiferina extraída de las hojas de Mangifera persiciformis C.Y. Wu et T.L. Ming.9 En él, la separación se llevó a cabo usando un voltaje de 20 kV y detección UV a 254 nm y como electrolito de separación se utilizó una mezcla de borato (50 mmol/L y pH 7,4) y metanol [1:0,3 (v/v)].9 La introducción de la muestra en el capilar se logró aplicando presión durante 6 segundos.9 Las condiciones de análisis descritas anteriormente (detección electroquímica e inyección electrocinética8 y pH 7,4 y metanol en el electrolito de separación9) fallaron en la separación desde la línea base del pico correspondiente a la mangiferina en el IFA VIMANG®. En tal sentido, se desarrolló y validó un método simple y rápido por EC para la determinación cuantitativa de mangiferina en lotes de IFA VIMANG® y para la determinación de pureza de lotes de mangiferina (material de referencia químico, MRQ) obtenidos en el laboratorio, empleando detección UV, electrolito de separación borato a pH 9 sin el empleo adicional de disolvente orgánico y la inyección por presión.10 Tomando como punto de partida este último, el presente trabajo tuvo como objetivo la validación del método EC para la determinación cuantitativa de mangiferina en la formulación farmacéutica tabletas VIMANG® 300 mg.
MÉTODOS
Todos los reactivos empleados fueron de calidad puro para análisis. Las disoluciones se prepararon con agua ultrapura Milli-Q (Millipore, Milford, MA, EE. UU.). La mangiferina (MRQ) con pureza del 93,92 % se obtuvo en el Centro de Química Farmacéutica (La Habana, Cuba), el IFA VIMANG® en el Laboratorio Farmacéutico "Mario Muñoz" (La Habana, Cuba) y las tabletas VIMANG® 300 mg y su placebo en los Laboratorios Oriente (Santiago de Cuba, Cuba).
Las determinaciones se realizaron en un sistema de electroforesis capilar Agilent 3D-CE (Agilent Technologies, EE. UU.) equipado con un detector de arreglo de diodos y el programa HP 3D Chemstation (Rev. A. 09.01) para el control del instrumento, la adquisición y el análisis de datos. Se empleó un capilar de sílice fundida sin relleno de 56,0 cm (47,5 cm de longitud efectiva) y 50 ìm de d.i., termostatado a 25 °C. Las corridas electroforéticas se realizaron en tetraborato de di-sodio 50 mmol/L y pH 9 como electrolito de separación con polaridad normal a 25 kV (generándose una corriente cercana a los 60 µA) y detección directa UV a 254 nm. Las muestras se inyectaron por presión a 50 mbar (equivalente a 5 000 Pa) durante 3 s (aproximadamente 3,3 nL) en el extremo anódico del capilar. La corrida se completa a los 9 min.
Preparación de las muestras y la sustancia de referencia
Las muestras de IFA VIMANG® y mangiferina MRQ se prepararon del mismo modo que en la validación del método de determinación del IFA VIMANG®.10 Para las tabletas VIMANG® se pesaron 10 tabletas, se trituraron y mezclaron. De dicha mezcla se pesó el equivalente a 1 tableta, se adicionaron 50 mL de metanol al 85 % y se agitó durante 20 min. La disolución resultante se filtró a través de un filtro de 0,2 mm. En el caso del placebo se repitió el procedimiento anterior pero adicionando a la muestra 10 mg de mangiferina MRQ.
Los parámetros evaluados durante la validación del método desarrollado fueron selectividad, precisión (repetibilidad y precisión intermedia), exactitud y linealidad siguiendo los procedimientos reportados.11,12
Especificidad
Los posibles productos de degradación de la mangiferina y el resto de los componentes del IFA VIMANG®, no interfieren en la determinación de mangiferina en el IFA VIMANG®.10 Por lo anterior, en este trabajo se determinó si existían interferencias de los excipientes de la formulación o de sus productos de degradación. Para ello, en el estudio de especificidad se analizaron: la sustancia de referencia de mangiferina, el IFA VIMANG®, el placebo y el producto terminado. También se analizó el placebo sometido a condiciones drásticas de degradación ácida y básica. Debe cumplirse que no se observen interferencias de los excipientes de la formulación en la zona de migración del marcador mangiferina, para que el método se considere específico.
Linealidad
Para evaluar la linealidad se realizó el modelo de 2 determinaciones para 6 concentraciones diferentes (0,05; 0,15; 0,20; 0,25; 0,35 y 0,50 mg/mL) de mangiferina sustancia de referencia, lo que representa un rango de análisis del 25 al 250 % de la concentración teórica de análisis igual al 100 % de analito (0,20 mg/mL). Se calcularon los parámetros asociados a la ecuación de la recta y= bx + a: el coeficiente de correlación (r), el coeficiente de determinación (r2), la probabilidad (p) asociada al valor de F del modelo, la probabilidad (p) asociada a la prueba de la t de Student del intercepto y el coeficiente de variación de los factores de respuesta.
Precisión
La precisión del método se evaluó mediante el estudio de la repetibilidad y la precisión intermedia. La repetibilidad se estudió sobre la base de 6 determinaciones independientes de placebo cargado con mangiferina sustancia de referencia a la concentración equivalente al 100 %. Se determinaron los valores medios, la desviación estándar y el coeficiente de variación de la respuesta para n= 6. El estudio de precisión intermedia se realizó repitiendo este procedimiento por otro analista en días diferentes. Se tomaron los datos experimentales de ambos analistas y se determinó el coeficiente de variación global (n= 12).
Exactitud
Como el objetivo del método es la valoración de un compuesto mayoritario en una formulación de producto terminado, se empleó el procedimiento de aplicar el método EC a 6 muestras independientes de placebo cargado con una cantidad conocida de mangiferina sustancia de referencia. Se determinó el por ciento de recobrado, el intervalo de confianza para el recobrado y la prueba de la t de Student para determinar diferencias significativas entre la recuperación media y el 100 %.
RESULTADOS
Durante el estudio de especificidad se compararon los perfiles de separación de la mangiferina, el IFA VIMANG®, el placebo y la tableta VIMANG® 300 mg (Fig. 1). Como se observa en el electroferograma correspondiente a la muestra placebo no se obtiene ninguna señal en la zona de interés, alrededor de los 7 min, al ser comparado con los electroferogramas obtenidos para la sustancia de referencia, el IFA y la tableta. Por otra parte, la figura 2 muestra la comparación del perfil de separación de la sustancia de referencia con los perfiles de separación del placebo sometido a condiciones drásticas de degradación ácida y básica; puede observarse que en las muestras de placebo degradado aparecen picos adicionales, pero alejados de la zona de interés.
En el estudio de linealidad se obtuvo la ecuación de regresión de la recta expresada según: y= 371,7 x - 4,5. El coeficiente de correlación fue r= 0,9979 y el coeficiente de determinación fue r2= 99,58 %. La probabilidad (p= 0,0000) asociada al valor de F del modelo fue mucho menor que 0,05, por lo que el valor de la pendiente "b" fue significativamente diferente de cero. La probabilidad (p= 0,0689) asociada a la prueba de la t de Student del intercepto es mayor que 0,05 por lo que se acepta que el intercepto (- 4,5) no difiere de cero. El coeficiente de variación de los factores de respuesta fue de 4,51 %.
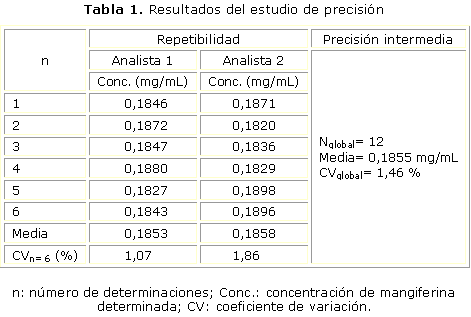
Los resultados del estudio de precisión (repetibilidad y precisión intermedia) del método propuesto se muestran en la tabla 1. En el estudio de repetibilidad, los valores de coeficiente de variación obtenidos (n= 6) fueron 1,07 % para el analista 1 y 1,86 % para el analista 2. En el caso de la precisión intermedia, el coeficiente de variación global (n= 12) fue de 1,46 %.
Los resultados del estudio de exactitud (tabla 2) muestran que la media (n= 6) de por ciento de recobrado fue de 100,20 %, el intervalo de confianza fue de 98,60 a 101,81 % y la t experimental fue de 0,328.
DISCUSIÓN
Los resultados obtenidos en el estudio de especificidad (figs. 1 y 2) demuestran que los excipientes de la formulación de tabletas VIMANG® o sus productos de degradación no interfieren en la determinación del marcador mangiferina en tabletas VIMANG® 300 mg.
En el estudio de linealidad se encontró que los coeficientes de correlación y determinación fueron superiores a los exigidos, 0,99 y 0,98 respectivamente.11,12 El valor obtenido del coeficiente de variación de los factores de respuesta fue inferior a lo exigido (5 %) y el intercepto no difiere significativamente de cero.11,12 De esta manera se demuestra la linealidad del método.
Los resultados obtenidos en el estudio de precisión mostraron valores de coeficiente de variación para la repetibilidad y la precisión intermedia inferiores a 2,0 % que es la variabilidad permitida para métodos cromatográficos.11,12 Por lo anterior, se demuestra que el método es preciso.
Los resultados obtenidos en el estudio de exactitud muestran que el por ciento de recobrado medio obtenido (100,20 % para n= 6) no difiere del 100 % ya que su intervalo de confianza incluye el 100 % y en la prueba de significación se obtuvo una t experimental menor que la t tabulada. Estos resultados demuestran la capacidad del método de brindar resultados cercanos al valor verdadero por lo que se considera que es exacto.11,12
En conclusión, el método analítico de electroforesis capilar de zona desarrollado para la cuantificación de la mangiferina en la tableta VIMANG® 300 mg, es específico, lineal, preciso y exacto. Este método constituye una alternativa ventajosa al método CLAR establecido con anterioridad en el laboratorio, teniendo en cuenta el bajo consumo de disolventes, alta eficiencia de separación, disminución del tiempo de análisis y fácil lavado de las columnas capilares.
AGRADECIMIENTOS
Los autores desean agradecer el financiamiento otorgado por el Ministerio de Ciencia, Tecnología y Medio Ambiente de Cuba y al VLIR (Vlaamse Interuniversitaire Raad, Consejo Interuniversitario Flamenco) de Bélgica por la donación del equipo de electroforesis capilar.
REFERENCIAS BIBLIOGRÁFICAS
1. Núñez AJ, Vélez HT, Agüero J, González J, Naddeo F, De Simone F, et al. Isolation and quantitative analysis of phenolic antioxidants, free sugars, and polyols from mango (Mangifera indica L.) stem bark aqueous decoction used in Cuba as a nutritional supplement. J Agric Food Chem. 2002;50(4):762-6.
2. Garrido G, González D, Delporte C, Backhouse N, Quintero G, Núñez AJ, et al. Analgesic and anti-inflammatory effects of Mangifera indica L. extract (Vimang). Phytother Res 2001;15(1):18-21.
3. Sato T, Kawamoto A, Tamura A, Tatsumi Y, Fujii T. Mechanism of antioxidant action of pueraria glycoside (PG)-1 (an isoflavonoid) and mangiferin (a xanthonoid). Chem Pharm Bull (Tokyo). 1992;40(3):721-4.
4. Guha S, Ghosal S, Chattopadhyay U. Antitumor, immunomodulatory and anti-HIV effect of mangiferin, a naturally occurring glucosylxanthone. Chemotherapy. 1996;42(6):443-51.
5. Dai R, Gao J, Bi K. High-performance liquid chromatographic method for the determination and pharmacokinetic study of mangiferin in plasma of rats having taken the traditional Chinese medicinal preparation Zi-Shen pill. J Chromatogr Sci. 2004;42(2):88-90.
6. Dai R, Li K, Li Q, Bi K. Determination of mangiferin, jateorrhizine, palmatine, berberine, cinnamic acid, and cinnamaldehyde in the traditional Chinese medicinal preparation Zi-Shen pill by high-performance liquid chromatography. J Chromatogr Sci. 2004;42(4):207-10.
7. Nedialkov P, Kitanov G, Tencheva J. HPTLC densitomeric determination of justicidin B in Linum in vitro cultures. Acta Pharm. 1998;48:211-4.
8. Cao Y, Wang Y, Ye J. Differentiation of Swertia Mussotii Franch from Artemisiae Capillaris Herba by capillary electrophoresis with electrochemical detection. J Pharm Biomed Anal. 2005;39:60-5.
9. Nong C, He W, Fleming D, Pan L, Huang H. Capillary electrophoresis analysis of mangiferin extracted from Mangifera indica L. bark and Mangifera persiciformis C.Y. Wu et T.L. Ming leaves. J Chromatogr B. 2005;826:226-31.
10. Curiel H, Sordo L, Vélez H. Determinación cuantitativa por electroforesis capilar de zona de mangiferina en ingrediente farmacéutico activo VIMANG®. Revista CENIC Ciencias Químicas. 2007;38(2):337-43.
11. United States Pharmacopoeial Convention. USP XXX. United States Pharmacopoeia Convention. Validation of compendial methods. 30 ed. Rockville: Mack Printing; 2007.
12. Regulación No. 41. Validación de métodos analíticos. La Habana: CECMED; 2007.
Recibido: 28 de febrero de 2011.
Aprobado: 15 de abril de 2011.
MSc. Harold Curiel Hernández. Centro de Química Biomolecular. Calle 200 y Avenida 21, Atabey, Playa, Apartado Postal 16042, La Habana, Cuba. Correo electrónico: harold.curiel@cqb.cu