Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Farmacia
versión On-line ISSN 1561-2988
Rev Cubana Farm vol.48 no.4 Ciudad de la Habana oct.-dic. 2014
ARTÍCULO ORIGINAL
Utilización de sulfato de cobre para la elaboración de un jabón líquido antiséptico
Use of cooper sulphate for production of antiseptic liquid soap
Lic. Priscila Sandoval Rodríguez,I MSc. Sandra Gajardo Solari,II DrC. Julio Benites Vílchez,II Dr. José López VivarII
I Facultad de Ciencias de la Salud, Universidad Arturo Prat. Iquique, Chile.
II Facultad de Ciencias de la Salud, Universidad Arturo Prat. Instituto de Etnofarmacología, Universidad Arturo Prat. Iquique, Chile.
RESUMEN
Introducción: las manos poseen un papel importante en la transmisión de infecciones en instituciones de salud, entornos industriales como la industria alimentaria y en toda la comunidad, por lo que su higiene no puede pasar desapercibida. Los jabones líquidos son actualmente una herramienta fundamental para la limpieza de las manos y así también evitar la transmisión de agentes patógenos.
Objetivo: evaluar la efectividad del sulfato de cobre como agente antiséptico en un jabón líquido y caracterizar el producto mediante controles de calidad.
Métodos: se evaluó la capacidad antiséptica del jabón líquido mediante el método de dilución en agar y la disminución del crecimiento bacteriano a través de una variación del recuento por microgota, a tiempos 1, 5 y 10 min. Posteriormente se realizaron controles fisicoquímicos, microbiológicos, prueba de parche y estudios de estabilidad en estantería y acelerada durante 6 meses.
Resultados: las cepas Staphylococcus aureus, Staphyloccus epidermidis, Escherichia coli, Pseudomona aeruginosa y Klebsiella pneumoniae fueron sensibles a una concentración de 0,5 % de sulfato de cobre. El crecimiento bacteriano en las cepas S. aureus y S. epidermidis mostró una reducción considerable en los tiempos 5 y 10 min a concentraciones de 0,3 y 0,5 % de sulfato de cobre. El producto elaborado cumplió con los criterios de calidad establecidos, el cual mantuvo su estabilidad durante el tiempo de estudio.
Conclusiones: es posible elaborar un jabón líquido en base a sulfato de cobre como agente antiséptico, al ser eficaz frente a las cepas estudiadas.
Palabras clave: jabón, antiséptico, sulfato de cobre, control de calidad.
ABSTRACT
Introduction: the hands play a significant role in the transmission of infections at health institutions, industrial environments such as the food industry and at the community; therefore, hand hygiene cannot be ignored. Liquid soaps are now a fundamental tool for hand cleaning and prevention of pathogen transmission.
Objective: to evaluate the effectiveness of copper sulfate as an antiseptic agent in a liquid soap and to characterize the product by using quality controls.
Methods: aliquid soap was developed, in which its antiseptic capacity was evaluated through the agar dilution method and the reduction of bacterial growth by using a variant of microdrop counting at 1, 5 and 10 minutes. Then physicochemical and microbiological controls were performed, as well as patch test and shelf life and accelerated stability studies for six months.
Results: Staphylococcus aureus, Staphyloccus epidermidis, Escherichia coli, Pseudomona aeruginosa and Klebsiella pneumoniae were susceptible to 0.5 % copper sulfate concentration. Bacterial growth showed considerable reduction in S. aureus and S. epidermidis strains at 5 and 10 minutes at copper sulphate concentrations of 0.3 and 0.5 %. The finished product met the quality criteria for this type of product, maintaining its stability during the study period.
Conclusions: it is possible to produce a copper sulfate-based liquid soap as an antiseptic since it was effective to control the studied strains
Keywords: soap, antiseptic, copper sulfate, quality control.
INTRODUCCIÓN
La piel es colonizada normalmente por un gran número de organismos que viven inofensivamente sobre la superficie cutánea, los cuales están distribuidos en microcolonias de diferentes tamaños. Representa una barrera notablemente eficaz contra las infecciones microbianas, sin embargo, cuando se produce una disrupción de su superficie, sea accidental o intencionalmente, el lecho de la herida o lesión puede verse invadida por bacterias autóctonas de la piel o no habituales en ella, comenzando así un proceso que puede derivar en una infección clínicamente establecida.1
La creciente preocupación por la posibilidad de contaminación microbiana ha supuesto un incremento en el uso de biocidas (antisépticos y desinfectantes), los cuales son agentes químicos, usualmente de amplio espectro, que inactivan a los microorganismos. Estos y otros agentes antimicrobianos se han utilizado en diversas formas durante siglos, ya que constituyen una herramienta esencial para controlar la diseminación de agentes infecciosos.2,3
Muchos minerales se han utilizado desde la antigüedad, con conocidos efectos sobre la salud, entre ellos se encuentra el cobre, que actualmente ha recobrado su atención en un campo distinto, que no es la minería, sino la salud.4 Los productos químicos de cobre han sido históricamente utilizados como bactericidas, alguicidas y fungicidas. Estudios recientes indican que bacterias, incluyendo algunas cepas nocivas de Escherichia coli y Staphylococcus aureus meticilin-resistente, mueren en pocas horas cuando se colocan sobre superficies de aleaciones de cobre a temperatura ambiente.5 Esta habilidad natural para reducir la carga biológica de los microorganismos del medio ambiente se explota en la purificación del agua, pintura, material de construcción y la industria textil.6 Los compuestos de cobre, como sulfato de cobre e hidróxido de cobre, son materiales inorgánicos tradicionales que tienen un amplio uso como antibacterianos.7
Entre las formulaciones que otorgan limpieza, se destaca el jabón líquido, herramienta fundamental para mantener una limpieza higiénica de las manos y así también evitar la transmisión de agentes patógenos. Las manos juegan un papel importante en la transmisión de infecciones en instituciones de salud, en entornos industriales como la industria alimentaria, en toda la comunidad y en el ámbito familiar. Es por esto que la importancia de la higiene de las manos en el control de las infecciones no puede pasar desapercibida.8
La finalidad del presente trabajo es evaluar un producto cosmecéutico con propiedades antisépticas, en base a sulfato de cobre, puesto que se ha documentado que tiene actividad antimicrobiana sobre algunas cepas bacterianas.9,10 Para la confirmación de dicha hipótesis se efectuarán ensayos para analizar la capacidad antiséptica de esta formulación.
MÉTODOS
Se ensayaron distintas formulaciones con diferentes concentraciones de sulfato de cobre (0,1; 0,3 y 0,5 %), las cuales fueron escogidas por encontrarse dentro del rango en que esta materia prima se utiliza por vía tópica, para así obtener un jabón líquido estable y que fuese agradable por sus características organolépticas.
PREPARACIÓN DE JABÓN LÍQUIDO
Se pesó en un vaso precipitado cloruro de sodio y sulfato de cobre pentahidratado, estos se disolvieron en agua destilada y luego se incorporó glicerina. En otro vaso precipitado se pesó lauril éter sulfato de sodio (LESS). Se vertió la mezcla acuosa al LESS y se agitó cuidadosamente para evitar la formación de espuma.
DETERMINACIÓN DE LA CAPACIDAD ANTISÉPTICA
Las cepas de las bacterias Staphylococcus aureus, Staphyloccus epidermidis, Escherichia coli, Pseudomona aeruginosa y Klebsiella pneumoniae, fueron cultivadas en 5 tubos, en caldo soya tripticasa. Se incubaron a 37 ºC por 24 h.
Dilución en agar: se utilizaron 20 placas Petri, en las cuales se agregó agar Müeller-Hinton enriquecido con distintas concentraciones de sulfato de cobre (0,1; 0,3 y 0,5 %) más un control sin sulfato de cobre. Cada cepa bacteriana se sembró en 4 placas, las que se incubaron en estufa por 24 h a 37 ºC. Posteriormente, se evaluó el crecimiento bacteriano, verificando si había o no presencia de bacterias.
Variación del método de recuento bacteriano a través de microgota: por cada concentración de sulfato de cobre se prepararon 50 mL de caldo soya tripticasa, volumen que se dividió en tubos separados que contenían 5 mL cada uno, y se dividieron en tres tiempos (1, 5 y 10 min). Esta secuencia se repitió para cada una de las 5 cepas bacterianas. Todos estos tubos se esterilizaron a 121 ºC, por 15 min. Posteriormente, fueron inoculados con una cepa bacteriana, tomándose de estos una alícuota de 20 μL a los distintos tiempos (1, 5 y 10 min); este volumen se depositó en placas Petri con agar soya tripticasa. Las placas obtenidas se incubaron en estufa a 37 ºC por 24 h, y se evaluó la disminución del crecimiento bacteriano. Todo este procedimiento se realizó por triplicado.
CONTROLES DE CALIDAD11-13
Los controles de calidad y estudios de estabilidad, se realizaron teniendo en cuenta el cumplimiento de los requerimientos establecidos en el Reglamento del Sistema Nacional de Control de Cosméticos D.S. 239/02 de Chile, país en que fue realizado el estudio, por lo que las condiciones de almacenamiento corresponden a una zona climática II.
Evaluación de características organolépticas: se llevó a cabo una evaluación de color, aspecto, olor y sensación al tacto, mediante la utilización de los órganos sensoriales.
Centrifugación: se realizó 24 h después de haber elaborado el jabón, en una centrífuga a 3 000 r.p.m. y 25 ºC, durante 30 min.
Medición de pH: se realizó a temperatura ambiente, introduciendo directamente los electrodos de un pH-metro portátil, marca WTN, modelo pH 330i, en la formulación.
Control microbiológico: se sembraron muestras de jabón líquido a distintas concentraciones de sulfato de cobre (0,1; 0,3 y 0,5 %), en agar Müeller-Hinton y se llevaron a estufa de cultivo a 37 °C, evaluando el crecimiento microbiano a las 24, 48 y 72 h posincubación.
Prueba de parche: se realizó a 30 voluntarios, previa firma del consentimiento informado. Se aplicó 2 muestras de 20 μL; la primera de jabón líquido y la segunda correspondiente a un control con la base de la formulación (sin sulfato de cobre). Se aplicó en la cara interna del brazo, se cubrió con una gasa estéril, y luego se fijó con un parche. Luego de 48 h se retiró el parche y se observó la reacción producida en la piel.
ESTUDIOS DE ESTABILIDAD14
Estrés térmico: las muestras se sometieron a temperaturas de 4 ºC y 40 ºC, alternando cada 24 h entre un ciclo y otro, por un período de 12 días. Este estudio de estabilidad preliminar, se realizó con el fin de auxiliar en la elección de la formulación.
Estabilidad en estantería: las muestras se mantuvieron a 25 ºC por un período de 12 meses.
Estabilidad acelerada: las muestras se mantuvieron a 40 ºC, durante 6 meses.
RESULTADOS
Luego de ensayar distintas formulaciones, se optó por la fórmula porcentual de jabón líquido que se observa en la tabla 1, debido a que presentó mejores características de calidad.
DETERMINACIÓN DE LA ACTIVIDAD ANTISÉPTICA
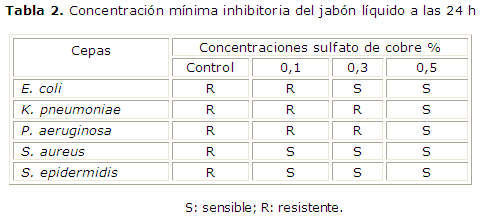
Dilución en agar: se realizó con tres concentraciones crecientes de sulfato de cobre (0,1; 0,3 y 0,5 %) puesto que a estas cantidades se utiliza terapéuticamente a nivel tópico en productos cosmecéuticos.15 Se evaluó el crecimiento a través de un control sin sulfato de cobre, el cual fue positivo para cada cepa, y se marcó como resistente, así como también en las concentraciones de sulfato de cobre que no fueron suficientes para inhibir el crecimiento bacteriano. Los resultados obtenidos a las 24 h, para las 5 cepas en estudio, se expresan en la tabla 2.
VARIACIÓN DEL MÉTODO DE RECUENTO EN PLACA A TRAVÉS DE MICROGOTA16
Las cepas bacterianas afectadas al tiempo de exposición en estudio fueron S. aureus y S. epidermidis, las cuales presentaron una disminución notoria del crecimiento bacteriano. Las bacterias gramnegativas E. coli, K. pneumoniae y P. aeruginosa no presentaron disminución del crecimiento bacteriano expuestas a este rango de tiempo. Los resultados se muestran en la tabla 3.
CONTROLES DE CALIDAD
Evaluación de características organolépticas: el jabón presentó un color azul claro, aspecto homogéneo y viscoso, olor característico, textura suave.
Centrifugación: las muestras no presentaron ningún tipo de inestabilidad o separación de componentes.
Medición de pH: el pH de la formulación fue de 6, manteniéndose este valor estable a diferentes temperaturas así como también a través del tiempo.
Control microbiológico: no se evidenció crecimiento bacteriano en el producto en estudio luego de 24, 48 y 96 h posincubación.
Prueba de parche: la formulación no produjo irritación en ninguno de los voluntarios.
ESTUDIOS DE ESTABILIDAD
Los resultados obtenidos demuestran que el producto elaborado, conserva sus características organolépticas, estabilidad fisicoquímica y microbiológica durante el tiempo de estudio, al ser almacenado a temperatura ambiente, elevada y ser sometido a ciclos de congelamiento-descongelamiento. En la figura se observan los resultados de la medición de pH de la formulación almacenada a 25 °C y 40 °C, durante los primeros 6 meses.
DISCUSIÓN
El jabón líquido requiere de ciertas características para su funcionalidad. Estas son otorgadas por determinadas materias primas, entre ellas, el cloruro de sodio se utilizó como espesante a la concentración del 4 % ya que a esa concentración se obtiene un jabón líquido con una viscosidad adecuada para su manejo y posterior dispensación. El carácter de detergencia está a cargo de lauril éter sulfato de sodio, que fue el tensioactivo seleccionado, porque cumple con la mezcla de limpieza y humectación de la piel. Para su labor de detergencia se utiliza a una concentración cercana al 10 %. Para darle un mayor carácter humectante al producto, se incorporó glicerina. La importancia de esto radica en que tras reiteradas aplicaciones del jabón, se podría producir una resequedad del estrato córneo y de esta manera se tiende a evitar. Este producto no incluye preservantes ni colorantes debido a que la sustancia activa es el sulfato de cobre, que tiene propiedades antimicrobianas y antifúngicas,17,18 y además proporciona un color azul a la formulación.
Al realizar los estudios para determinar la capacidad antiséptica, se realizó una modificación del método de recuento en placa a través de microgota, ya que no se contaron las unidades formadoras de colonia (UFC), si no que se vio la disminución de forma cualitativa del crecimiento bacteriano, puesto que de esta forma se puede apreciar visualmente una disminución notable de las UFC.
La diferencia entre las cepas grampositivas, que se vieron afectadas notoriamente a la exposición al sulfato de cobre, en comparación a las gramnegativas, que no lo hicieron, puede deberse a la variación estructural que existe entre ellas, que es la existencia de peptidoglicano presente en las gramnegativas, lo que las hace más resistentes al ataque de un agente antiséptico.
Los resultados de los controles de calidad y estabilidad realizados, fueron óptimos para este tipo de producto, destacando el pH, que se mantuvo durante todo el tiempo de estudio en un valor que está dentro del pH fisiológico cutáneo, lo cual disminuye el grado de irritación que podría llegar a producirse con un uso continuo. En toda elaboración de productos farmacéuticos y cosméticos es necesario realizar controles microbiológicos, ya que por norma general, las formulaciones que presentan agua entre sus componentes están expuestas a contaminación. Es por esto que no se permite la proliferación de los patógenos S. aureus, E. coli, P. aeruginosa y Salmonella.11 El jabón elaborado, fue sometido a este análisis siendo sus resultados negativos para la presencia de los microorganismos mencionados. Esto se le atribuye a las propiedades del sulfato de cobre antes mencionadas.
La prueba de parche se enfoca en la posible irritación que podría causar un producto, debido a componentes irritantes o a una sinergia entre ellos en la formulación. Después de 48 h, se evaluó la posible irritación, ya que la reacción inmunológica de tipo IV o hipersensibilidad tardía, se presenta 24-48 h después del contacto con el antígeno. La formulación no presentó irritación en ninguno de los voluntarios; es por esto que se puede concluir que el producto elaborado es apto para ser utilizado en humanos sin un riesgo inminente de producir alguna lesión en la piel.
Se puede concluir que es posible la elaboración de un producto cosmecéutico, específicamente un jabón líquido, en base a sulfato de cobre como agente antiséptico, el cual demostró ser seguro y estable durante el periodo de estudio.
REFERENCIAS BIBLIOGRÁFICAS
1. Sánchez-Saldaña L, Sáenz-Anduaga E. Infecciones cutáneas bacterianas. Dermatol Peru. 2006;16:1-29.
2. Mcdonnell G, Russell D. Antiseptics and disinfectants: activity, action and resistance. Clin Microbiol Rev. 1999;12:147-79.
3. Department of Health and Human Services. Toxicological Profile for Copper. United Stated: Public Health Service, Agency for Toxic Substances and Disease Registry; 2004.
4. Russell AD. Introduction of biocides into clinical practice and the impact on antibiotic-resistant bacteria. J Appl Microbiol Symp Suppl. 2002;92:121-35.
5. Hostýnek JJ, Maibach HI. Copper and Copper Alloys. In: Hostýnek JJ, Maibach HI. Copper and skin. EE.UU.: Informa Healthcare USA Inc; 2006. p. 1-6.
6. Mehtar S, Wiid I, Todorov SD. The antimicrobial activity of copper and copper alloys against nosocomial pathogens and Mycobacterium tuberculosis isolated from healthcare facilities in the Western Cape: an in-vitro study. J Hosp Infect. 2008;68:45-51.
7. Zhoua Y, Xiab M, Yea Y, Hu C. Antimicrobial ability of Cu+2 montmorillonite. Appl Clay Sci. 2004;27:215-8.
8. Jumaa PA. Hand hygiene: simple and complex. Int J Infect Dis. 2005;9:3-14.
9. Noyce JO, Michels H, Keevil CW. Potencial use of copper surfaces to reduce survival of epidemic methicilin-resistant Staphilococcus aureus in the healthcare environment. J Hosp Infect. 2006;63:289-97.
10. Noyce JO, Michels H, Keevil CW. Use of Copper Cast Alloys to Control Escherichia coli O157 Cross-Contamination during Food Processing. Appl Environ Microbiol. 2006;72(6):4239-44.
11. Ministerio de Salud. Decreto Nº 239. Chile. Reglamento del Sistema Nacional de Control de Cosméticos. Sep 2002. Diario Oficial de la República de Chile, 20 de junio de 2003.
12. Agência Nacional de Vigilância Sanitária. Guia de controle de qualidade de produtos cosméticos. 2da ed. Brasilia: Anvisa; 2007. p. 26-37.
13. Ardusso L. Prueba del parche. Rev Enfoques. 2002;3(1):7-9.
14. Agencia Nacional de Vigilancia Sanitaria. Guía de estabilidad de productos cosméticos. Brasilia: Anvisa; 2005. p. 17-28.
15. Alía E. Formulario tópico dermatológico. España: Universidad Santiago de Compostela; 1988.
16. Da Silva R. Técnica de microgota para contagem de células bacterianas viáveis em uma suspensão. Brazil: Universidade Federal de Viçosa; 1996. p. 1-7.
17. Borkow G, Gabbay J. Putting copper into action: copper-impregnated products with potent biocidal activities. FASEB J. 2004;18:1728-30.
18. Casey AL, Adams D, Karpanen TJ, Lambert PA, Cookson BD, Nightingale P, et al. Role of copper in reducing hospital environment contamination. J Hosp Infect. 2010;74:72-7.
Recibido: 21 de julio de 2014.
Aprobado: 28 de agosto de 2014.
Julio Benites Vílchez. Instituto de Etnofarmacología, Universidad Arturo Prat. Av. Arturo Prat 2120. Iquique, Chile. Tel. 56-57-2526210. Correo electrónico: julio.benites@unap.cl