Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina
versión impresa ISSN 0034-7523
Rev cubana med vol.53 no.2 Ciudad de la Habana abr.-jun. 2014
TRABAJO ORIGINAL
Comparación de resultados entre el retrasplante y el trasplante renal primario en el Hospital "Hermanos Ameijeiras" de 1984 a 2012
Comparison of results between retransplantation and primary kidney transplantation on Hermanos Ameijeiras Hospital from 1984 to 2012
Dr.C. Gerardo Borroto Díaz
Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
RESUMEN
Introducción: el retrasplante constituye la mejor opción terapéutica para los enfermos que pierden un primer trasplante renal y vuelven a diálisis, existen disímiles criterios en cuanto a sus resultados al compararlos con los trasplantes renales primarios.
Objetivo: analizar el porcentaje de retrasplantes, revisar la supervivencia del injerto y del enfermo, el comportamiento de variables que pueden incidir en los resultados y compararlos con los de los enfermos que reciben un primer trasplante renal.
Métodos: se realizó un estudio analítico, descriptivo, retrospectivo, de los trasplante renales realizados en el Hospital "Hermanos Ameijeiras" desde 1984 hasta diciembre de 2012; quedaron excluidos, los terceros trasplante, dobles (2 riñones a un mismo receptor), combinados (páncreas-riñón e hígado-riñón) y aquellos en los que no fue posible obtener la información requerida para la investigación. Se compararon (entre los grupos retrasplantes y primeros trasplantes) variables de índole general: edad de los receptores y donantes, sexo del receptor, enfermedad que ocasionó la insuficiencia renal, porcentaje de reactividad ante un panel de linfocito (PRA), compatibilidades HLA, tipo de donante (vivo o cadáver), tiempos de isquemia, presencia y duración de necrosis tubular aguda (donante cadáver), rechazo y supervivencia del injerto y el paciente.
Resultados: los retrasplantes constituyeron el 5,4 % de la muestra. No existieron diferencias entre edades, sexo, PRA, compatibilidades ni tipo de donante entre los segundos y primeros injertos. Los enfermos que llegaron a la insuficiencia renal por riñones poliquísticos nunca han recibido en nuestro centro un segundo trasplante. Resultó significativamente estadístico el uso de terapia cuádruple secuencial como inmunosupresión de inducción en los retrasplantes (55,9 % vs. 9,7 % de los primarios). La frecuencia de rechazo fue ligeramente menor en los que reciben un segundo injerto, no así los tiempos de isquemia, la presencia y duración de la NTA y la supervivencia del injerto que fueron muy parecidas en ambos grupos.
Conclusiones: el retrasplante constituye una modalidad terapéutica eficaz para los enfermos que pierden un primer injerto y vuelven a los métodos de diálisis.
Palabras clave: retrasplante, trasplante renal primario, inmunosupresión de inducción, supervivencia del injerto y paciente, complicaciones.
ABSTRACT
Introduction: retransplant constitutes the best therapeutic choice for patients who lose a first renal transplant and return to dialysis, existing dissimilar criteria as to its results when ranking them with renal primary transplant.
Objective: to analyze the percentage of retransplantation, to revise graft and patient survival, to review the behavior of variables that can affect the results and to compare them with patients receiving a first renal transplant.
Methods: an analytic, descriptive, retrospective study was accomplished, including all renal transplant performed at the Hermanos Ameijeiras Hospital from 1984 to December of 2012. Third transplants, double transplants (two kidneys to the same receptor), combined transplants (pancreas-kidney and liver-kidney) and those where it was not possible to obtain the information required for this research were excluded. Variables of general nature were compared between retransplantation groups and first transplants, such as: age of recipient and donor, sex of the recipient, a disease that caused kidney failure, percentage of reactivity to a lymphocyte panel (PRA), HLA compatibility, donor type (living or dead), ischemia time, presence and duration of acute tubular necrosis (dead donor), rejection and graft and patient survival.
Results:rRetransplant constituted only 5.4 % of the sample (34 patients). There were no differences in age, sex, PRA, donor type or compatibilities between the second and first grafts. Patients who reached the renal failure due to polycystic kidneys have never had a second transplant in our institution. The use of sequential quadruple therapy as induction immunosuppression, retransplantation (55.9 % vs. 9.7 % of primary) was statistically significant. The rejection rate was slightly lower in those receiving a second graft, but it was different for ischemic times, the presence and duration of NTA and graft survival which were very similar in both groups.
Conclusiones: retransplant constitutes the best therapeutic choice for patients who lose a first renal transplant and return to dialysis methods.
Key words: retransplantation, primary renal transplant, induction immunosuppression, graft and patient survival, complications.
INTRODUCCIÓN
A pesar de los avances en el tratamiento inmunosupresor y en los cuidados de los enfermos trasplantados renales, a los 3 años del trasplante, 20-30 % de los receptores habrá perdido el injerto y la pérdida continuará a razón de 2-4 % anual. Estos enfermos son incluidos de nuevo en programas de diálisis y constituyen entre 4-10 % de los pacientes admitidos anualmente para tratamiento dialítico.1 De ellos, 40-60 %, según la literatura revisada, son incluidos en lista de espera para un segundo trasplante (retrasplante). Lo que origina un aumento del número de enfermos en espera de trasplante y plantea el dilema acerca de los derechos a trasplantarse en los programas basados en donantes cadáver.2 El retrasplante constituye la mejor forma de tratamiento de la insuficiencia renal crónica para aquellos que pierden un primer injerto y retornan a la diálisis, otorga mayor calidad de vida a los enfermos, disminuye los costes económicos y los resultados en cuanto a la supervivencia del injerto se acercan a los del primer trasplante a pesar de ser considerados pacientes de alto riesgo.3 También mejora la supervivencia del enfermo con respecto al que permanece en lista de espera.3
A pesar de estas ventajas terapéuticas del retrasplante, el porcentaje de enfermos que son sometidos a un segundo trasplante permanece estacionario, posiblemente por la aplicación de criterios más amplios en cuanto a la aceptación de candidatos a trasplantarse, la percepción de muchos grupos dedicados a esta actividad de menores resultados en el segundo trasplante, secundarios a una mayor frecuencia de rechazos por hipersensibilización de estos enfermos por el trasplante previo, así como una mayor incidencia de función retrasada del injerto por daño isquémico y otras complicaciones secundarias a la exposición previa a la inmunosupresión.4 Además, la elección de un receptor para un segundo trasplante plantea un dilema ético, pues se restan órganos a aquellos receptores que están esperando un primer trasplante contraviniendo el principio de igualdad de oportunidades.
El problema investigativo radica en dilucidar si con las condicionales que rodean nuestro accionar y partiendo de las aseveraciones en pro y en contra antes expuestas, el segundo trasplante renal constituye una opción terapéutica eficaz para aquellos enfermos que retornan a la diálisis después de perder el primer injerto.
Nuestra hipótesis es que con una adecuada valoración y estudio del receptor, disminuyendo el daño isquémico e individualizando el tratamiento de estos enfermos, sobre todo la inmunosupresión, se pueden lograr resultados satisfactorios.
El objetivo del presente trabajo es analizar el porcentaje de retrasplantes en nuestro grupo, revisar lo logrado en cuanto a supervivencia del injerto y del enfermo así como el comportamiento de variables que envuelven el desarrollo de esta actividad y pueden influenciar los resultados obtenidos, comparándolos con aquellos enfermos que reciben un primer trasplante renal.
MÉTODOS
Diseño del estudio
Se realizó un estudio analítico, descriptivo, retrospectivo de todos los trasplante renales realizados en el Hospital "Hermanos Ameijeiras" desde 1984 hasta diciembre del 2012, quedaron excluidos, los terceros trasplante, dobles (2 riñones a un mismo receptor), combinados (páncreas-riñón e hígado-riñón) y aquellos en los que no fue posible obtener toda la información para la investigación.
La información se obtuvo de la base de datos de trasplante del Servicio de Nefrología del hospital donde fueron tomadas y categorizadas las variables siguientes:
- Edad del receptor: años, dado en valor de media y desviación estándar.
- Edad del donante: años, dado en valor de media y desviación estándar.
- Sexo del receptor.
- Tipo de trasplante renal: primer trasplante renal (trasplante renal primario) o segundo trasplante renal (retrasplante).
- Tipo de donante: vivo o cadáver.
- Enfermedad de base del receptor: diabetes mellitus, hipertensión arterial, nefritis tubulointersticiales crónicas, glomerulonefritis crónicas, enfermedad renal poliquística y desconocida (cuando no fue posible determinarla).
- Tratamiento inmunosupresor de inducción: asociación de drogas inmunosupresoras utilizadas al inicio del trasplante para prevenir el rechazo.
- Presencia de rechazo: confirmado histológicamente, sí o no.
- Tiempo de isquemia fría (TIF) (horas): período que va desde que se inicia la perfusión con líquido de preservación hasta el desclampaje arterial e inicio de la reperfusión con sangre en el implante, dado en valor de media y desviación estándar. Solo en trasplante donante cadáver, por ser no apreciable en el donante vivo.
- Tiempo de isquemia caliente secundaria (TICS) (minutos): período que va desde que se saca el riñón de la bolsa refrigerada hasta que se inicia la reperfusión del injerto con sangre, desclampaje, dado en valor de media y desviación estándar.
- Presencia de necrosis tubular aguda (NTA): sí o no. Ausencia de función del injerto en el postrasplante inmediato con necesidad de diálisis, excluidas otras causas. Solo en el trasplante donante cadáver, por ser una complicación no existente en el donante vivo.
- Tiempo de necrosis tubular aguda (TNTA) (días): tiempo desde el trasplante hasta la última diálisis realizada con recuperación de la función renal, dado en valor de media y desviación estándar. Solo en el donante cadáver.
- Creatinina al alta en postrasplante inmediato (µmol/L): cifras de creatinina al alta después de la operación, dado en valor de media y desviación estándar.
- Función al alta en el postrasplante inmediato: sí o no.
- Porcentaje pretrasplante de reactividad ante un panel de linfocito (PRA), prueba de sensibilización, dado en valor de media y desviación estándar.
- Compatibilidades entre donante y receptor en el sistema mayor de histocompatibilidad (human leucocite antigens, HLA siglas en anglosajón), dado en valor de media y desviación estándar.
- Supervivencia del injerto: dado por la diferencia entre la fecha de pérdida del injerto y la fecha de realización del trasplante.
- Supervivencia del paciente: dado por la diferencia entre la fecha de muerte del enfermo y la fecha de realización del trasplante.
Análisis de la información
Se comparan las variables estudiadas entre los segundos trasplante y aquellos que reciben por primera vez un injerto. Para comparar variables cuantitativas expresadas por valores de medias y desviaciones estándares se utilizó la prueba T. Las variables expresadas en valores de frecuencias se compararon mediante la aplicación de la prueba de chi cuadrado.
Se comparó entre grupos la supervivencia del injerto y del paciente mediante las curvas de Kaplan y Meier y la aplicación de un test de rango logarítmico. En todos los casos se consideró significativo desde el punto de vista estadístico si el valor de la p fue menor de 0,05.
RESULTADOS
En la tabla 1 comparamos las variables generales entre aquellos pacientes que se retrasplantaron con los que reciben por primera vez un injerto, los retrasplantes constituyen solo el 5,4 % de los trasplante realizados (34 enfermos), no hubo diferencias significativas entre la edad del receptor, edad del donante, porcentaje de reactividad ante un panel linfocítico, compatibilidad entre donante y receptor, enfermedad que condicionó la insuficiencia renal en el receptor o tipo de donante utilizado. No hubo pacientes con enfermedad renal poliquística entre los que recibieron un segundo injerto.
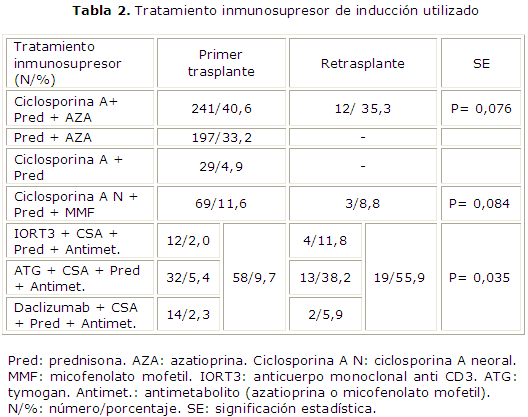
La utilización del tratamiento inmunosupresor en los primeros momentos del trasplante se refleja en la tabla 2, la terapia dual con azatioprina y prednisona o ciclosporina y prednisona nunca se empleó en los enfermos que reciben un segundo injerto. Se empleó un protocolo de 3 drogas, con ciclosporina A, azatioprina y prednisona en los primeros retrasplantes, 12 (35,3 %), mientras que una variante parecida, pero con la formulación neoral de la ciclosporina y sustituyendo la azatioprina por el micofenolato mofetil se ha empleado recientemente en 3 enfermos retrasplantados (8,8 %), estas cifras no difieren significativamente al compararla con la medicación empleada en los trasplantes renales primarios. En la mayoría de los segundos trasplantes se aplicó una terapia cuádruple secuencial con globulinas antilinfociticas policlonales: tymogan (13/38,2 % -pacientes/porcentaje de utilización), o monoclonales: IORT3 (4/11,8 %), daclizumab (2/5,9 %), o sea que en el 55,9 % se empleó este tipo de protocolo, lo cual fue estadísticamente significativo al compararlo con los primeros trasplantes 58/9,7 %, p= 0,035.
Menor fue la frecuencia de rechazo agudo en los segundos trasplantes al compararla con la de aquellos que recibían un primer injerto, 7/20,6 % vs. 207/34,9 %, lo cual arrojó resultados cercanos a la significación estadística, p= 0,056. Las variables relacionadas con el daño isquémico como los tiempos de isquemia fría, caliente secundaria, la presencia y la duración de necrosis tubular aguda, resultaron solo ligeramente inferiores en los retrasplantes sin significación estadística. Muy similares fueron los valores de creatinina al alta así como el porcentaje de enfermos que salieron del postrasplante inmediato con función al establecer comparaciones estadísticas entre los 2 grupos de estudio (tabla 3).
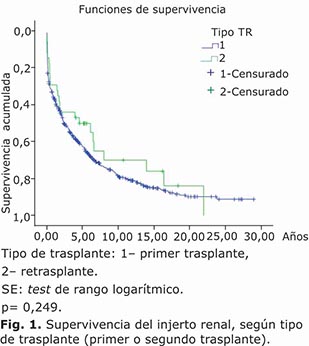
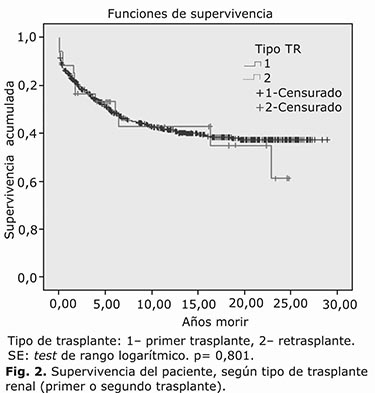
Las figuras 1 y 2 muestran las curvas de supervivencia del injerto y del paciente, respectivamente, se comparan entre grupos mediante el método de Kaplan y Meir. En ambos casos los resultados son muy similares y la comprobación mediante un test de rango logarítmico no mostro diferencias significativas.
DISCUSIÓN
La realización de un segundo trasplante renal fue baja en esta investigación al compararla con las frecuencias que alcanzan otros grupos dedicados a la actividad de trasplante. Datos algo antiguos del registro de la EDTA mostraban que entre 1984 y 1993, el 5 % de los trasplantes correspondía a retrasplantes.5 En los Estados Unidos, durante el mismo período, el 13 % de los trasplante se realizaron a enfermos que habían perdido un injerto, pero los enfermos que esperaban un retrasplante constituían 25-30 % de la lista de espera.6 En Francia, entre 1989 y 1999, el 13,3 % de los trasplantes eran retrasplantes, pero el 42 % de los enfermos en lista de espera eran candidatos a un segundo trasplante.7 A pesar del incremento del número de trasplantes, el porcentaje de enfermos admitidos para retrasplante ha cambiado poco en la última década. Según datos de la Organización Nacional para Trasplantes (ONT) en España, en el año 2005, entre 10 % y 13 % de los trasplantes realizados fueron retrasplantes y el grupo etario, entre 18 y 49 años el que presentaba el mayor porcentaje de segundos o terceros trasplantes (13).8 Reportes como los de Howard y otros9 (16 %), Marcen y otros10 (37 %) y Rao y otros11 (40 %), ofrecen frecuencias mayores de enfermos retrasplantados.
No existen en este estudio diferencias en cuanto a la edad de los receptores y de los donantes al compararlas entre grupos. Existen reportes de menor edad tanto de los receptores como de los donantes para segundos trasplantes. Esto se debe a que los pacientes de mayor edad que reciben un primer trasplante y lo pierden, después de un período de inmunosupresión, quedan, en la mayoría de las ocasiones, sin aptitud para recibir un segundo injerto, sobre todo si la supervivencia del primero fue larga, lo que es sinónimo de exposición prolongada a los medicamentos inmunosupresores y las complicaciones secundarias a su uso.12
En cuanto a los donantes, el considerar el retrasplante como un factor de riesgo, ha llevado a la comunidad médica encargada de la atención de estos enfermos a procurar donantes óptimos para estos pacientes y, entre ellos, injertos que se obtengan de personas con menor edad.13
El porcentaje de reactividad ante un panel de linfocitos es una de las condiciones que limita, en muchos casos, la realización de un segundo trasplante, los enfermos que ya han recibido un primer injerto quedan en ocasiones, después de la pérdida, sensibilizados, con elevadas tasas de anticuerpos que reaccionan ante el panel, lo cual dificulta, primero, lograr un cross match pretrasplante negativo lo cual es indispensable para la realización del trasplante y, de lograrlo, la hipersensibilización puede favorecer posteriormente la aparición de rechazo.14 En nuestra investigación, el PRA fue solo ligeramente mayor en los retrasplantes, pero sin evidenciar significación estadística.
Otra de las variables involucradas en la evolución de los injertos, a largo plazo, es el grado de histocompatibilidad entre donante y receptor en el sistema HLA, La mayoría de los grupos trasplantadores buscan para el retrasplante altas compatibilidades, lo cual parece ineludible si los candidatos a recibir un segundo injerto están hipersensibilizados.15 En la serie que nos ocupa no se lograron altas compatibilidades, hecho muy similar entre los trasplantes primarios y retrasplantes.
La enfermedad de base fue otras de las variables pesquisadas por esta investigación, llama la atención que no hubo ningún paciente con enfermedad renal poliquística que recibiera un segundo trasplante. No encontramos en la literatura nada al respecto, en el resto de las enfermedades que contribuyen al daño renal crónico las frecuencias se comportaron de forma similar, lo mismo ocurrió con la comparación en cuanto al tipo de donante cuyas frecuencias entre grupos fueron similares.
Gjertson reporta una baja tasa de empleo del donante vivo para aquellos pacientes que precisan de un segundo trasplante, resultados estos muy parecidos a los nuestros.16
Un elemento de singular importancia en la evolución del trasplante renal es el tratamiento inmunosupresión de inducción. Muchos autores preconizan el empleo de los protocolos cuádruples secuenciales en los segundos trasplantes, estos se fundamentan en el uso de un anticuerpo antilinfocítico, ya sea monoclonal o policlonal, con introducción retardada del anticalcinuerínico, lo cual ofrece las ventajas de lograr una inmunosupresión más potente, así como evitar, en los primeros días del injerto, la vasoconstricción inducida por las drogas anticalcineurínicas cuando más deletérea esta pudiera ser por las secuelas del daño isquémico producido por los períodos de mantenimiento del donante, extracción, preservación e implante del injerto.17-19
Arnol, en su serie de retrasplantes usa una terapia cuádruple secuencial en 100 % de sus enfermos.20
Gruber considera a los pacientes que reciben un segundo injerto, como de alto riesgo para la aparición de rechazo y función retardada, por lo que utiliza un tratamiento con 4 drogas de inicio o en variedad secuencial en todas las oportunidades.21
Los resultados del presente estudio no difieren de lo comentado, el 55,9 % de los retrasplantes realizados utilizan una inducción cuádruple secuencial, protocolo que solo se usó en 9,7 % de los trasplantes renales primarios, diferencia que resultó significativa. Cabe destacar que en los primeros 15 retrasplantes realizados no se usaron las globulinas antilinfocíticas por no contar con estos inmunosupresores.
Al analizar los valores medios de tiempos de isquemia fría en los trasplantes renales de donante cadáver, esta fue ligeramente inferior en los segundos trasplantes aunque no resultó una diferencia estadísticamente significativa.
Una de las condiciones propicias para lograr el éxito en la realización de un segundo trasplante renal es disminuir los tiempos de isquemia fría y caliente secundaria, variables que se vinculan a la aparición y severidad de la necrosis tubular aguda.
Algunos reportes vinculan el retrasplante a tiempos prolongados de isquemia caliente secundaria, por el deterioro vascular del receptor como consecuencia de la aterogénesis incrementada por el uso de esteroides en un primer injerto.22 Nosotros encontramos tiempos medios de isquemia fría menores en el caso de los segundos trasplantes como política del grupo para minimizar el daño isquémico, en cuanto a los tiempo de isquemia caliente secundaria no existen diferencias entre los primeros y segundos trasplantes lo que sin dudas influyó en que no existieran diferencias entre la aparición y la duración de la necrosis tubular aguda.
Cho y Cecka encontraron mayor frecuencia de necrosis tubular aguda en los retrasplante donante cadáver y estas fueron más duraderas, lo cual no coincide con los resultados del presente estudio.23
La complicación más temida del trasplante renal es la reacción inmunológica de rechazo, esta sin dudas se condiciona por la hipersensibilización del enfermo a los antígenos extraños del receptor así como se relaciona con el daño isquémico del injerto cuya expresión anatómica es la necrosis tubular aguda.
La literatura recoge mayor incidencia de rechazo en los retrasplante al compararlos con los trasplante renales primarios,24 lo cual no se constató en este estudio donde el rechazo fue menos frecuente en los segundos trasplantes. Esto responde a que, en nuestra serie, el estado de sensibilización, dado por el PRA, el grado de compatibilidades en el sistema HLA, los tiempos de isquemia y la frecuencia y severidad de la necrosis tubular aguda fueron muy similares entre los 2 grupos de estudio, a lo que se añade que en los retrasplantes se usó en más de la mitad de los casos, como tratamiento inmunosupresor de inducción, una terapia cuádruple secuencial con mayor potencia inmunosupresora e introducción tardía del anticalcineurínico, lo cual protege el injerto del daño isquémico, estas condiciones no se dieron en los trasplantes primarios donde solo el 9,7 % usó este protocolo de inducción.
Al comparar la frecuencia de injertos funcionantes al alta, en el postrasplante inmediato, el valor medio de la creatinina sérica de los que egresan sin necesidad de empleo de los métodos de diálisis, la supervivencia del injerto y del paciente, no existieron diferencias entre los primeros y los segundos trasplantes.
Existen en la literatura resultados dispares en cuanto a los resultados de supervivencia del injerto en los segundos trasplantes renales. Muchos consideran que la supervivencia del injerto es menor al compararla con la de los trasplantes primarios. Kasike y otros encontró una supervivencia menor de 20 % a los 5 años en los retrasplantes.25 Otros plantean que perfeccionando los aspectos involucrados en la terapéutica de estos enfermos, los resultados entre el primer y segundo trasplante son superponibles.8
En conclusión, el retrasplante constituye una modalidad terapéutica eficaz para los enfermos que pierden un primer injerto y vuelven a los métodos de diálisis. Si se logra buena compatibilidad entre donante y receptor, se disminuyen los tiempos de isquemia y el daño inicial del injerto y, sobre todo, si se individualiza el tratamiento inmunosupresor de inducción y se potencializa un protocolo con 4 drogas, que utilice las globulinas antilinfocíticas con introducción posterior del anticalcineurínico, se pueden lograr resultados similares a los que se obtienen en un primer trasplante renal.
REFERENCIAS BIBLIOGRÁFICAS
1. Wolfe RA, Ashby VB, Milford EL. Comparison of mortality in all patients on dialysis, patients on dialysis awaiting transplantation, and recipients of a first cadaveric transplant. N Engl J Med. 2007;341:1725-30.
2. Berthoux F, Jones E, Gellert R, Mendel S, Saker L, Briggs D. Epidemiological data of treated end-stage renal failure in the European Union (EU) during the year 1995: report of the European Renal Association Registry and the National Registries. Nephrol Dial Transplant. 1999;14:2332-42.
3. Denny RR, Sumrani N, Miles AMV. Survival on hemodialysis versus renal transplantation following primary renal allograft failure. Transplant Proc. 1997;29:3602-4.
4. Gallichio MH, Hudson S, Young CJ, Diethelm AG, Deierhoi MH. Renal retransplantation at the University of Alabama at Birmingham: incidence and outcome. En: Cecka JM, Terasaki PI, eds. Clinical transplants. Cap. 14. Los Ángeles, CA: UCLA Tissue typing laboratory; 1998. p. 169-75.
5. Rigden S, Mehls O, Gellert R. on behalf of the scientific advisory board of the ERA-EDTA registry. Nephrol Dial Transplant. 1999;14:566-9.
6. Magee JC, Barr ML, Basadona GP. Repeat organ transplantation in the United States, 1996-2005. Am J Transplant. 2007;7:1424-33.
7. Coupel S, Giral-Clase M, Karam G. Ten-years survival of second kidney transplants: impact of immunologic factors and renal function at 12 months. Kidney Intern. 2003;64:674-80.
8. Marcen R, Fernández A, Fernández M, Terruel JL, Pérez-Flores I, Sánchez FA. El retrasplante. Cap.10. En: Guías SEN. Recomendaciones sobre la vuelta a diálisis del paciente trasplantado. Nefrología 2012 [citado 15 Nov. 2013]. Disponible en: http://www.senefro.org/modules/webstructure/files/cap_10_guias_dialisis_retx.pdf?check_idfile=3653
9. Howard RJ, Reed AI, van der Werf WJ, Hemming AW, Patton PR, Scornik JC. What happens to renal transplant recipients who lose their graft? Am J Kidney Dis. 2001;38:31-5.
10. Marcén R, Pascual J, Tato AM. Renal transplant recipients outcome after losing the first graft. Transplant Proc. 2003;35(5):1679-81.
11. Rao PS, Schaubel DE, Wei G, Fenton SSA. Evaluating the survival benefit of kidney retransplantation. Transplantation. 2006;82:669-74.
12.Ojo AO, Wolfe RA, Agodoa LY. Prognosis alter primary renal transplant failure and the beneficial effect of repeat transplantation. Transplantation. 1998;66:1651-9.
13.Sellers MT, Velidedeoglu E, Bloom ED. Expanded -criteria donor kidneys: a single-center clinical and short-term financial analysis-cause for concern in retransplantation. Transplantation. 2004;78:1670-5.
14.Jordan SC, Pescovitz MD. Presensitization: the problem and its management. Clin J Am Soc Nephrol. 2006;1:421-32.
15.Hirata M, Terasaki PI. Renal retransplantation. In: Cecka JM, Terasaki PI, eds. Clinical transplants. Cap. 34. Los Ángeles, CA: UCLA Tissue Typing Laboratory; 1994. p. 419-33.
16.Gjertson DW. A multi-factor analysis of kidney regraft outcomes. ClinTranspl. 2002;3:335-49.
17.Salvadori M, Bertoni E. Renal transplant allocation criteria, desensitization strategies and immunosuppressive therapy in retransplant renal patients. J Nephrol. 2012;25(6):890-9.
18.Borroto DG. Individualización de la inmunosupresión de inducción en el trasplante renal, editorial. Rev Cubana Med 2013 [citado 15 Nov. 2013];52(1):1-3. Disponible en: http://scielo.sld.cu/pdf/med/v52n1/med01113.pdf
19.Borroto DG, Guerrero DC. Inmunosupresión de inducción en el trasplante renal en el hospital Hermanos Ameijeiras de 1984-2012. Rev Cubana Med 2013 [citado 12 Nov. 2013];52(2):88-98. Disponible en: http://scielo.sld.cu/pdf/med/v52n2/med02213.pdf
20. Arnol M, Prather JC, Mittalhenkle A, Barry JM, Norman DJ. Long-term kidney regraft survival from deceased donors: risk factors and outcomes in a single center. Transplantation. 2008;86(8):1084-9.
21.Gruber SA, Brown KL, El-Amm JM, Singh A, Mehta K, Morawski K, et al. Equivalent outcomes with primary and retransplantation in African-American deceased-donor renal allograft recipients. Surgery. 2009;146(4):646-52.
22.Humar A, Key N, Ramcharan T, Payne WD, Sutherland DE, Matas AJ. Kidney retransplants after initial graft loss to vascular thrombosis. Clin Transplant. 2001;15(1):6-10.
23. Cho YW, Cecka JM. Cadaver-donor renal retransplants. ClinTranspl. 1993;32:469-84.
24.Nankivell BJ, Alexander SI. Rejection of the kidney allograft. New Engl J Med. 2010;363:1451-62.
25.Kasike BL, Israni AK, Syder JJ, Skeans MA. Relationship between kidney function and long term graft survival after kidney transplant. Am J Kidney Dis. 2011;57(3):466-75.
Recibido: 3 de marzo de 2014.
Aprobado: 14 de marzo de 2014.
Dr. Gerardo Borroto Díaz. Servicio de Nefrología. Hospital Clinicoquirúrgico "Hermanos Ameijeiras", San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana, La Habana, Cuba. CP 10300.