Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina
versión On-line ISSN 1561-302X
Rev cubana med vol.57 no.2 Ciudad de la Habana abr.-jun. 2018
ARTÍCULO ORIGINAL
Función de la amiloidosis en la neuropatía periférica de los pacientes con anemia drepanocítica
Function of amyloidosis in peripheral neuropathy of patients with sickle cell anemia
Adalberto Fortún Prieto, Mirta Caridad Campo Díaz
Hospital Clínico Quirúrgico Docente "León Cuervo Rubio". Pinar del Río, Cuba.
RESUMEN
Introducción: El estado inflamatorio que acompaña la anemia drepanocítica puede asociarse a amiloidosis sistémica, complicación que ha sido comunicada en esta enfermedad, que también puede afectar los nervios periféricos por el proceso vaso-oclusivo crónico en esta.
Objetivos: Evaluar la función de la amiloidosis en el desarrollo de la neuropatía periférica en un grupo de pacientes con hemoglobinopatía SS.
Métodos: Para determinar si la amiloidosis participa en el desarrollo de neuropatía periférica en los pacientes con drepanocitosis se estudiaron 45 sujetos mediante evaluación clínica, biopsia de grasa abdominal y estudio de conducción nerviosa, evaluándose si existía relación entre ambos trastornos.
Resultados: Se encontraron signos de neuropatía predominantemente sensitiva. Las alteraciones del estudio de conducción fueron constantes, comprobándose que la existencia de amiloidosis aumentó la frecuencia y la severidad de la neuropatía en estos pacientes. La biopsia de nervio peroneo demostró amiloidosis en dos casos.
Conclusiones: Los resultados indican que la amiloidosis se relaciona con el desarrollo de neuropatía periférica en los pacientes con anemia drepanocítica.
Palabras clave: Anemia drepanocítica; amiloidosis sistémica; neuropatía periférica.
ABSTRACT
Introduction: The inflammatory condition that accompanies sickle cell anemia can be associated to systemic amyloidosis, a complication of this disease which can also affect the peripheral nerves because of its chronic vaso-occlusive process.
Objectives: To assess the function of amyloidosis in the development of peripheral neuropathy in a group of patients with hemoglobinopathy SS.
Methods: In order to determine if amyloidosis takes part in the development of peripheral neuropathy in patients with sickle cells disease, 45 subjects were studied by means of clinical evaluation, biopsy of abdominal fat and a study of nervous conduction, being evaluated if there was any relation between both disorders.
Results: Signs of predominantly sensitive neuropathy were found, and the alterations of the study of conduction were constant, being verified that the existence of amyloidosis increased the frequency and the severity of neuropathy in these patients. Peroneal nerve´s biopsy demonstrated that amyloidosis was present in two cases.
Conclusions: The results indicate that amiyloidosis is related to the development of peripheral neuropathy in patients with sickle cell anemia.
Keywords: Sickle cell anemia; systemic amyloidosis; peripheral neuropathy.
INTRODUCCIÓN
La drepanocitosis se define como un conjunto de anemias hemolíticas caracterizadas por la presencia de hemoglobina S (HbS) incluido su estado homocigótico, la hemoglobinopatía SS o anemia drepanocítica (AD).
El evento primario del proceso vaso-oclusivo de la enfermedad es la polimerización de la HbS desoxigenada que distorsiona al hematíe en forma de drepanocito,1 lo que puede provocar oclusión vascular a nivel de la microcirculación, la que aún en estado basal ocasiona daño tisular por isquemia-reperfusión que, junto al stress oxidativo y la inflamación, son factores que condicionan el daño crónico de los órganos.2
Las manifestaciones neurológicas y las complicaciones en los pacientes que la padecen influyen fundamentalmente el sistema nervioso central; sin embargo, durante las últimas dos décadas se ha prestado atención a la afectación de los nervios periféricos en el curso de la enfermedad.3
El aumento de la supervivencia de los enfermos con AD y la necesidad de mantener y mejorar su calidad de vida determina que el conocimiento de sus manifestaciones a largo plazo sea un aspecto esencial para lograr un adecuado seguimiento de estos.
En el año 1993 apareció la primera comunicación sobre amiloidosis asociada a la AD.4 Se trataba de un paciente con crisis vaso-oclusivas graves de inusitada frecuencia y múltiples transfusiones que desarrolló un síndrome nefrótico en el que se identificó como causa la presencia de amiloidosis renal. En un estudio realizado en Cuba se comprobó la presencia de amiloidosis sistémica en 8 de 20 pacientes con AD,5 lo que indicó que la existencia de dicho trastorno puede potencialmente tener importancia en la evolución de la enfermedad.
La exploración clínica, junto a la búsqueda de amiloidosis sistémica en estos pacientes, ha evidenciado que estas complicaciones son hallazgos frecuentes en estos enfermos, lo que indica la necesitad su evaluación en la etiopatogenia de muchas de sus manifestaciones en diversos órganos.
Con la realización de estudios de conducción nerviosa se evidencia la existencia de neuropatía mixta en una alta proporción de los pacientes adultos con AD6 lo que se interpreta usualmente como resultado del proceso vaso-oclusivo a nivel de la vasa-nervorum.
La amiloidosis, enfermedad infiltrativa asociada a estados de inflamación crónica como el que acompaña la amiloidosis sistémica puede limitarse a un solo órgano o causar lesiones que incluyen el hígado, corazón, páncreas, glándulas suprarrenales, riñones o nervios periféricos.7,8 Por antes expuesto se decidió evaluar su función en el desarrollo de la neuropatía periférica en un grupo de pacientes con hemoglobinopatía SS.
MÉTODOS
Se realizó un estudio con 45 pacientes adultos con AD y seguimiento estable durante 5 años en consulta externa, los que se encontraban en estado basal de la enfermedad (ausencia de episodios agudos durante 3 meses) y que no tuvieran antecedentes de diabetes, nefropatía o hubieran padecido neuropatía epidémica. Se estudió un grupo de comparación de 40 individuos sanos con promedio de edad similar, siguiendo los mismos criterios de exclusión.
El diagnóstico de amiloidosis se realizó en ambos grupos mediante biopsia por aspiración con aguja fina (BAAF) de la grasa abdominal9 con el uso de las técnicas de rojo congo y cristal violeta.
A todos los pacientes se les realizó un estudio de conducción nerviosa con el equipo Neurónica-02 a temperatura ambiente entre 22 y 24° C. Los potenciales de acción muscular fueron registrados en los miembros superiores en el flexor del pulgar y abductor del dedo meñique respectivamente; la velocidad de conducción motora fue medida en la muñeca y el codo. Los potenciales de acción nerviosa fueron registrados en la muñeca y la velocidad de conducción nerviosa sensitiva fue calculada mediante un método ortodrómico. En las extremidades inferiores se estudiaron los nervios motores tibial y peroneo y el nervio sensitivo sural. La velocidad de conducción motora fue medida entre el tobillo y la rodilla y se utilizó el método antidrómico para el estudio del nervio sural, se colocó el electrodo de registro detrás del maléolo lateral y el sitio de estimulación fue en la porción dorsal de la pantorrilla. Se definió la presencia de neuropatía cuando se comprobó una lesión axonal con una amplitud menor de 5 mV. Se clasificó su severidad de ligera cuando el latido se encontró entre 130-150 %, moderada cuando fue superior a 150 % y severa ante la presencia de bloqueo en la conducción. Se realizó biopsia de nervio peroneo a dos enfermos con AD y neuropatía severa.
La aprobación del estudio de conducción, la biopsia de la grasa abdominal en enfermos y en los individuos del grupo de control y la realización de la biopsia de nervio peroneo en los 2 pacientes con neuropatía severa se obtuvo mediante el consentimiento informado a los pacientes. En el caso de los pacientes con AD se explicó la importancia de los resultados para el seguimiento y control de la enfermedad, se ofreció la posibilidad de abandonar el estudio si se deseaba.
Los pacientes y el grupo control se agruparon según las edades y el sexo. Los pacientes con hemoglobinopatía SS se reunieron de acuerdo con las manifestaciones clínicas de su enfermedad neurológica, así como por sus resultados del estudio de conducción nerviosa realizado.
Las variables cuantitativas se expresaron en frecuencias absolutas y porcentajes y se midió la asociación entre variables operacionales como categóricas mediante el estadígrafo odds ratio y asociación mediante la prueba de X2, todas se efectuaron con un 95 % de confianza.
RESULTADOS
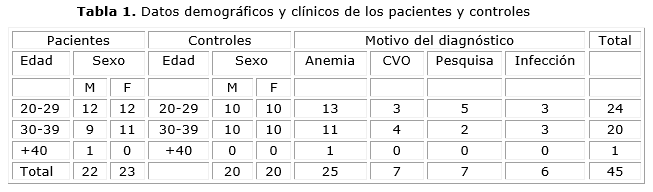
Hubo un ligero predominio del sexo femenino entre los pacientes con AD, la mayoría fueron del grupo de menor edad y la principal causa del diagnóstico fue la existencia de anemia (Tabla 1).
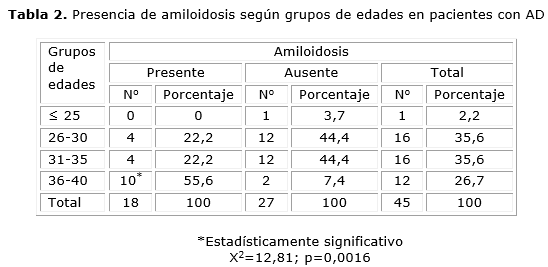
La presencia de amiloidosis fue encontrada en 18 de los pacientes con AD y su incidencia fue mayor en el grupo de edades más avanzadas, en el que estuvo presente la mayor parte de los afectados, lo que resultó estadísticamente significativo (Tabla 1). No se encontró ningún caso positivo entre los 40 individuos sanos a los que se les realizó la búsqueda de amiloidosis mediante BAAF de la grasa abdominal.
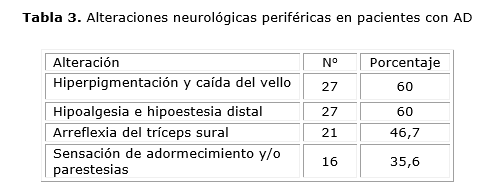
Más de la mitad de los pacientes estudiados presentó al menos una anomalía en el examen físico neurológico, las más frecuentes fueron la hiperpigmentación con caída del vello y la hipoalgesia e hipoestesia distales (Tabla 2). La disfunción sensitiva fue más frecuente que la motora. La manifestación menos frecuente fue la percepción subjetiva de adormecimiento o parestesias.
Los estudios de conducción mostraron la presencia de neuropatía axonal mixta con tendencia al microvoltaje en todos los enfermos, prolongación del tiempo de latencia y enlentecimiento de la velocidad de conducción sensitiva y motora, lo que evidenció una afección constante del sistema nervioso periférico en los pacientes. En el caso del grupo de observación se encontró que 3 de los individuos presentaron tendencia al microvoltaje y solamente en 1 de ellos pudo demostrarse la existencia de enlentencimiento de la velocidad de conducción.
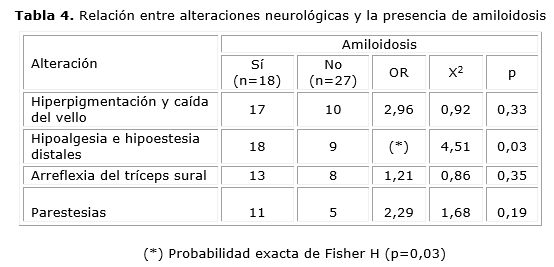
Al evaluar la relación entre la existencia de amiloidosis y los síntomas de neuropatía periférica (Tabla 3) se comprobó que en todos los casos las alteraciones clínicas estaban representadas con mayor frecuencia en el grupo con amiloidosis; sin embargo, la asociación sólo fue significativa en el caso de la hipoalgesia e hipoestesia.
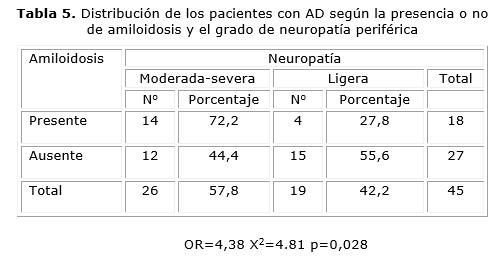
Lla severidad de la neuropatía y su relación con la presencia o no de amiloidosis se muestra en la Tabla 4. La disfunción ligera se presentó en 19 pacientes, por lo que puede observarse que de los 18 con amiloidosis, 14 presentaron disfunción moderada a severa; sin embargo, en aquellos que no tienen este trastorno, la distribución de la severidad de la disfunción neurológica fue proporcional, esto evidencia que la mayoría de los que presentaron amiloidosis tuvieron disfunción neurológica más intensa (Tabla 5).
DISCUSIÓN
El presente estudio fue realizado sobre la base de los resultados de dos trabajos previos, en uno se reportó la existencia de disfunción de nervios periféricos en todos los pacientes con AD y en el otro hubi presencia de amiloidosis en 40 % de los casos estudiados.6
Se conoce que la afección del sistema nervioso central (SNC) es la más frecuente entre las alteraciones neurológicas de la AD. Sin embargo, las alteraciones del sistema nervioso periférico pocas veces se reportan aunque se presentan como casos aislados,10,11 se considera que la isquemia dependiente de la vaso-oclusión subclínica sostenida podría ser su causa en función de la desmielinización segmentaria y degeneración11 aunque se han sugerido otras causas como la utilización terapéutica de óxido nítroso y citrato sódico o la pica.12 La limitada expresión clínica de esta disfunción neurológica acompañada de la infrecuente indicación de estudio de conducción nerviosa podrían ser las causas de la baja frecuencia con que se reporta esta anomalía.
En un estudio previo6 se reportó la presencia de neuropatía periférica predominantemente sensitiva en pacientes con AD que presentaban escasa traducción clínica, en este se señaló que no existía relación entre la severidad de la enfermedad de base y la presencia o intensidad de la neuropatía encontrada, lo que coincide con estudios anteriores.13 Otra investigación realizada mostró la presencia de amiloidosis sistémica en el 40 % de un grupo de enfermos con esta enfermedad.5
El grupo de observación estudiado no presentó amiloidosis en ninguno de sus individuos, lo que constituye una característica del desarrollo de la enfermedad explicable por la presencia de un estado inflamatorio crónico microvascular14 y la tendencia aumentada al desarrollo de infecciones, que como se conoce, favorecen el desarrollo de la entidad. En la AD existe un estado de inflamación crónico que se mantiene aún en estado basal y el riesgo de infecciones es alto debido a las alteraciones inmunológicas propias de la enfermedad.15
La disfunción sensitiva fue encontrada con más frecuencia, con predomino de las anomalías de la sensibilidad superficial. Todos los enfermos presentaban tendencia al microvoltaje, prolongación del tiempo de latencia y enlentecimiento de la velocidad de conducción, tanto sensitiva como motora. La ausencia de alteraciones clínicas en los individuos del grupo de comparación y la existencia de alteraciones aisladas no significativas en los estudios de conducción realizados a estos indican que dichos hallazgos pueden ser considerados como parte de las manifestaciones propias de esta enfermedad.
La evaluación de la severidad de la disfunción de nervios periféricos evidenció que en aquellos con amiloidosis predominó la disfunción moderada o severa. De los 19 pacientes que mostraron neuropatía ligera, solamente 4 tenían amiloidosis, lo que sugiere que esta última podría influir en la intensidad de la expresión clínica de la neuropatía en los enfermos.
La neuropatía periférica es un trastorno asociado a diversas enfermedades sistémicas,16 pero en el caso de la AD puede ser el resultado de isquemia crónica en dependencia del proceso oclusivo microvascular. No obstante, la demostración de amiloidosis sistémica indica que esta última podría influir en el desarrollo de esta complicación.17 La realización de biopsia de nervio peroneo en dos pacientes con amiloidosis evidenció el depósito de sustancia amiloide y demuestra morfológicamente que la presencia de amiloidosis participa como un elemento adicional en la disfunción de los nervios periféricos de los pacientes con AD.
La existencia de esta complicación neurológica y la presencia de amiloidosis en su desarrollo se convierte en un aspecto adicional para la evaluación y el seguimiento de los pacientes con AD, sobre todo en el momento actual, en que la mortalidad por eventos agudos disminuye y la sobrevida de estos pacientes se prolonga, lo que obliga a tener en cuenta las complicaciones crónicas que pueden presentar dichos pacientes.
Los resultados evidencian que la amiloidosis sistémica, complicación frecuente en los pacientes con AD, participa junto a la lesión isquémica de la vasa-nervorum propia de la enfermedad en la etiopatogenia de la neuropatía periférica de los pacientes que la padecen. Esto requiere de la determinación del tipo de proteína amiloide presente en estos pacientes para su correcta tipificación18, así como de estudios futuros para determinar con precisión el significado de la amiloidosis en el daño crónico de órganos de los pacientes con esta enfermedad.
Conflicto de intereses
Los autores declaran que no existe conflicto de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Pollion WN, Kim BC, Castro O. Intracellular hemoglobin S polymerization and the clinical severity of sickle cell anemia. Blood. 1998;91:1777-81.
2. Olujohungbe A, Howard J. The clinical care of adult patients with sickle cell disease. Br J Hosp Med. 2008;69(11):616-9.
3. Stuart MJ, Nagel R. Sickle cell disease. Lancet. 2004;364:1343-60.
4. Win N, Brozocic F, Gabriel R. Secondary amyloidosis accompanying multiple sickle cell crisis. Trop Doct. 1993;23:45-6.
5. Fortún A, León CA, Campo MC, López MV, Pileta A. La amiloidosis como complicación de la anemia drepanocítica. Rev Cubana Med. 2005;44 ISSN 0034-7523.
6. Campo MC, Fortún A, Mustelier R. Alteraciones del sistema nervioso periférico en la drepanocitosis. Rev Cubana Hematol Inmunol Hemoter. 2000;16(1):45-8.
7. Gertz MA. Immunoglobulin light chain amyloidosis: 2016 update on diagnosis, prognosis, and treatment. American Journal of Hematology. 2016;91(9):947-56.
8. Figueroa JJ, Bosch EP, Dyck PJ, Singer W, Vrana JA, Theis JD, et al. Amyloid-like IgM deposition neuropathy: a distinct clinico-pathologic and proteomic profiled disorder. Journal of the Peripheral Nervous System. 2012;17(2):182-90.
9. Bogov B, Lubomirova M, Kiperova B. Biopsy of subcutaneous fatty tissue for diagnosis of systemic amyloidosis. Hippokratia. 2008;12(4):236-9.
10. Simsek B, Bayazit AK, Ergin M, Soran M, Dursun H, Kilinc Y. Renal amyloidosis in a child with sickle cell anemia. Pediatr Nephrol. 2006;21(6):877-9.
11. Okuyucu EE, Turhanoglu A, Duman T, Kaya H, Melek IM, Yilmazer S. Peripheral nervous system involvement in patients with sickle cell disease. Eur J Neurol. 2009;16(7):814-8.
12. Alexy T, Sangkatumvong S, Connes P, Pais E, Tripette J, Barthelemy JC, et al. Sickle cell disease: selected aspects of pathophysiology. Clin Hemorheol Microcirc. 2010;44(3):155-66.
13. Nebor D, Bowers A, Hardy-Dessources MD, Knight-Madden J, Romana M, Reid H, et al. Frequency of pain crises in sickle cell anemia and its relationship with the sympatho-vagal balance, blood viscosity and inflammation. Hematologica. 2011;96(11):1589-94.
14. Zhang D, Xu C, Manwani D, Frenette PS. Neutrophils, platelets, and inflammatory pathways at the nexus of sickle cell disease pathophysiology. Blood. 2016;127(7):801-09. doi: https://doi.org/10.1182/blood-2015-09-618538.
15. Montalembert M. Management of sickle cell disease. Br Med J. 2008;337:1036-7.
16. Wilmshurst JM, Ouvrier RA. Neuropathies secondary to systemic disorders. Chapter 22: A Clinician's Approach En: Neuromuscular disorders of infancy, childhood and adolescence. 2nd Edition. Elsevier; 2014. p. 418-30.
17. Tumblin A, Tailor A,Hoehn GT, Mack AK, Mendelsohn L, Freeman L, et al. Apolipoprotein A-I and serum amyloid A plasma levels are biomarkers of acute painful episodes in patients with sickle cell disease. Hematologica. 2010;95(9):1467-72.
18. Klein CJ, Vrana JA, Theis JD,Dyck PJ, Dyck PJ, Spinner RJ, et al. Mass spectrometric-based proteomic analysis of amyloid neuropathy type in nerve tissue. Arch Neurol. 2011;68(2):195-9.
Recibido: 3 de abril de 2018.
Aprobado: 15 de julio de 2018.
Adalberto Fortún Prieto. Hospital Clínico Quirúrgico Docente "León Cuervo Rubio". Pinar del Río, Cuba.
Correo electrónico: adalbertofp@infomed.sld.cu