My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Pediatría
Print version ISSN 0034-7531
Rev Cubana Pediatr vol.85 no.4 Ciudad de la Habana Oct.-Dec. 2013
PRESENTACIÓN DE CASO
Oclusión intestinal por hernia de Bochdalek
Intestinal occlusion caused by Bochdalek hernia
MSc. Dra. María Eugenia Ferro Moreira, Dr. Evenildo Martínez Ortega, Dr. Luis Valle Garrido, Dr. Edel González Yoli, Dra. María de las Mercedes Cárdenas Herrera
Hospital Pediátrico "Juan Manuel Márquez". La Habana, Cuba.
RESUMEN
La hernia de Bochdalek es un defecto congénito de la región posterolateral del diafragma, usualmente del lado izquierdo, se presenta en 1 de cada 2 000-5 000 nacidos vivos, su diagnóstico en el momento del nacimiento es relativamente fácil, no así cuando este debe realizarse después del período neonatal, pues puede conllevar a evaluaciones erróneas desde el punto de vista clínico y radiológico. La presentación tardía de esta entidad no es frecuente, por lo que nos proponemos dar a conocer un caso de oclusión intestinal por hernia diafragmática de presentación tardía y revisar la literatura al respecto. Se presenta un lactante de 5 meses producto de un tercer embarazo, parto distócico por presentación pelviana, oligoamnios, Apgar 9-9, antecedentes de salud hasta el cuarto mes en que se le introduce leche de chiva y comienza con regurgitaciones bastante frecuentes. Se le realiza diagnóstico a los 5 meses de oclusión intestinal por hernia diafragmática congénita. Se interviene quirúrgicamente sin complicaciones posoperatorias, es dado de alta a los 7 días, y seguido por consulta externa, con evolución satisfactoria. La hernia diafragmática congénita, cuando se presenta después del periodo neonatal, puede diagnosticarse incidentalmente en un estudio radiológico, o por complicaciones secundarias al paso de las vísceras abdominales al tórax.
Palabras clave: hernia de Bochdalek, hernia diafragmática congénita, hernia diafragmática congénita de presentación tardía.
ABSTRACT
Bochdalek hernia is a congenital defect of the posterolateral region of the diaphragm, usually located on the left side. It appears in one per 2000 to 5000 live births; the diagnosis at birth is relatively easy but after the neonatal period, it can lead to erroneous assessments from the clinical and radiological viewpoints. The late-presenting hernia is not frequent, so we intended to present a case of intestinal occlusion caused by late-presenting diaphragmatic hernia and to make a literature review on this topic. Here is the case of a 5 months-old infant born from a third pregnancy, which was dystotic as a result of pelvic presentation and with oligohydramnios. He had an Apgar score of 9.9 and a history of health problems until his fourth month of life when he began to be fed with goat's milk and it appeared pretty frequent regurgitation. He was diagnosed at 5 months of life with intestinal occlusion due to congenital diaphragmatic hernia. He was operated on, no complications were observed and then he was discharged from the hospital after 7 days and followed-up at outpatient service, with satisfactory recovery. The congenital diaphragmatic hernia that occurs after the neonatal period can be incidentally diagnosed in a radiological study or because of secondary complications when abdominal viscerae passed into the thorax.
Keywords: Bochdalek hernia, congenital diaphragmatic hernia, late-presenting congenital diaphragmatic hernia.
INTRODUCCIÓN
La primera cita de una hernia diafragmática fue realizada por Ambrosio Paré en 1579, y originalmente descrita por Lazarus Riverius en 1679, quien describió su hallazgo posmortem en un hombre de 24 años de edad. Charles Holt fue el primero en describirla en el niño, y Vincent Alexander Bochdalek, en 1848, describió desde el punto de vista embriológico la herniación del intestino por un agujero dorsal diafragmático, variedad que hoy lleva su nombre. La primera reparación en un niño de menos de 24 horas de nacido fue hecha por Gross en 1946.1,2
Se define como hernia diafragmática congénita (HDC) un defecto en la formación del diafragma durante la vida fetal, de tamaño variable, que permite que una parte del contenido del abdomen ascienda a la cavidad torácica y comprima el pulmón ipsilateral en mayor o menor grado.
Su incidencia es de 1 por cada 2 000-5 000 nacidos vivos, el 50 % de los casos presentan anomalías congénitas asociadas, el 90 % de los casos son izquierdas y el 95 % corresponden al tipo Bochdaleck. Es una enfermedad que tiene una alta mortalidad, y la sobrevida en distintos centros va desde 40 a un 80 %.2 Su morbilidad y mortalidad no está dada tanto por el tamaño del defecto, sino por los defectos asociados, el grado de hipoplasia pulmonar y la hipertensión pulmonar persistente.
Son numerosas las clasificaciones que se utilizan para la hernia diafragmática congénita, pero de forma práctica pueden dividirse según el lugar del defecto:
1. Posterolaterales o de Bochdalek (en general son grandes, en el lado izquierdo, y se presentan en el recién nacido).
2. Anterolaterales o de Morgagni (son pequeñas y asintomáticas hasta que se produce la estrangulación de un segmento intestinal).
3. Canal esofágico (se manifiestan generalmente como reflujo gastroesofágico).
Existe una variedad de HDC que se diagnostica después del período neonatal, su diagnóstico puede ser un hallazgo radiológico o porque se presente con complicaciones digestivas, y es llamada por muchos autores como HDC de presentación tardía.3
En estos casos se presume que la herniación se produce por el orificio del diafragma previamente ocluido por el hígado o el bazo.3,4 El cuadro clínico, diagnóstico, tratamiento y complicaciones de estos casos difieren de los que se diagnostican en la etapa neonatal. La literatura plantea que estos casos se presentan entre 5 y un 25 %, e incluso, hay autores que plantean que pueden presentarse en 50 %.3
A pesar de que la HDC de presentación tardía no es una afección muy frecuente, cuando esta de presenta, en ocasiones, puede ser motivo de errores diagnósticos y poner en riesgo la vida de nuestros pequeños pacientes, por lo que nos proponemos presentar un caso de oclusión intestinal por hernia de Bochdalek y revisar la literatura referente a esta entidad.
PRESENTACIÓN DEL CASO
Lactante masculino, de 5 meses, producto de un tercer embarazo, parto distócico por presentación pelviana, oligoamnios, Apgar 9-9, antecedentes de salud hasta el cuarto mes, en que se le introdujo leche de chiva y comenzó con regurgitaciones bastante frecuentes. En horas de la madrugada del día de su ingreso, presentó vómitos abundantes de contenido alimentario y fiebre de 38º C, además de irritabilidad.
Al examen físico existían signos de deshidratación isotónica ligera con globos oculares hundidos, y murmullo vesicular disminuido en los dos tercios inferiores del hemitórax izquierdo. Se le realizó rayos x de tórax, en el que se observó radiopacidad en los dos tercios inferiores del hemitórax izquierdo (fig. 1), ultrasonido (US) torácico y abdominal, y el primer diagnóstico radiológico, fue de una neumonía de base izquierda para la cual se intuye tratamiento.
El paciente dejó de vomitar al segundo día de su ingreso, pero al tercer día comenzó nuevamente con vómitos biliosos refractarios a tratamiento antiemético. Se realizó una nueva evaluación clínico radiológica (con estudio de esófago, estómago y duodeno), en la que se observó una gran dilatación gástrica, del marco duodenal y la primera asa intestinal, que se perdía a nivel del diafragma, y no había paso del contraste al resto del intestino. Con este cuadro clínico radiológico se planteó el diagnóstico de oclusión intestinal por HDC.
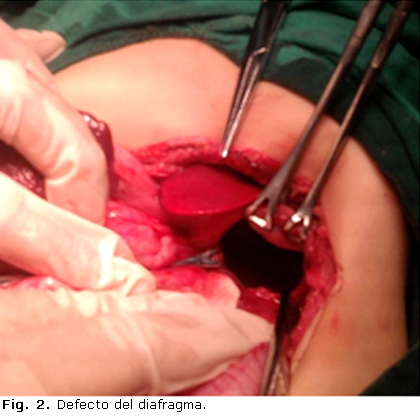
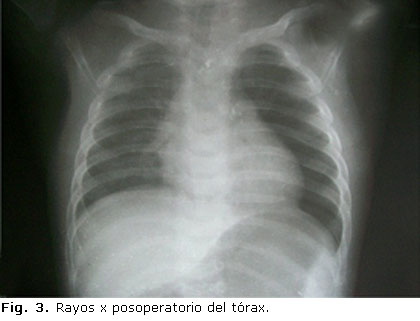
Se realizó laparotomía exploradora, y se encontró en el abdomen el estómago muy distendido, el duodeno y el colon descendente, y el bazo desplazado hacia abajo, fuera del hipocondrio izquierdo. Existía un gran defecto en el hemidiafragma izquierdo (fig. 2), y dentro del tórax se encontraban todas las asas delgadas, ciego, colon ascendente y transverso, todo el intestino estaba colapsado, pero se recuperó rápidamente después de haberlo colocado en el abdomen y aplicarle compresas tibias. El pulmón, que estaba pequeño y replegado hacia el vértice del hemitórax, se recuperó en los primeros 5 días (fig. 3) sin necesidad de ventilación asistida, y no existieron complicaciones posoperatorias, por lo que el paciente fue dado de alta a los 7 días y seguido por consulta externa con evolución satisfactoria.
DISCUSIÓN
La HDC es una enfermedad relativamente poco frecuente y generalmente se le consideró una enfermedad mortal a principios del siglo XX. A pesar de los muchos adelantos en el diagnóstico prenatal, y del cuidado médico y quirúrgico a estos niños, la HDC continúa siendo una enfermedad de alto riesgo de mortalidad,5 sobre todo, cuando se presenta en el período neonatal, o cuando su presentación tardía es por una complicación digestiva del tipo de abdomen agudo. Nuestro paciente es un varón con antecedentes de oligoamnios, que se complicó a los 5 meses de edad, con un cuadro oclusivo por HDC de la variedad posterolateral izquierda.
Cuando se revisa la literatura se encuentra que la HDC en el 95 % de los casos se debe a un defecto posterolateral (Bochdalek) del lado izquierdo, y precisamente debido a su mayor incidencia, es que para muchos autores el término HDC se reserva para esta variedad.6-8 La presentación bilateral es rara (1 %) y casi siempre fatal, las anteriores, de Morgagni, se presentan en un 2 %, y lo que resta corresponde a hernias a través del hiato esofágico.9
La mayoría de los autores coinciden en que existe una prevalencia del sexo masculino. Ulises Tabares presentó un estudio de 11 pacientes con HDC de presentación tardía, 7 de ellos varones. De estos 11 pacientes, 2 comenzaron con un cuadro de dificultad respiratoria aguda sin antecedentes de síntomas respiratorios previos, 7 con cuadros respiratorios recurrentes y 2 con cuadro de oclusión gastrointestinal parcial. En una serie de 362 pacientes estudiados, predominó el sexo masculino en una relación de 2 a 1.3
Gracias a los avances tecnológicos, actualmente la HDC puede diagnosticarse por ecografía prenatal, si se encuentran vísceras abdominales dentro del tórax. En caso de que la hernia sea derecha, el diagnóstico prenatal es más difícil, debido a la similitud ecográfica que presentan el hígado y el pulmón fetal, pero en estos casos puede ayudar una imagen sugerente de vesícula biliar en el tórax.10
Actualmente existe la posibilidad de realizar resonancia nuclear magnética fetal, lo que permite precisar el grado de hipoplasia pulmonar y la posición de vísceras sólidas como el hígado. Se debe estudiar al feto para descartar otras anomalías. La amniocentesis, o la biopsia de las vellosidades coriónicas, se realizan para descartar anomalías cromosómicas o metabólicas. Si la HDC es una anomalía aislada, existen criterios para corregir el defecto en el feto.5
Después del nacimiento el diagnóstico se hace por el cuadro respiratorio, dado por cianosis, polipnea, presencia de abdomen excavado, latido cardiaco audible en el hemitórax derecho, así como ruidos hidroaéreos audibles en el tórax. Cerca del 64 % de los niños con HDC muere poco después del nacimiento, mientras que el 5 % o más vive asintomático por meses o años, antes de que se haga el diagnóstico (presentación tardía).1,7 En las revisiones hechas se comprobó que en estos casos el diagnóstico se hace cuando por alguna razón, por lo general una infección respiratoria o problemas gastrointestinales, se descubre en un estudio radiológico que tienen una hernia diafragmática, como ocurrió en nuestro pequeño paciente.
En el 20 al 70 % de las HDC se ha presentado polihidramnios, lo que se considera de mal pronóstico.9 La causa de polihidramnios parece deberse a una obstrucción de la unión gastroesofágica, del píloro o de ambos; el estómago se hernia hacia el tórax, y por lo tanto, impide la deglución del líquido amniótico.11
Es importante tener en cuenta otras enfermedades que pudieran confundir a la hora de realizar el diagnóstico diferencial, como serían las neumonías de base, la eventración diafragmática, la enfermedad quística del pulmón, la agenesia del pulmón y el secuestro pulmonar, entre otras.
Nuestro paciente fue tratado inicialmente como una neumonía de base, se pensó que el colapso intestinal encontrado en el acto quirúrgico pudiera explicar el error, al interpretar las imágenes y la ausencia de ruidos hidroaéreos a la auscultación. En cuanto a la presentación clínica, es evidente que difiere según el momento en que esta ocurra. Los niños que en el momento del nacimiento tienen hipoplasia pulmonar bilateral o unilateral presentan una insuficiencia respiratoria severa, durante las primeras horas de vida, dada por la hipertensión pulmonar secundaria a esa hipoplasia.
Los neonatos con hipoplasia pulmonar leve, cuya herniación ocurrió tardíamente en la gestación, pueden presentar los síntomas a las 24 horas de vida, y estarían dados por la tríada diagnóstica de: cianosis, disnea y dextrocardia aparente. A la exploración física el paciente presenta abdomen excavado, tórax en tonel, disminución o abolición del murmullo vesicular, así como la presencia de ruidos hidroaéreos en el tórax.
En la presentación tardía puede haber síntomas digestivos dados por vómitos, disfagia o dolor abdominal; o síntomas respiratorios, dados por disnea o dolor toráxico,1 los que conllevan a realizar estudios que sugieren la sospecha de la hernia.
Robledo-Ogazon plantea que las hernias sintomáticas son 9 veces más comunes en el hemidiafragma izquierdo, mientras que las hernias pequeñas, asintomáticas, son solo 2 veces más comunes en el lado izquierdo que en el derecho.1 Otros estudios revisados arrojan que el 65 % de niños con hernia derecha presentaron sintomatología dentro del primer año de vida, mientras que solamente 41,7 % pacientes con hernia izquierda pertenecieron a esta categoría de edad.3 Este punto es algo controversial, si tenemos en cuenta que muchas veces la proporción del contenido herniado no está en relación con el tamaño del defecto.
El 25 al 75 % de las HDC se asocian a otras anomalías,8 entre las que se encuentran las cardiacas, gastrointestinales, genitourinarias, neurológicas y esqueléticas. Alrededor del 10 % de todos los individuos con HDC tienen anomalías cromosómicas.12 Cerca del 20 al 40 % de los casos presentan un saco pleuroperitoneal,11 y la presencia o no de saco herniario juega un papel fundamental en la gravedad del cuadro.2,13 Generalmente las hernias pequeñas y las que tienen saco aparecen más tardíamente, con sintomatología insidiosa y menos grave. Las hernias diafragmáticas izquierdas o hernias de Bochdaleck, generalmente son grandes, no tienen saco, y en su mayor por ciento provocan síntomas precoces y graves, por lo que la conducta será definida en las primeras horas de vida.2,13,14
El contenido de la hernia varía en dependencia del lado afectado: en las derechas se involucran el hígado, el riñón derecho y grasa; sin embargo, cuando el defecto es izquierdo, puede contener el tubo digestivo, el bazo, el hígado, el riñón izquierdo, el páncreas o el epiplón.
Los objetivos de tratamiento diferirán según presenten o no síntomas. En las hernias que aparecen en la etapa neonatal, la cirugía urgente del defecto se consideraba anteriormente esencial para corregir la insuficiencia respiratoria. Después de la cirugía existía un período de aparente estabilidad clínica, que es llamado por muchos autores como luna de miel de la hernia diafragmática; sin embargo, horas o días después ocurría un deterioro caracterizado por hipoxia, acidosis y muerte.8
Actualmente existe la tendencia a diferir la operación por 24 horas o más, para lograr una ventilación óptima estable, con la esperanza de reducir o eliminar la hipertensión pulmonar reactiva, pues se ha demostrado que la cirugía está asociada con un deterioro de la elasticidad pulmonar, que puede mejorarse con estabilización preoperatoria. Varios informes publicados en la década de 1980 sugirieron que la supervivencia no era diferente con reparación retardada, y recomendaron un período de estabilización anterior a la operación, por lo que no es necesaria la cirugía de urgencia.15,16
Muchos cirujanos pediátricos están empleando actualmente una estrategia de demora durante un cierto período antes de la corrección del defecto, para lograr un nivel mínimo de apoyo respiratorio, documentar la ausencia de hipertensión pulmonar, mostrar una mejoría de la elasticidad pulmonar, o para demostrar que el aspecto radiográfico del pulmón ha mejorado antes de la reparación.15 Se han utilizado estrategias de ventilación alternativas como la hipercapnia permisiva, la administración de óxido nítrico y la ventilación líquida para estabilizar a estos neonatos antes de la intervención quirúrgica, o como terapia de rescate posterior a la cirugía. La oxigenación con membrana extracorpórea (OMEC) se ha usado como un modo alternativo de apoyo ventilatorio en niños con hipoxemia severa e insuficiencia respiratoria en el período preoperatorio, intraoperatorio y posoperatorio.15,17
En resumen, actualmente existe la tendencia a evitar la operación de emergencia y permitir cierto período de estabilización antes de la reparación. Datos publicados de un registro de más de 1 000 pacientes con HDC indican que la mayoría de los cirujanos pediátricos utilizan en la actualidad una estrategia de retraso de la corrección del defecto durante algún período, con el 62 % de pacientes que reciben la operación más allá de las 24 horas de vida.15
En el caso de que la hernia se presente tardíamente de forma asintomática, se debe realizar su cirugía electiva para evitar futuras complicaciones. En cuanto a la vía de acceso existen controversias, pero a la hora de tratar las hernias izquierdas la mayoría autores apoyan el acceso abdominal, ya que tiene mayores ventajas para el reconocimiento de malrotaciones y su tratamiento.18 Apoyamos esta vía, pues creemos que es la más factible para tratar probables lesiones de los órganos intraabdominales, y la reparación del defecto es posible de forma expedita. El acceso por vía abdominal permitirá una mayor facilidad de reducción del contenido herniario, así como la correcta identificación de otras lesiones acompañantes, tanto diafragmáticas como a cualquier otro nivel de la cavidad abdominal.
La reparación transtorácica es la de elección para hernias derechas, y en los casos agudos la vía abdominal es la más recomendada. Más recientemente se han utilizado con buenos resultados técnicas por toracoscopia y laparoscopia para la resolución del padecimiento, sin embargo, todos los autores coinciden en que este tipo de tratamiento representa mayor tiempo quirúrgico.1,19 La solución quirúrgica de este defecto antes del parto tiene futuro promisorio, aunque en nuestro medio no hay experiencia al respecto.
De forma general el tratamiento persigue 3 objetivos: diferenciar entre casos asintomáticos y sintomáticos, reducir el contenido abdominal, así como reparar el defecto.
Las complicaciones más comunes de un paciente operado para corrección de una hernia diafragmática son la obstrucción intestinal por bandas fibrosas, el reflujo gastroesofágico y la hernia hiatal, y el pronóstico depende del tipo de presentación clínica. El índice de mortalidad para cirugía electiva es de menos de 3 %, pero se eleva a 32 % cuando se presenta de forma aguda, cuando el diagnóstico se retrasa, o se desarrolla alguna complicación (isquemia gástrica, necrosis de intestino delgado, oclusión colónica, e incluso, síndrome compartimental abdominal).1 Las HDC diagnosticadas antes de las 25 semanas de gestación y/o que contienen hígado, condicionan un peor pronóstico.
Otro factor pronóstico utilizado es el índice ecográfico lung to head ratio (LHR, relación pulmón/cabeza), medido entre las 22 y 27 semanas de gestación. Valores de LHR bajos indican mayor hipoplasia pulmonar y peor sobrevida. Se ha evidenciado menor sobrevida ante la presencia de malformaciones o síndromes asociados.8
En las pequeñas hernias que aparecen clínicamente cuando se estrangula una porción del contenido intestinal, o que suponen un hallazgo casual, el desarrollo pulmonar es bueno y la mortalidad es muy baja. Puede resumirse, que el principal factor pronóstico en estos niños es el grado de desarrollo de los pulmones, que se han visto comprimidos durante su periodo de desarrollo intrauterino en grado variable.10
Se concluye que a pesar de que la HDC es una enfermedad no muy frecuente en el recién nacido, la de aparición tardía es una entidad bien descrita, y aunque poco frecuente, se debe sospechar en los pacientes que, independientemente de la edad, presenten sintomatología -respiratoria o gastrointestinal- que no se soluciona con tratamiento convencional. Habitualmente su diagnóstico se establece de 2 maneras: por un hallazgo incidental en estudios imagenológicos, o porque aparezcan complicaciones secundarias al paso de las vísceras al tórax, que pueden provocar dolor torácico intenso, así como encarceración, estrangulación o perforación de las vísceras intratorácicas.1
REFERENCIAS BIBLIOGRÁFICAS
1. Felipe Robledo-Ogazón. Hernia diafragmática congénita en el adulto. Informe de un caso. Cir Ciruj. 2008;76:61-4.
2. Rodríguez Núñez BR. A propósito de un lactante de 3 meses con hernia diafragmática congénita. MEDICIEGO [serie en Internet]. 2000 [citado 10 de agosto 2012];6(2). Disponible en: http://www.bvs.sld.cu/revistas/mciego/vol6_02_00/casos/c2_v6_0200.htm
3. Tabares Martínez-Carreño U. Hernia diafragmática congénita de presentación tardía: una serie de casos. Rev Mex Cirugía. 2008;15(1):6-9.
4. Congenital Diaphagmatichernia Study Group: Late-presenting congenital diaphagmatic hernia. J Pediatr Surg. 2005;40:1839-43.
5. Navarrete-Arrellano M. Hernia diafragmática congénita izquierda. Presentación de un caso. Rev Sanid Milit Mex. 2006;60(3):195-8.
6. Gaougaou R. Hernia diafragmática congénita. Form Med Contin Aten Prim. 2011;18(8):528-9.
7. Baeza C. Complicaciones tardías imprevistas de las hernias diafragmáticas. Acta Pediatr Mex. 2011;32(6):319-22.
8. García H. Factores pronósticos asociados a mortalidad en recién nacidos con hernia diafragmática congénita. Gaceta Médica Mex. 2003;139(1):7-14.
9. Bolaños Nava I. Hernia diafragmática congénita. Rev Mexicana de Anestesiología. 2005;28(1):126-8.
10. Muñiz Escarpanter J, Veitía Collazo L. Hernia diafragmática congénita. Medisur [serie en Internet]. 2005 [citado 13 de septiembre de 2012];3(5). Disponible en: http://www.medisur.sld.cu/index.php/medisur/article/view /156
11. Blank C. Nuevos conceptos de terapia neonatal en el manejo de la hernia diafragmática congénita. Acta Pediatr Méx. 2002;23(6):363-8.
12. Arráez-Aybar LA. Hernia diafragmática paraesternal de Morgagny-Larrey en adulto. Rev Esp Enferm Dig. 2009;101(5):357-66.
13. Kurzenne JY, Sapin E. Hernies diaphragmatiques congenitales: 120 cases neo-nataux. Etude preliminaire. Chir Pediatr. 1988;29:11-7.
14. Welch Kenneth J, Randolph Judson G, Ravitch Mark M. Pedriatic Surgery. 4ta ed. Nueva York: Medical Publishers INC; 1986. p. 589-99.
15. Moyer V. Corrección quirúrgica tardía versus corrección temprana de la hernia diafragmática en recién nacidos. La Biblioteca Cochrane Plus [serie en Internet]. 2008 [citado 10 de agosto de 2012];(4). Disponible en: http://cochrane.bvsalud.org/cochrane/main.php?lib=BCP&searchExp=Herniaanddiafragmaticaandcongenita&lang=es
16. Cartlidge PH, Mann NP, Kapila L. Preoperative stabilisation in congenital diaphragmatic hernia. Arch Dis Child. 1986;61:1226-8.
17. Lally KP, Paranka MS, Roden J. Congenital diaphragmatic hernia. Stabilization and repair on ECMO. Ann Surg. 1992;216:569-73.
18. Asz-sigall J. Vólvulo gástrico intratóracico y hernia diafragmática congénita de diagnóstico tardío. Informe de u caso. Acta Pediatr Mex. 2010;31(1):32-5.
19. Brusciano L, Izzo G, Maffettone V, Rossetti G, Renzi A, Napolitano V, et al. Laparoscopic treatment of Bochdalek hernia without the use of a mesh. Surg Endosc. 2003;17:1497-8.
Recibido: 21 de enero de 2013.
Aprobado: 1º de abril de 2013.
María Eugenia Ferro Moreira. Hospital Pediátrico "Juan Manuel Márquez". Avenida 31 y calle 76, municipio Marianao. La Habana, Cuba. Correo electrónico: marige.ferro@infomed.sld.cu