Introducción
La colocación paliativa de stents mediante cateterismo cardiaco en recién nacidos con cardiopatías congénitas complejas se realiza usualmente en medio de situaciones clínicas difíciles tales como insuficiencia cardiaca, distrés respiratorio, uso de ventilación mecánica y soporte inotrópico con aminas. El bajo peso que estos pacientes usualmente presentan dificulta el proceder intervencionista y favorece la presencia de complicaciones. Sin embargo, el uso de stents en estos niños permite que puedan llegar a una cirugía correctiva, paliativa o trasplante cardiaco; de lo contrario fallecen en las primeras horas de nacido.1,2,3,4) El objetivo del presente trabajo es evaluar el resultado del implante percutáneo de stent en pacientes recién nacidos con cardiopatías congénitas complejas.
Presentación de casos
Se presentan cinco pacientes con cardiopatías congénitas complejas. Dos pacientes con diagnóstico de síndrome de hipoplasia de cavidades izquierdas (SHCI) y otros tres pacientes con los diagnósticos de coartación aórtica, interrupción del arco aórtico y atresia pulmonar. Se obtuvo consentimiento informado de los padres en cada caso.
La mayoría de los pacientes presentaron signos de insuficiencia cardiaca congestiva, se medicaron con dosis elevadas de furosemida y espironolactona y requirieron además inotrópicos como epinefrina, dobutamina, dopamina y milrinona, según el caso. Todos los pacientes mostraron dependencia a la administración de prostaglandina E1 para mantener la permeabilidad del ductus arterioso. Los procederes intervencionistas se realizaron con anestesia general, bajo intubación endotraqueal y ventilación mecánica. Después de ser puncionada la arteria femoral se administró heparina EV a 100 u/kg la cual se mantuvo en terapia intensiva en infusión continua por 7 días como promedio. Se administró cefazolina como tratamiento antibiótico profiláctico. La administración de prostaglandina E1 se interrumpió inmediatamente después que se canalizó la arteria femoral en todos los casos, excepto en el caso de coartación aórtica en el cual este medicamento se mantuvo todo el tiempo del proceder y se fue retirando progresivamente en la unidad de terapia intensiva. En los cinco pacientes se utilizó introductor arterial 4F que se intercambió posteriormente por introductor 5F. Una vez en la aorta se avanzó catéter coronario derecho 5F hasta sitio de la lesión, ya sea el ductus o la zona coartada. Se utilizó guía Choice intermediate 0.014 X182 cm /J- Tip, Boston Scientific en la paciente con atresia pulmonar y en el resto, guía coronaria Galeo de punta flexible y configuración en J de 0.014 (Galeo F .014/J- Tip, Biotronik SE &Co. KG). En todos los casos se realizó angiografía en proyecciones lateral y frontal. Se determinó el diámetro y longitud de las lesiones mediante calibración de rejilla del angioscopio. Se introdujo a través de la guía el catéter - balón con el stent premontado a utilizar sin el uso de vainas de liberación. Se utilizó un protector para el stent al pasar este por la vaina del introductor. Se procedió al inflado del balón hasta impactar dicho stent en las paredes del ductus arterioso o de la aorta, según el caso. Se procedió posteriormente a realizar angiografía demostrativa de la permeabilidad del stent y en el caso de la coartación aortica se realizó toma de presiones en la aorta pre- y posstent.
Se realizó en otro momento, mediante cirugía, cerclaje de la arteria pulmonar a tres de estos pacientes. La enfermedad de los pacientes, el sitio de colocación del stent, así como la edad (mediana 28 días, rango 4-31 días), sexo y peso (mediana 2 700 gramos, rango 1 800-3 500 gramos) se resumen en la tabla.
Tabla Características generales
| Paciente No. | *Edad (dias) | Sexo | Peso (gramos) | Enfermedad | Proceder intervencionista |
|---|---|---|---|---|---|
| 1 | 4 | Femenino | 3 180 | **SHCI | ***Stent en PCA |
| 2 | 31 | Masculino | 1 820 | Coartación aortica | Stent en aorta |
| 3 | 30 | Femenino | 3 500 | SHCI | Stent en PCA |
| 4 | 28 | Femenino | 1 800 | Interrupción arco aórtico | Stent en PCA |
| 5 | 5 | Femenino | 2 700 | Atresia pulmonar | Stent en PCA |
*Edad a la que se realizó el cateterismo cardiaco intervencionista
**SHCI: síndrome de hipoplasia de cavidades izquierdas
*** PCA: persistencia del conducto arterioso
Los resultados de cada caso en particular (tabla 1) se describen a continuación. La primera paciente se diagnosticó como hipoplasia de cavidades izquierdas y presentó al examen ecocardiográfico un ventrículo izquierdo hipodesarrollado, tracto de salida del ventrículo izquierdo hipoplásico (2,1mm), raíz aortica de 1,9 mm, la aorta ascendente de solo 2,7mm, la válvula mitral atrésica y como cardiopatías acompañantes una comunicación interventricular (CIV) en su porción muscular de 2,9 mm, una comunicación interauricular (CIA) fosa oval de 8,1 mm y un conducto arterioso persistente (PCA) de 5 mm de diámetro en su sitio más estrecho que se confirmó por cineangiografía. Mediante el proceder realizado se colocó en el PCA stent periférico (RXHerculink Elite 5X15mm. 135cm) vía arteria femoral izquierda y se infló balón del stent a presión de 17 atmósferas para lograr un diámetro final del stent de5,6 mm (Fig. 1). La paciente llegó a la sala de hemodinámica con apoyo inotrópico de dobutamina y previo a la colocación del stent se le añadió epinefrina a 0,018 mcg/kg/min. Inmediatamente después de terminarse el proceder intervencionista la paciente estuvo estable hemodinámicamente y trasladada al salón de cirugía cardiovascular donde se le realizó cerclaje de ambas ramas pulmonares.
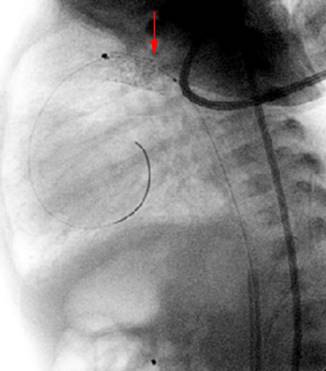
El segundo paciente, con diagnóstico ecocardiográfico de coartación aórtica tuvo como antecedente ser un segundo gemelar, pretérmino con 36,2 semanas. En el ecocardiograma se encontró adicionalmente arco aórtico hipoplásico de 2,5 mm de diámetro a partir de la emergencia del tronco arterial braquiocefálico con segmento alargado hasta el istmo aórtico donde termina coartado, aorta bivalva, CIV fibromuscular de entrada de 4,4 mm de diámetro, CIA tipo fosa oval de 2 mm y vena cava izquierda persistente. Se constató durante el cateterismo cardiaco diámetro aórtico precoartación de 3,5 mm, en el segmento coartado diámetro de 1,2 mm y poscoartación 4,3 mm. El segmento coartado midió 6 mm de longitud y en la aorta abdominal a nivel del diafragma se documentó diámetro de 3,5 mm. El gradiente de presión inicial a nivel de la coartación fue de 60 mmHg. Después de colocado el stent se recogió gradiente de presión a ese nivel de 20 mmHg. El paciente también fue abordado vía arteria femoral izquierda y se colocó en la zona coartada dispositivo Jostent 4.5 X 12 mm (Fig.2). Como complicaciones el paciente presentó parada cardiaca de 30 segundos de duración que requirió medidas de reanimación cardiovascular y además presentó compromiso arterial en el miembro inferior izquierdo para lo cual fue tratado con heparina. El paciente llega al proceder con infusión de dobutamina a 5 mcg/kg/min y es necesario incrementar esta dosis hasta 8,7 mcg/kg/min. Se traslada a terapia intensiva donde sigue necesitando ventilación mecánica y medicamentos de apoyo por lo que se realizó cerclaje de la arteria pulmonar 14 días después de colocado el stent.

Fig. 2 Angiografía aortica. A: plano frontal. B: plano lateral. Coartación aortica (flecha). C: plano frontal. Stent en sitio de la coartación (flecha).
La tercera paciente de la serie tiene diagnóstico de SHCI con hipoplasia marcada del ventrículo izquierdo, atresia valvular aortica e hipodesarrollo del anillo mitral (relación mitro-tricuspídea de 0,38). Como defectos estructurales acompañantes presentó un PCA de 5 mm de diámetro y una CIA fosa oval de 5,3 mm. A esta paciente se le realizó diagnóstico prenatal de su cardiopatía y se le realizó cesárea a la madre a las 40 semanas de edad gestacional en una institución cercana al Cardiocentro Pediátrico
Se instauró tratamiento con prostín dentro de la primera hora de nacida y se trasladó ese mismo día al Cardiocentro donde de forma temprana presentó manifestaciones de insuficiencia cardiaca severa y se decidió realizar primero el cerclaje de las ramas pulmonares a las 72 horas de nacida y 47 días después se procedió a la colocación del stent en el ductus. Este proceder se realizó con infusión continua de epinefrina, la cual se pudo retirar dos días después de realizado este proceder. Se puncionó en este caso la arteria femoral derecha. El diámetro del PCA obtenido por angiografía fue de 5,6 mm. Se colocó dispositivo Omnilik 7.0 X 28 mm. 135cm en el PCA para obtener diámetro final en la luz del dispositivo de 7,76 mm.“William Soler.”
La cuarta paciente presentó una interrupción del arco aórtico tipo B, una comunicación interventricular subaórtica de 5 mm y una comunicación interauricular tipo fosa oval de 3 mm. El PCA en su sitio más estrecho midió 2,1 mm de diámetro. Se colocó stent Herculink Elite 5 mm dejándolo impactado y permeable en el PCA. Esta paciente llegó al hospital con cianosis generalizada intensa, bradicardia, hipotensión arterial sistémica y sospecha de sepsis, requirió intubación endotraqueal, ventilación mecánica y apoyo con drogas inotrópicas (dobutamina). El proceder de cateterismo intervencionista se realizó en medio de condiciones clínicas muy difíciles. No fue posible realizarle cerclaje pulmonar por la sepsis e inestabilidad hemodinámica severa y fallece 27 días después del proceder en evento no relacionado directamente con la intervención sino con un cuadro de disfunción múltiple de órganos.
La última paciente de nuestra serie, presentó una atresia pulmonar con cianosis significativa acompañada de CIV de entrada de 7,7 mm, comunicación interauricular tipo fosa oval de 4,5 mm, situs inversus, mesocardia, mesoápex y arco aórtico derecho. En este caso se colocó en el ductus stent periférico del tipo RxHerculink Elite 5.0 X 15 mm y se infló el balón a 11 atm (presión nominal) con permeabilidad del PCA.
Discusión
Todos los pacientes se abordaron vía retrógrada arterial similar a otros estudios5 sin utilizar vainas de liberación y con stents premontados de muy bajo perfil, lo cual es muy favorable sobre todo en los niños con escaso peso corporal.6) Para la colocación del stent el operador efectuó angios manuales realizados desde el puerto lateral de los introductores. Este es un momento crítico del proceder ya que una mala ubicación del stent, en los casos de su colocación en el ductus, pudiera hacerlo protruir hacia el tronco de la arteria pulmonar y ramas pulmonares7,8 o hacia la aorta. Por otro lado, la selección de un stent más pequeño que el ductus pudiera favorecer el cierre natural del ductus en el sitio no cubierto por el stent. En el caso de coartación aortica para la liberación del stent es necesario tener en cuenta dejar fuera de su alcance los vasos del cuello.
En los pacientes con indicación de implante de stent y cerclaje de la arteria pulmonar, se realizó un proceder combinado en el cual la toma de la decisión de cuál de los dos procederes realizar primero ya sea el proceder intervencionista (colocación de stent) o el quirúrgico (cerclaje pulmonar) estuvo relacionada con la situación clínica predominante: bajo gasto, distrés respiratorio o cianosis. La paciente con atresia pulmonar presentada en nuestro trabajo, solo fue tributaria de colocación del stent en el ductus ya que la sintomatología apremiante fue la cianosis y las manifestaciones de insuficiencia cardiaca consiguiente que se manejaron clínicamente sin requerir aparentemente cerclaje pulmonar. No obstante, es conocido que la colocación de stent y el cerclaje de la arteria pulmonar, en los casos con indicación de ambos procederes, deben acometerse en un tiempo corto, mientras más próximo uno de otro mejor.9 En nuestra serie, el deterioro hemodinámico de nuestros pacientes no lo permitió de esa manera, y por otro lado, carecemos de los llamados
con lo cual se facilita el abordaje de los pacientes y se evita su traslado desde un salón a otro.10“salones híbridos”
Los resultados del presente estudio demuestran la factibilidad y eficacia de la colocación de stents en un grupo de pacientes donde se requiere un mayor peso corporal y una adecuada estabilidad hemodinámica para mejores indicadores de morbilidad y mortalidad quirúrgica. Se demuestra además que la presentación clínica del paciente puede actuar como guía para precisar el momento adecuado para realizar el proceder de implante del stent.
Podemos concluir que la colocación de stent en el grupo de pacientes analizado es factible y el momento de su implante según el evento hemodinámico apremiante pudiera ser una forma alternativa del cateterismo cardiaco.