Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Obstetricia y Ginecología
versión impresa ISSN 0138-600Xversión On-line ISSN 1561-3062
Rev Cubana Obstet Ginecol v.32 n.2 Ciudad de la Habana Mayo-ago. 2006
Hospital Ginecoobstétrico Docente Sur de Santiago de Cuba Mariana Grajales Coello
Misoprostol en la inducción y fase latente del trabajo de parto
Al inicio de la década del 30, Kurzrok Lieb (1930), Goldblatt (1933) y Von Euler (1935), trabajando en forma independiente observaron que extractos de las glándulas genitales de mamíferos inducían actividad en preparaciones de músculo liso aislado. Von Euler identificó el compuesto activo como un ácido liposoluble que denominó prostaglandina, al considerar que estas eran producidas por la próstata.
La prostaglandina es un término genérico que denomina a una familia de ácidos carboxílicos de 20 átomos de carbono, 5 de los cuales forman un anillo ciclopentano, por lo que se ha tomado como estructura hipotética el ácido prostanoico. Las prostaglandinas endógenas son antacoides y se forman en todos los tejidos, aunque en pequeñas cantidades, así como en líquidos orgánicos y se le conceden múltiples efectos biológicos que abarcan prácticamente todas las funciones del organismo.
En el campo de la obstetricia, por sus efectos sobre la actividad contráctil del músculo uterino y la madurez del cérvix, se emplea en muchos lugares del mundo.
En 1985 el misoprostol fue por primera vez registrado bajo la marca del fabricante como Cytotec y fue rápidamente aceptado en múltiples países para el tratamiento de la úlcera péptica y en los pacientes que ingerían antiinflamatorios no esteroideos (NSAIDS).
Es verdaderamente sorprendente la cantidad de literatura que actualmente evidencia el uso de misoprostol en el campo de la obstetricia y la ginecología. Parece ser, según opiniones muy autorizadas, la más apropiada de todas las prostaglandinas para emplear en la práctica de esta disciplina.1,2
Características
El misoprostol, (Cytotec, Searle) es análogo de la prostaglandina; E1 metilada a partir del carbono,16 es de bajo costo y se almacena con facilidad a la temperatura ambiente, así como presenta pocos efectos secundarios sistémicos. El mismo se absorbe con rapidez por vía oral, vaginal, rectal y sublingual.
Estudios recientes señalan que el misoprostol puede usarse con seguridad en pacientes con enfermedades subyacentes como asma bronquial y algunos desórdenes cardiovasculares en contraste con otras prostaglandinas.
La mayor parte de la degradación de las prostaglandinas, en la que se incluye el misoprostol , se produce por la 15 hidroxilo prostaglandina deshidrogenasa sobre el grupo 15 hidroxilo, por lo que un proceso de metilación permite bloquear la acción de esta enzima y crear un compuesto estable y de una adecuada duración.
En estudio realizado, el pico medio sérico del ácido, el misoprostol después de la administración oral, es de 227 picogramos por mL y luego de la administración vaginal de 167 picogramos por mL; los tiempos para alcanzar los niveles máximos son de 34 y 80 minutos respectivamente.
No se conoce con exactitud cómo se absorbe el fármaco, y se desconoce si es capaz de atravesar la placenta o de excretarse en la leche materna, el misoprostol experimenta una extensa metabolización de primer paso, produciendo el metabolito más importante y activo, el ácido misoprostólico .
Por vía oral es rápidamente absorbido, extensamente metabolizado y se estima que el grado de absorción oral es de un 88 %. El misoprostol es rápidamente metabolizado por el sistema de oxidantes de ácidos grasos del organismo. Más recientemente se ha señalado que por esta vía puede alcanzar concentraciones máximas más rápidas que la anteriormente señaladas entre 15 y 30 min y que desaparecen con una vida media aproximada de 21 min.
Sin embargo, los beneficios de la vía vaginal se señalan a un mayor tiempo de actividad plasmática, así como a menos efectos colaterales que la vía oral, contrastando con la alta eficacia de la primera, que por estas razones ha logrado imponerse.3-7
Mecanismo de acción
El mecanismo de acción está mediado por receptores específicos, algunos de sus efectos colaterales requieren de activación o inhibición de la adenilciclasa con regulación de la producción del monofosfato cíclico de adenosina (AMPc).
Las prostaglandinas en general aumentan el AMPc intracelular en algunos tejidos, mientras que en otros lo reduce o se opone a su aumento. En otros tejidos el mediador intracelular es el monofosfato cíclico de guanosina (GAMPc); otras veces el mecanismo intracelular es independiente de los nucleótidos cíclicos, como por ejemplo, la acción sobre el músculo liso vascular de la prostaglandina E 2 y sobre el miometrio de la prostaglandina E 2 y F 2 α. En estos casos actúa facilitando la entrada del ión calcio y otros iones a la célula, en este proceso inhibe el secuestro de calcio por la ATP asa dependiente del calcio en el retículo endoplásmico y de este modo aumenta la concentración del calcio citoplasmático; un proceso que lleva a la activación de la linaza de cadena ligera de la miosina, a la fosforilación de la miosina y de este modo a la interrelación de la miosina fosforilada y la actina y, por lo tanto, el aumento de la actividad contráctil.
Se invoca además que a nivel del músculo uterino produce aumento de la actividad de los receptores de oxitocina permitiendo una mayor acción biológica de esta hormona.
El mecanismo de acción para la maduración cervical está basado en la actividad de esta sustancia sobre los componentes del cérvix, el cual está constituido por músculo liso, colágeno y tejido conectivo que constituye la sustancia base donde se forman compuestos importantes del cérvix (glucosaminoglicano).
El contenido muscular del cérvix varía de arriba a bajo de un 25 a un 6 %. La disminución del colágeno, elemento que da rigidez al cuello, se produce al final del embarazo por digestión proteolítica del mismo, en este proceso intervienen las colagenasas que están presentes y que son activadas al final de la gestación.
En el tejido conectivo se encuentran los glucosaminoglicanos que desempeñan importantes funciones en la resistencia cervical y posteriormente en la maduración del cuello, cuando se produce un cambio en la correlación de las concentraciones entre ellos. El sulfato de dermatán y el condroitil sulfato se mantienen predominando durante el embarazo, dándole fijeza a la fibra colágena, pero al final del embarazo disminuyen las concentraciones de los mismos y predominan las del ácido hialurónico, que es de ellos el que menos fija la fibra colágena y permite la entrada de agua al cérvix, disminuyendo la textura del mismo. Puede resumirse que un cambio de los glucosaminoglicanos al final del embarazo permite que el cuello alcance una consistencia blanda. Este proceso es inducido por el misoprostol.8-9
Comentarios
En el año 1987 Mariani Neto fue el primero en utilizarlo por vía oral para la inducción del trabajo de parto tras el diagnóstico de muerte fetal y posteriormente describió la taquisistolia como un patrón de 5 contracciones en 10 minutos durante 20 minutos y de hipersistolia-hipertonía como una contracción de más de 2 min de duración, o el síndrome de hiperestimulación uterina dado por taquisistolia o hipersistolia uterina con cambios en la frecuencia cardiaca fetal. Cuttis más adelante definió los términos de forma más simplificada: hiperestimulación con alteración de la frecuencia cardiaca fetal o hiperestimulación sin alteración de la frecuencia cardiaca fetal.4-10
Un problema debatido en relación con esta complicación del uso del misoprostol es buscar la dosis óptima. El rango de dosis utilizado. En el mundo en la maduración e inducción del parto ha estado entre 12,5 μg y 100 μg, y muchos estudios se han dirigido a la búsqueda de la dosis ideal.11-13
En el servicio de obstetricia del hospital ginecobstétrico docente sur de Santiago de Cuba comenzamos a utilizar la dosis de 50 μg para la maduración e inducción definitiva del parto, el rango de polisistolia fue de un 8 % y de hiperestimulación de un 4 %, más bajo que lo expresado por otros autores; después de un año de trabajo se redujo la dosis a 25 μg, obteniéndose resultados muy satisfactorios, el rango de hiperestimulación ha sido de un 2 % y de polisistolia de un 4 %.
Los reportes en la literatura con respecto al indicador cesárea han sido controvertidos, aunque la mayoría abogan por una reducción de este indicador. En 1999 Cochar Pregnacy and Chilberth group, señaló una reducción de un 48 % del indicador cesárea.
En el hospital ginecobstétrico docente sur de Santiago de Cuba la cesárea primitiva se ha mantenido en un rango entre un 7 y 13 % en los años 2000-2004, llegando a tener un indicador de cesárea global de 15,9 % en el año 2000.
Una posible explicación para los diferentes hallazgos entre los diferentes estudios clínicos en relación con la cesárea puede tener su explicación en las diferentes formas de manejo de la hiperestimulación y en una política de recurrir tempranamente a la cesárea para resolver esta eventualidad.4-14
La mayoría de los estudios que comparan el misoprostol con otras prostaglandinas lo han hecho con la dinoprostona en gel, y hay consenso en aprobar el misoprostol como más efectivo y económico, evidenciándose además un mayor número de partos en menos de 24 horas, menor uso de oxitocina y cesárea con la utilización del misoprostol.15-19
Efectos beneficiosos
- Disminuye el índice de inducción fallida.
- Disminuye el tiempo de inducción e inicio del trabajo de parto.
- Disminuye el tiempo de inducción y parto.
- Disminuye el indicador cesárea.
- Disminuye la hemorragia posparto.
- Se plantean beneficios sobre el puntaje de Apgar .
- En nuestro medio ha alcanzado la novedad de ser el agente indicado como terapéutica de base etiológica en el tratamiento de la fase latente prolongada.
Misoprostol en la fase latente del trabajo de parto
La fase latente prolongada constituye una variedad del parto disfuncional que puede comportarse incluso como disfunción primaria con efectos negativos posteriores sobre la fase activa, con resultados que pueden ser desfavorables sobre la madre y el producto de la concepción.
Después que Friedman en 1954 graficara el comportamiento del trabajo de parto, sus resultados han sido aplicados en muchas latitudes, en épocas recientes otros autores han aceptados como favorables acortar el tiempo para definir la fase latente como prolongada y buscar una intervención más temprana que beneficie el binomio madre-feto.20-22
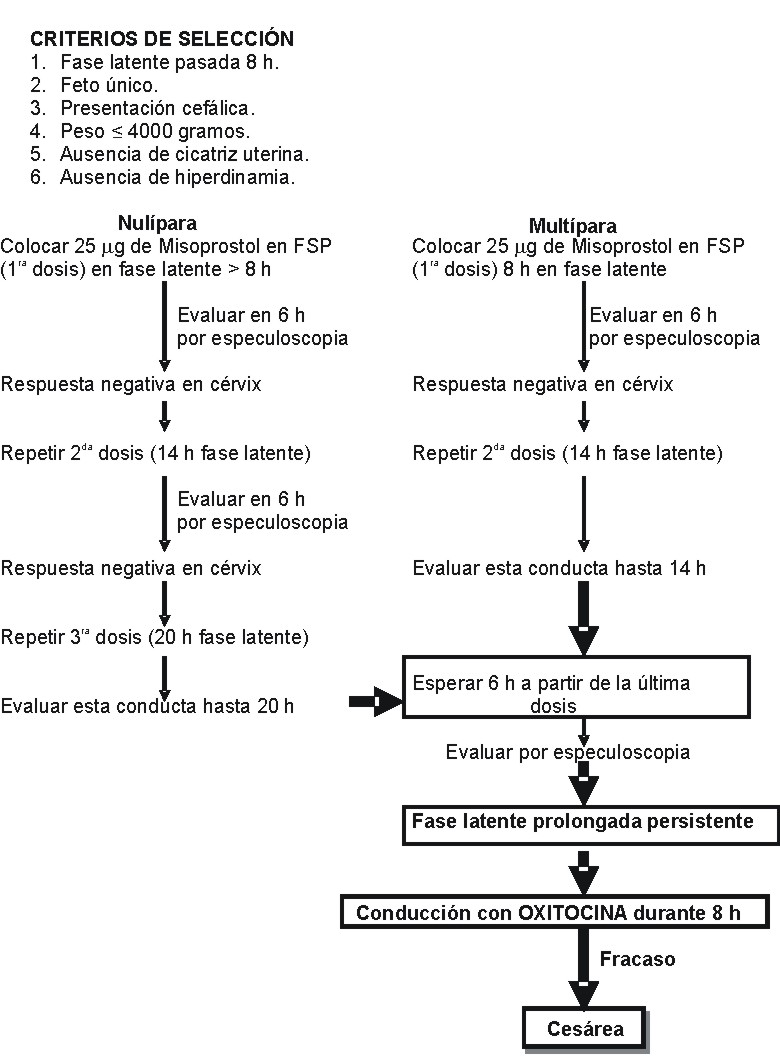
En el hospital ginecoobstétrico docente sur de Santiago de Cuba, se realizó un estudio de caracterización de la fase latente durante 5 años donde se demostró que el 85,2 % de las gestantes tenían una duración de la fase latente por debajo de las 8 h. En esta institución se emplea pasadas las 8 h de fase latente un protocolo que incluye el uso de misoprostol a dosis de 25 μg cada 6 h hasta un total de 3 dosis en nulíparas y de 2 dosis en multíparas (ver esquema). Con el mismo se ha reducido el tiempo en que se pasa a la fase activa en comparación con el método convencional, así como una reducción de las distocias de fase activa, del indicador cesárea y mejoras en los resultados materno perinatales. Esto se demostró mediante un ensayo clínico en el cual se utilizó el misoprostol en una nueva indicación: fase latente prolongada. Esta terapéutica es considerada como de base etiológica, teniendo en cuenta que la primera causa de este tipo de distocia es la inmadurez cervical y es definida como tratamiento activo no invasivo (TANI).
Anexo I: Introducción de madurez cervical con Pg (Misoprostol)
Método Iterativo
- Colocar 25mcg de Misoprostol en fondo de saco posterior.
- Seguimiento de FF y DU cada 30 min hasta que se establezca DU de 3 en 10.
- Luego FF y DU cada 15 min hasta que desaparezca la actividad uterina.
- Monitoraje fetal intermitente c/ 3 h con un mínimo de 30 min si disponibilidad.
De no lograrse el efecto deseado:
- Al día siguiente iniciar segundo ciclo, con igual dosis, previa evaluación del cérvix y perfil biofísico
- Repetir un tercer ciclo si fuera necesario.
- Si no desencadena trabajo de parto después de cumplido el tercer ciclo.
Anexo II: Método continuo
Inducción definitiva con Pg
- Colocar 25 μg de Misoprostol en fondo de saco posterior.
- Repetir igual dosis en 6 h, si se requiere.
Si no hay respuesta, después de dos dosis de 25 μg y se trata de una nulípara:
- Aumentar la dosis a 50 μg c/ 6h por 4 dosis (Total 250 μg)
Si paciente multípara:
- 25 μg c/6h hasta 6 dosis (Total 150 μg).
- Seguimiento de FF y DU cada 15 min.
- Monitoraje fetal intermitente cada 3 h por 30 min.
- Evaluación de cuello uterino cada 3 h después de iniciada actividad uterina útil (3-4 contracciones en 10 min).
Anexo III: Esquema fase latente > 8 h (TANI)
Referencias bibliográficas
1. Sampaio ZS, Almear CA, Feitosa FE, Amorim M. Factores asociados al parto vaginal en gestantes de alto risco submetidas à induzão do parto com Misoprostol. Rev Bras Ginecol Obstet 2004;26(1):21-9.
2. Valenti E. Guías de manejo. Inducción al trabajo de parto. Rev Hosp Matern Infant. Ramón Sardá . 2002; 21(2):75-91.
3. Alfirevic Z. Misoprostol oral para la inducción del trabajo de parto. En: La Biblioteca Cochrane plus, Número 2, 2005. Oxford, update Soft Ware Ltd. Disponible en: www.Update.Software.com.
4. Hofmeyr GJ, Gülmezoglu AM. Misoprostol vaginal para la maduración cervical y la inducción del trabajo de parto. En: La Bibliot. Cochrane plus, Número 2, 2005.
5. Saggaf A, Rouzi AA, Facharzt BR. Misoprostol for preinduction cervical ripening and induction of labor: a randomized controlled trial. Saudi J Obstet Gynecol 2001;1(2):89-93.
6. Stitely ML, Browning J, Fowler M, Gendron RT, Gherman RB. Outpatient cervical ripening with intravaginal Misoprostol. Obstet Gynecol 2000;96:684-8.
7. Goldberg A, Greenberg M, Darney P. Misoprostol and pregnancy. N Engl J Med 2001;344:38-47.
8. Oliva JA. Maduración cervical e inducción del parto. Temas de Obstetricia y Ginecología. 2003.
9. Cecil Gavet A. Fitz Gerald. Tratado de Medicina Interna. 20ava. Ed. Volumen. II Pág. 1367-74 Mc Graw-Hill Interamericana. Prostaglandinas y compuestos relacionados.
10. Hofmeyer GJ, Gülmezoglu ES. El Misoprostol vaginal para el madurando cervical e inducción de labour (Cochrane Review). En: La Biblioteca de Cochrane Emita 1 2003. Oxford.
11. El – Sherbiny MT, El – Gharieb IH, Gewley HA. Vaginal Misoprostol for induction of labor: 25 vs so ug dose regimen. Int J Gynecol Obstet 2001;72:25-30.
12. Ghidini A, Spong CY, Korker V, Mariani E. Randomized controlled trial of 50 and 100 mcg of Misoprostol for induction of labor at term. Arch Gynecol Obstet 2001;265:128-30.
13. Casagrandi CD, Chio NJ, Pouymiro BM, Carbonell JL, Sánchez C. 25 μ g de Misoprostol vaginal para la maduración del cervix e inducción del trabajo de parto. Rev Cubana Obstet Gynecol 2004;30(1).
14. Ramsey P, Meyer L, Harris D, Ogburn PJ, Ramón K. Characterization of cardiotocographic abnormalities associated with dinoprostone and Misoprostol cervical ripening/ labor induction [abstract]. Am J Obstet Gynecol 2001;184(1):S 115.
15. Has R, Batukan C, Ermis H, Cevher E, Araman A, Kilic G. et al. A Comparison of 25 and 50 mcg vaginally administered Misoprostol for preinduction of cervical ripening and labor induction. Gynecol Obstet Invest 2002;53:16-21.
16. Khoury A, Ahou Q, Govenberg D, Nies B, Manley G, Mecklenburg F. A randomized clinical trial comparing Misoprostol suppositories with continuos dinoprostone for cervical ripening and labor induction [abstract]. Am J Obstetr Gynecol 2001;184(1):S 118.
17. Le Roux PA, Olarogun SO, Penny J, Anthony J. Oral and vaginal Misoprostol compared with dinoprostone for induction of labor: randomized controlled trial. Obstet Gynecol 2002;99(2):201-5.
18. Aquino M, Mariani C, Cecatti JG, Parpinelli M. Misoprostol of (or) oxytocin to labor induction? Femina 2002;30(9):649-54.
19. Jackson N, Irvine R, Edmonds D, Paterson-Brown S. Random allocation controlled trial of intravaginal Misoprostol vs intravaginal dinoprostone for the induction of labour. J Obstet Gynecol 2000;20(supply 1):S 52.
20. Chelmow D, Kilpatrick SJ, Laros RK. Maternal and neonatal outcomes after prolonged latent phase. Obstet Gynecol 1993;81(4):486-91.
21. Maghoma J, Buchmann EJ. Maternal and fetal risks associated with prolonged latent phase of labour. J Obstet Gynecol 2002;22(1):16-9.
22. Progreso insatisfactorio del trabajo de parto. En: Manejo de las complicaciones del embarazo y el parto. Guía para obstetras y médicos. 2002:563-4. Recibido: 3 de febrero de 2006. Aprobado: 5 de marzo de 2006.
Dr. Danilo Nápoles Méndez. Hospitl Ginecoostétrico Docente Sur de Santiago de Cuba"Mariana Grajales Coello, Santiago de Cuba, Cuba.
1Especialista de I y II grados en ginecología y obstetricia. Profesor auxiliar.