Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina Militar
versión On-line ISSN 1561-3046
Rev Cub Med Mil vol.47 no.3 Ciudad de la Habana jul.-set. 2018
ARTÍCULO DE INVESTIGACIÓN
Variables predictoras de riesgo de cáncer de pulmón en fumadores
Predictive variables of lung cancer risk in smokers
Edgar Benítez Sánchez1
Armando Ernesto Pérez Cala1
Esguel Vilaseca Sanabria1
Ernesto Ramírez Ramírez1
Idalis Colón Blanco1
1Hospital Militar "Dr. Joaquín Castillo Duany". Santiago de Cuba, Cuba.
RESUMEN
Introducción: El cáncer de pulmón encabeza la lista de incidencia y mortalidad por cáncer en hombres. Es la cuarta neoplasia más frecuente en mujeres, y segunda causa de muerte por enfermedades neoplásicas en personas pertenecientes al sexo femenino.
Objetivo: Determinar los parámetros de eficiencia y la relación entre variables predictoras del riesgo de ser diagnosticadas con cáncer de pulmón en personas fumadoras.
Métodos: Estudio analítico tipo casos y controles. Casos: 55 pacientes, controles: 115 individuos. Variable resultado: riesgo de ser diagnosticado con cáncer de pulmón. Variables predictoras: edad, sexo, tiempo fumando, color de la piel, número de cigarrillos al día, paquetes/años, antecedentes familiares de cáncer de pulmón, antecedentes familiares de cánceres relacionados con el tabaquismo distintos del cáncer de pulmón, tiempo de abstinencia al tabaco, edad de iniciación en el hábito. Método estadístico: regresión logística multivariada.
Resultados: Las variables que mayores odds ratio mostraron: efecto acumulativo del tabaquismo de más de 30 paquetes por año (OR= 8,5; IC 95 % 3- 23); antecedentes familiares de cáncer de pulmón en parientes de primer grado (OR= 6,5; IC 95 % 4,6- 7,0) y el color de piel negra (OR= 6,3; IC 95 % 3,2- 12,7).
Conclusiones: Las variables que mayor relación mostraron con el riesgo de cáncer de pulmón fueron: color de piel negra, tiempo fumando mayor de 35 años, consumo de más de 30 paquetes por año, y antecedente familiar de cánceres relacionados con el tabaquismo en órganos distintos del pulmón.
Palabras clave: cáncer de pulmón; tabaquismo; factor de riesgo; sensibilidad; especificidad.
ABSTRACT
Introduction: Lung cancer tops the list of cancer incidence and mortality in men. It is fourth most frequent neoplasm in women, and second cause of death by neoplastic diseases in the female sex.
Objectives: To determine the parameters of efficiency and the relationship between predictor variables and the risk of being diagnosed with lung cancer in smokers.
Methods: An analytical study was conducted in type cases and controls. Cases: 55 patients, controls: 115 individuals. Variable result: risk of being diagnosed with lung cancer. Predictor variables: age, sex, smoking history, skin color, number of cigarettes per day, packets / years, family history of lung cancer, family history of cancer related to smoking other than lung cancer, time of tobacco withdrawal, age of initiation into the habit. Statistical method: multivariate logistic regression.
Results: The variables that showed higher OR: cumulative effect of smoking of more than 30 packages / years (OR= 8,5; CI 95 % 3- 23); family history of lung cancer in first-degree relatives (OR= 6,5; CI 95 % 4,6- 7,0); and the black skin color (OR= 6,3; CI 95 % 3,2- 12,7).
Conclusions: The most related variables with the risk of lung cancer were: black skin color, smoking time over 35 years, consumption of more than 30 packages / years, and family history of cancer related to smoking in organs other than lung.
Keywords: lung cancer; smoking; risk factor; sensitivity; specificity.
INTRODUCCIÓN
El cáncer de pulmón encabeza la lista de todas las variedades de tumores malignos, tanto en incidencia como en mortalidad por cáncer en hombres, y es la cuarta neoplasia más frecuente en mujeres, aunque ocupa la segunda causa de muerte por enfermedades neoplásicas en personas pertenecientes al sexo femenino.1 Resulta alarmante que la incidencia de este tumor en las mujeres ha manifestado un sustancial aumento en las últimas décadas.2
Cuba comparte con EE.UU. los mismos índices de incidencia y mortalidad por cáncer de pulmón y es significativo que el "fenómeno femenino" se comporte de igual manera.3,4 Durante el 2016, en Cuba se registraron 3 482 muertes por cáncer pulmonar en hombres (tasa ajustada por sexo de 62,2 por 100 mil habitantes) y 2 053 fallecimientos en mujeres por la misma causa (tasa ajustada por sexo de 36,4 por 100 mil habitantes).5
En las últimas décadas se ha asistido a una estabilización de la incidencia y mortalidad por esta neoplasia en los países desarrollados, fundamentalmente relacionada con un mayor número de hombres que abandonan o no se inician en el hábito. Sin embargo, en los países en vías de desarrollo el cáncer de pulmón se mantiene como un serio problema de salud.1 Esta inquietante situación es agravada por el hecho de que: se trata de una enfermedad con elevada letalidad, con muy bajas tasas de curación, dado que su detección ocurre en estadios avanzados, y que a pesar de su conocida relación con el tabaquismo, resulta muy difícil erradicar el hábito por la fuerte adicción que provoca la nicotina. 6 En los países subdesarrollados, la incidencia del tabaquismo, lejos de disminuir, va en aumento.1
Debido a lo anterior, se han creado numerosos modelos predictivos con el objetivo de identificar a aquellos individuos con mayor riesgo de desarrollar cáncer de pulmón, que serían beneficiados con pruebas de pesquisas capaces de detectar el tumor en sus etapas más tempranas, y por ende con mayores probabilidades de curación.7 Por ejemplo, el National Lung Screening Trial (NLST) considera que su modelo predictivo ha logrado disminuir en un 20 % la mortalidad por cáncer de pulmón en EE.UU. La mayoría de estos modelos emplean variables predictoras clínicas, demográficas, así como las referidas a la intensidad y el efecto acumulativo del tabaco. Sin embargo, al ser extrapolados dichos resultados a distintas poblaciones de estudio, resultan variables.7
La presente investigación tiene el objetivo de determinar los parámetros de eficiencia y la relación entre variables predictoras del riesgo de ser diagnosticado con cáncer de pulmón en personas fumadoras.
MÉTODOS
Se realizó un estudio analítico observacional, del tipo casos y controles. En el grupo de los casos, fueron incluidos 55 pacientes diagnosticados con cáncer de pulmón no microcítico, atendidos en el Hospital Militar "Dr. Joaquín Castillo Duany" de Santiago de Cuba, durante el periodo 2009 - 2015. Fueron seleccionados por muestreo probabilístico a partir de un universo de 112 enfermos con esta afección.
Los criterios de inclusión fueron; la confirmación histológica de la neoplasia y su pertenencia al grupo de los tumores de pulmón no microcítico. El grupo control se conformó a partir de encuestas realizadas a individuos fumadores en varios escenarios hospitalarios (consultas externas, chequeos periódicos de salud, Cuerpo de Guardia, salas de ingreso), no diagnosticados con cáncer de pulmón, hasta conformar un total de 115 participantes.
A ambos grupos se les solicitó el consentimiento informado para participar en el estudio.
Las variables evaluadas como predictoras de riesgo fueron: edad mayor de 70 años; sexo masculino; color de la piel negra; edad de iniciación en el hábito antes de los 18 años; tiempo fumando mayor de 35 años; más de 30 paquetes-años (número promedio diario de cigarrillos, dividido entre 20 y multiplicado por el número de años fumando); tiempo de abandono del hábito mayor de 10 años; enfermedad pulmonar obstructiva crónica (EPOC); antecedentes familiares de cáncer pulmonar en parientes de primer orden; y el antecedente familiar de cánceres relacionados con el tabaquismo (cavidad oral, faringe, esófago, estómago, páncreas, riñón).
La categorización de las variables del modo antes señalado obedeció a la implementación de estas a partir de la codificación dicotómica de 1 (presencia de la variable) y 0 (ausencia de la variable o pertenencia a categoría distinta), según las necesidades de su evaluación en el modelo de regresión logística multivariada.
La predicción del riesgo fue evaluada a partir de la razón de oportunidades u Odds ratio (OR), sus intervalos de confianza (CI) con el 95 % de confiabilidad y un nivel de significación menor de 0,05. Previo al análisis de regresión logística de la variable dependiente, en este caso el riesgo de padecer cáncer de pulmón, se determinó la relación bivariada de cada una de las variables predictoras, con el fin de seleccionar aquellas estadísticamente significativas. No obstante, las que fueron consideradas de interés para la investigación, fueron incluidas en el análisis aun careciendo de significación estadística. A partir de la propia regresión logística, se obtuvo un modelo para el cual fueron calculadas la sensibilidad, especificidad, valor predictivo positivo (VPP) y valor predictivo negativo (VPN). La consistencia del modelo fue determinada mediante el test de Cox y el contraste de Wald. Los resultados fueron expuestos en tablas distintas de 2 x 2, para las que se calcularon la chi-cuadrado de Pearson y la de razón de verosimilitud.
El procesamiento estadístico antes expuesto fue realizado en el programa SPSS V 20.0.
RESULTADOS
La tabla 1 muestra la contribución de cada una de las variables predictoras en función de su OR en el riesgo de ser diagnosticado con cáncer de pulmón no microcítico. Como puede apreciarse, aunque más del 70 % de los individuos estudiados, tanto en el grupo de los casos como en el control, pertenecían al sexo masculino. Esta variable no se comportó como un factor de riesgo (OR de 0,7 con IC 0,3- 1,5).
Las variables que mayores Odds ratio mostraron fueron: tener un efecto acumulativo del tabaquismo en más de 30 paquetes/ años (8,5 veces el riesgo, con IC 3 - 23); antecedentes familiares de cáncer de pulmón en parientes de primer grado (6,5 veces, IC 4,6- 7,0) y el color de piel negra (6,3 veces el riesgo con intervalo de 3,2 - 12,7 para un 95 % de IC). En lo referente al consumo de más de 30 cigarrillos al día, se obtuvo un riesgo de 44,8 veces. Este valor se considera inadmisible, al estimar además la dispersión del OR demasiado amplia (IC 11- 168).
Haber abandonado el hábito tabáquico no demostró ser factor de riesgo, ni factor protector.
La tabla 2 muestra los resultados obtenidos, luego de realizar la regresión logística multivariada, así como los parámetros de eficiencia del modelo. En esta ocasión, las variables que mostraron mayor poder predictivo (en orden de importancia) fueron: un efecto acumulativo del tabaco de más de 30 paquetes/años; color de piel negra; antecedentes familiares positivos de cánceres relacionados con el tabaquismo, distintos del cáncer pulmonar y un tiempo de fumador activo mayor de 35 años. La sensibilidad resultante fue del 58 % y la especificidad del modelo obtenido fue de 92 %.
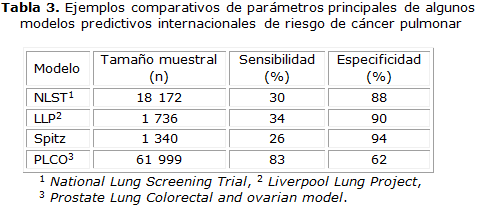
La tabla 3 muestra una selección de los modelos predictivos de riesgo de cáncer pulmonar utilizados a nivel internacional y su relación con el tamaño muestral, sensibilidad y especificidad. Con excepción del Prostate, Lung, Colorectal and Ovarian model (PLCO), el resto de los modelos representados muestran porcentajes de sensibilidad, incluso inferiores a los obtenidos por el modelo utilizado en la presente investigación. En contraste, la especificidad en la mayoría de los modelos ejemplificados en la tabla 3, es superior al 80 % a excepción nuevamente del PLCO.
DISCUSIÓN
Las variables de mayor interés en la presente investigación -dado que difieren con estudios análogos- están representadas en el sexo, los antecedentes de EPOC y la condición de exfumador. La mayoría de la literatura versada sobre el tema, coincide en que la frecuencia de cáncer pulmonar es mayor en fumadores masculinos.8-10 Sin embargo, el patrón de incidencia y prevalencia ha sufrido cambios sustanciales en las últimas décadas.11-14
En la actualidad se asiste a un incremento significativo de tumores malignos de pulmón en pacientes femeninas, lamentablemente proporcional al mayor número de mujeres que se inician y prevalecen en el nocivo hábito.11,12 Otros estudios señalan mayor vulnerabilidad de las mujeres al efecto oncogénico del tabaquismo.3,14 Estos elementos podrían justificar los hallazgos de la presente investigación.
En lo concerniente al antecedente de enfermedad pulmonar obstructiva crónica, también la literatura revisada advierte acerca de la estrecha relación existente entre esta y el cáncer de pulmón.15 No obstante, para algunos autores, tanto la EPOC como los tumores malignos pulmonares representan dos expresiones finales de una vía fisiopatológica común: el efecto nocivo del tabaco sobre el epitelio respiratorio.16 Mientras en algunos pacientes la EPOC, y en especial el enfisema pulmonar, es la consecuencia final del efecto acumulativo del tabaquismo, en otros el desarrollo de una neoplasia (con o sin la presencia de enfisema) significa el resultado de la acción tóxica de los componentes derivados de la combustión del tabaco.16 Existen evidencias que apuntan hacia diferencias fenotípicas y genotípicas entre fumadores/as que condicionan riesgos distintos para enfermar de EPOC o de cáncer pulmonar, al menos en lo referente al carcinoma microcítico.17
Otro tanto sucede con respecto a la relación existente entre la condición de exfumador y el riesgo de cáncer de pulmón. Si bien es cierto que el abandono del hábito tabáquico incide de manera positiva al disminuir dicho riesgo, este hecho depende de manera directa con el tiempo transcurrido como fumador activo.18 O sea, mientras más tiempo fume la persona, mayor riesgo tiene de sufrir una neoplasia de pulmón, aun cuando se suspenda la práctica del tabaquismo.
Los modelos actuales de carcinogénesis pulmonar, sugieren que aunque este proceso comienza en etapas tempranas en fumadores/as, el efecto más pronunciado del tabaquismo se expresa en el aumento de las probabilidades de que clones celulares mutados alcancen satisfactoriamente los estadios finales de la transformación maligna; y a mayor tiempo de exposición, mayor riesgo de que la transformación ocurra.19 En apoyo de esta teoría existen estudios que señalan hacia un aumento desproporcionado del riesgo de cáncer de pulmón en exfumadores/as aun 30 años después de haber abandonado el hábito.20
El modelo obtenido a partir de la regresión logística sugiere que ciertas variables poseen mayores valores predictivos positivos y negativos al ser evaluadas en su conjunto. Por consiguiente, una de las conclusiones más interesantes radica en la complejidad subyacente en la carcinogénesis pulmonar asociada al tabaquismo. Los clásicos resultados obtenidos por Peter B. Bach al respecto se hacen patentes.21 Este autor llamaba la atención sobre la marcada variación existente entre fumadores/as, en relación con el riesgo de desarrollar cáncer de pulmón; variación que sin dudas obedecía a numerosos factores, dígase genéticos o ambientales; fumar constituye sin dudas un factor de riesgo, pero no exclusivo e intervienen otros factores disimiles, quizás, propios o actuantes de manera diferencial para ciertos individuos, e incluso para ciertas poblaciones.
Solo desde esta perspectiva podrían explicarse las diferentes contribuciones de las distintas variables utilizadas en varios de los modelos predictivos de uso más extendido. El NLST, por ejemplo, emplea como variables predictoras a la edad comprendida entre los 55 y 64 años, un efecto acumulativo del tabaquismo mayor de 30 paquetes/años, y un tiempo de abandono del hábito menor de 15 años.7 Por otro lado, el PLCO incluye aparte de la edad, el índice de masa corporal, el nivel de educación, la condición de fumador o de nunca haber fumado, el tiempo de exfumador, el antecedente familiar de cáncer pulmonar, el antecedente de EPOC, el número de paquetes/años, etc. y es aplicable incluso a no fumadores.7 Fangyi Gu y otros,22 demostraron que una única variable se relaciona de manera sustancial con el riesgo de cáncer de pulmón: el menor tiempo entre despertar y consumir el primer cigarrillo.
El resto de los modelos difieren en el número y la categoría de variables empleadas, sin que la variación entre sus parámetros de eficiencia sea significativa; aun cuando sí existen diferencias en cuanto a los métodos utilizados para su calibración.7 Uno de los aspectos limitantes de la presente investigación (entre otros que serán citados más adelante), estriba en la no realización de validación externa, así como la no medición de parámetros de eficiencia como el índice de Youden, por ejemplo.
Uno de los elementos más llamativos de los modelos predictores estriba precisamente en la heterogeneidad de métodos utilizados para su elaboración, las diferencias muestrales, los resultados, utilidad, etc. En una revisión sistemática realizada sobre la metodología empleada para la elaboración y validación de los distintos modelos predictivos de riesgo de cáncer de pulmón, Gaelle Coureau y otros concluyen que no es recomendable la realización de tomografía axial computadorizada a bajas dosis -en la pesquisa de cáncer pulmonar en fumadores)-, dado que no hay información fidedigna sobre la eficacia de esta para reducir la mortalidad por la enfermedad. La ausencia de otros aspectos esenciales, tales como el impacto psicológico que trae aparejada la realización de estas pesquisas, el número de falsos positivos, la ausencia de definiciones homogéneas sobre las características de los nódulos que deben tomarse como sugerentes de malignidad, así como el efecto nocivo de las radiaciones, potencialmente carcinogénicas a largo plazo.23
El propósito inmediato de la presente investigación dentro del objetivo propuesto, reside en establecer la probable relación causal entre distintas variables clínicas y el riesgo de ser diagnosticado con una neoplasia pulmonar, (siempre partiendo del principio de que las relaciones identificadas son propias para la población objeto de estudio). Los resultados pueden calificarse como válidos a la luz de los conocimientos actuales. En efecto, el mayor tiempo fumando, y el mayor número de paquetes/ años consumidos, podrían correlacionarse de manera lineal con el riesgo de desarrollar un tumor maligno de pulmón, tal como sugieren otros estudios.20
Con respecto a la relación entre el color de piel negra y el riesgo particular de padecer cáncer de pulmón también versan resultados positivos.24 En cuanto al antecedente familiar de cánceres relacionados con el tabaquismo que aparecen en localizaciones distintas del pulmón, resulta cierto que está incluido en otros modelos predictivos, pero no existe uniformidad en relación a la explicación más plausible. La existencia de polimorfismos genéticos que aumentan la susceptibilidad oncogénica al tabaquismo, podría ser una de ellas.25 Es innegable no obstante, que los resultados actuales son inherentes y particulares a la población de estudio, y no puede objetarse que la extrapolación de estas variables a otros grupos poblacionales, muestre resultados distintos, aun dentro del mismo marco geográfico.
Tampoco es posible obviar que, en términos probabilísticos, el riesgo de ser diagnosticado con cáncer de pulmón, supera el marco de las variables utilizadas en esta investigación y depende de factores tan diversos como la zona de residencia, la labor de promoción de salud llevada a cabo por los facultativos, las motivaciones personales del individuo, etc.
Los presentes resultados podrían ser el preámbulo de estudios futuros con consideraciones predictivas más amplias. Llama la atención sin embargo, la coincidencia observada en relación a la sensibilidad y especificidad que propone el modelo obtenido, a partir de la regresión logística lograda en la presente investigación, con los mismos parámetros medidos en otros modelos, incluso para tamaños de muestras más grandes. Baja sensibilidad y elevada especificidad son elementos que, según la clasificación epidemiológica de las enfermedades, los incluiría dentro del grupo II: afecciones en las cuales el peor error que se puede cometer es diagnosticar falsos positivos (enfermedades graves pero difícilmente curables o sin remisión). Es muy importante para el paciente o para la población, saberse un verdadero negativo, ya que el tratamiento de los falsos positivos ocasiona serios perjuicios al paciente).26
Las fundamentales limitaciones del presente estudio radicarían en: tamaño muestral insuficiente, la presencia de falacias derivadas de la dicotimización de las variables predictivas, y la no incorporación de otras variables de interés (exposición al asbesto y otros carcinógenos ambientales, antecedentes de enfermedades parenquimatosas previas, etc.) que incrementarían el poder discriminativo del estudio.
En conclusión, las variables que en la población definida demostraron poseer mayor relación con el riesgo de ser diagnosticado con cáncer de pulmón fueron: un tiempo fumando mayor de 35 años, el consumo de más de 30 paquetes/años, el color de piel negra, y el antecedente familiar de cánceres relacionados con el tabaquismo, localizados en órganos distintos del pulmón. Aunque estos resultados muestran coincidencias con lo reportado en otros estudios, es probable que representen características propias de la población estudiada, y se hace necesaria la extrapolación de las variables analizadas a otros grupos muestrales. A pesar de que muestran parámetros de sensibilidad y especificidad característicos de las enfermedades tipo II, no puede hacerse referencia a un modelo predictivo hasta tanto no se complementen las fases imprescindibles para su estructuración.
La confección de un modelo predictivo, con cada una de sus fases cumplidas, demanda una mayor amplitud de la investigación, así como la coordinación interdisciplinaria capaz de crear bases sostenibles, tanto logísticas como administrativas, que aseguren resultados fidedignos, extrapolables y útiles.
La necesidad de abordar el manejo preventivo y terapéutico del cáncer de pulmón partiendo de la identificación de grupos de riesgo específicos, es una realidad perentoria.
Conflictos de intereses
Los autores del presente trabajo declaran no presentar conflictos de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, ParkinDM, Forman D, Bray F. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2015[cited 2017 Feb 5];136(5):359-86. Available from: https://onlinelibrary.wiley.com/doi/full/10.1002/ijc.29210
2. Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D. Global cancer statistics. CA Cancer J Clin. 2011 April;61:69-90.
3. Torre L A, Siegel R L,Ward E M, and Jemal A. Global Cancer Incidence and Mortality Rates and Trends-An Update. Cancer Epidemiol Biomarkers Prev. [Internet]. 2016 Jan [cited 2017 Feb 5]; 25(1): 32-45. Available from: http://cebp.aacrjournals.org/content/25/1/16.long
4. Siegel R, Miller KD, Jemal A. Cancer statistics, 2017. CA Cancer J Clin 2017;67(1):7-30.
5. Dirección nacional de registros médicos y estadísticas de salud. Anuario Estadístico de Salud. Ministerio de Salud Pública. La Habana; abril 2016 [citado 16 nov 2016]. Disponible en: http://files.sld.cu/bvscuba/files/2016/05/anuario-2015-e.pdf
6. Bergen AW, Javitz HS, Krasnow R. Nicotinic acetylcholine receptor variation and response to smoking cessation therapies. Pharmacogenet. Genomics. 2013;23(2):94-103.
7. Gray PE, Teare MD, Stevens J, Archer R. Risk Prediction Models for Lung Cancer: A Systematic Review. Clin Lung Can. 2016;17(2):95-106.
8. Powell HA, Iyen-Omofoman B, Hubbard RB, Baldwin DR, Tata LJ. The association between smoking quantity and lung cancer in men and women. Chest. 2013;143:123-9.
9. Kiyohara C, Ohno Y. Sex differences in lung cancer susceptibility: a review. Gend Med. [Internet] 2010 [cited 2017 Apr 12];7(5):381-401. Available form: https://www.ncbi.nlm.nih.gov/pubmed/21056866
10. Vavalá T, Mariniello A, Reale ML, Novello S. Gender differences in lung cancer. Ital J Gender-Specific Med 2016;2(3):99-109.
11. Risch HA, Howe GR, Jain M, Burch JD, Holowaty EJ, Miller AB. Are female smokers at higher risk for lung cancer than male smokers? A case-control analysis by histologic type. Am J Epidemiol. 1993;138:281-93.
12. Malvezzi M, Bertuccio P, Rosso T, Rota M, Levi F, Vecchia C La, et al. European cancer mortality predictions for the year 2015 : does lung cancer have the highest death rate in EU women ? Ann Oncol [Internet]. 2015 [cited 2017 Feb 5]; 26(4):779-86. Avaiable from: https://www.ncbi.nlm.nih.gov/pubmed/25623049
13. North CM, Christiani DC. Women and Lung Cancer: What's New? Semin Thorac Cardiovasc Surg. 2014;25(2):1-13.
14. Pirie K, Peto R, Reeves GK, Green J, Beral V. The 21st century hazards of smoking and benefits of stopping: a prospective study of one million women in the UK. Lancet. 2013;381:133-41.
15. Young RP, Hopkins RJ, Whittington CF, Hay BA, Epton MJ, Gamble GD. Individual and cumulative effects of GWAS susceptibility loci in lung cancer: associations after sub-phenotyping for COPD. PLoS One. 2011;6(2):222-35.
16. Irwin RS. Are COPD and Lung Cancer Two Manifestations of the Same Disease? CHEST. 2005;128(4):1895-7.
17. Ruyi H, Yongyue W, Rayjean J H, Geoffrey L, Li S, Ruyang Z, et al. Associated Links Among Smoking, Chronic Obstructive Pulmonary Disease, and Small Cell Lung Cancer: A Pooled Analysis in the International Lung Cancer Consortium. EBioMedicine 2015;8(4):1677-85.
18. Hall FS. Genetic Risk for Lung Cancer and the Benefits of Quitting Smoking. EBioMedicine. 2016;(11):19-20.
19. Gatenby RA, Brown J. Mutations, evolution and the central role of a self-defined fitness function in the initiation and progression of cancer. Biochim Biophys Acta [Internet]. 2017 [cited 2017 Sep 16];1867(2):162-6. Available from: https://www.ncbi.nlm.nih.gov/pubmed/28341421
20. Mong C, Garon EB, Fuller C, Mahtabifard A, Mirocha J, Mosenifar Z, et al. High prevalence of lung cancer in a surgical cohort of lung cancer patients a decade after smoking cessation. Jour Card Surg. 2011;6(19):1-7.
21. Bach PB, Kattan MW, Thornquist MD, Kris MG, Tate RC, Barnett MJ, et al. Variations in Lung Cancer Risk Among Smokers. Jour Nat Can Inst. 2003;95(3):470-8.
22. Gu F, Wacholder S, Kovalchik S, Panagiotou OA, Reyes-Guzman C, Freedman ND, et al. Time to Smoke First Morning Cigarette and Lung Cancer in a Case-Control Study. J Natl Cancer Inst. 2014;107(6):1-8.
23. Coureau G, Salmi LR, Etard C, Sancho-Garnier H, Sauvaget C, Mathoulin-Pélissier S. Low-dose computed tomography screening for lung cancer in populations highly esposed to tobacco: A systematic methological appraisal of published randomized controlled trials. Euro J Cancer. 2016;81(4511):146-56.
24. Carol J E, Sumesh K, Mei L, D'Amelio A, Qiong D, Cote ML. Development and Validation of a Lung Cancer Risk Prediction Model for African-Americans. Cancer Prev Res 2008;1(4):255-65.
25. Chen L.-S, Baker T, Hung RJ, Horton A, Culverhause R, Hartz S, et al. Genetic risk can be decreased: quitting smoking decreases and delays lung cancer for smokers with high and low CHRNA5 risk genotypes - a meta-analysis. EBioMedicine. 2016;11(6):219-26.
26. du Prel J-B, Roling B, Blettner M. Statistical Methods in Medical Research. Dtsch Arztebl Int. 2009;106(7):99-127.
Recibido: 1 de marzo de 2018.
Aprobado: 19 de abril de 2018.
Armando Ernesto Pérez Cala. Hospital Militar "Dr. Joaquín Castillo Duany". Punta Blanca s/n, Santiago de Cuba, Cuba.
Correo electrónico: armando.perez@infomed.sld.cu