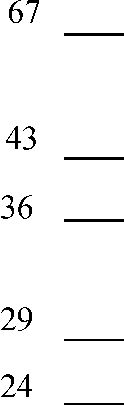Meu SciELO
Serviços Personalizados
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Cubana de Medicina Tropical
versão On-line ISSN 1561-3054
Rev Cubana Med Trop v.51 n.3 Ciudad de la Habana jul.-dez. 1999
Comunicación breve
Instituto de Medicina Tropical "Pedro Kourí"
Actividad semejante a catepsina L en la hemolinfa de hembras repletas de Boophilus microplus
Resumen
Se demostró la presencia de actividad cisteíno-proteinasa en la hemolinfa de hembras repletas de Boophilus microplus en el día 2 de oviposición. El ensayo enzimático se realizó con el sustrato sintético N-carbobenzoxi-fenilalanil-arginil-4-metoxi-beta-naftilamida y se observó hidrólisis tanto para el extracto crudo de ovarios como para la hemolinfa. La actividad se inhibió en 100 % ante la presencia de trans-epoxisuccinil-L-leucilamido (4-guanidinio) butano, un inhibidor específico para cisteíno-proteinasas. La electroforesis en geles de poliacrilamida y gelatina incluida mostró la presencia de una sola banda activa en ambas muestras ensayadas con igual corrimiento electroforético (alrededor de 38 kDa).
Descriptores DeCS: CATEPSINAS/sangre; HEMOLINFA.
Boophilus microplus es un ectoparásito del ganado, vector de hemoparásitos como Babesia sp y Anaplasma sp, que causa pérdidas económicas significativas en áreas tropicales y subtropicales. En intentos para proteger el ganado contra este artrópodo se han utilizado extractos proteicos como vacunas experimentales y se han identificado antígenos relacionados con la protección en el epitelio intestinal, tal es el caso de Bm 86.1 Esta proteína obtenida por vía recombinante se ha comercializado como vacuna, sin embargo, se han detectado diferencias en cuanto a la susceptibilidad de las garrapatas en diversas locaciones geográficas.2 La carencia de efectos inmediatos e individuales la excluye del mercado de productos para limpiar y proteger al ganado de garrapatas antes de su traslado.3 Por otra parte, no existe similitud de secuencia aminoacídica entre este antígeno y alguna proteína de función conocida. Esto pudiera dificultar la búsqueda de antígenos eficaces en otras especies de garrapatas.1
En los animales ovíparos la embriogénesis depende de la utilización de las proteínas de la yema de los huevos. Se han reportado muchas proteinasas como responsables de esta degradación. La mayoría de estas enzimas en artrópodos son sintetizadas como precursores y algunas se transportan desde su órgano de síntesis hasta el ovario, a través de la hemolinfa para acumularse en los ovocitos durante el proceso de ovogénesis.4 Se conoce que la IgG del hospedero puede atravesar el intestino de insectos hematófagos y garrapatas y ser encontrada en la hemolinfa;5 retiene su actividad biológica y anticuerpos específicos pueden enlazarse a órganos internos (glándulas salivales y ovario).6 Cantidades significativas de anticuerpos anti Bm91 (carboxipeptidasa de la garrapata localizada en el intestino y las glándulas salivales, que potencia el efecto de la vacunación con Bm86) atraviesan el intestino y se enlazan al antígeno en la glándula salival. En este caso se propone que el mecanismo de daño del ectoparásito pueda ser de 2 tipos: mediante la unión de anticuerpos a la superficie de los tejidos o por medio de la inhibición de una función bioquímica o fisiológica crítica.1
En estudios realizados en el laboratorio se demostró la presencia de actividad semejante a la catepsina L de mamíferos, como la actividad proteolítica fundamental en el ovario de adultas de B. microplus y su estrecha asociación con el proceso de vitelogénesis.7 El objetivo del presente trabajo fue determinar la presencia de actividad proteolítica, similar a la encontrada en ovarios, en la hemolinfa de hembras repletas de B. microplus.
Las garrapatas utilizadas en el estudio correspondían a una cepa de campo, libre de Babesia sp, mantenida en los Laboratorios Biológicos Farmacéuticos (LABIOFAM) sobre ganado Holstein. Se colectaron 100 hembras repletas y se incubaron a 27 ± 1 °C hasta el día 2 posterior al comienzo de la oviposición, cuando la actividad enzimática en el ovario era máxima.7 Se extrajeron aproximadamente 15 µL de hemolinfa de cada garrapata;6 el volumen total colectado se diluyó en 400 µL de salina fisiológica (NaCl 0,9 %) a 4 °C, se centrifugó a 7 000 gravedades durante 5 min para separar los hemocitos; el sobrenadante se utilizó para realizar los ensayos enzimáticos y la electroforesis. Se realizó la disección de los ovarios en salina fisiológica a 4 °C, se homogeneizaron con un Polytron a 3 000 rpm durante 3 min, después se centrifugó a 7 000 gravedades durante 30 min y se colectó el sobrenadante. El ensayo enzimático se realizó con el sustrato N-carbobenzoxi-fenilalanil-arginil-4-metoxi-beta-naftilamida (Z-Phe-Arg-betaNA) como se describió antes,7 se usó como tampón ácido cítrico 100 mmol/L-fosfato disódico 200 mmol/L a pH 4,0 y se incorporó a la mezcla de reacción L-cisteína 5 mmol/L para una mayor sensibilidad; el ensayo de inhibición se realizó con trans-epoxisuccinil-L-leucilamido (4-guanidinio)-butano (E-64), un inhibidor específico de cisteíno-proteinasas y se utilizó dimetilsulfóxido (diluente del E-64) como control. La actividad gelatinolítica se detectó por electroforesis en geles de poliacrilamida a 12,5 %, con SDS 0,1 % y gelatina incluida a 0,2 %;8 los geles se lavaron en tritón X-100 a 2,5 % durante 2 h a temperatura ambiente y por último se incubaron toda la noche en tampón ácido cítrico 100 mmol/L-fosfato disódico 200 mmol/L a pH 3,0 con 5 mmol/L de L-cisteína y 200 µmol/L de E-64 en el caso del estudio de inhibición. La concentración de proteínas se midió con albúmina de suero bovino como patrón.9
Se obtuvo un valor de actividad enzimática en la hemolinfa, frente a Z-Phe-Arg-betaNA, de 0,37 x 10-2 µmol de beta-naftilamina/min/mg de proteína presente, que se inhibió en 100 % con E-64; mientras que el extracto de ovarios presentó una actividad cisteíno-proteinasa muy superior, 7,8 x 10-2 µmol de beta-naftilamina/min/mg de proteína presente en el extracto. Por otra parte, se observó una sola banda de actividad gelatinolítica ácida del tipo cisteíno proteinasa tanto para la hemolinfa como para el extracto de ovarios, ambas con igual corrimiento electroforético, alrededor de los 38 kDa (fig.).
Fig. Electroforesis en gel de poliacrilamida (12,5 %), con gelatina incluida (2 %) y SDS (0,1 %). A: Hemolinfa; B: Hemolinfa, incubada con E-64; C: Extracto de ovarios y D: Extracto de ovarios, incubado en presencia de E-64. Las marcas corresponden a los patrones de peso molecular (albumina bovina, 67 kDa; ovoalbúmina, 43 kDa; gliceraldehído 3 fosfato deshidrogenasa, 36 kDa; anhidrasa carbónica, 29 kDa; tripsinógeno, 24 kDa).
Estos resultados demuestran la circulación hemolinfática de una cisteíno proteinasa; muy similar a la descrita para el ovario, lo que permite especular sobre una vía de transporte común de esta enzima y las vitelogeninas en su tránsito hacia el ovocito.10 Adicionalmente, sugieren la posibilidad de intervención en la reproducción de garrapatas con el uso de esta enzima proteolítica como un blanco de la acción de los anticuerpos que pasan a la hemolinfa. Es necesario realizar estudios para determinar el(los) sitio(s) de síntesis de la enzima y su papel en el proceso de formación de los huevos.
Summary
The cysteine-proteinase activity present in the hemolymph of females crammed with Boophilus microplus at the second oviposition was proved. The enzime assay was performed using the synthetic N-carbobenzoxi-phenilalanyl-arginil-4-metoxi-betan-naphthylamide substrate, and hydrolisis in both raw ovarim extract and hemolymph were observed. The activity was 100 % inhibited by trans-epoxisuscinyl-L- leucidamide (4-guadinine) butane, an specific inhibitor for cysteine-proteinase. Polyacrylamide and gelatin-gel electrophoresis showed the existance of only one active band in both samples tested with the same electrophoretic sliding (approximately 38 kDa).
Subject headings: CATHEPSINS/blood; HEMOLYMPH.
Referencias bibliográficas
- Willadsen P. Novel vaccines for ectoparasites. Vet Parasitol 1997;71:209-22.
- De la Fuente J, Rodríguez M, Fragoso H, Ortiz M, Massard CL, García O, et al Efficacy of vaccination with GavacTM in the control of Boophilus microplus infestations. En: De la Fuente, I ed. Recombinant vaccines for the control of cattle tick La Habana: Elfos Scientiae, 1995: 177-85.
- Floyd RB, Sutherst RW, Hungerford J. Modelling the field efficacy of genetically engineered vaccine against the cattle tick Boophilus microplus. Int J Parasitol 1995;25(3):285-91.
- Takahashi SY, Yamamoto Y, Zhao X, Watabe S. Bombyx acid cysteine proteinase. Investebr Reprod Develop 1996; 30(1-3):265-81.
- Da Silva I, Moraes RE, Oliveira A, Heck A, Logullo C, González JC et al. Functional bovine immunoglobulins in Boophilus microplus hemolymph. Vet Parasitol 1996;62:155-60.
- Ackermann S, Clare FB, Mc Gill TW, Sonenshine DE. Passage of hosts serum components, including antibody, across the digestive tract of Dermacentor variabilis (Say). J Parasitol 1981;67(5):737-40.
- Fernández-Calienes A, Mendiola J, Hernández H, Valdés M, Finlay C. Occurrence of Cathepsin L-like Activity in the Ovary of Boophilus microplus. Mem Inst Oswaldo Cruz. En prensa.
- Fagotto F. Yolk degradation in tick eggs: I. Ocurrence of a cathepsin L-like acid proteinase in yolk spheres. Arch Insect Biochem Physiol 1990;14:217-35.
- Lowry OH, rosebrough NJ, Farr AL, Randall RJ. Protein measurement with the folin phenol reagent. J Biol Chem 1951;113:265-75.
- Diehl PA, Aeschlimann A, Obenchain FD. Tick reproduction: oogenesis and oviposition. En: Obenchain FD, Galun R, eds. Physiology of ticks New York: Pergamon Press, 1982:277-350.
Recibido: 24 de septiembre de 1999. Aprobado: 30 de septiembre de 1999.
Lic. Aymé Fernández-Calienes Valdés. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
E-mail: ayme@ipk.sld.cu
1 Licenciada en Bioquímica. Aspirante a Investigadora.
2 Licenciada en Bioquímica. Investigadora Agregada.
3 Doctor en Medicina. Doctor en Ciencias Biológicas. Investigador Titular.