Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Medicina Tropical
versión On-line ISSN 1561-3054
Rev Cubana Med Trop vol.67 no.3 Ciudad de la Habana dic. 2015
Rev Cubana Med Trop vol.67 no.3 La Habana. 2015
ARTÍCULO ORIGINAL
Evaluación del sistema serológico Febrille Antigen Brucella para la pesquisa de anticuerpos contra brucelas, en Cuba
Evaluation of the serological system Febrile Antigen Brucella for the detection of anti-Brucella antibodies in Cuba
DraC. Ana Margarita Obregón Fuentes, Dra. Kiryan Muñoz Núñez, Téc. Eduardo Echevarría Pérez, MSc. Yaindrys Rodríguez Olivera, Lic. José Rodríguez Silveira, Téc. Yanais Valdés Labrador, DrC. Alberto Baly Gil, DrC. Maria Eugenia Toledo Romaní
Instituto de Medicina Tropical “Pedro Kourí”. La Habana, Cuba.
RESUMEN
Introducción: la brucelosis es una zoonosis perjudicial para la salud humana y veterinaria. Cuba incrementa la ganadería no controlada productora de alimentos que unida a otras prácticas agrícolas, inciden en el aumento de la morbilidad por esta enfermedad. La red nacional de laboratorios de salud pública de Cuba, carece de métodos de laboratorio para el diagnóstico de la brucelosis humana.
Objetivos: evaluar cualitativamente el sistema serológico comercial Febrille Antigen Brucella, para detección de anticuerpos contra brucelas, con el uso de sueros de casos y controles. Confirmar la infección por brucelas con la aplicación del sistema serológico comercial para la detección de anticuerpos contra brucelas y los sistemas comerciales de referencia ELISA-IgM e IgG, en sueros de pacientes sospechosos de brucelosis. Realizar una descripción parcial de costos, del sistema serológico comercial Febrille Antigen Brucella.
Métodos: se realizó una investigación en servicios y sistemas de tipo observacional con un estudio de caso control anidado, con cuarenta sueros de casos, 80 controles y 466 muestras de pacientes sospechosos, para evaluar el sistema comercial Febrille Antigen Brucella, (Diagnostic Senese SpA), al que se le efectuó también una evaluación económica parcial de costos. Se utilizaron como pruebas de referencia ELISA-IgM y ELISA-IgG (VIRCELL, España).
Resultados: el sistema de Febrille Antigen Brucella mostró valores de sensibilidad de 100,00%, especificidad de 97,50 % y una concordancia de 98,33 %. De los 72 casos clínicos, 25 presentaron títulos ≥ 160 por Febrille Antigen Brucella, fueron positivos también por ELISA IgM o ELISA IgG. El uso de los sistemas ELISA-IgM e IgG en los sueros reactivos y sospechosos por Febrille Antigen Brucella, incrementó la positividad serológica. El costo medio total (21,46 CUP) para una determinación por Febrille Antigen Brucella resultó económico.
Conclusión: el diagnóstico de laboratorio de la brucelosis humana en Cuba, se fortalece al demostrar que el Febrille Antigen Brucella tiene un costo económico y que es útil para la detección de anticuerpos contra brucelas.
Palabras clave: brucelosis, diagnóstico, Febrill Antigen Brucella, serología.
ABSTRACT
Introduction: brucellosis is a zoonosis detrimental to human and animal health. Cuba increases food-producing uncontrolled stockbreeding, a fact that, together with other farming activities, influences the increase in morbidity for this disease. The Cuban national network of public health laboratories lacks laboratory methods for diagnosis human brucellosis.
Objectives: to qualitatively evaluate the commercial serological system Febrile Antigen Brucella for the detection of anti-Brucella antibodies, with the use of serums from cases and controls; to confirm Brucella infection, by means of the application of the commercial serological system for anti-Brucella antibodies detection and the commercial systems of reference ELISA-IgM and ELISA-IgG in serums from patients suspected of brucellosis; and to partially describe the costs of the commercial serological system Febrile Antigen Brucella.
Methods: observational research carried out in services and systems, by a nested case-control study, with 40 serums from cases, 80 controls and 466 samples from suspect patients, in order to evaluate the commercial system Febrile Antigen Brucella (Diagnostica Senese SpA), which besides was object to a partial economic evaluation of costs. As reference tests, ELISA-IgM and ELISA-IgG (VIRCELL, España) were used.
Results: the Febrile Antigen Brucella system showed sensitivity values of 100.00%, specificity of 97.50% and agreement coefficient of 98.33%. Out of the 72 clinical cases, 25 presented titles greater than or equal to 160 by Febrile Antigen Brucella and were positive also by ELISA-IgM and ELISA-IgG. The use of the systems ELISA-IgM and ELISA-IgG in Febrile Antigen Brucella-reactive and suspect serums increased serological positivity. Mean average cost (21.46 CUP) for one determination by Febrile Antigen Brucella proved economical.
Conclusion. The laboratory diagnosis of human brucellosis in Cuba becomes stronger upon proving that Febrile Antigen Brucella has an economical cost and that it is useful for anti-Brucella antibodies detection.
Keywords: brucellosis; diagnosis, Febrile Antigen Brucella, serology test.
INTRODUCCIÓN
En Las Américas, la brucelosis es una de las zoonosis más perjudiciales, por las nocivas consecuencias en la salud humana y graves pérdidas económicas causadas por su extensa distribución en la ganadería productora de alimentos. Junto a la tuberculosis y la meningitis meningocócica, la brucelosis es una enfermedad bacteriana muy frecuente en países como España, México, Chile y Argentina. Sin embargo, se calcula que el número de casos contabilizados, es de tres a cinco veces inferior a la incidencia real, debido en parte, a la falta de declaración y a la existencia de infecciones asintomáticas.1
En Cuba, en los últimos años se ha incrementado la ganadería no controlada productora de alimentos, lo que puede incidir en el incremento la morbilidad por esta enfermedad. Sin embargo, desde el año 1959 se iniciaron diversas tareas para contrarrestar el incremento de las tasas de morbilidad entre ellas, la edición en 1962 del primer Programa para el Control y Erradicación de la Brucelosis en los Animales Domésticos.2 En el periodo 2008 al 2012, según la Dirección Nacional de Estadísticas, del Ministerio de Salud Pública (MINSAP) se registraron 74 casos de brucelosis humana en Cuba, en Pinar del Río, la provincia que mayor incidencia reporta con 41 pacientes confirmados. Estos hallazgos pueden estar sesgados por un subregistro a nivel nacional y las debilidades en el diagnóstico microbiológico, pilar fundamental en la confirmación de la enfermedad, el que se realiza en lo fundamental por la detección de títulos de anticuerpos específicos en muestras pareadas de sueros de los casos sospechosos.3,4
Existen pruebas de referencia como los sistemas ELISA-IgM y ELISA-IgG,5 que detectan la presencia de anticuerpos específicos (IgG o IgM) contra brucelas, con valores excelentes de sensibilidad y especificidad. Con esta técnica se conoce con mayor precisión el perfil de las inmunoglobulinas, se puede discernir entre infección aguda (IgM) o crónica (IgG).4
La firma comercial Diagnostic Senese SpA (DIESSE) ofreció al Laboratorio Nacional de Referencia de Brucelas (LNRB), del Instituto “Pedro Kourí” el estuche comercial de Antígeno Febril de Brucella (FAB),5 para su evaluación. El FAB está basado en la reacción de Widal-Wright, ensayo que se efectúa en dos partes, una prueba cualitativa rápida en lámina, conocida como reacción de HUDDLESON y un ensayo semicuantitativo lento en tubos, conocida como reacción de WRIGHT.5
Desde el año 2010, las autoridades cubanas del MINSAP, decidieron rescatar el diagnóstico serológico de los casos humanos sospechosos de brucelosis, y responsabilizaron al Laboratorio Nacional de Referencia de Brucelas (LNRB), de la Vicedirección de Microbiología del IPK. En la presente investigación se trazaron como objetivos: evaluar cualitativamente el sistema serológico comercial FAB, para detección de anticuerpos contra brucelas, con el uso de sueros de casos y controles; confirmar la infección por brucelas aplicando el sistema serológico comercial para la detección de anticuerpos contra brucelas y los sistemas comerciales de referencia ELISA-IgM e IgG, en sueros de pacientes sospechosos de brucelosis y realizar una descripción parcial de costos, del sistema serológico comercial FAB.
MÉTODOS
Se realizó una investigación en servicios y sistemas de tipo observacional. Se incluyeron en el universo de estudio 586 sueros de personas “supuestamente sanas”, enfermos o sospechosos de brucelosis recibidos en el LNRB, en el período comprendido entre abril de 2011 a diciembre de 2012.
La evaluación del sistema serológico rápido FAB, con referencia 21212/CUB, se realizó a través del diseño de un estudio caso control anidado, con muestras de sueros de pacientes confirmados en el LNRB, y del banco de sangre del municipio Plaza de la Revolución, en La Habana. Quedó conformados los siguientes grupos de estudio: grupo I (casos): 40 sueros de pacientes con brucelosis confirmada y grupo II (controles): 80 sueros de individuos sin brucelosis, de ellos 40 sueros de personas “supuestamente sanas” donantes de sangre y 40 sueros de pacientes con patologías que pueden cruzar antigénicamente con las brucelas. Además, 10 sueros de toxoplasmosis, 15 positivos a Virus de Epstein Bar, y 15 de Hepatitis (5 de Hepatitis A, 5 de B y 5 de C) fueron incluidos. Las técnicas serológicas comerciales de referencia ELISA-IgM y ELISA-IgG; sirvieron para confirmar sueros positivos y negativos a brucelosis humana.4
Se empleó el sistema serológico comercial,5 en 466 sueros de pacientes sospechosos de brucelosis (grupo III), remitidos al LNRB de instituciones de salud.
Los sueros positivos a toxoplasmosis fueron corroborados por el ELISA VIDAS TOXO IgM- IgG, bioMériueux, Francia; los de enfermos con el Virus de Epstein Bar, por el ELISA SMARTEST, Israel; los casos con los virus de las hepatitis A, B y C fueron identificados por ELISA-IgM “in house”, y UMELISA - HBsAg y UMELISA anti - HCV, producidos por el Centro de Inmunoensayo (CIE) de La Habana, Cuba.
La interpretación de los resultados de FAB se realizó según criterios del productor. Los sueros con títulos desde 20 y hasta 40 se consideraron reactivos a brucelosis, los que mostraron títulos de 80 como sospechosos de brucelosis y los que igualaron o superaron los títulos de 160 fueron positivos a brucelosis, muestras con alto valor diagnóstico.
Se calculó para el sistema FAB, los porcentajes de la sensibilidad, la especificidad, el valor predictivo positivo y negativo, el índice de concordancia o validez, el índice de Youden; así como la razón de verosimilitud, estimándose el intervalo de confianza (IC) del 95 % y el valor de p ≤ 0,05. Se emplearon como prueba de referencia los sistemas ELISA-IgM e IgG.
Para calcular los costos directos se utilizó la técnica de microcosteo,6 la que mide el gasto de recursos de “abajo hacia arriba”, de los elementos del costo (salarios, materiales y tiempo de utilización de los medios de capital) para cada una de las tareas que componen el proceso. Los costos indirectos se supusieron de un 20 % y hasta un 49 % de los costos directos. Fueron realizadas 30 mediciones por cada actividad, lo que permitió obtener un número de datos suficientes y así ajustarlos a distribuciones de probabilidad.
Se aplicó una simulación Monte Carlo, consistente en asignarle distribuciones de probabilidad a las variables “inputs” sobre las cuales se tiene incertidumbre y a continuación muestrear un número repetido de veces (500 veces en nuestro caso) para obtener así 500 valores distintos de la variable “input “con lo cual se calcula la media muestral y la desviación estándar.6
La media de las variables “input” fue multiplicada por su precio constante y así se calculó el costo medio por cada muestra colectada, registrada y determinada, según corresponda el tipo de actividad. A la vez, este cálculo se introdujo en la expresión analítica de las variables “output“ para calcular su media y distribución de frecuencias. Las distribuciones de las variables “inputs” fueron asignadas con el uso de la prueba de Kolmogorov-Smirnov,6 con la que se puede determinar la distribución teórica que se le asigna a los datos con la misma distribución.
Por último, se hallaron los costos medios totales6 por actividad y los porcentajes de los costos totales para un diagnóstico por FAB. Se calculó el intervalo de confianza del 95 % de los costos totales medios por cada tipo de actividad. La depreciación de los medios de capital se hizo por el método de anualización a una tasa de interés del 3 %, valor de restitución según precios de mercado del 2013, tiempo promedio de vida útil según medio de capital y un valor de desecho del 20 %. No se tuvieron en cuenta la depreciación de los medios de capital de la oficina de recepción de muestras ya que la proporción de muestras de brucelas con respecto al número de muestras que allí se recepcionan es casi cero. Todos los costos fueron expresados en CUP con el uso de la tasa oficial de cambio de 1 USD = 1 CUP.
RESULTADOS
Del total de las muestras confirmadas con brucelosis humana (grupo I) por ELISA IgM y/o IgG, 40 (100 %) resultaron positivas por el sistema comercial FAB. De los 80 sueros controles (grupo II), dos (2,5 %), correspondientes a individuos donantes de sangre “supuestamente sanos”, mostraron reacciones cruzadas, fueron positivos por el sistema FAB. Los títulos de anticuerpos (20 y 40) de estos sueros resultaron ser bajos. Todos los controles fueron negativos por los sistemas ELISA (IgM e IgG). Ciento dieciocho sueros de los 120 sueros evaluados correspondientes a los grupos I y II coincidieron por FAB y ELISA IgM o ELISA IgG, para un 98,3 %.
El sistema FAB presentó una sensibilidad del 100 %, con un intervalo de confianza del 95 % (IC = 98,75-100,0), una especificidad del 97,5 % (IC = 93,45-100,0), un valor predictivo positivo y otro negativo del 95,24 % y de 100 % en orden (IC = 87,61-100,00; IC = 99,36-100,00). Por su parte el Índice de Youden fue de 0,98 % (IC = 0,94-1,01) y la razón de verosimilitud positiva fue de 40 % (IC = 10,18-157,17).
De los 466 sueros de pacientes con sospecha clínica de brucelosis (grupo III), las variables cualitativa fueron positivas 72 muestras (15,5 %) y las semicuantitativa resultaron reactivas 28 (38,9 %), de ellas 12 y 16 con títulos de 20 y 40 en orden, 19 muestras fueron sospechosas (26,4 %) y 25 positivas (34,7 %). Mediante los sistemas ELISA-IgM y/o ELISA-IgG el 52,8 % de las muestras resultaron positivas (38/72) y 11 sueros fueron indeterminados para un 15,2 %.
En la tabla se observan los títulos de anticuerpos por FAB semicuantitativo, en los 38 sueros positivos por los sistemas ELISA (IgM, IgG, o IgM+IgG). Nótese, para los sueros con títulos de 20 por FAB, un caso resultó positivo por ELISA (2,6 %). De igual manera, tres sueros con títulos de 40 por FAB fueron positivos por ELISA IgG (7,9 %). Nueve (23,7 %) y uno (2,6 %) de los sueros positivos por ELISA IgG e IgM al respecto presentaron títulos de 80 por el sistema FAB. De los sueros con títulos de 160 por FAB se encontraron positivos por el sistema ELISA IgM un 13,2 %, por ELISA IgG un 39,5 % y por ambos sistemas ELISA IgM + ELISA IgG un 10,5 %. Hubo solo un caso positivo por FAB con títulos iguales o superiores a 160, que no fue confirmado por los sistemas ELISA utilizados.
Por otra parte, de las 38 muestras positivas por ELISA, el mayor porcentaje de los sueros mostraron anticuerpos de la clase IgG [73,7 %; (28/38)], seguidos por aquellos que mostraron anticuerpos de la clase IgM [15,8 %; (6/38)] y por último los que tenían anticuerpos IgM e IgG [10,5 %; (4/38)].
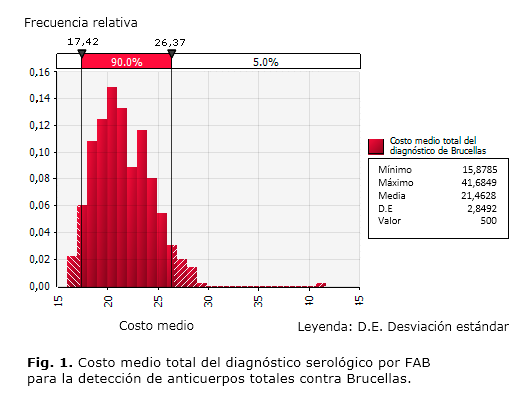
La figura muestra la distribución de la variable “output”, costo total, se utilizó la simulación Montecarlo . Se obtuvo alrededor de la media (21,46 CUP), un mínimo de 15,87 CUP y un máximo de 41,68 CUP, con una desviación estándar de 2,85 CUP.
Los costos medios por diagnóstico alcanzan la cifra de 21,46 CUP [IC 95 % (21,21-21,71)]. Según los costos medios por actividad, el mayor peso lo tuvo el traslado y la recepción de las muestras, desde su origen y hasta el IPK, con 7,66 CUP (35,7 %), seguido en orden decreciente por la prueba FAB semicuantitativa con el 35,5 %, la recepción y ejecución de la prueba cualitativa en el LNRB del IPK, con el 23,6 %, y por último la extracción de la muestra en el laboratorio de microbiología del municipio Consolación del Sur de un 5,2 %. Cuando la prueba de FAB resultó negativa, el costo medio por diagnóstico fue de 5,06 CUP [IC = 95 %, (5,058-5,062)], lo que representa el 23,6 % de los costos en el LNRB.
DISCUSIÓN
La prueba de FAB es un procedimiento técnico sencillo, simple y fácil de ejecutar si se compara con el cultivo bacteriológico de las brucelas y los sistemas ELISA–IgM y ELISA-IgG.4 No existen reportes en la literatura del uso del sistema FAB para el serodiagnóstico de la brucelosis humana, sin embargo, existen publicaciones que utilizan la prueba de rosa de bengala y otras técnicas de seroaglutinación para estos fines. En estos reportes los porcentajes de coincidencia fluctúan entre el 54,2 % y el 95,7 %. Los resultados de esta investigación superaran a los reportados por estos autores.7-9
En Estados Unidos, en el 2012 se analizan 50 muestras de sueros de pacientes con enfermedades y agentes etiológicos que cruzan antigénicamente con las brucelas, entre ellas la enfermedad de Lyme, sífilis, virus de Epstein Bar, Fiebre Q, y artritis reumatoidea y adicional, 50 muestras de individuos “sanos”, y no se encontraron reacciones cruzada mediante la prueba de seroaglutinación.7 En la presente investigación, los dos sueros reactivos por el sistema FAB pertenecientes a donantes de sangre; pudieran corresponder a individuos que en algún momento hayan estado en contacto con Brucella spp. y mantienen cierto grado de reactividad.
La sensibilidad del FAB superó las cifras reportadas en otras investigaciones. Por su parte la especificidad del FAB supera el 95 % lo que coincide con la literatura internacional.7-10
Los valores predictivos positivo (VPP) y negativo (VPN) del FAB superaron la cifra del 95 %. Otros reportes describen cifras inferiores a las encontradas en este trabajo, para la prueba de Rosa de Bengala (VPP del 94 % y VPN del 36,8 %). Por otra parte, la evaluación de la prueba de seroaglutinación, muestraa un VPP y un VPN de 98 % y 55,9 % correspondiente.7-10
Fueron aceptables los valores encontrados para el índice de Youden, cifra igual a 0,98; valor cercano a 1 y el índice de Validéz (98,3 %). No fue posible calcular RV- porque la especificidad del sistema FAB fue de un 100 %.
Resulta difícil establecer comparaciones en cuanto a la incidencia y prevalencia de una enfermedad infecciosa porque estos parámetros varían de forma considerable en las diferentes áreas geográficas, y depende en gran medida de las condiciones sociales, económicas y políticas de los países. En el mundo, se reportan cerca de 500000 casos anuales de brucelosis humana, la mayor parte de ellos ubicados en la cuenca del mediterráneo.1 En Cuba la incidencia de esta enfermedad es baja, lo cual pudiera deberse a la falta de diagnóstico confirmatorio. Es probable que esta razón determine el 15 % de positividad por FAB, encontrada en esta investigación. Pabuccuoglu O y colaboradores reportaron un 55,4 % de positividad en muestras estudiadas por un ELISA-IgM y un 84,8 % para ELISA-IgG. Estos valores son superiores a los encontrados en este estudio.9
En el actual estudio, predominaron los pacientes con brucelosis crónica, lo que puede explicarse a que durante esta fase de la enfermedad en los humanos, los síntomas y signos clínicos están bien establecidos, lo que permite establecer un diagnóstico clínico acertado; a diferencia de la fase aguda, en que los síntomas son muy inespecíficos y polimórficos, y tienden a confundirse con el cuadro clínico de entidades infecciosas y no infecciosas, por lo que se dificulta el diagnóstico microbiológico. Se observó que mientras más elevado era el título de anticuerpos totales por el sistema FAB, más alta era el número de sueros con anticuerpos IgG o IgM detectados por los sistemas ELISA usados para la confirmación de la infección. Se tomó en consideración, el valor de corte del sistema FAB (título ≥ 160) reportado por el productor,5 se obtuvieron 25 sueros positivos por ELISA (IgM e IgG). Sin embargo, al extender el uso de los sistemas ELISA-IgM y ELISA-IgG, a los sueros reactivos y sospechosos, se incrementaron los positivos de 25 a 38 sueros, lo que sugiere, que se debe confirmar por ELISA los sueros reactivos, sospechosos o positivos por FAB.
No existen reportes en la literatura sobre los costos del sistema FAB para el serodiagnóstico de la brucelosis humana. El costo medio total pudiera ser la cota superior, de los costos en que se incurriría si se generalizara el diagnóstico en la atención primaria y en el nivel terciario, donde los costos indirectos son mayores.6 En este estudio no se tuvo en cuenta los costos asociados a la consulta médica y la solicitud de la prueba serológica por parte del médico de asistencia.
El gasto de materiales, el traslado y la recepción de las muestras en el IPK, impactaron de forma negativa en los gastos generales. El costo de extracción de la muestra en el laboratorio de microbiología de Consolación del Sur, resultó ser el más bajo, ya que se trata de una institución perteneciente al Sistema de Atención Primaria de Salud, donde los equipamientos son más escasos y los costos indirectos menores. Se ha demostrado en esta investigación que el costo medio total para una determinación por FAB, resulta económico de forma general, pudiéndose reducir más este indicador, si se realiza la prueba en la atención primaria de salud, donde las condiciones técnicas, y los costos indirectos son menores.
El futuro inmediato del FAB como sistema para la detección de anticuerpos totales, está dirigido a perfeccionar la vigilancia microbiológica de la brucelosis en Cuba y a ofrecer una información oportuna a los médicos de asistencia, lo que influye de forma directa en la prevención y el control de la enfermedad.
REFERENCIAS BIBLIOGRÁFICAS
1. Franco MP, Mulder M, Gilman RH, Smits HL. Human brucellosis. Lancet Infect Dis. 2007;7:775–86.
2. Cruz de la Paz R, Gandul L, Blanco MO, Machado O, Rodríguez C, Seoane G, et al. Programa Nacional de Prevención y Control de Brucelosis humana. Segunda versión. La Habana: MINSAP; 1998.
3. Ministerio de Salud Pública. Dirección Nacional de Estadísticas. La Habana: MINSAP; 2012.
4. VIRCELL SL. España. Brucella ELISA IgM. Brucella ELISA IgG. Taller Nacional de Laboratorio para el Diagnóstico de Brucelosis humana. La Habana: MINSAP. 11 Mar 2012 [citado 12 Mar 2014]. Disponible en: www.vircell.com
5. DIESSE, Diagnostica Senese SpA. Italia. Febrile Antigen Brucella [citado en el Taller Nacional de Laboratorio para el Diagnóstico de Brucelosis humana. La Habana: MINSAP. 11 Mar 2012 [citado 12 Mar 2014]. Disponible en: www.diesse.com
6. Baly A. Costo y costo-efectividad de estrategias comunitarias para el control de Aedes Aegypti y la prevención del dengue. [Tesis presentada en opción al grado científico de Doctor Ciencias de la Salud]. La Habana: IPK; 2010.
7. Dashti AS, Karimi A, Javadi V, Shiva F, Fallah F, Alaei MR, et al. ELISA cut-off point for the diagnosis of human brucellosis; a comparison with serum agglutination test. Iran J Med Sci. 2012;37(1):9-14.
9. Pabuccuoglu O, Ecemis T, El S, Coskun A, Akcali S, Sanlidag T, et al. Evaluation of serological tests for diagnosis of brucellosis. Jpn J Infect Dis. 2011;64(4):272-6.
10. Gómez MC, Nieto JA, Rosa C, Geijo P, Escribano MA, Muñoz A, et al. Evaluation of seven tests for diagnosis of human brucellosis in an area where the disease is endemic. Clin Vaccine Immunol. 2008;15:1031–3.
Recibido: 22 de abril de 2015.
Aprobado: 21 de julio de 2015.
Ana Margarita Obregón Fuentes. Instituto de Medicina Tropical “Pedro Kourí”. Autopista Novia del Mediodía Km61/2. Apdo. 601. Marianao 13. La Habana, Cuba.
Correo electrónico: amobregon@ipk.sld.cu