Introducción
El virus Dengue (DENV) es un miembro del género Flavivirus dentro de la familia Flaviviridae. Se transmite por mosquitos del género Aedes (A. aegypti y A. albopictus) y es la ocurrencia continua del ciclo de transmisión de mosquito-vertebrato-mosquito lo que permite el mantenimiento de este arbovirus en el ambiente.1,2
Actualmente se considera el arbovirus mas importante y frecuentemente transmitido en todo el mundo. Son los responsables de millones de casos de infecciones y miles de muertes. Se estima que aproximadamente de 50-100 millones de nuevas infecciones ocurren anualmente en más de 100 países endémicos y se ha esparcido hacia áreas que previamente no eran afectadas por estos agentes.3
Teniendo en cuenta la severidad de las infecciones que estos virus producen, cuyas manifestaciones pueden ir desde una infección asintomática, a una de las formas de la enfermedad (fiebre dengue y dengue severo), unido a la carencia de tratamiento, actualmente se realizan diversas investigaciones con la finalidad de identificar compuestos para su tratamiento. Así el desarrollo de terapias antivirales es de alta prioridad para la Organización Mundial de la Salud.4 Numerosas propuestas y criterios o estrategias se utilizan en este sentido para el descubrimiento de drogas antivirales entre las que se encuentra el uso de productos naturales. (5
En este sentido, el trabajo tiene el objetivo de evaluar la actividad antiviral de cuatro extractos provenientes de Ageratina havanensis y dos flavonoides aislados de dicha planta frente al virus dengue 2 (DENV 2).
Métodos
Extractos de la planta
Diferentes partes aéreas de la especie A havanensis (Kunth) R. M. King & H. Robinson, en etapa de floración fueron colectadas en Alamar (La Habana) en noviembre del 2012 e identificados por la profesora Iralys Ventosa , del Instituto de Ecología y Sistemática (La Habana, Cuba) , donde se depositó en la colección Voucher de la misma (Ref. HAC-24498). Los metabolitos secundarios fueron extraídos como fue previamente reportado.6,7 Los extractos a evaluar fueron: etanólico de tallo (AH-T-EtOH), butanólico de hojas (AH-H-ButOH), etanólico de hojas (AH-H-EtOH) y de acetato de etilo de hojas, (AH-H-AcEtO).
Los componentes aislados de hojas de Ageratina havanensis,,3-O-β-D-glucosil-7-metoxiaromadendrina (7-metoxiaromadendrina) y 5-O-β-D-glucosilsakuranetina (sakuranetina), fueron identificados y estandarizados mediante técnicas espectroscópicas.6
Para disolver la forma liofilizada de los compuestos se empleó DMSO (Sigma-Aldrich, St Louis, MO.EUA). Una solución madre se preparó con cada extracto y compuestos aislados en el medio de cultivo de la línea celular C6/36 HT (Medio Mínimo Esencial (MEM) suplementado con 1 % de aminoácidos no esenciales (100X), 2 mM de glutamina). Estas soluciones se esterilizaron mediante filtro con poro de 0,2 um (Millipore, MA, EUA).
Células y virus
La línea celular de mosquito (Aedes albopictus) C6/36-HT, sublínea de la C6/36 (ATCC CRL 1660), donada al Laboratorio de Cultivos Celulares del Instituto de Medicina Tropical “Pedro Kourí”, por el doctor Javier Díaz del Laboratorio Departamental de Medellín, Colombia , y la línea BHK21 clono -15 fibroblastos de riñón de hámster sirio recién nacido) ,donada por el Prof. S.B. Halstead , fueron propagadas en medio de crecimiento medio mínimo esencial (MEM) suplementado con 1 % de aminoácidos no esenciales (100X), 2mM de glutamina, y 10 % de suero fetal bovino (Sigma). Ambas líneas celulares se mantuvieron en el medio mencionado anteriormente con concentraciones reducidas de suero al 2 %.
En los ensayos de actividad antiviral se empleó la cepa de virus dengue 2 (DENV-2 A15) aislada del suero de un paciente con fiebre dengue (FD) durante la epidemia cubana de fiebre hemorrágica del dengue en 1981, perteneciente al Banco de Cepas Virales del Laboratorio de Arbovirus del Departamento de Virología del Instituto de Medicina Tropical “Pedro Kourí”. El virus se replicó en la línea celular C6/36 HT y se tituló mediante la formación de placas en células BHK21.
Ensayo de citotoxicidad
La viabilidad celular se determinó mediante el método del MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide, Sigma-Aldrich).8) Para ello, células C6/36-HT (2 x104 células/pocillo) fueron sembradas en placas de 96 pocillos de fondo plano, (Costar®) e incubadas a 33 °C con 5 % CO2 durante 48-72 h, hasta alcanzar una confluencia de la monocapa del 90 %. Diferentes concentraciones crecientes de los extractos (1000 µg/mL hasta 4500 µg/mL y compuestos aislados (entre 100 y 1 000 µg/mL para la sakuranetina y entre 100-950 µg/mL para la 7-metoxiaromadendrina) fueron añadidos empleando 6 pocillos por concentración. Tras 48 h de incubación en dichas condiciones, se añadió 3-(4,5-dimethylthiazol-2-yl)- 2,5-diphenyl tetrazolium bromide (MTT) (concentración final 0,5 mg/mL) a cada pocillo y las placas se incubaron por 4 h. Los cristales de formazán se resuspendieron empleando 100 μL de dimetilsulfóxido anhidro (Panreac®, India) por pocillo. La lectura de los resultados se realizó a una absorbancia de 560 nm, con filtro de referencia de 620 nm, empleando un espectrofotómetro lector de placas multipozos (MRX Revelation, Dynex Technologies, EUA) con el programa integrado Dynex Revelation 4.02.
Ensayos antivirales
La actividad antiviral se evaluó mediante el ensayo de inhibición de la productividad vírica. Monocapas celulares de C6/36-HT crecidas en placas de 96 pocillos se preincubaron con concentraciones subtóxicas crecientes de los extractos y compuestos aislados en estudio, empleando 6 pocillos para cada concentración (de 31 µg/mL hasta 500 µg/mL). Tras una hora de incubación a 33 °C en atmósfera de 5 % CO2 se infectaron con DENV-2 (200 UFP/mL) exceptuando la columna correspondiente al control de células y los controles de los extractos y compuestos evaluados.
Luego de 48 h de incubación en las condiciones requeridas para la línea celular, (33 ºC, en atmósfera con 5 % de CO2) (Binder®, EUA), los sobrenadantes se colectaron y se procedió a la titulación viral mediante la formación de placas en células BHK21. Las placas fueron contadas a los 5 días de incubación a 37 °C. Toda muestra tratada que exhibió un porcentaje de reducción ≥ 50 fue considerada como positiva (presencia de inhibición viral).9 Todas las determinaciones fueron realizadas dos veces por triplicado.
Actividad virucida
La actividad virucida extracelular contra DENV-2 A15 se realizó mediante ensayo de reducción del número de placas. La suspensión viral de DENV 2 (2 x 104 UFP/mL) se mezcló con un volumen idéntico del extracto de planta a evaluar o de medio de cultivo (control negativo) y se incubó 1 h a 37 ºC. Las mezclas se añadieron a las células BHK 21 por 1 h at 37 °C, tras lo cual se procedió a lavarlas tres veces con PBS y añadir el medio de crecimiento con carboximetilcelulosa al 1,5 %, incubándose a 37 °C por 5 días en presencia de 5 % CO2.Tras lo cual se procedió a la tinción, conteo de los focos, y determinación del título infectivo viral.9 El valor de reducción del título infectivo por acción virucida del extracto se obtuvo restándole el log10 del título de cada tratamiento al log10 de su control correspondiente. El ensayo se realizó por duplicado.
Procesamiento estadístico
Para determinar la influencia de los diferentes tipos de extractos y compuestos, o de las diferentes concentraciones ensayadas, sobre el número de placas de lisis contados en cada ensayo, se empleó el análisis de varianzas de Kruskal-Wallis, seguido de un test de Nemenyi para la comparación múltiple de medias, con un nivel de significación estadística de p< 0,05.
Todas las pruebas estadísticas se llevaron a cabo con la ayuda del programa Statistica 6.0 (StatSoftInc 2001). Los gráficos se construyeron empleando el Microsoft Office Excel® 2013.
Se determinó el valor de la CC50 mediante regresión lineal a partir de la ecuación de la línea de tendencia de la curva dosis- porcentaje de viabilidad celular. El ensayo de citotoxicidad fue realizado 2 veces en sextuplicados.
Resultados
Para estudiar las propiedades inhibitorias de la replicación del DENV2 de los extractos (AH-H-EtOH, AH-H-AcEtO, AH-H-ButOH and AH-T-EtOH) y compuestos aislados (flavonoides) obtenidos de A havanensis se realizó un ensayo previo de citotoxicidad en la línea celular de mosquito C6/36HT.
En la figura 1 se muestran los resultados del ensayo de determinación de la CC50 de los cuatro extractos provenientes de A havanensis en células C6/36HT. Para ninguno de los extractos se evidenció citotoxicidad en el rango de concentraciones ensayadas (1 000-4 500 µg/mL).
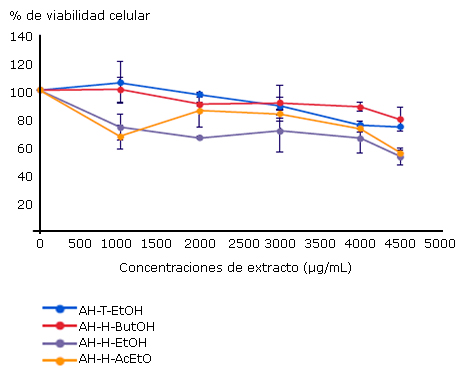 El ensayo MTT se realizó en C6/36 HT tras 48 h de tratamiento con diferentes concentraciones de los extractos. Los resultados son presentados como porcentaje de viabilidad celular realizados por duplicado y utilizando seis pocillos por concentración ensayada.
El ensayo MTT se realizó en C6/36 HT tras 48 h de tratamiento con diferentes concentraciones de los extractos. Los resultados son presentados como porcentaje de viabilidad celular realizados por duplicado y utilizando seis pocillos por concentración ensayada.Fig. 1 Citotoxicidad de cuatro extractos de A. havanensis en la línea celular C6/36 HT.
En la figura 2 se muestran los resultados del ensayo de citotoxicidad con los compuestos aislados. Para ambos flavonoides estudiados sakuranetina and 7-methoxyaromadendrina, la CC50 fue mayor que 1 000 µg/mL.
 El ensayo MTT se realizó en monocapas confluentes de C6/36 HT tras 48 h de tratamiento con las diversas concentraciones de los flavonoides. Los resultados se presentan como porcentaje de la viabilidad celular por triplicado empleando seis pocillos por concentración ensayada.
El ensayo MTT se realizó en monocapas confluentes de C6/36 HT tras 48 h de tratamiento con las diversas concentraciones de los flavonoides. Los resultados se presentan como porcentaje de la viabilidad celular por triplicado empleando seis pocillos por concentración ensayada.Fig. 2 Citotoxicidad de los flavonoides sakuranetina y 7-metoxiaromadendrina en células C6/36 HT.
En la figura 3 se ilustran los valores en porcentaje de la inhibición viral ocurrida como consecuencia de la acción de los extractos evaluados mediante el ensayo de inhibición del rendimiento viral o productividad vírica por conteo de placas en células BHK21.
Los extractos AH-T EtOH y AH-H ButOH provocan una disminución del número de placas de lisis a partir de la concentración de 125 µg/mL. Sin embargo, para el extracto AH-H EtOH esta disminución se manifiesta a partir de la concentración 250 µg/mL, y en el caso del extracto AH-H AcEtO, se evidenció ya en la máxima concentración evaluada, de 500 µg/mL. Los tratamientos con AH-H ButOH, AH-H EtOH y AH-T EtOH no muestran diferencias significativas entre sí (p<0,005). Por otro lado, la comparación estadística de los resultados obtenidos para los extractos etanólicos de ambas partes de la planta (hoja y tallo) evidenció que no existen diferencias estadísticamente significativas entre estos valores (p< 0,005).

Fig. 3 Porcentaje de inhibición de la productividad vírica como consecuencia de la acción de los extractos evaluados en C6/36HT para la cepa DENV-2 A15.
En resultados que no forman parte de este estudio pudimos comprobar también la ocurrencia de inhibición viral, mediante la reducción de genomas virales en aquellos cultivos tratados con extractos y concentraciones que mostraron mayor actividad, mediante una RT-PCR. En el mismo se obtuvo que la banda correspondiente al control viral se observa más gruesa e intensa, y exhibe notable diferencia respecto al resto de los cultivos tratados.
Los resultados obtenidos tras el ensayo virucida extracelular de los dos extractos seleccionados (AH-T EtOH y AH-HButOH) frente a la cepa DENV-2 A15 se muestran en la tabla.
Tabla Actividad virucida extracelular de los extractos AH-T EtOH y AH-HButOH frente a la cepa DENV-2 A15
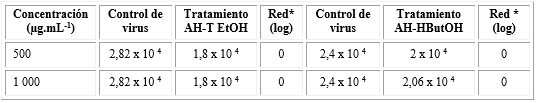
* Reducción del logaritmo del título infectivo viral.
Ensayo de pesquisa primaria de actividad antiviral de sakuranetina y 7-metoxiaromadendrina
El tratamiento con la sakuranetina arrojó valores de inhibición de la productividad viral entre un 61-91 %, mientras que para la 7-metoxiaromadendrina se registraron valores de reducción viral comprendidos entre 64-86 % (Fig. 4). El análisis estadístico no exhibe diferencias significativas entre sí para un nivel de significación de 0,05.
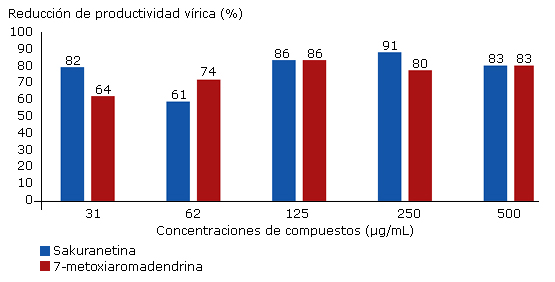
Fig. 4 Porcentaje de reducción de la productividad vírica registrados para las diferentes concentraciones de los flavonoides evaluados, con respecto a los controles virales, los que se toman como un valor referencial de 0 % de reducción.
Sin embargo, al comparar el número de UFP, debido a las diferentes concentraciones ensayadas de ambos compuestos, con respecto al control sin tratar, se encontró que cualquiera de estas provoca una marcada disminución de la productividad viral.
Discusión
El Dengue es una infección viral re-emergente de gran impacto actual en el mundo. El número de casos de enfermedad severa continúa creciendo en áreas endémicas del sudeste de Asia, América Central y Sudamérica, y en otras regiones subtropicales.10
Consta de cuatro serotipos transmitidos por mosquitos. La infección produce un amplio espectro de enfermedad clínica desde asintomáticos hasta enfermedad febril autolimitante. La fiebre del dengue conocida como fiebre quebranta huesos incluye síntomas de fiebre, dolor muscular y rash. Un porcentaje menor de individuos presenta fiebre hemorrágica y síndrome de shock (DHF/DSS).11
En la actualidad no se dispone de algún agente antiviral para su empleo en terapia a pesar del incremento en los estudios dirigidos a la búsqueda y desarrollo de antivirales contra dengue.12,13) De ahí la urgente necesidad del desarrollo de compuestos efectivos anti dengue para combatir esta infección epidémica.14,15
En este sentido y con el objetivo de revelar un candidato contra DENV a partir de plantas, en el presente trabajo se realizó una pesquisa antiviral a partir de extractos provenientes de Ageratina havanensis y compuestos aislados a través de ensayos in vitro en la línea celular C6/36HT, con concentraciones crecientes de los mismos y detectando la acción inhibitoria mediante reducción de la productividad vírica.
Se conoce que DENV puede infectar un amplio rango de diferentes tipos de células y el tropismo celular parece estar directamente relacionado a la patogénesis del virus.16,17 Las células de mosquitos constituyen verdaderos blancos tisulares en la infección natural y consecuentemente dichas células son apropiadas para estudios antivirales.18
Como ensayo de pesquisa primaria empleando el DENV infeccioso se realizó un ensayo de tratamiento continuo para determinar la actividad antiviral en cualquier etapa del ciclo de replicación viral en los cultivos de células C6/36HT, detectándose la inhibición a través de evaluación del rendimiento viral o productividad vírica por conteo de placas en células BHK21, a partir de las muestras tratadas y no tratadas del ensayo de pesquisa primaria.
Los resultados de los ensayos primarios de actividad antiviral muestran que todos los extractos poseen actividad inhibitoria sobre la multiplicación in vitro de DENV 2 cepa A 15 en células C6/36HT. Los valores de citotoxicidad de todos los extractos se encuentran por encima de 4 500 µg/mL (ya que hasta tal concentración estudiada no muestran efecto citotóxicos), lo que demuestra baja citotoxicidad, aspecto positivo en los ensayos de evaluación de un candidato antiviral. Estos resultados son similares a los descritos por del Barrio y otros en 2011 frente al virus herpes simple (HSV) en la línea celular Vero.6 Igualmente García et al informaron la baja citotoxicidad de extractos etanólicos procedentes tanto de hojas como de tallo de esta planta en células de mamífero.7Por lo que resultaría de gran interés analizar el comportamiento de estos extractos en células de mamíferos frente al virus dengue.
Los ensayos antivirales evaluados por inhibición de la productividad vírica mostraron actividad inhibitoria de todos los extractos lo que permite afirmar que son activos frente a virus dengue A2 cepa A 15.
Similar actividad antiviral ha sido informada previamente para extractos de esta planta frente al virus herpes simple. Así como la carencia de actividad virucida extracelular frente a este virus.6
Si bien los datos aquí mostrados no se dirigen al estudio del modo de acción de los extractos y flavonoides aislados provenientes de esta planta si es posible afirmar que no ejercen acción directa extracelular sobre el virus, Ulteriores estudios permitirán evidenciar el paso o pasos inhibidos.
Pocas investigaciones existen respecto a las propiedades biológicas de Ageratina havanensis, limitándose la información disponible sobre todo a su caracterización fitoquímica.7
Los resultados obtenidos en este trabajo han demostrado el potencial que encierra la planta Ageratina havanensis para la obtención de un posible fármaco antiviral contra DENV a partir de una evaluación más detallada de sus fracciones y compuestos. Más investigaciones se requieren con el objetivo de profundizar en los mecanismos de acción y en la naturaleza de la interacción que puede existir entre los flavonoides aislados, los cuales mostraron gran potencial antiviral.
El hallazgo de actividad de los diferentes extractos de Ageratina havanensis frente a virus dengue constituye un resultado significativo, teniendo en cuenta la importancia epidemiológica de esta infección, sus niveles, hospitalización y posibles complicaciones que acarrea.
Existen numerosos informes que muestran el potencial antiviral de diversos flavonoides. Como ejemplo, se ha encontrado que la epigalocatecina y la quercetina, inhiben la replicación viral de HHV-1 y HHV-2 en células Vero19 y también se conoce la actividad antiherpética de extractos de plantas ricos en flavonoides.20,21 Otros autores informan la determinación de actividad antiviral contra DENV en flavonoides como la quercetina y daidzeína, también rutina y fisetina.22,23 En el presente estudio para ambos compuestos, sakuranetina y 7-metoxiaromadendrina, se registró un porcentaje de reducción de la productividad vírica superior a 50 % a partir de la mínima concentración evaluada. Los datos obtenidos demuestran por primera vez la acción antiviral contra DENV de los flavonoides sakuranetina y 7-metoxiaromadendrina, los que resultan adicionalmente novedosos desde el punto de vista fitoquímico, ya que nunca antes se habían encontrado descritos para esta especie vegetal.
Teniendo en cuenta los datos epidemiológicos relacionados con las infecciones por este virus, el potencial de estos virus de provocar eventos epidémicos y la elevada circulación, los resultados informados en este trabajo evidencian la importancia y perspectivas en el estudio de los productos naturales como alternativas para la búsqueda de posibles antivirales.














