Introducción
En todo proceso infeccioso causado por una bacteria, la interacción entre las bacterias patógenas y los tejidos del hospedero constituye un evento crucial para la adhesión primaria y la colonización tejido-específica. La adherencia bacteriana se considera un prerrequisito para la colonización, pues las bacterias no adherentes son rápidamente eliminadas por mecanismos inespecíficos de defensa del hospedero, como el peristaltismo, el movimiento ciliar y el flujo de líquidos, o por el recambio de células del epitelio y de la capa mucosa.1)
La adhesión es también el primer paso para mantener a los miembros de la microbiota normal en el intestino; en donde se comporta de manera inocua y constituye un miembro importante Escherichia coli. Sin embargo, los patotipos de E. coli son una de las causas más importantes de diarrea aguda y persistente en niños de países en vías de desarrollo.2 Actualmente, se reconocen seis grupos en base a criterios clínicos, epidemiológicos y moleculares: E. coli enteropatogénica (EPEC, de sus siglas en inglés), E. coli enterotoxigénica (ETEC, de sus siglas en inglés), E. coli enteroinvasiva (EIEC, de sus siglas en inglés), E. coli productora de shiga toxina (STEC, de sus siglas en inglés), E. coli enteroagregativa (EAEC, de sus siglas en inglés) y E. coli de adherencia difusa (DAEC, de sus siglas en inglés).1,2,3
El proceso de adherencia es fundamental en el desarrollo de la mayoría de las infecciones ocasionadas por E. coli, y las investigaciones encaminadas a analizar este evento incluyen estudios in vitro utilizando cultivos de líneas celulares. El ensayo de adherencia sobre células epiteliales HEp-2 se considera el estándar de oro dentro de las pruebas fenotípicas de diagnóstico para la identificación de cepas de E. coli patógenas intestinales.4
Inicialmente, en las cepas patógenas humanas de E. coli intestinales se informaron tres patrones morfológicos de adherencia in vitro a células epiteliales: adherencia localizada, adherencia difusa y adherencia agregativa.2,3 Estos diferentes patrones de adherencia se han relacionado con los procesos patogénicos específicos que ocasionan los patotipos de E. coli; por ejemplo, el patrón de adherencia localizada fue detectado inicialmente en EPEC, mientras que cepas de E. coli que muestran patrones de adherencia difusa, han sido aisladas de heces de infantes con diarrea aguda. Por su parte, EAEC ha sido asociada a brotes o casos esporádicos de diarrea persistente.3,5 Recientemente se han observado estos patrones de adherencia in vitro en ensayos con aislados de E. coli uropatogénica, siendo la adherencia agregativa la que se presenta con más frecuencia.2 En contraparte, existen pocos estudios en relación con los fenotipos de adherencia in vitro de E. coli aisladas del ambiente, como por ejemplo ecosistemas acuáticos.
El presente trabajo tuvo como objetivo determinar los fenotipos de adherencia de cepas de E. coli aisladas de ecosistemas dulceacuícolas de La Habana en células epiteliales en cultivo.
Métodos
Microorganismos
Se estudiaron un total de 108 cepas de Escherichia coli ambientales, las cuales fueron aisladas de muestras de agua colectadas de los ríos Almendares, Quibú y Luyanó de La Habana. Para la identificación de las cepas se empleó el sistema API 20E (bioMérieux). Las cepas forman parte de la colección microbiana del Departamento de Microbiología y Virología de la Facultad de Biología de la Universidad de La Habana.
Ensayos de adherencia en células HEp-2
Se realizaron ensayos de adherencia a células de la línea celular HEp-2 utilizando el método propuesto por Cravioto y otros.6,7 Las células HEp-2 en cultivo in vitro infectadas durante 3 h con las cepas de E. coli evaluadas se fijaron con metanol al 70 % y se realizó una tinción con colorante de Giemsa para su posterior observación. Se emplearon como controles las cepas: E. coli O42 (patrón de adherencia agregativa), E. coli 87124 (patrón de adherencia difusa) y E. coli 2348/169 (patrón de adherencia localizada) conservadas en el Laboratorio de Investigación Básica del Departamento de Salud Pública de la Facultad de Medicina de la Universidad Nacional Autónoma de México (UNAM).
El ensayo de adherencia se realizó por triplicado para cada cepa. Se consideraron positivas para algún patrón aquellas cepas que se encontraban adheridas en el 40 % o más de las células de la preparación.
La observación se realizó en un microscopio óptico (Microscopio ZEISS AX10LAB), en campo claro, con un aumento de 100X con aceite de inmersión. En los casos pertinentes se realizó una micrografía (Microscopio ZEISS AX10LAB HBO 50 conectado a una cámara Cool Snap-Pro, Color and Integrated Solution, Media Cybernetics the Imaging Experts). Las microfotografías se capturaron en el programa LAB WORK 45.
Serotipificación
La serotipificación de las cepas de E. coli se realizó según el procedimiento descrito por Orskov y Orskov.8 Se emplearon sueros específicos anti-O (antígeno somático) y anti-H (antígeno flagelar) (SERUMAN, México) para 174 antígenos somáticos y 56 flagelares. Las reacciones de aglutinación se efectuaron en microplacas de 96 pozos de fondo en forma de “u” (COSTAR).
Resultados
El 25 % de las cepas presentó adherencia a las células HEp-2, mientras que el 75 % resultó no adherente. En las cepas adherentes se observaron dos de los tres patrones de adherencia típicos descritos previamente en cepas de E. coli causantes de diarrea en humanos. Veintidós cepas mostraron el típico patrón de adherencia difusa en el que las bacterias se adhieren sobre toda la superficie celular. Cinco cepas mostraron una adherencia agregativa (Fig.). Se encontraron cepas de los dos patrones de adherencia en los tres ríos evaluados.
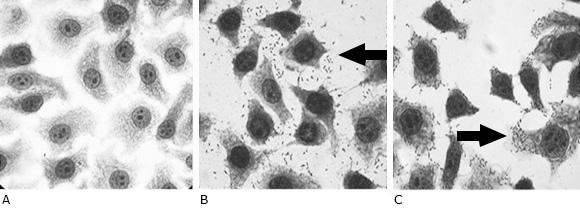
Fig Células HEp-2 en cultivo in vitro infectadas durante 3 h con cepas de E. coli aisladas de tres ecosistemas dulceacuícolas de La Habana, fijadas con metanol al 70 %, teñidas con el colorante de Giemsa y observadas bajo microscopia de luz convencional (aumento 100x).
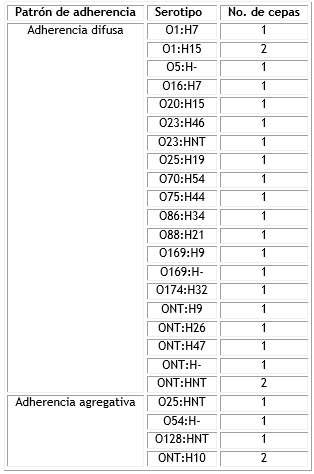
De los 24 serotipos descritos en las cepas que presentaron adherencia, los serotipos O1:H7, O5:H-, ONT:H47, ONT:HNT y ONT:H10 se han informado en la literatura asociados a brotes diarreicos. Los cuatro primeros asociados a la categoría STEC con un patrón de adherencia difusa y el último a EAEC con un patrón típico de adherencia agregativa (Tabla).
Discusión
El patrón de adherencia difusa es el patrón característico del grupo patógeno ADEC aunque se ha descrito también en cepas atípicas de EPEC y el patotipo STEC. Las cepas ADEC se pueden aislar tanto de personas sanas como de personas con diarrea, siendo más importantes en niños de 4 a 5 años.9 Aunque aún no se conoce todo sobre el mecanismo de patogenicidad de este patotipo, se han caracterizado fimbrias de superficie las cuales están directamente involucradas en el fenómeno de adherencia difusa. Los genes que codifican para estas fimbrias se pueden encontrar en el cromosoma o en un plásmido.10) Los factores de virulencia asociados al fenotipo de adherencia difusa incluyen las fimbrias Afa/Dr, AIDA, y Daa codificadas en operones con su mismo nombre los cuales se han detectado también en cepas de E. coli no patógenas.5,11) El fenómeno de adherencia en este patotipo está directamente relacionado con su patogenicidad. Al realizar ensayos in vitro en células HEp-2 y otras líneas celulares,7 las cepas ADEC tienen la capacidad de inducir la formación de estructuras protuberantes, semejantes a dedos, las cuales confieren protección a las bacterias, pero la presencia de dichas estructuras no se ha demostrado in vivo. ADEC es el patotipo menos caracterizado de todos y tal vez el grupo más heterogéneo desde el punto de vista serológico.12 Se han descrito una amplia variedad de serogrupos y serotipos entre las cepas de ADEC,13 lo cual está en correspondencia con los resultados obtenidos en el presente trabajo.
Las cepas de EAEC causan diarreas de larga duración principalmente en niños y viajeros de países del tercer mundo, pero también son una causa significativa de diarrea en Europa.14,15,16 Su reservorio es únicamente el ser humano. Presentan un plásmido (pAA) que codifica para una adhesina fimbrial que es responsable del patrón de adherencia agregativa a las células HEp-2 y al epitelio intestinal. Este tipo de adherencia favorece no solo la colonización intestinal de este patotipo sino que también favorece la formación de biopelículas sobre superficies no biológicas.17,18 EAEC necesita de otros factores de virulencia para inducir enfermedad, sobre dichos factores se continúa investigando en la actualidad, pero se cree incluyen el factor de regulación global AggR, varias enterotoxinas y proteasas séricas.12,18
Las proteasas séricas son proteínas autotransportadoras capaces de translocarse del periplasma a través de la membrana externa al exterior de la bacteria. Las de clase I son citotóxicas para las células epiteliales, y su miembro más importante es Pet (Plasmid-endoded toxin).19,20 La de clase II son capaces de cortar proteínas asociadas a la respuesta inmunitaria y expresadas en la superficie de células intestinales y ejercer una función inmunomoduladora.21
Entre las cepas enteroagregativas asociadas a eventos diarreicos se han descrito un número reducido de serogrupos y serotipos en la literatura.3,13 Sin embargo, las cepas de EAEC han cobrado gran importancia en la clínica en los últimos tiempos, sobre todo después del brote en que más casos de síndrome urémico hemolítico (SUH) se han producido en el mundo hasta la fecha.22 Este brote tuvo lugar en Alemania en el año 2011, con más de 852 casos de SUH y 3 469 casos de diarrea, en el que fallecieron 50 pacientes, incluídos 32 con SUH. La cepa responsable de este brote se sabe fue una cepa nueva, probablemente de origen humano que emergió a partir de una cepa enteroagregativa del serotipo O104:H4 que adquirió un fago portador del gen stx2a a partir de una cepa E. coli productora de toxina shiga.22 Se consideró una cepa muy virulenta, que contaba con un gran número de genes de virulencia. Se plantea que su capacidad enteroagregativa le permitía colonizar mejor el epitelio intestinal y además contaba con un mecanismo que le permitía liberar mayor cantidad de la toxina STX2 variante a, además tenía al menos tres adhesinas (AAF/I, LPF-lpfAO26 e Iha), dos sideróforos (aerobactina y yersiniabactina) y tres tipos de proteasas SPATE (Pic, Sig A y SepA).23
Investigaciones epidemiológicas apoyan la hipótesis de que el brote de Alemania24 fue causado por el consumo de brotes obtenidos a partir de semillas de fenogreco importadas de Egipto.22 Aunque el vehículo más frecuente en los brotes causados por STEC es la carne de vacuno poco cocinada,25 en los últimos años cada vez son más los brotes causados por productos vegetales, especialmente de ensaladas y brotes de diferentes semillas.22 Se desconoce cómo han podido contaminarse las semillas, pero se supone que puede haberse debido al empleo de agua de riego contaminada con aguas residuales de origen humano.22
Curiosamente el brote más grande en número de casos de diarrea y colitis hemorrágica fue producido por una cepa de STEC O157:H7 en el año 1996 en la ciudad de Sakai (Osaka, Japón) y se asoció con el consumo de brotes de rábano.26 Las cepas EAEC también han causado varios brotes asociados con el consumo de vegetales frescos, incluyendo un brote por el serotipo ONT:H10 sucedido en Japón en 1993 que afectó a más de 2 000 personas,27 serotipo que también se aisló en los ecosistemas dulceacuícolas evaluados.
Estudios futuros examinaran si las cepas enteroagregativas tienen mecanismos especiales que le permitan adherirse a la superficie de los vegetales. Lo que es evidente que las condiciones de producción de los brotes vegetales (humedad y temperatura) favorecen el crecimiento de los microorganismos contaminantes.28
Este ejemplo demuestra la importancia de la detección de cepas de esta categoría en cualquier ambiente, ya que la circulación de cepas hipervirulentas como la responsable del brote en Alemania podría representar un serio problema para la salud pública.
La transmisión de microorganismos que causan enfermedades diarreicas agudas (EDA) a través de alimentos y agua es importante en países en vía de desarrollo como también en países industrializados. Se cree que el intercambio comercial de productos alimentarios contribuye a la transmisión de patógenos intestinales de país a país, entre ellos las cepas de E. coli enteropatógenas.28
Estudios realizados en Colombia plantean que el consumo de agua contaminada es tal vez el factor más importante en la transmisión de E. coli enteropatógenas. La calidad de agua para consumo humano en áreas rurales del país es más deficiente que la calidad del agua en áreas urbanas, lo cual puede en parte resultar en mayor número de casos de EDA en la población rural.2,29) Por otra parte, el consumo de productos alimentarios contaminados con E. coli patógenos intestinales se asocia también a EDA. En el 2010, se informó que el 30 % de los productos alimentarios disponibles en supermercados en Bogotá estaban contaminados con E. coli patógenas intestinales. Los agentes más comunes aislados de vegetales y carne de res fueron STEC y EAEC.30
Teniendo en cuenta que la contaminación del agua y los alimentos son los mecanismos más importantes de la transmisión de patógenos entéricos, es primordial que la comunidad consuma agua potable y que elimine los agentes microbianos de alimentos contaminados mediante cocción (carnes y vegetales) o lavado (frutas), o que se retiren del mercado alimentos altamente contaminados.2,31) Para determinar el grado de contaminación del agua y alimentos para consumo humano, una vigilancia epidemiológica de estos microorganismos es primordial.
En Cuba, se han descrito muy pocos brotes de diarrea causados por estas cepas relacionados con aguas contaminadas, sin embargo, la presencia de estas cepas con características adherentes en los ríos evaluados constituye una alerta de la deficiente calidad microbiológica que presentan las aguas de estos ríos y del riesgo para la salud que podría representar el uso inadecuado de las aguas de estos ecosistemas por la población de La Habana.