Introducción
El dengue es la enfermedad arboviral más importante a nivel mundial en términos de número de infecciones anuales y morbilidad global.1 Cada año ocurren 390 millones de infecciones de ellas 100 millones son asintomáticos.2 Su agente causal es el virus dengue (VDEN) un complejo de cuatro serotipos (VDEN-1 a 4).3 Presenta un genoma ARN de simple cadena positiva rodeado por una nucleocapsida (C), la proteína de envoltura (E) y la proteína de membrana (M). La proteína E es la más externa de los viriones, la más conservada del género y el mayor determinante antigénico de la partícula viral.4 La expresión de esta proteína ha sido determinada por varios investigadores en la superficie de líneas celulares de mamíferos (Vero, riñón de mono verde africano) y mosquitos (mosquito (C6/36-HT, Aedes albopictus) mediante inmunomicroscopía y ensayos inmunoenzimáticos respectivamente.5,6
Se han usado diferentes estrategias en la búsqueda de antivirales, como el estudio extensivo de compuestos que actúen sobre enzimas virales e incluso estudios bioinformáticos.7 Durante las últimas décadas, se evaluaron determinados compuestos naturales, tratando de identificar aquellos con posible actividad antiviral contra VDEN.8) Se utilizaron múltiples plataformas novedosas como, la cuantificación del efecto del compuesto sobre el rendimiento viral y/o el efecto de producción de ARN, la propuesta de máxima capacidad de tamizaje (High-throughput screening approach) entre otros.9,10 No obstante, estas nuevas tecnologías abarcan el uso de equipos, robots y programas computarizados muy caros que restringe su uso.11
Tradicionalmente, se han empleado diferentes técnicas para evaluar agentes antivirales, entre ellas se encuentra la neutralización por reducción del número de placas (NRNP).12 Esta prueba se ha utilizado para cuantificar la actividad lítica de virus, llegando a convertirse en la regla de oro. La actividad lítica es detectada en células infectadas, mediante el análisis macroscópico de las placas virales, a través de la tinción con colorantes. No obstante, a pesar de su utilidad posee también desventajas.13 Existen pocos reportes que empleen el ELISA in situ o celular para detectar actividad antiviral. Uno de ellos, ha sido para evaluar la actividad anti-VDEN de extractos de algas marinas, por sus resultados rápidos y objetivos empleando materiales y reactivos comunes en muchos laboratorios.11
Esta investigación, realiza una evaluación preliminar de la actividad antiviral de extractos de Ageratina havanensis utilizando dos sistemas inmunoenzimáticos constituidos por un ELISA celular (ELISAc) y la técnica de inmunoperoxidasa a través de la detección de la expresión de la proteína E.
Métodos
Líneas celulares y virus
Líneas celulares empleadas: C6/36-HT (de la línea C6/36, Aedes albopictus, ATCC® CRL 1660), crecidas en Medio Mínimo Esencial (MEM) con 1 % de aminoácidos no esenciales (100X), 2 mM de glutamina, antibióticos (penicilina 100 UI/mL y estreptomicina 100 mg/mL) y 10 % de suero fetal bovino inactivado (SFBI) e incubadas a 33 ºC y células Vero, (células de riñón de mono verde africano, Cercopithecus aethiops, ATCC CRL-1586™), mantenidas en Medio 199 (medio de mantenimiento, MM) con antibióticos (penicilina 100 UI/mL y estreptomicina 100 mg/mL) y 10 % de SFBI, incubadas a 37 ºC.
El virus DEN-2 cepa A15, del Laboratorio de Arbovirus del IPK, obtenida del suero de un paciente durante la epidemia cubana de fiebre hemorrágica de dengue en 1981.14 Las reservas de virus fueron preparadas mediante dos pases en cerebros de ratones lactantes y cinco pases enC6/36-HT para su posterior titulación en células Vero por el método de formación de placas líticas.15
En el ELISA de doble anticuerpo se aplicó como antígeno, una suspensión del virus en células C6/36-HT. Las líneas crecieron a 33 y a 37 ºC respectivamente.
Extractos, anticuerpos y compuestos
Los extractos fueron obtenidos a partir de la planta Ageratina havanensis. El material vegetal fue colectado e identificado por la Prof. Iralys Ventosa del Instituto de Ecología y Sistemática (Ref. HAC-42498). Los metabolitos secundarios fueron obtenidos como se ha reportado previamente.16
Extractos: Etanólico de tallo, AH-T-EtOH (5 mg/mL); butanólico de hoja, AH-H-ButOH (5mg/mL); acetato de etilo de hoja, AH-H-AcEtO (5mg/mL).
El anticuerpo monoclonal (AcM H3/6) que reconoce la proteína E de los cuatro serotipos del VDEN,17 fue producido in vivo (Laboratorio de Anticuerpos Monoclonales, IPK) y utilizado en forma de líquido ascítico hiperinmune (LAH, AcM-LAH).
En los ensayos inmunoenzimáticos se utilizaron como controles un anticuerpo policlonal anti-dengue (AcPαD, IPK) e interferón Alfa recombinante (IFN AR, Heberon® Alfa R 10 M, 100 UIF/Ml).
Determinación del reconocimiento de la proteína E por ELISA de doble anticuerpo
Las placas de poliestireno sensibilizadas con inmunoglobulinas totales humanas anti-dengue a una concentración de 10 mg/mL se incubaron durante toda la noche a 4ºC. A continuación, se bloquearon con albúmina bovina sérica (ABS) al 1 % durante 1h, posteriormente, se adicionó el antígeno (VDEN- 2A15) en tampón fosfato salina (PBS). Se incubó 1h y se añadió el AcM-LAH (diluciones al doble 1/100 a 1/6400). Como controles positivo y negativo se aplicaron sueros de ratón hiperinmune y negativo a VDEN, respectivamente. El conjugado fue anti-ratón peroxidasa (Sigma-Aldrich, St. Louis, MO, USA) y posteriormente se añadió ortofenilendiamina (OPD) y peróxido de hidrógeno (H2O2) como sustrato. La lectura se efectuó en un lector de microplacas ELISA a una longitud de onda de 492 nm.18
Se determinaron las condiciones óptimas del sistema utilizando varias diluciones de los componentes. Se emplearon dos tipos de antígenos del VDEN- 2 A15 uno proveniente de una línea celular (C6/36-HT, AgC) (dilución optima 1/4) y el otro de cerebro de ratón lactante19 (AgCR) (dilución óptima 1/40). La dilución óptima del conjugado fue 1/1000. Se consideró como criterio de valor de corte el doble de la DO del control negativo.
Normalización de un ELISA celular (ELISAc) para la detección de la proteína E de VDEN
Apoyados en estudios previos, en la utilización del ELISAc11,20) se establecieron las condiciones óptimas del ensayo, considerando: Líneas celulares (C3/36-HT y Vero), tiempo de incubación (48-96 h), solución fijadora (glutaraldehído de 0,05 %-0,025 % y metanol-acetona v/v, solución de bloqueo (ABS al 1% y leche descremada (LD) al 1% y al 3% en solución salina fosfato).
La detección de la proteína E de VDEN se realizó en células C6/36-HT y Vero (2x105 cel/mL). Veinticuatro horas después, las monocapas fueron inoculadas con VDEN-2 A-15 a una multiplicidad de infección (m.o.i) de 0.1 durante 1hr de adsorción a las temperaturas óptimas de crecimiento de cada línea celular (33 ºC y 37 ºC, respectivamente). Transcurrida la adsorción, fue añadido el medio de mantenimiento e incubadas las monocapas durante 48 h (C6/36-HT) y 72-96 h (Vero) fijándolas posteriormente con glutaraldehído (0,05 % y 0,025 %) y metanol-acetona v/v durante 15 min a temperatura ambiente. Eliminado el contenido de la placa, se bloqueó con ABS al 1 % en PBS (células Vero) o LD al 1% y 3% (células C6/36-HT), durante 1 h a 37 ºC. El AcM-LAH fue añadido en diluciones al doble desde 1/100 a 1/3 200. Como controles negativos fueron adicionados PBS y medio de cultivo (MEM y 199, según la línea celular) y como control positivo AcPαD. Las muestras se incubaron durante 2h a 37º C y posteriormente lavadas 4 veces con tampón de lavado (0,01 % Tween-20 PBS). El conjugado, anti-ratón peroxidasa (1/1000, Sigma-Aldrich, St. Louis, MO, USA) fue aplicado y la incubación se realizó durante 1h a 370 C. La reacción se desarrolló utilizando OPD y H2O2 como sustrato. La lectura se efectuó en un lector de microplacas (Multiskan) a una longitud de onda de 492 nm. Se consideró como el título de mayor expresión de la proteína E el VDEN la máxima dilución del AcM-LAH donde se observó un valor de densidad óptica (DO) mayor o igual al doble del control celular (medios de cultivo).
Determinadas las condiciones óptimas para el ensayo, fueron utilizadas para la evaluación de los extractos con posible actividad antiviral.
Evaluación de la actividad antiviral de Ageratina havanensis al VDEN-2 mediante el ELISAc
Este estudio se realizó a partir de resultados previos,16) utilizando los mismos lotes de extractos y sustrato celular donde la concentración citotóxica media (CC50) estuvo por encima de 4 500 μg/mL. Se seleccionó la concentración de 500μg/mL como concentración de partida para determinar la actividad antiviral de los tres extractos acuosos procedentes de Argeratina havanensis por el ELISAc. Las células Vero en placas de 96 (Costar®) a una concentración de 2 x 105 células/mL, fueron incubadas durante 72 h a 37 ºC hasta la confluencia de la monocapa.
Los extractos se agregaron a diferentes concentraciones (AH-T-EtOH, AHH-ButOH, AH-H-AcEtO a 125; 250 y 500 μg/mL en medio de cultivo) en dos tiempos. En el T0 (tiempo 0) la adición se realizó una 1h antes de la inoculación con el VDEN A-15 a una m.o.i de 0.1, mientras que el T1, (tiempo 1) los extractos se añadieron 1 h posinoculación. En ambos casos, después de la adición, las placas se incubaron 1 h a 37 ºC y se utilizaron como control negativo medio de cultivo y como positivo IFN AR (100 UIF/mL). Posterior a 96 h de incubación, las células fueron fijadas agregando metanol-acetona (v/v) durante 15 min a temperatura ambiente. Se bloqueó con LD al 1 % en PBS durante 1h a 37 ºC y añadido el AcM H3/6 en dilución 1/25 en PBS para incubar durante 2 h a 37 ºC y el anticuerpo secundario anti-ratón peroxidasa (1/1000, Sigma-Aldrich, St. Louis, MO, USA) 1 h a 37 ºC. Cada evento fue acompañado por 4 lavados con 0,01 % Tween-20 PBS. La reacción se reveló con OPD yH2O2 al 0,001 % como sustrato y la lectura efectuada en un lector de microplacas (Multiskan) a una longitud de onda de 492 nm utilizando como referencia una lectura a 620 nm. La muestra se consideró positiva a la dilución en que DO fue dos veces mayor a la DO del control celular. Se incluyeron controles apropiados como células Vero infectadas y no tratadas y células infectadas y tratadas con el IFN AR. Todas las determinaciones fueron realizadas dos veces y cada una por duplicado.
Los % de inhibición fueron calculados según la fórmula:
Donde av es el antiviral con el virus y v es el virus sin el antiviral. A todos los valores les fue restado el valor del control celular (CC).20
Evaluación preliminar de la actividad antiviral de A. havanensis frente al virus dengue 2 mediante inmunoperoxidasa
El ensayo se utilizó a partir del reconocimiento del AcM H3/6AcM murino, en las células infectadas con el VDEN2 y su reacción con el conjugado antiratón peroxidasa revelado por el sustrato.
Basado en resultados precedentes21 se utilizó este AcM. Las placas de 24 pozos sembradas con una suspensión de células Vero a 2 x 105 células/mL se incubaron por 72 h hasta la obtención de monocapas confluentes. Posteriormente, el medio de las placas fue retirado y se ejecutaron dos protocolos:
Adición de 100 uL de una suspensión de virus DEN-2 A15 con un título de 2x104 ufp/mL, incubación a 37 ºC por 1 h y seguidamente adición de los diferentes extractos en concentraciones subtóxicas (500 μg/mL) de los extractos (AH-T-EtOH, AH-H-ButOH y AH-H-AcEtO), preparados en medio 199.
Adición de los diferentes extractos (AH-T-EtOH, AH-H-ButOH y AH-H-AcEtO), en las mismas condiciones del protocolo 1, incubación por 1 h seguida por la incorporación de la suspensión viral descrita anteriormente.
Ambos protocolos siguieron idéntico procedimiento. Las placas se incubaron durante 96h a 37 ºC y seguidamente se descartó el contenido. Las células se fijaron al soporte con metanol acetona (v-v) durante 15 min. El bloqueo fue con LD al 1 %, y la incubación 1 h a 37 ºC. Se adicionó el conjugado anti-ratón peroxidasa por 1hr y su sustrato diaminobencidina diluida en PBS y H2O2 al 0,001 % y se observó al microscopio.
Como controles, en ambos casos, se designaron pozos sin extractos solo con medio 199 (controles virales) y pozos sin suspensión viral (controles de extracto).
Como control positivo de la expresión de la proteína E se administró el AcM-LAH a diluciones seriadas (1:25, 1:50, 1:100) durante 2 h a 37 ºC.
Como control positivo de actividad antiviral se aplicó el interferón alfa 2 A recombinante (100 UI/mL) y se incubó durante 96h a 37 ºC.
En cada paso se realizaron los lavados correspondientes empleando PBS 1 %.
Resultados
La proteína E del VDEN media la entrada del virus a la célula hospedera, por ello fue tomada como blanco para la determinación preliminar de la actividad antiviral al VDEN. A partir de la disponibilidad del AcM H3/6 murino especifico a la proteína E; su no expresión indicaba la actividad antiviral de los diferentes extractos obtenidos de la planta Ageratina havanensis.
Normalización del ensayo inmunoenzimático celular (ELISAc)
El cuadro muestra los parámetros óptimos en la normalización del ELISAc.
Evaluación preliminar de la actividad antiviral de los extractos acuosos de Ageratina havanensis ante VDEN-2
La inhibición de la replicación viral en ambos tiempos de adición del extracto AH-T-EtOH fue baja (Fig. 1), alcanzando un valor menor al 50 % de inhibición. Hubo un incremento discreto (de 38 % a 43 %) de la misma, al adicionar dicho extracto 1 h después de la inoculación, presentando su mayor valor a la concentración de 500 μg/mL. Este incremento del efecto inhibitorio sobre la replicación viral indica una menor expresión de la proteína E.
Extracto AH-T-EtOH
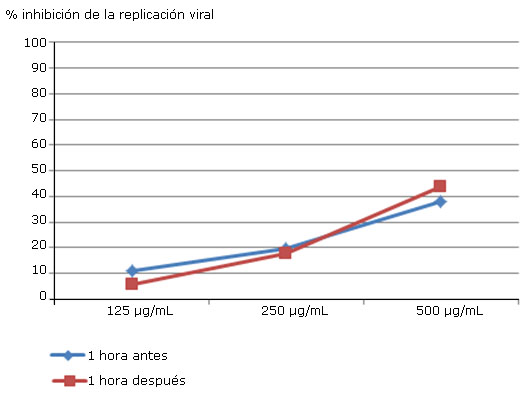
Fig. 1 Valores de inhibición de la replicación del virus DEN-2 obtenidos al añadir concentraciones crecientes de AH-T-EtOH 1 h antes y 1 h posinoculación.
El extracto AH-H-BuTOH (500 μg/mL) (Fig 2), inhibió el 90% de la replicación viral en ambos tiempos. La adición 1 h posinoculación tuvo un comportamiento gradual a diferencia de 1 h antes de la inoculación. En la concentración 125 μg del extracto se evidenció un 30 % de inhibición de la replicación viral sugiriendo que la misma podría iniciarse a valores inferiores a 125 μg/mL
Extracto AH-H-ButOH
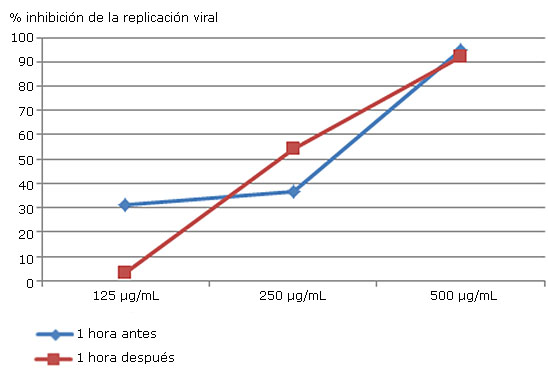
Fig. 2 Valores de inhibición de la replicación del virus DEN-2 obtenidos al añadir concentraciones crecientes de AH-H-ButOH 1 h antes y 1 h posinoculación.
El extracto AH-H-AcEtO (Fig. 3) mostró poco efecto inhibitorio alcanzando como valor máximo un 20 % de inhibición a la concentración de 250 μg/mL añadido 1 h después de la inoculación
Evaluación preliminar de la actividad antiviral de los extractos acuosos de A. havanensis ante VDEN-2 utilizando el ensayo de imunoperoxidasa
Los extractos de A. havanensis fueron también preliminarmente evaluados utilizando el ensayo de imunoperoxidasa en células Vero. La figura 4 muestra los resultados obtenidos al aplicar los extractos y controles del ensayo.
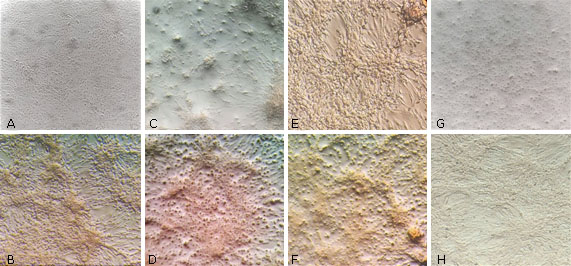
Fig 4 Microscopia de células Vero con los extractos añadidos en concentraciones subtóxicas (500 μg/mL): AH-T-EtOH (A: 1 h antes de inocular; B: 1 h después de inocular); AH-H-But OH (C: 1 h antes de inocular; D: 1 h después de inocular). Control células Vero sin extracto (Medio 199, E: 1 h antes de inocular; F: 1 h después de inocular). Control células Vero con IFN AR (G: 1 h antes de inocular; H: 1 h después de inocular). Las imágenes fueron visualizadas en un aumento de 40X.
El extracto AH-T-EtOH (500 μg/mL) adicionado 1 h antes limitó la expresión de la proteína E, indicada por la ausencia de inmunotinción en la monocapa celular. El extracto adicionado 1 h posinoculación, presentó un patrón diseminado en la monocapa y retracción celular (Fig. 4, A y B).
El compuesto AH-H-ButOH agregado 1 h antes de la inoculación produjo inmunofocos en la monocapa (Fig. 4, C), mientras que 1 h posinoculación la tinción fue diseminada (Fig. 4, D).
El extracto AH-H-AcEtO, presentó una escasa tinción sin diferencias evidentes en ambos tiempos de adición del extracto (datos no mostrados).
Como controles del ensayo, la expresión de la proteína E anti VDEN fue revelada en ausencia de extractos y con la adición del AcM-LAH (Fig. 4, E y F) presentando patrones de tincion similares. Mientras, la acción antiviral se manifestó utilizando el IFN AR en sustitución de los extractos (Fig. 4, G y H) sin apariencia general de inmunotinción.
Discusión
Existen una gran variedad de ensayos para determinar la actividad antiviral de numerosos compuestos, no obstante, en su mayoría son costosos, laboriosos o consumen un tiempo considerable.22 Evadiendo este problema, algunos investigadores utilizan ensayos inmunoenzimáticos por su especificidad, rapidez, facilidad de automatización y asequibilidad como el ELISA celular20 o in situ11,23 así como el ensayo de inmunoperoxidasa.21 Ambos se han utilizado entre otros fines, en determinar la expresión de proteínas virales.
La normalización de cualquier ensayo requiere valorar múltiples parámetros, para utilizarlos en condiciones óptimas. En el ELISAc, uno de ellos es el sustrato celular, este debe ser sensible a la replicación viral y capaz de evidenciar el efecto citopático. Igualmente, la utilización adecuada de compuestos fijadores y bloqueadores es indispensable para permitir la adhesión de un mayor número de células, una buena permeabilidad y la eliminación de reacciones inespecíficas.
Las líneas celulares C6/36-HT y Vero, han sido usadas por la alta susceptibilidad en la replicación del VDEN y la demostración de la proteína de envoltura (E) en la superficie celular de ambas, infectadas con dicho agente.5,20 La línea Vero resultó ser el mejor sustrato. Son células adherentes y para su desprendimiento requieren de un tratamiento enzimático. En cambio, las C6/36 HT son células semi-adherentes, capaces de desprenderse mecánicamente, por los continuos lavados que disminuyen el número de células por pozo.21,23)
Otro de los parámetros está relacionado con los compuestos fijadores para maximizar la permanencia de las células intactas y preservar la antigenicidad viral.24) La acetona, el etanol y el metanol, son conocidos por su capacidad de extraer lípidos de membrana y facilitar la exposición extracelular del antígeno.25 La mezcla de metanol-acetona proporcionó mejores resultados, comparado con los obtenidos por el glutaraldehído. Posiblemente, debido a que la extracción de los lípidos de membrana expone mejor el antígeno viral en las células y mejora también la penetración de los anticuerpos usados en el ensayo e incrementa su sensibilidad.26 El glutaraldehído, no ocasionó perdida de células en la monocapa, pero no generó una buena resolución entre células no infectadas e infectadas. Reportes previos plantean que puede ocasionar la perdida de antigenicidad en moléculas de la superficie celular.20
Otro aspecto importante son los compuestos bloqueadores que reducen las uniones inespecíficas en los ensayos inmunoenzimáticos y representan un compromiso entre la reducción del “ruido de fondo” y el mantenimiento de la especificidad. Las proteínas lácteas son las más comunes como, la ABS, la LD y el suero normal.11 Aquí, la LD al 1 % fue seleccionada por sus buenos resultados y disponibilidad.
Otro factor considerable, es la m.o.i, quien influye en el curso del ciclo de multiplicación del virus y por tanto en la expresión de las proteínas virales. Apoyados en estudios previos se utilizó una moi= 0,1 y un tiempo de incubación de 72-96 h para la expresión de la proteína.6 Estos parámetros resultaron óptimos en la normalización del ELISAc.
El ELISAc fue útil al evaluar de forma preliminar diferentes extractos de la planta A. havanensis con potencial antiviral. Coincidiendo estos resultados con reportes previos, que plantean que substancias compuestas con metabolitos como los flavonoides, entre otros,27 ejercen actividad antiviral en un número de virus que incluyen hepatitis B, herpes simple, citomegalovirus y el virus dengue.28
Barrio y otros reportaron la actividad antiviral de estos compuestos contra el VDEN 2 A15, obteniendo los mayores valores de inhibición de la replicación 1 h después de añadido el extracto y a la máxima concentración del mismo (500 μg/mL), detectado por la técnica de NRNP.16 En el presente estudio, de forma similar al de Barrio y otros, todos los extractos presentaron actividad inhibitoria sobre la multiplicación in vitro de DENV-2 A15. No obstante, el porcentaje de inhibición del AH-T-EtOH fue menor (20 %) y el mayor se logró con el AH-H-ButOH (90 %) en ambos tiempos de agregación. Este último inhibió un 30 % de la replicación viral a 125 μg /mL, lo que sugiere que pudiera actuar de la misma forma a concentraciones menores. Estas divergencias pueden estar dadas por los métodos de determinación de la inhibición de la replicación viral y el modelo celular utilizado.
La determinación de la inhibición de la replicación mediante la NRNP está basado en la capacidad del virus al producir placas líticas en la monocapa celular (5-7 días posinoculación) y destruirlas. En este caso, la infectividad es impedida por el efecto antiviral ejercido por el extracto. En este estudio, la inhibición de la replicación fue determinada por el ELISAc detectando la expresión de la proteína E viral con el uso del AcM específico. Este procedimiento implica la fijación de las células al soporte (placa) del ensayo en el tiempo prefijado (tiempo óptimo de expresión de E, 96 h posinoculación) semejándose a una foto en un estadio del ciclo replicativo viral.
La inhibición de la replicación viral por los compuestos (AH-T-EtOH < 50 %, 1 h posinoculación; AH-H-BuTOH 90 %, ambos tiempos de adición y AH-H-AcEtO 20 %, ambos tiempos de adición) sugiere que los viriones entran a la célula ocurriendo una escasa replicación viral. Esta disminuye posiblemente a causa de que los eventos que conducen al desnudamiento de la nucleocapsida y el escape del endosoma, pudieran estar bloqueados por la acción de algún componente de los extractos.
Se ha reportado que entre los metabolitos secundarios aislados de la especie A. havanensis se encuentran, el acetato de pucherril, flavonas, flavonoles, chalconas, glucósidos, sakuranetina, 7 metoxiaromadendrina, entre otros.27
Diversos reportes sugieren la actividad antiviral de los flavonoides por múltiples mecanismos involucrados en los efectos anti-DEN. Entre estos, se plantea que reduce la adsorción de la partícula viral, los pasos de fusión a la membrana celular, la cantidad de gotas de lípidos, la expresión de proteínas virales (NS1 y NS3) de NF-(B y de la proteína E.28
En esta investigación la evaluación antiviral fue posible también mediante el ensayo de inmunoperoxidasa. La tinción por inmunoperoxidasa, se utiliza para detectar la expresión de antígenos virales principalmente utilizando anticuerpos monoclonales y con diversos fines como, la localización precisa de sitios antigénicos en las diferentes proteínas del VDEN,21 la titulación del virus y principalmente, en el diagnóstico de casos fatales de esta infección.29 Recientemente, se ha reportado como un ensayo apropiado para el tamizaje de grandes cantidades de drogas antivirales.22
Los resultados de este procedimiento no correspondieron totalmente con los del ELISAc, aunque ambos ensayos están basados en el mismo principio. Ello se manifestó en la presencia de focos de inmunotinción cuando el extracto AH-H-ButOH fue agregado 1 h antes de la inoculación, quien en el ELSAc mostró un 90 % de inhibición de la replicación viral; y en el AH-T-EtOH 1 h posinoculación, que presentó una inmunotinción difusa.
El patrón de tinción en el ensayo de inmunoperoxidasa es generalmente considerado como representativo de la verdadera distribución del antígeno, siempre que los controles sean adecuados. No puede excluirse la presencia de artefactos de difusión y re-adsorción que se supone son aplicables a todas las técnicas citoquímicas basadas en la diaminobencidina (DAB), como, por ejemplo, la demostración de peroxidasas endógenas y exógenas entre otros. Estos artefactos son atribuidos a los productos oxidados en la reacción de la DAB que no precipitan eficientemente en el sitio de reacción.
Estudios recientes en la evaluación de antivirales por este procedimiento, plantea que la presencia de inmunofocos en las células infectadas es derivada de la progenie viral que infectan las células vecinas conduciendo a la formación de grupos de células teñidas o inmunofocos, mientras que en una tincion difusa o no específica todas las células son regular y ligeramente teñidas.22
La presencia de inmunofocos cuando el extracto AH-H-ButOH fue agregado 1h antes de la inoculación pudo ser debida al 10 % donde no hubo inhibición de la replicación viral. Sin descartar que la utilización del H2O2 al 0,001 % pudo ser insuficiente para realizar el bloqueo de las peroxidasas endógenas. Lo cual es también aplicable al patrón de tincion por el extracto AH-T-EtOH.
Estos resultados, no impiden sugerir la utilización de ambos ensayos inmunoenzimáticos en la evaluación de compuestos con potencialidad antiviral para el VDEN 2. Dichos métodos pueden ser usados también en el tamizaje de drogas antivirales para otras entidades, siempre que se disponga de anticuerpos policlonales o específicos a los mismos.
En el presente, se llevan a cabo nuevos ensayos con vistas a establecer las condiciones óptimas de su procedimiento.
















