Introducción
Pneumocystis jirovecii es un patógeno oportunista capaz de provocar neumonía intersticial en pacientes inmunocomprometidos, especialmente en los infectados por el virus de la inmunodeficiencia humana (VIH). Aun en la era de la terapia antirretroviral y quimioprofilaxis la infección por P. jirovecii (PcP) es una de las enfermedades con mayor impacto negativo a nivel mundial. Recientes estudios, en Europa y Estados Unidos de América, evidencian que la PcP se diagnostica como la enfermedad más común que define sida.1,2,3,4,5
El diagnóstico clínico de la PcP es un verdadero desafío debido a que no existen síntomas, signos, características radiológicas ni datos de gasometría específicos que la distingan de otras enfermedades. Por otra parte, el microorganismo que causa esta enfermedad no es cultivable, lo que limita extraordinariamente su identificación. Además, la muestra con mayor rentabilidad diagnóstica es el lavado broncoalveolar, procedimiento invasivo que no se utiliza como rutina en los centros hospitalarios de países en vías de desarrollo.6,7)
La técnica de referencia para el diagnóstico de la PcP es la visualización del microorganismo (quistes o formas tróficas) por métodos de microscopia óptica. Entre ellos se destacan los métodos tintoriales y el empleo de la inmunofluorescencia con anticuerpos específicos. La primera carece de sensibilidad diagnóstica y la segunda es costosa para instaurarlo como rutina en los servicios de atención a los pacientes con sospecha de la infección.8,9) Recientemente, con el advenimiento de los métodos moleculares, la detección de P. jirovecii se hace más rápida y con excelente sensibilidad y especificidad. Sin embargo, estás técnicas resultan costosas, no están al alcance de muchos laboratorios a nivel mundial y no logran discriminar entre el estado de colonización y el de infección.10,11
Ante estas limitaciones para el diagnóstico de la PcP, las pruebas serológicas ganan un espacio considerable. Estudios previos, constatan que los valores de 1,3 beta D glucano (elemento estructural en la pared quística de los hongos), S adenosil metionina (SAM, enzima encargada de procesos de metilación), antígeno Krebs von den Lungen-6 (KL-6, glicoproteína presente en los neumocitos alveolares tipo II) y la lactato deshidrogenasa (LDH) se encuentran elevados en los casos con infección por P. jirovecii. Sin embargo, ninguna de las pruebas serológicas nombradas se utiliza como único método para el diagnóstico de la PcP, pues no son específicas para tal fin.8,12,13
La lactato deshidrogenasa (LDH) es una molécula huésped que se expresa en los tejidos humanos, se libera principalmente en el espacio broncoalveolar por el daño que ocurre en la membrana citoplasmática. Esta enzima constituye un biomarcador inespecífico de inflamación y lesión alveolar como resultado de infecciones o enfermedades pulmonares y de otras infecciones extrapulmonares.13)
Fujii y colaboradores en Japón reportaron cifras de LDH aumentadas en 32 de 34 episodios de PcP.14) De la misma manera, Tasaka y colaboradores mediante un estudio de casos y controles evaluaron los valores de la LDH en 279 pacientes (16 de ellos con infección VIH). Esos autores calcularon la sensibilidad y especificidad de la prueba, al emplear cifras superiores a 268 U/l, de 86 % y 45,3 %, respectivamente.15)
En Cuba los estudios sobre la PcP son limitados y han sido encaminados, fundamentalmente, a la caracterización molecular del patógeno.16,17,18,19) Por esa razón, la búsqueda de nuevas alternativas diagnósticas sencillas, menos costosas y basadas en muestras fáciles de obtener sería una alternativa importante del empleo de la LDH como prueba diagnóstica de la PcP en los pacientes con sida.
El objetivo de la presente investigación es demostrar la utilidad de la prueba de la LDH como diagnóstico de la PcP en fallecidos cubanos por sida.
Métodos
Se realizó un estudio de casos y controles (proporción de casos y controles (25:30), de 1:1,2 emparejados por sexo, edad, color de la piel y año del deceso) en fallecidos cubanos por sida con PcP atendidos en el Instituto de Medicina Tropical "Pedro Kourí" y donde se realizó la autopsia, durante el período comprendido entre enero de 1996 hasta diciembre de 2016.
El universo de estudio para los casos incluyó pacientes cubanos fallecidos por sida con diagnóstico anatomopatológico de causa directa de muerte de sida con P. jirovecii en el periodo analizado. Resultaron de la investigación 80 casos. El diagnóstico de la PcP se realizó en cortes histológicos de un fragmento de pulmón previamente fijado en formol y embebido en parafina. El diagnóstico histopatológico (PcP) se realizó por microscopía óptica con la coloración de hematoxilina y eosina (HE) y plata metenamina de Grocott (GMS). Se utilizó como criterio diagnóstico, la visualización microscópica de cualquier estadio de vida del patógeno en la muestra analizada.
Criterios de inclusión:
‒ Fallecido mayores de 18 años, con diagnóstico histopatológico de PcP.
‒ Prueba de la LDH realizada con al menos 5 días antes del fallecimiento.
Criterios de exclusión:
Presencia de hepatopatías crónicas o agudas, infección por virus hepatotrópicos o citólisis hepática.
Finalmente, se seleccionaron 25 casos que cumplían con estos criterios.
Controles. Fallecidos por sida sin PcP en el periodo comprendido de la investigación. Se tomó un control por cada caso analizado. Se conformaron tres grupos, ellos incluyeron: fallecidos por neumonía bacteriana (grupo I, 14 casos), linfoma (grupo II, 12 casos) y tuberculosis (grupo III, 4 casos).
Criterio de inclusión de los controles:
Fallecidos durante el periodo de estudio mayores de 18 años, sin el diagnóstico de PcP comprobado histológicamente.
Prueba de la LDH realizada con al menos cinco días antes del fallecimiento.
Diagnóstico por microbiología y hallazgos anatomopatológicos de cada uno de los individuos que pertenecen a los grupos analizados según corresponda (I,II,III).
Criterio de exclusión de los controles:
Métodos estadísticos
La fuente de los datos y los valores de la prueba de LDH se recolectaron de las historias clínicas (HC) de cada fallecido. El rango de valores se describe y se adjunta en el mismo resultado extraído de la HC. Se considera como valores de referencia para hombres (135-225 U/l) y para mujeres (135-214 U/l), con valores de consenso hasta 250 U/I. Para la construcción de la curva ROC, se tomaron cinco rangos de corte (250-<350, 350-<550, 550-<800, 800-1 000, >1 000 U/l), con lo cual se seleccionó la mejor razón de sensibilidad/especificidad.20 Todas las pruebas de la LDH se realizaron con el sistema automatizado Analizador químico marca Hitachi 912, Roche, Japón con sus correspondientes reactivos suministrado por la propia firma. Se calculó la sensibilidad (S), especificidad (E), valores predictivo positivo (VPP) y negativo (VPN), la razón de verosimilitud positiva (LRN+) y negativa (LNR-) y el índice de Youden (IJ).21)
Se determinó la razón de oportunidad (OR, Odds Ratio) entre los grupos de casos y controles, teniendo en cuenta el rango de corte óptimo de la técnica. La prueba estadística U de Mann-Whitney se utilizó para determinar las diferencias entre la distribución de los niveles de LDH de los diferentes grupos analizados (casos y controles). Para identificar las diferencias entre los grupos: casos, neumonía bacteriana (grupo I), linfoma (grupo II) y tuberculosis (grupo III) se utilizó la prueba de Kruskal-Wallis.
Se calculó la sensibilidad (porcentaje de pacientes con PcP correctamente identificados por la prueba de la LDH), especificidad (porcentaje de pacientes sin PcP correctamente identificado por la prueba LDH), valores predictivos positivos (VPP) (porcentaje de pacientes con PcP con una prueba de LDH positiva), valores predictivos negativos (VPN) (porcentaje de pacientes sin PcP con una prueba de LDH negativa) y las razones de verosimilitud positivo / negativo (LRP / LRN) (la proporción de las probabilidades de que la prueba sea positivo / negativo en casos con PcP frente a aquellos sin PcP). Con los valores de sensibilidad y especificidad de la prueba de LDH se construyó la curva Característica Operativa del Receptor (ROC, Reciever Operating Characteristic).
Se utilizaron tablas de contingencia para calcular la fuerza de asociación existente (OR) entre los valores de la prueba de LDH para ambos grupos (casos y controles), se considera p≤ 0,05 estadísticamente significativa para todos los análisis con un intervalo de confianza de 95 %. Los datos se agruparon, organizaron y procesaron en el paquete para el análisis estadístico SPSS Versión 21 (Chicago, EE UU).
Aspectos éticos
Toda la información se conservó bajo los principios de máxima confiabilidad y en ningún caso se reflejó la identidad de las personas. El uso de la misma ha sido únicamente con fines científicos. Los procedimientos se realizaron según lo aprobado por los comités internacionales para ensayos en humanos (Declaraciones de Helsinki, Asamblea Médica Mundial, 2000), de ética de manejo del paciente y de acuerdo con las regulaciones establecidas en Cuba.
Resultados
Al aplicar la prueba U de Mann-Whitney para los valores de la prueba de LDH entre los grupos de casos y controles analizados se obtuvo diferencias altamente significativas (p= 0,003).
El análisis entre los cuatro grupos del estudio (PcP, tuberculosis, linfoma y neumonía bacteriana) resultaron con diferencias significativas (p= 0,028) del grupo de linfoma con el resto.
En la tabla 1 se muestra la distribución de los casos y los controles de la serie analizada según los valores de la enzima LDH extraídos de cada una de las HC.
Los valores de sensibilidad y especificidad constata las diferencias para cada uno de los cinco rango seleccionados (250-<350, 350-<550, 550-<800, 800-1 000, >1 000 U/l). Se destaca como valor óptimo el correspondiente al rango de 550-<800, con sensibilidad de 80 % y especificidad de 63 %. Es válido destacar que existe un caso de PcP con valores normales de LDH. De la misma manera, en el grupo control se constatan tres controles con valores elevados de la enzima (Tabla 1).
Tabla 1 Sensibilidad y especificidad de los valores de la prueba de la enzima lactato deshidrogenasa en los casos y controles analizados
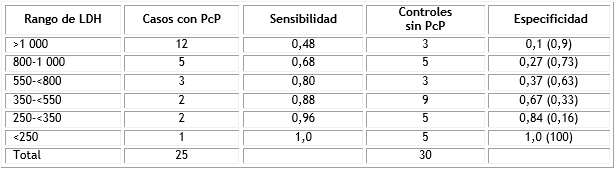
LDH: lactato deshidrogenasa; PcP: neumonía por Pneumocystis jirovecii.
En la tabla 2 se describe los parámetros estadísticos de la prueba utilizada según los rangos analizados en el estudio.
Tabla 2 Parámetros estadísticos y sus intervalos de confianza según rango de LDH analizado
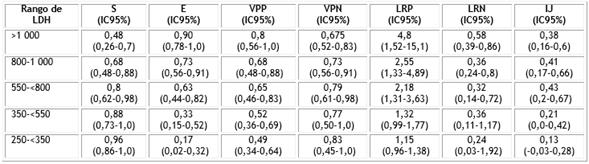
S: sensibilidad; E: especificidad; VPP: valor predictivo positivo; VPN: valor predictivo negativo; LRP: razón de verosimilitud positiva; LRN: razón de verosimilitud negativa; IJ: índice de Youden.
En la figura se observa la curva ROC obtenida con los valores de sensibilidad y especificidad de cada uno de los puntos de rango seleccionados para los casos y controles analizados. El área ROC es de 0,76, con un error estándar de 0,066 (0,63-0,89).
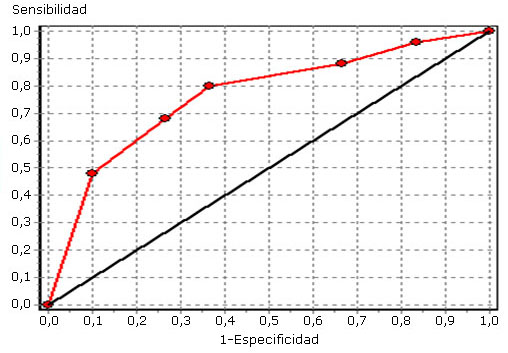
Fig Curva ROC de los casos y controles según valor de la prueba de la enzima lactato deshidrogenasa.
Para el valor de rango óptimo seleccionado (550-<800 U/l), la razón de disparidad (datos no mostrados) calculada fue de OR= 6,91 (2,07-22,89) con un valor de p de 0,0031. Se resalta que los pacientes por PcP (casos) tienen casi 7 veces más probabilidades de contar con un valor de rango óptimo de LDH que los pacientes con tuberculosis, linfoma, neumonía bacteriana (controles) con diferencias altamente significativas.
El IJ en el presente trabajo es aceptable, pues su valor es intermedio (0,43).
Discusión
La enzima LDH es una proteína en el hospedero humano que posee diversas isoformas.22) Más que asociarse con procesos infecciosos, se relaciona con alteraciones tisulares de inflamación y daño. Varios estudios demuestran la utilidad de detectar los niveles séricos de la molécula en el diagnóstico de diversas infecciones. Trabajos previos, ejemplifican que altos valores de la LDH se relacionan positivamente con la PcP.8,13,20,22,23) No obstante, no es diagnóstico patognomónico de la misma. Cifras elevadas de LDH se asocian con infección por toxoplasma, histoplasma, tuberculosis pulmonar, enfermedad de Castleman y neumonía de etiología bacteriana.23,24,25 Además, la actividad elevada de la enzima se observa en pacientes con anemia megaloblástica y carcinoma diseminado. Aumento moderado de la misma se constata en trastornos musculares, síndrome nefrótico y cirrosis. En casos de infarto del miocardio o pulmonar, leucemia, anemia hemolítica y hepatitis no vírica, la actividad de la LDH solo está ligeramente elevada.20,22,23) Por esas razones los controles para la presente investigación son fallecidos por sida diagnosticados con algunas de dichas enfermedades.
En el actual estudio existieron diferencias estadísticamente significativas al comparar cada uno de los grupos según el diseño utilizado (casos de PcP y controles [fallecidos por tuberculosis, linfoma, neumonía bacteriana]). Este resultado se traduce en que ambos grupos son claramente distintos y que los valores de la prueba de LDH pueden discriminar a los casos de PcP del resto de los individuos incluidos en el grupo control.
Por otra parte, cuando se fragmenta el grupo control, se precisa que existen diferencias significativas entre los tres grupos analizados y el de los fallecidos con linfoma. No obstante, estos datos deben interpretarse con cautela, pues los grupos poseen pocos individuos fallecidos (pequeño tamaño muestral) y puede alterar los resultados. Los mismos pudieran ser de utilidad para los individuos con linfomas en los que sospeche previamente una PcP.
Es válido destacar que un individuo con diagnóstico de PcP poseía valores normales para la prueba de la LDH, de la misma manera tres fallecidos controles (10 %) tenían títulos de más de 1 000 U/I. Estos datos demuestran que deben tomarse con precaución los resultados de dicha prueba. Recientemente, un estudio desarrollado en China evaluó 13 investigaciones con 825 pacientes casos, de ellos 650 con sida y 1 341 controles (888 con sida). Los autores del estudio demostraron que para los casos sida la prueba tiene buena sensibilidad (80-100 %), sin embargo, la especificidad varía enormemente desde 6-85 % con valores de la LDH de 200-598 U/I.23 Los resultados del presente estudio coinciden con el meta análisis mencionado (sensibilidad 80 % y 63 % de especificidad) para un rango de corte de 550-<800 U/I.
En 1947, Yerushalmy introduce los términos de sensibilidad y especificidad como indicadores estadísticos que evalúan el grado de eficacia inherente a una prueba diagnóstica.21) La sensibilidad y la especificidad son las medidas tradicionales y básicas del valor diagnóstico de una prueba. Miden la discriminación diagnóstica de un examen en relación con un criterio de referencia, que se considera la verdad. Estos indicadores en principio permiten comparar directamente la eficacia de una prueba con el de otras y esperar resultados similares cuando son aplicadas en diferentes países, regiones o ámbitos.13,20,23) En la actual investigación se compara la prueba de la LDH con la técnica de tinción de Grocott (método de referencia).
En el presente estudio a medida que aumenta el rango de corte de la LDH se evidencia el aumento de la especificidad y la disminución de la sensibilidad. Esto indica la capacidad que tiene la prueba de identificar como sanos (no enfermos) a los que efectivamente lo son en detrimento de detectar a un sujeto enfermo. En este caso se pierden un buen número de enfermos que no son detectados y la prueba carece de sentido para su uso como cribado o tamizaje.
Ante estas situaciones complejas se requiere de un rango de corte óptimo que permite al mismo tiempo detectar a los enfermos y descartar la enfermedad en los sujetos sanos. De la misma manera, se llega a los valores predictivos positivos y negativos, así como a la razón de verosimilitud positiva y negativa. Esteves y colaboradores en un excelente artículo de revisión que involucra 100 individuos VIH y 50 donadores sanos demuestran que la sensibilidad de la prueba de la LDH fue 91,3 %, especificidad 35,5 %, VPP 75,9 %, VPN 64,7 %, LRP 14,15 y LRN 0,245.20) Valores ligeramente menores con respecto al actual estudio. Algunas causas como la prevalencia de la enfermedad, la técnica para el diagnóstico de la PcP y el tamaño muestral pueden ser la razón de esta disparidad.
Una medida conjunta de eficiencia de un medio diagnóstico fue propuesta por Youden en 1950. Refleja la diferencia entre la tasa de verdaderos positivos y la de falsos positivos. Una buena prueba debe tener alta esta diferencia. Teóricamente es igual a 1 solo cuando la prueba diagnóstica es perfecta, o sea, cuando S + E= 2, de modo que puede decirse que cuanto más cercano es a 1, mejor es la prueba diagnóstica.21
El IJ tiene la ventaja de no estar afectado por la selección de la prevalencia y es preferido por la combinación de los sencillos valores de la sensibilidad y la especificidad.21) Sin embargo, tiene la desventaja de que, al resultar de la combinación de los valores de S y E, se pierde la idea de si la prueba diagnóstica es buena en sensibilidad o especificidad. En el presente estudio el IJ fue de 0,43, lo que corresponde a un valor de aceptable, pues es intermedio entre 0 y la unidad.
Al construir la curva ROC para los puntos analizados el área debajo de la misma es 0,73 para el rango (550-<800 U/l), valor que se considera bueno si se conoce que mientras más próximo se encuentre a 1 más logra discriminar la prueba entre sanos y enfermos.
El presente estudio presenta algunas limitaciones, dentro de ellas podemos destacar: la imposibilidad de buscar más controles fallecidos de manera general. Se describe en la literatura que la potencia de un estudio de casos y controles se incrementa cuando la relación de controles:casos es aproximadamente (3:1). De la misma manera, los pocos casos de tuberculosis que existen en el periodo dificulta el análisis (Cuba posee una tasa baja de la enfermedad 7,2 x 100 mil habitantes). No obstante, se estudió la totalidad de casos que fallecieron en ese espacio de tiempo a los cuales se le realizó las necropsias en el IPK. Por otra parte, no se conoce el estado de colonización por Pneumocystis jirovecii en los controles, lo cual pudiera alterar los resultados. Sin embargo, los casos fueron correctamente identificados por métodos histológicos, lo cual es una fortaleza indudable del estudio. Por otra parte, es el resultado de 21 años de necropsias realizadas en el centro de referencia nacional para el estudio de VIH/sida en Cuba. Es válido destacar que la prueba debería tratar de demostrar su utilidad en los pacientes vivos con la necesidad de brindar un diagnóstico positivo e instaurar tratamiento oportuno. Finalmente, la prueba de LDH es simple, costo/efectiva y se utiliza de rutina en los servicios médicos.
El desarrollo tecnológico de los últimos decenios ha permitido incorporar a la práctica clínica novedosos y sofisticados medios diagnósticos que, sin duda, constituyen adelantos en el perfeccionamiento del trabajo médico. La necesidad de herramientas cuantitativas que contribuyan a dirigir con racionalidad las indicaciones médicas es indispensable. Se trata, en particular, de obtener índices o medidas de eficacia de cada medio diagnóstico que se empleen de pauta orientadora para su selección en el momento necesario.
En resumen, el presente estudio logra identificar un rango de corte para la prueba y diferenciar la PcP de otras infecciones, lo cual resultaría en un método útil para la formulación de un diagnóstico de certeza. Todo ello permite identificar la prueba de la LDH como una valiosa herramienta adicional/complementaria en el diagnóstico de la PcP.














