Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Hematología, Inmunología y Hemoterapia
versión impresa ISSN 0864-0289
Rev Cubana Hematol Inmunol Hemoter vol.29 no.4 Ciudad de la Habana oct.-dic. 2013
ARTÍCULO ORIGINAL
Evaluación del tratamiento de inducción y consolidación clásico en la leucemia aguda no linfoblástica de Novo
Evaluation of induction and consolidation classic treatment in de Novo acute non-lymphoblastic leukemia
Dra. Yusselys Cabrera-Payne, Dr. Aramis Núñez-Quintana, Prof. José Carnot-Uria, Dr. Jorge Muñío-Perurena, Dr. Calixto Hernández-Cruz, Dra. Yusaima Rodríguez-Fraga
Hospital Clinicoquirúrgico «Hermanos Ameijeiras». La Habana, Cuba.
RESUMEN
Introducción: la validación de las alteraciones citogenéticas y moleculares presentes al diagnóstico constituyen los factores pronósticos más importantes de la leucemia aguda no linfoblástica y ha permitido establecer el riesgo individual, estratificar a los pacientes e individualizar su tratamiento.
Objetivo: describir el comportamiento clínico y la evolución de pacientes con leucemia aguda no linfoblástica, no promielocítica, de novo, que recibieron tratamiento de inducción y consolidación clásico en el servicio de Hematología del Hospital Clínico Quirúrgico «Hermanos Ameijeiras».
Método: se realizó un estudio descriptivo, longitudinal y prospectivo que incluyó 23 pacientes ingresados entre mayo de 2008 y enero de 2011. Se estratificaron los pacientes en grupos de riesgo favorable, intermedio y desfavorable, teniendo en cuenta factores pronóstico clínicos, biológicos, citogenéticos y moleculares.
Resultados: el 60,9 % presentó recuento de leucocitos menor de 25 x 109/L; el 47,8 % tuvo la variante mielomonocítica, el 21,7 % presentó cariotipo normal y el 10 % la translocación (8;21). Las mutaciones del gen FLT3 y el gen NPM1 estuvieron presentes en 2 y 4 pacientes respectivamente. Con el tratamiento de inducción, el 84,2 % alcanzó la remisión completa, predominaron los pacientes en el grupo de riesgo favorable sin diferencias significativas. En el grupo de riesgo molecular favorable el número de remisiones completas fue significativamente mayor (85,7 %) (p = 0.05). El grupo de pacientes de riesgo favorable que se mantuvo en remisión completa con el tratamiento de consolidación representó el 54,5 %, aunque no resultó significativo.
Conclusiones: la sobrevida libre de enfermedad fue mayor mientras que la sobrevida global se comportó igual a lo reportado en la literatura internacional, ambas fueron mayores en el grupo de riesgo favorable aunque no de forma significativa, siendo esto un logro importante del Sistema Cubano de Salud.
Palabras clave: leucemia aguda no linfoblástica, estratificación de riesgo, sobrevida libre de enfermedad y sobrevida global.
ABSTRACT
Introduction: validation of cytogenetic and molecular abnormalities present at diagnosis is the most important prognostic factors of acute non-lymphoblastic leukemia. This has allowed us to establish the individual risk, stratify the patients and individualize their treatment.
Objective: to describe the clinical behavior and outcome of patients with acute de novo non-lymphoblastic non-promyelocytic leukemia, receiving induction and classic consolidation therapy at the Department of Hematology of the Clinical Surgical Hospital «Hermanos Ameijeiras».
Methods: a descriptive, prospective longitudinal study was carried out with 23 patients admitted between May 2008 and January 2011. Patients were stratified into: favorable, intermediate, poor risk groups, according to biological, molecular and cytogenetics clinical prognostic factors.
Results: 60.9 % of patients had leukocyte counts less than 25 x 109/L, 47.8 % had myelomonocytic variant, 21.7 % had normal karyotype and 10% had translocation (8; 21). Mutations of the genes FLT3 and NPM1 were present in 2 and 3 patients respectively. 84 % of patients undergoing induction therapy achieved complete remission, predominantly the ones in the favorable risk group with no significant differences. In the favorable molecular risk group, the number of complete remissions was significantly higher (85.7 %) (p=0.05). The group of favorable risk patients remaining in complete remission with the consolidation treatment had 54.5 %, although it was not significant.
Conclusions: the disease free survival was greater whereas overall survival rate was similar to the data reported in the international literature. Both were higher within the favorable risk group but without no significant difference, what is considered an important achievement of Cuban Healthcare System.
Keywords: acute non-lymphoblastic leucemia, risk stratification, disease-free survival, overall survival.
INTRODUCCION
En los últimos años han ocurrido importantes avances en el conocimiento de las alteraciones citogenéticas y moleculares relacionada con la patogenia de la leucemia aguda no linfoblástica (LANL), siendo esta una enfermedad heterogénea, compleja y con múltiples vías de activación. 1 La validación de las alteraciones citogenéticas y moleculares presentes al diagnóstico constituyen los factores pronósticos más importantes, lo que permite establecer el riesgo individual, estratificar a los pacientes en tres grandes grupos (favorable, intermedio y desfavorable), influir en la decisión terapéutica y predecir la respuesta al tratamiento 2,3 La dificultad de usar la citogenética radica en que la mayoría de los pacientes están incluidos en el riesgo intermedio (hasta el 40 - 50 % tienen un cariotipo normal), lo que resulta en un grupo muy heterogéneo. La inclusión de nuevos marcadores moleculares define nuevas entidades biológicas, tanto de buen pronóstico, como son la presencia de mutaciones en genes como NPM1 (Nucleophosmine gene) o CEBPA (CCAT/enhancer binding protein family), como del mal pronóstico: mutación o sobreexpresión de genes FLT3-ITD (The FMS-like tyrosinekinase type 3 gene).4
El régimen de inducción a la remisión más comunmente usado es el esquema «3 + 7» que combina la citarabina a 100 mg/m2 por día en infusión continua durante 7 días, con la daunorubicina a 60 mg/m2/ día por tres días en bolo o infusión corta. 5, 6 Existe un grupo de pacientes en los que persiste la leucemia y que requiere un segundo ciclo de terapia de inducción, con mitoxantrone y dosis intermedias o altas de citarabina (HAM). 7
La terapia post remisión es un componente esencial en el tratamiento de la LANL, donde existen tres opciones que incluyen quimioterapia de consolidación, trasplante autólogo o alogénico de células progenitoras hematopoyéticas (TCHP), con el objetivo de prolongar la sobrevida libre de enfermedad y curación.8
En nuestro país, y en particular el servicio de hematología del Hospital Clínico Quirúrgico «Hermanos Ameijeiras» recibe un grupo grande de pacientes con LANL de novo desde hace más de 25 años, y desde entonces dispone de recursos y de una unidad de tratamiento intensivo en la que se aplican regímenes de quimioterapia de inducción y post remisión, que por su extraordinaria complejidad y costo constituyen un verdadero reto para cualquier sistema de salud. Los resultados de tratamiento de la LANL en el centro no se corresponde con lo reportado por la literatura actual; los porcentajes de remisión completa, sobrevida libre de enfermedad y sobrevida global son inferiores a los obtenidos por otros grupos de estudios internacionales.
Considerando que en los últimos años las posibilidades del uso de la citogenética y la biología molecular son mayores, nos propusimos realizar un trabajo para describir el comportamiento clínico en pacientes con LANL no promielocítica de novo, que reciben tratamiento de inducción y consolidación clásico y evaluar la respuesta en términos de logro de la remisión completa, sobrevida libre de enfermedad y sobrevida global en dependencia del grupo de riesgo.
MÉTODOS
Se realizó un estudio descriptivo, longitudinal y prospectivo del comportamiento clínico y la evolución de los pacientes con LANL de novo, que recibieron tratamiento de inducción y consolidación clásico en el periodo entre mayo de 2008 a enero de 2011 en el servicio de Hematología del Hospital Clínico Quirúrgico «Hermanos Ameijeiras».
La muestra estuvo conformada por 23 pacientes que cumplieron los criterios de inclusión y exclusión, con el previo consentimiento informado de cada paciente para iniciar el tratamiento y participar en la investigación. Los pacientes recibieron como tratamiento de inducción el esquema «3+7»: citosina arabinósido (ARA-C): 100 mg/m2/d en infusión continua en los días 1 al 7; y rubidomicina: 60 mg/m2/d por vía endovenosa (EV) en los días 1 al 3. Aquellos que no obtuvieron la remisión completa recibieron un segundo esquema de inducción HAM: ARA-C: 3 g/m2, EV en 3 horas, cada 12 horas, días 1, 3 ,5; y mitoxantrone: 10 mg / m2, EV, días 2 y 4. Aquellos pacientes que lograron remisión completa recibieron como esquema de consolidación altas dosis de ARA-C: 3 g/ m2 EV durante 3 horas/ cada 12 horas los días 1, 3 y 5. Cada 28 días y hasta 3 ciclos.
Se analizaron las variables edad, sexo, color de la piel, hallazgos clínicos iniciales, conteo inicial de leucocitos, morfología, estudio citogenético y molecular. Se evaluó la remisión clínica y hematológica después de concluido el tratamiento de inducción y después de cada ciclo de consolidación. Para la estratificación de los pacientes en grupos de riesgo favorable, intermedio y desfavorable se tomaron en cuenta los factores pronósticos clínicos, bioquímicos, morfológicos, citogenéticos y moleculares. En los pacientes a los que se les realizó el estudio citogenético y molecular el riesgo se determinó por estos parámetros, mientras que en aquellos en que no se pudieron realizar estos estudios solo se tuvieron en cuenta las variables clínicas, bioquímicas y morfológicas. Además, se determinó la mortalidad durante la terapia de inducción y consolidación, así como sus causas, y se analizó la sobrevida libre de enfermedad y la sobrevida global de acuerdo con los grupos de riesgo.
Para las variables cuantitativas se calcularon las medias y desviaciones estándar; y para las variables cualitativas, los números absolutos y los porcentajes. Se aplicó la prueba de Chi Cuadrado para comparar porcentajes entre las variables cualitativas, y la prueba de comparación de medias en muestras independientes con varianzas desconocidas (estadígrafo t-Student) para las variables cuantitativas. Para calcular las variables: sobrevida libre de enfermedad y sobrevida global se utilizó el método de Kaplan Meier.
En todas las pruebas de hipótesis realizadas se usó la Prueba de Fisher con un nivel de significación á = 0.05, y el procesamiento estadístico se realizó mediante el programa SPSS versión 13.0.
RESULTADOS
Se estudiaron 23 pacientes cuyas características demográficas y de la enfermedad al inicio se muestran en la tabla 1. El 60,9 % (n = 23) fue del sexo masculino e igual porcentaje presentaban la piel blanca. El promedio de edad fue de 36,30 años (21 - 54) y 19 pacientes (82,6 %) fueron menores de 45 años.
Entre los hallazgos clínicos iniciales encontrados está la presencia de adenopatías en 13 pacientes (56,5 %), palidez cutáneo mucosa en el 47,8 %, mientras que la fiebre, el síndrome purpúrico-hemorrágico y la hepatomegalia se presentaron en igual número de pacientes (43,5 %). El compromiso extramedular estuvo presente en 6 pacientes (26,1 %), de los cuales 5 (83,3 %) presentaron sarcoma granulocítico (2 en órbita, 1 en cuero cabelludo, 1 intracraneal y 1 en canal medular) y 1 paciente (16,7 %) tuvo infiltración meníngea.
Respecto al conteo de leucocitos al inicio de la enfermedad, presentaron hiperleucocitosis 2 pacientes (8,7 %) y 14 (60,9 %) tuvieron un conteo de leucocitos menor de 25 x 109/L. De acuerdo con la clasificación morfológica según los criterios del grupo Franco Americano Británico (FAB), presentaron la variedad M4 (mielomonocítica) 11 pacientes (47,8 %); 5 (21,7 %) M1 (mieloides sin maduración); 4 (17,5 %) M2 (mieloides con maduración); 2 (8,7 %) M5 (monocítica); y 1 paciente (4,3 %) M7 (megacarioblástica).
Se realizó el estudio citogenético a 14 pacientes (60,9 %), de ellos 5 (21,8 %) tuvieron la citogenética normal y en 9 (39,1 %) fue no útil.
Se realizó el estudio molecular a 11 pacientes (48 %), de ellos, la translocación (8;21) fue positiva en 1 paciente (10 %), la inversión del cromosoma 16 y la translocación (4;11) no se detectaron. El estudio de las mutaciones de los genes FLT3 y NPM1 mostró la presencia del FLT3 en dos pacientes; en uno asociado a la mutación NPM1 y en otro, en ausencia de esta última (9,1 % respectivamente), la mutación NPM1 se presentó de forma aislada en 3 pacientes (27,3 %); en 6 (54,5 %) no se encontró ninguna de las dos mutaciones.
De los 23 pacientes que recibieron el tratamiento de inducción no fueron evaluables 4; 2 fallecieron por sepsis durante el primer ciclo de inducción y 2 abandonaron el tratamiento. Completaron el tratamiento de inducción 19 pacientes; de ellos, 16 (84,2 %) lograron la remisión completa (RC) y 3 (15,8 %) se consideraron refractarios. Catorce pacientes (73,7 %) necesitaron un segundo ciclo de inducción para lograr la remisión completa.
En cuanto a la respuesta al tratamiento de inducción según el grupo de riesgo de los 19 pacientes, el porcentaje de RC del grupo de riesgo favorable (n=8) fue mayor que en el grupo desfavorable (n=7) sin diferencias significativas (p = 0.25), mientras que la respuesta al tratamiento de inducción, teniendo en cuenta el riesgo molecular, el porcentaje de RC del grupo de riesgo favorable (85,7 %) fue significativamente mayor (p = 0.05) (tabla 2).
De los 16 pacientes que lograron la remisión completa, 3 fueron no evaluables: uno por abandono del tratamiento y dos por recaída antes de iniciar la consolidación. Los 13 pacientes restantes realizaron el primer ciclo de consolidación. De ellos, dos recayeron (15,4 %); y 11 mantuvieron la remisión completa (84,6 %). Los 11 pacientes realizaron el segundo ciclo de consolidación. De ellos, dos fallecieron durante el tratamiento por sepsis, uno recayó postratamiento y ocho (72,7 %) continuaron en RC. Estos últimos realizaron el tercer ciclo de consolidación, de los cuales 5 (62,5 %) terminaron en RC, dos fallecieron por sepsis y uno recayó.
La respuesta al tratamiento de consolidación en términos de mantenimiento de la RC según el grupo de riesgo, fue mayor en el grupo de riesgo favorable que en el desfavorable (54,5 % vs 45,5 %), sin significación estadística (p = 0.26) (tabla 2). Los 5 pacientes con riesgo molecular favorable se mantuvieron en RC.
De los 23 pacientes incluidos en el estudio, 14 fallecieron (60,9 %); 11 por sepsis (78,6 %), dos por hemorragia (14,3 %) y uno por progresión de la enfermedad (7,1 %). La mortalidad relacionada con el tratamiento de inducción fue del 8,7 % y la relacionada con el tratamiento de consolidación fue del 30,8 %.
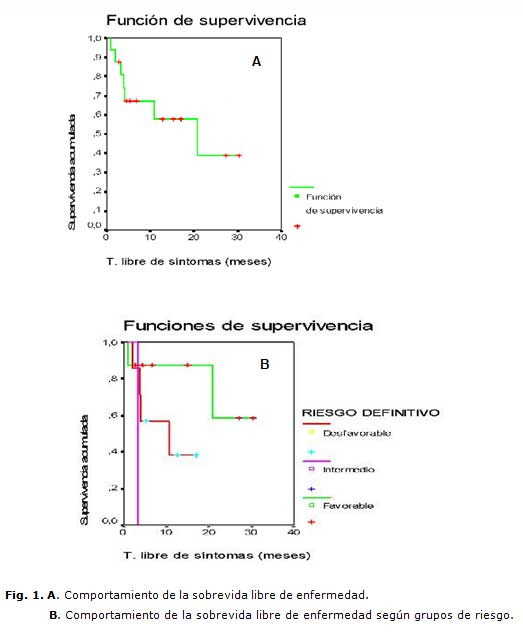
La sobrevida libre de enfermedad (SLE) de los pacientes que lograron remisión completa fue del 56,3 % con una media de 17,62 meses (11,02 - 24,22), intervalo de confianza (IC) del 95 %, y según los grupos de riesgo, el promedio de SLE fue del 75 % en el grupo de riesgo favorable con una media de supervivencia de 23,9 meses (16,41 - 31,33). En el grupo de riesgo intermedio la media de supervivencia fue de 3,27 meses; en el grupo de riesgo desfavorable la media de supervivencia fue de 9,93 meses (5,21-14,64), con un promedio del 42,9 %, (p = 0.076). (Figura 1)
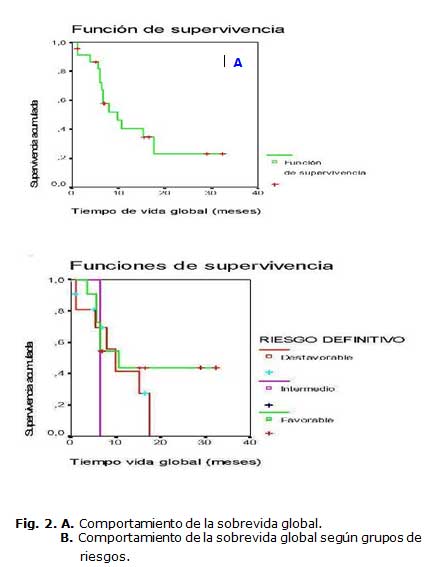
Respecto al comportamiento de la sobrevida global (SG) de los 23 pacientes estudiados, el tiempo medio de supervivencia fue de 14,07 meses (8,77-19,37) IC 95 %, con un promedio de sobrevida de 39,1 %, mientras que la SG según los grupos de riesgo: la media de supervivencia del grupo de riesgo favorable fue de 17,92 meses (10,11-25,73), con un promedio del 45,5 %; en el grupo de riesgo intermedio la media de sobrevida fue de 6,47 meses; en el grupo de riesgo desfavorable la media de sobrevida fue de 10,27 meses (5,89 - 14,65) con un promedio del 36,4 %, (p = 0.52). (Figura 2)
DISCUSIÓN
Como se describe en la literatura consultada, la LANL es más frecuente en el sexo masculino con una relación 5:3 9,10. En nuestra serie se encuentra un predominio en el sexo masculino con una relación 1,6:1.
La mayoría de los estudios reportan una mayor incidencia de LANL en pacientes de piel blanca 11, lo que coincide con los resultados de nuestro estudio donde el 60,9 % de los enfermos tenía ese color de piel.
La edad media de presentación de la LANL está en torno a los 65 - 68 años 12, 13. El promedio de edad de nuestros pacientes fue de 36,30 años (21 - 54) menor que en la mayoría de los estudios, lo que está en relación con la inclusión en este trabajo solo de pacientes menores de 60 años, por ser este grupo de individuos habitualmente elegibles para quimioterapia intensiva y remitidos a nuestro centro.
Los signos y síntomas clínicos presentes al diagnóstico son inespecíficos y muy variados; en general directamente relacionados con la infiltración leucémica de la médula ósea y la citopenia secundaria, que incluye palidez cutáneo mucosa, fiebre relacionada con infección o sin relación con esta, y sangramiento cutáneo mucoso, así como aquellos relacionados con la infiltración extamedular (hígado, bazo, sistema nervioso central, piel o ganglios). 12,13 Las manifestaciones relacionadas con infiltración de la médula ósea fueron también frecuentes en nuestro estudio. La mayor frecuencia de adenopatías, hepatomegalia y esplenomegalia y compromiso extramedular en nuestra serie, pudiera estar en relación con la mayor frecuencia en la muestra, de pacientes con LANL con componente monocítico que representaron aproximadamente la mitad de los casos.
El conteo de leucocitos al inicio se comportó de forma similar a la literatura consultada, donde se refiere que aproximadamente la mitad de los pacientes al diagnóstico tienen un conteo de leucocitos menor de 25 x 109/L y la hiperleucocitosis ocurre en aproximadamente el 5 % de los casos. 12
Alrededor del 15 % de los pacientes con LANL presentaron una variante mielomonocítica y el 45 % fueron mieloblásticas con maduración o sin ella 12, 13. En nuestra serie se observa una inversión de esta frecuencia; la frecuencia de variante mielomonocítica fue significativamente mayor que lo descrito (47,8%).
En aproximadamente el 60 % de los pacientes con LANL el estudio citogenético reveló una anomalía del cariotipo y hasta el 40 - 50 % de los pacientes tenían un cariotipo normal, por lo que resultó un grupo muy heterogéneo. 10,12 En nuestra serie, la positividad de este estudio fue baja, en el 21,7 % la citogenética fue normal y el porcentaje de cariotipos no útiles fue elevado (39,1 %), lo que demuestra la necesidad de mejorar nuestras técnicas.
En las últimas tres décadas han ocurrido importantes avances en el conocimiento de la lesión citogenética y molecular relacionada con la patogenia de la leucemia mieloide aguda (LANL) 10, 14. Se ha encontrado un número importante de alteraciones moleculares, lo que es evidencia de la heterogeneidad de esta enfermedad. La frecuencia de aparición varía en diferentes estudios, la t (8;21) se presenta en aproximadamente el 8 % de los casos, inv. 16 en el 5 %, las mutaciones que involucran el gen MLL en el 5 % de todas las LANL; más recientemente se han estudiado otras alteraciones moleculares que han revolucionado el enfoque pronóstico y terapéutico de las LANL con cariotipo normal, la mutación FLT3-ITD se ha encontrado presente en el 25 - 30 % de los casos, mientras que la mutación NPM1 está presente en el 20 % y puede encontrarse hasta en el 50 - 60 % de los pacientes con cariotipo normal 14-17. En los pacientes se estudiaron 5 alteraciones moleculares (t (8;21), inv.16, t (4;11), FLT3-ITD, NPM1). Solo en el 48 % de los pacientes incluidos, la frecuencia de presentación de la t (8;21) y de la mutación NPM1 fue similar a lo reportado en la literatura, la frecuencia de la mutación FLT3-ITD fue inferior, y no se detectaron la inversión del cromosoma 16 y la t (4;11).
El primer objetivo en el tratamiento de la LNAL es alcanzar la remisión completa (RC). Los esquemas de quimioterapia de inducción para pacientes menores de 60 años, basados en la combinación de una antraciclina (daunorubicina o idarubicina) y ARA-C, no han variado prácticamente en los últimos años, y habitualmente se administra un ciclo inicial para inducir a la remisión. Hasta el 60 -80 % de los adultos alcanzan de esta forma la RC. 12, 13, 18 Sin embargo, se ha visto que aproximadamente en la mitad de los pacientes no se logra la RC después del primer ciclo de inducción clásica 19, 20. Algunos autores recomiendan para este grupo de pacientes un segundo ciclo de terapia de inducción con mitoxantrone y dosis intermedia o alta de ARA-C (HAM). 20- 22 Aproximadamente el 40 % de los pacientes que no logran la RC con el primer ciclo de inducción, la obtienen con el segundo ciclo. El porcentaje de RC alcanzado en nuestra serie (84,2 %) se corresponde con lo reportado por la mayoría de las series consultadas. Hay que señalar que el porcentaje de pacientes que necesitaron un segundo ciclo de inducción para lograr la remisión completa (73,7 %) fue muy superior a lo reportado en la literatura; para algunos autores esto representa un factor pronóstico adverso en términos de SLE y SG. 21 En un meta-análisis realizado por un grupo cooperativo entre 1983 y 1993, se sugirió que los pacientes que lograron la RC después de un segundo ciclo de inducción tienen un pronóstico similar que aquellos que obtienen la RC con el ciclo de inducción inicial. 22
Cuando se analizaron los resultados del tratamiento según el grupo de riesgo, de los 19 pacientes que completaron la inducción, aunque el porcentaje de RC del grupo de riesgo favorable fue mayor que en el grupo desfavorable (50 vs 43,8 %), no se encontraron diferencias significativas (p = 0,25). AL evaluar esta respuesta teniendo en cuenta el riesgo molecular, el porcentaje de RC del grupo de riesgo favorable (85,7 %) fue significativamente mayor (p = 0.05). Estos resultados ponen de manifiesto la importancia de las alteraciones moleculares como factor pronóstico en la LNAL. Visani G y colaboradores 22 evaluaron el valor pronóstico de las alteraciones citogenéticas y moleculares en 848 pacientes con LANL y encontraron una asociación significativa entre el riesgo citogenético y molecular (favorable, intermedio, desfavorable) y el rango de RC (88 vs 65 vs 36 %, respectivamente, p = 0.0001). Otros trabajos han planteado que el perfil de expresión genética permite identificar subgrupos pronósticos importantes de LANL con cariotipo normal. Esta expresión genética está asociada, además, con la proliferación, la apoptosis y con la desregulación de vías de señales oncogénicas, lo que altera el microambiente tumoral y la sensibilidad a las drogas quimioterapéuticas específicas, como las antraciclinas, y por tanto, influyen, además, en la respuesta terapéutica e identifica a pacientes con alto riesgo de no responder a los tratamientos convencionales. 14, 23
Al analizar la respuesta al tratamiento de consolidación vemos que el 84,6 % de los casos se mantuvieron en remisión completa con el primer ciclo de tratamiento y más del 60 % mantiene la remisión completa al completar el tercer ciclo. En términos de mantenimiento de la RC según el grupo de riesgo, el porcentaje de pacientes que mantuvo la RC del grupo de riesgo favorable fue mayor que en el grupo de riesgo desfavorable (54,5 vs 45,5 %), pero no existieron diferencias con significación estadística (p = 0.26). Los 5 pacientes con riesgo molecular favorable se mantuvieron en RC. Estos resultados están influidos por el escaso número de pacientes con estudio molecular en esta serie. RF Schlenk y colaboradores demostraron el impacto en la evolución clínica de las alteraciones moleculares en pacientes con LANL y cariotipo normal. En el análisis retrospectivo de 872 pacientes menores de 60 años, en el marco del grupo germano-austriaco de estudio de la LANL; el riesgo de recaída y muerte fue significativamente menor en pacientes con la mutación NPM1 sin mutación del FLT3-ITD (0,44; 95 % IC, 0,32 0,61), los pacientes no incluidos en esta categoría favorable (incluidos aquellos con la mutación FLT3-ITD) tuvieron una evolución significativamente peor. 14
En el presente estudio, la mortalidad durante el tratamiento de inducción fue del 8,7 %, lo que se corresponde con lo reportado por otros autores, que oscila entre el 5 y el 10 % en pacientes menores de 50 años; y del 10 - 20 % en pacientes de 50 - 60 años. 24 Algunos autores refieren que la mortalidad durante el tratamiento de inducción se correlaciona con la edad y posiblemente con el conteo de leucocitos 25. Las causas de muerte encontradas en el estudio en términos de frecuencia se corresponden con lo reportado en la literatura revisada. 25,26 La sepsis fue la causa más frecuente de mortalidad, seguidas por la hemorragia y la progresión de la enfermedad, mientras que la mortalidad relacionada con el tratamiento de consolidación fue elevada (30,8 %) comparado con lo que reporta la literatura, y fue la sepsis la causa más frecuente.
La sobrevida libre de enfermedad (SLE) de los pacientes que lograron remisión completa fue ligeramente mayor que lo reportado en la literatura, la media fue de 17,62 meses y el promedio de 56,3 %. Un trabajo anterior realizado en el servicio reportó una SLE a los 12 meses de 30,6 % en pacientes menores de 60 años 27. Otros estudios encuentran una SLE a los 4 años del 44 % 13 y del 30 % a los 3 años 27. Las diferencias en los resultados obtenidos pueden deberse al tiempo considerado para el cálculo de este parámetro.
Cuando se analizó la SLE según el grupo de riesgo, se encontraron diferencias entre los grupos de riesgo, aunque no de forma significativa. En el grupo de riesgo favorable la media de supervivencia fue de 23,87 meses, con un promedio del 75 %; en el grupo de riesgo intermedio la media de supervivencia fue de 3,27 meses y en el grupo de riesgo desfavorable la media fue de 9,93 meses, promedio del 42,9 %, (p = 0.076). Estos resultados pueden estar influenciados por el tamaño de la muestra. Otro estudio también encontró diferencias en la SLE a los 4 años en dependencia de los grupos de riesgo: 60 % para el bajo riesgo, 30 % para el riesgo intermedio y 12 % para el alto riesgo 13.
Los resultados de la SG, con un tiempo medio de supervivencia de 14,07 meses y un promedio de sobrevida del 39,1 %, se corresponden con lo encontrado en la bibliografía revisada. En un estudio realizado con anterioridad en el servicio se encontró una SG en pacientes menores de 60 años del 38,1 % a los 12 meses.27 Otros reportan una media de SG de 12 meses y aproximadamente el 30 % de SG a los 5 años en pacientes menores de 55 años
Cuando se analizó la SG en relación con el grupo de riesgo, la media de supervivencia del grupo de riesgo favorable fue de 17,92 meses con un promedio del 45,5 %; grupo de riesgo desfavorable media de sobrevida 10,27 meses con un promedio del 36,4%. Los resultados también fueron congruentes con lo reportado por otros autores. 12, 13, 27 Es difícil establecer una comparación en relación con la SLE y la SG debido a que los estudios realizados por lo general son heterogéneos en cuanto a la uniformidad de la muestra y los esquemas terapéuticos aplicados, tanto de inducción como de consolidación. Es por eso que se recomienda realizar los estudios citogenéticos y moleculares, que nos permitan estratificar a todos los pacientes e individualizar su tratamiento, al mayor número de pacientes con diagnóstico de LANL.
REFERENCIAS BIBLIOGRAFICAS
1. Appelbaum FR, Rosenblum D, Arceci RJ, Carroll WL, Breitfeld PP, Forman SJ, et al. End points to establish the efficacy of new agents in the treatment of acute leukaemia. Blood 2007 Mar;109 (5):1810-6.
2. Renneville A, Roumier C, Biggio V, Nibourel O, Boissel N, Fenaux P, et al. Cooperating gene mutations in acute myeloid leukemia: a review of the literature. Leukemia. 2008 May;22(5):915-31.
3. Kiyoi H, Naoe T Biology, clinical relevance, and molecularly targeted therapy in acute leukemia with FLT3 mutation. Int J Hematol. 2006 May;83(4):301-8.
4. Mrozek K, Marcucci G, Paschka P, Whitman SP, Bloomfield CD. Clinical relevance of mutations and gene-expression changes in adult acute myeloid leukemia with normal cytogenetics: are we ready for a prognostically prioritized molecular classification? Blood. 2007 Jan 15;109(2):431-48.
5. Castaigne S, Chevret S, Archimbaud E, Fenaux P, Bordessoule D, Tilly H, et al. Randomized comparison of double induction and timed-sequential induction to a «3 + 7» induction in adults with AML: long-term analysis of the Acute Leukemia French Association (ALFA) 9000 study. Blood 2004 Oct 15;104(8):2467-74.
6. Robak T, Wierzbowska A. Current and emerging therapies for acute myeloid leukemia. Clin Ther. 2009;31 Pt 2:2349-70.
7. Rowe JM, Kim HT, Cassileth PA, Lazarus HM, Litzow MR, Wiernik PH et al. Adult patients with acute myeloid leukemia who achieve complete remission after 1 or 2 cycles of induction have a similar prognosis: a report on 1980 patients registered to 6 studies conducted by the Eastern Cooperative Oncology Group. Cancer. 2010 Nov 1;116(21):5012-21.
8. VisaniG, Olivieri A, Malagola M, Brunori M, Piccaluga PP, Capelli D et al. Consolidation therapy for adult acute myeloid leukemia: a systematic analysis according to evidence based medicine. Leuk Lymphoma. 2006 Jun;47(6):1091-102.
9. Yamamoto JF, Goodman MT. Patterns of leukemia incidence in the United States by subtype and demographic characteristics, 1997-2002. Cancer Causes Control. 2008 May; 19(4):379-90.
10. Grimwade D. Impact of cytogenetics on clinical outcome in AML. In: Karp JE, ed. Acute Myelogenous Leukemia. Totowa, New Jersey: Humana Press; 2007:177-192.
11. Lichtman M, Liesveld JL. Leucemia mielogena aguda. En: Beutler E, Lichtman MA, Coller BS, editors. Hematología Williams, 6a Ed. Madrid: Marban Libros, S.L; 2005: 1047-83.
12. Lichtman M, Liesveld JL. Acute Myelogenous Leukemia. In: Kaushansky K, Beutler E, Seligsohn U, Lichtman M, Kipps T, editors. Williams Hematology, 8th Ed. New York: McGraw-Hill Companies; 2010.
13. Rodríguez G, Escudero A. Indicaciones actuales del trasplante alogénico en Leucemia Aguda Mieloblástica. Cuadernos de Hematología1ra ed; 2008.
14. Schlenk RF, Döhner K, Krauter J, Fröhling S, Corbacioglu A, Bullinger L, et al. German-Austrian Acute Myeloid Leukemia Study Group. Mutations and treatment outcome in cytogenetically normal acute myeloid leukemia. N Engl J Med. 2008 May 1;358(18):1909-18.
15. Scholl C, Gilliland DG, Fröhling S. Deregulation of signaling pathways in acute myeloid leukemia. Semin Oncol. 2008 Aug;35(4):336-45..
16. Green CL, Koo KK, Hills RK, Burnett AK, Linch DC, Gale RE. Prognostic significance of CEBPA mutations in a large cohort of younger adult patients with acute myeloid leukemia: impact of double CEBPA mutations and the interaction with FLT3 and NPM1 mutations. J Clin Oncol. 2010 Jun 1;28(16):2739-47.
17. Haferlach C, Mecucci C, Schnittger S, KohLANLnn A, Mancini M, Cuneo A, et al. AML with mutated NPM1 carrying a normal or aberrant karyotype show overlapping biologic, pathologic, immunophenotypic, and prognostic features. Blood. 2009 Oct ;114(14):3024-32.
18. Zhu X, Ma Y, Liu D. Novel agents and regimens for acute myeloid leukemia: 2009 ASH annual meeting highlights. J Hematol Oncol, 2010 Apr;3:17.
19. Kern W, Haferlach T, Schoch C, Loffler H, Gassmann W, Heinecke A, et al. Early blast clearance by remission induction therapy is a major independent prognostic factor for both achievement of complete remission and long-term outcome in acute myeloid leukemia: data from the German AML(AMLCG) 1992 Trial.. Blood 2003 Jan 1;101(1):64-70.
20. Rowe JM, Kim HT, Cassileth PA, Lazarus HM, Litzow MR, Wiernik PH et al. Adult patients with acute myeloid leukemia who achieve complete remission after 1 or 2 cycles of induction have a similar prognosis: a report on 1980 patients registered to 6 studies conducted by the Eastern Cooperative Oncology Group. Cancer. 2010 Nov 1;116(21):5012-21.
21. Schlenk RF, Benner A, Hartmann F, del Valle F, Weber C, Pralle H, et al. Risk-adapted postremission therapy in acute myeloid leukemia: results of the German multicenter AML HD93 treatment trial. Leukemia. 2003 Aug;17(8):1521-8.
22. Visani G, Bernasconi P, Boni M, Castoldi GL, Ciolli S, Clavio M, et al. The prognostic value of cytogenetics is reinforced by the kind of induction/consolidation therapy in influencing the outcome of acute myeloid leukemia—analysis of 848 patients. Leukemia 2001 Jun;15(6):903-9.
23. Grimwade D, Hills RK. Independent prognostic factors for AML outcome. Hematology Am Soc Hematol Educ Program. 2009;38595.
24. Estey E, Kantarjian H. Therapy for acute myeloid leukemia. In: Hoffman: Hematology: Basic Principles and Practice, 4th ed. Churchill Livingstone, An Imprint of Elsevier; 2005.
25. Tsimberidou AM, Estey E. Induction mortality risk in adult acute myeloid leukemia. Leuk Lymphoma. 2006 Jul;47(7):1199-200.
26. Jagarlamudi R, Kumar L, Kochupillai V, Kapil A, Banerjee U, Thulkar S. Infections in acute leukemia: an analysis of 240 febrile episodes. Med Oncol. 2000 May;17(2):111-6.
27. Hernández C, Pérez D, Carnot J, Castro R, Muñio J, Martinez C et al. Tratamiento con quimioterapia de la Leucemia mieloide aguda en Hospital Hermanos Ameijeiras. Experiencia de 20 años de trabajo. Rev Cubana Med. 2006; 45(1): 1-9.
Recibido: diciembre 28,2012
Aceptado: enero 30, 2013
Dra. Yusselys Cabrera Payne. INSTITUTO DE HEMATOLOGÍA E INMUNOLOGÍA. Apartado 8070, La Habana, CP 10800, CUBA
Tel (537) 643 8695, 8268
Fax (537) 644 2334
Email: rchematologia@infomed.sld.cu