Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión impresa ISSN 0864-0300versión On-line ISSN 1561-3011
Rev Cubana Invest Bioméd v.29 n.4 Ciudad de la Habana oct.-dic. 2010
ARTÍCULOS ORIGINALES
Obtención y evaluación del líquido ascítico murino hemoclasificador anti-B en las líneas de ratones Ofbalb (F1) y Balb/c
Obtainment and evaluation of the murine ascitic liquid anti-B hemo-classificatory in Ofbalb (F1) and Balb/c mice strains
Nelsa Esperanza Soria PeñalverI; Humberto Joaquín Morris QuevedoII; Sandra Rivera InfanteIII; Esteban Gutiérrez CalzadoIV
IDoctora en Medicina Veterinaria. Laboratorios de Anticuerpos y Biomodelos Experimentales. Santiago de Cuba, Cuba.
IIDoctor en Ciencias Biológicas. Profesor Auxiliar. Investigador Auxiliar. Centro de Estudios de Biotecnología Industrial (CEBI), Universidad de Oriente. Santiago de Cuba, Cuba.
IIILicenciada en Farmacia. Laboratorios de Anticuerpos y Biomodelos Experimentales. Santiago de Cuba, Cuba.
IVDoctor en Ciencias de la Salud. Investigador Auxiliar. Laboratorios de Anticuerpos y Biomodelos Experimentales. Santiago de Cuba, Cuba.
RESUMEN
La línea de ratón Balb/c ha sido utilizada tradicionalmente para la producción de líquido ascítico murino; sin embargo, actualmente se están introduciendo líneas híbridas, como la Ofbalb (F1).En el presente trabajo, se evaluó el comportamiento del hibridoma C6G4 (anti-B) expandido en ratones de la línea Balb/c y en la línea híbrida Ofbalb (F1). De cada línea se conformaron cuatro grupos, a los que se les administró por vía intraperitoneal las concentraciones celulares del inóculo: 1; 2,5; 3 y 4 x 106 células/0,5 mL/ratón. Los parámetros analizados fueron, el por ciento de prendimiento, el volumen y el rendimiento del líquido ascítico murino por ratón. Se demostró que con la línea Balb/c se obtienen mejores resultados para este hibridoma, en particular. El inóculo más adecuado fue el correspondiente a 2,5 x 106 células. La línea híbrida Ofbalb (F1) con tratamientos similares no mostró diferencias estadísticamente significativas en los parámetros considerados.
Palabras clave: Líquido ascítico murino, anticuerpos monoclonales, hemoclasificador anti-B, línea híbrida Ofbalb (F1).
ABSTRACT
The Balb/c mouse strain has been traditionally used for the production of murine ascitic fluid; however, nowadays hybrid strains are introduced including the Ofbalb (F1). The aim of present paper was to assess the behavior of C6G4 (anti-B) hybridoma scattered in mice of Balb/c strain and in the Ofbalb (F1) hybrid strain. From each strain four groups were created which received by intraperitoneal route the cell concentrations of the inoculum: 1; 2,5; 3 and 4 x 106 cells/0,5 mL/mouse. The analyzed parameters were the seizure percentage, the volume and the performance of murine ascitic fluid by mouse. It was demonstrated that with the Balb/c strain better results are obtained for this hybridoma in particular. The more appropriate inoculum was that corresponding to 2,5 x 106 cells. The Ofbalb (F1) hybrid strain with similar treatments not showed statistically significant differences in the analyzed parameters.
Key words: Murine ascitic fluid, monoclonal antibodies, Ofbalb (F1) hybrid strain anti-B blood classifier.
INTRODUCCIÓN
El uso masivo de los anticuerpos monoclonales (AcM) en la investigación, el diagnóstico y la terapéutica de enfermedades del hombre, ha motivado la necesidad de estrategias adecuadas para su producción y purificación en cantidades y calidad suficiente para cada aplicación específica.1 La obtención de estos compuestos ha estado muy estrechamente vinculada, desde sus inicios, con la producción intensiva de grandes volúmenes de ascitis tumoral, mediante la propagación de hibridomas murinos en ratones.2
En los seres humanos se identifican cuatro fenotipos principales dentro del sistema ABO de grupos sanguíneos, que son A, B, O y AB, que designan la presencia o la ausencia de los antígenos A y B. La transfusión de sangre continúa siendo un arma terapéutica imprescindible en la medicina moderna, por lo que la compatibilidad entre el donante y el receptor a través de la determinación de los grupos ABO y Rh (D), es un requisito indispensable para garantizar un tratamiento, sin riesgos para la vida del paciente.3
La producción de antisueros policlonales humanos confiables y de alta calidad para la tipificación de sangre es una tarea laboriosa, por lo que el suministro estable de este tipo de reactivo se hace cada día más difícil, además de los riesgos inherentes a la transmisión de enfermedades a través de las inmunizaciones.4 La aplicación de la tecnología de hibridomas desarrollada por Köhler y Milstein5 para la producción de anticuerpos monoclonales murinos,6 y su empleo para preparar reactivos hemoclasificadores de nuevo tipo, despertó un elevado interés internacional a partir de la década de los años 80.7
Los AcM están contribuyendo decisivamente a la definición de algunos antígenos sanguíneos cuyas características estructurales son desconocidas, así como a dilucidar la expresión de estos antígenos en los diversos tejidos, y su relación con la significación funcional, que probablemente esté asociada con los procesos de diferenciación y crecimiento celular.8.
El ratón Balb/c se ha utilizado tradicionalmente en numerosos centros de Biotecnología de nuestro país para la expansión in vivo de los hibridomas anti-A y anti-B, en la producción de líquido ascítico murino (LAM), rico en AcM hemoclasificadores.
Los datos preliminares relacionados con la obtención de LAM en ratones Balb/c informan una media de 2-3 mL por animal con pocas extracciones y el contenido proteico útil es del 40 %. Las referencias nacionales en hibridomas evaluados en los ratones Ofbalb (F1), evidencian un volumen promedio de LAM de 11 mL por ratón con un 90 % de concentración proteica. Los resultados sugieren su empleo en la producción de grandes volúmenes de ascitis, con un ahorro considerable de animales y un incremento sustancial de la productividad.4.Por otra parte, las facilidades de cría y reproducción de este modelo son semejantes a la de los ratones Balb/c.9
El comportamiento del hibridoma hemoclasificador anti-A en ratones híbridos de primera generación Ofbalb (F1) ha sido investigado en los Laboratorios de Anticuerpos y Biomodelos Experimentales.10 Desde el punto de vista productivo, también resulta de interés evaluar comparativamente el comportamiento y los rendimientos del hibridoma hemoclasificador anti-B en los biomodelos murinos Ofbalb (F1) y Balb/c, disponibles en nuestro país.
MÉTODOS
Biomodelos animales
Se emplearon ratones híbridos de primera generación Ofbalb (F1), con un peso promedio de 29 g y ratones Balb/c con un peso promedio de 21 g. En ambas líneas se utilizaron ratones machos de 10 semanas aproximadamente, procedentes del Centro Nacional para la Producción de Animales de Laboratorio (CENPALAB, La Habana), con calidad sanitaria y genética certificadas.
Los animales se mantuvieron en locales protegidos con un ciclo de iluminación de 10 horas luz-14 horas oscuridad, la temperatura osciló entre los 20-22 °C, la humedad relativa entre 60-65 % con inyección y extracción de aire a pleno. Se utilizaron cajas T2 como recinto primario, con tapas metálicas de acero inoxidable y biberones plásticos; como encamado se utilizó bagazo desecado y desmeollado estéril. Se suministró dieta peletizada (ALYco®, CENPALAB, La Habana). El agua administrada fue tratada y filtrada por membrana de acetato de celulosa (0,2 micras). Los animales recibieron agua y alimento convencional para la especie ad libitum.
Inóculo
El inóculo utilizado fue el hibridoma C6G4 secretor de un anticuerpo monoclonal anti-B, que es una inmunoglobulina del tipo IgG2b. El hibridoma resultó de la fusión del mieloma de ratón P3x63.Ag8.653, con los linfocitos del bazo de ratones Balb/c, inmunizados con el antígeno B sintético, obtenido en el Instituto Nacional de Hematología, Inmunología y Hemoterapia, de Ciudad de La Habana.
Grupos experimentales
Para cada línea se conformaron 4 grupos de 15 animales cada uno, que se preinocularon con 0,2 mL de petrolato ligero por animal vía intraperitoneal (i.p.). Transcurridos los 7 días, se inocularon con el hibridoma C6G4 anti B, con concentraciones de 1; 2,5; 3 y 4 x 106 células, respectivamente.
A partir aproximadamente de los 10 días de la inoculación, se comenzó la extracción del LAM por el método de punción. Como anticoagulante se utilizó el EDTA disódico al 2 %.
Se realizó la clarificación de la ascitis por centrifugación a 2 500 rpm durante 20 min, en una centrífuga refrigerada Universal 320 (Alemania).
En los diferentes grupos experimentales se evaluó el por ciento de animales prendidos, el volumen de LAM colectado y el rendimiento de ascitis por animal. Estos estudios fueron avalados por los procedimientos normalizados operacionales existentes en nuestro laboratorio.
El por ciento de prendimiento se determinó a partir de la relación entre los animales prendidos con el hibridoma respecto al total de animales inoculados. El rendimiento de LAM se expresó como la relación existente entre el volumen total de LAM respecto al número de ratones prendidos.
Análisis estadístico
Para las diferentes variables analizadas se determinaron las medias y desviación estándar. Para analizar los parámetros evaluados a diferentes concentraciones celulares en una misma línea de ratones se realizaron análisis de varianza de clasificación simple por rangos (prueba de Kruskal-Wallis). La comparación de los parámetros estudiados entre las dos líneas de ratones según la concentración celular se efectuó mediante la prueba no paramétrica de Mann-Whitney. Se empleó el Software Estadístico Graficador Pad Prism de la Universidad de Humboldt de Berlín (Alemania).
RESULTADOS
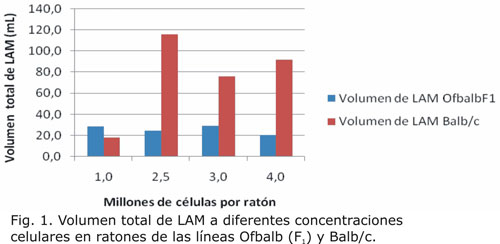
En la tabla 1 se presentan los volúmenes de LAM colectados durante extracciones sucesivas en los ratones Ofbalb (F1) y Balb/c, según las concentraciones de inóculo empleadas. En el caso de la línea Ofbalb (F1), los mayores volúmenes se obtuvieron con las concentraciones de 1 x 106 y 3 x 106, durante las tres primeras extracciones. Con relación a la línea Balb/c, los mayores volúmenes de LAM se colectaron en los grupos inoculados con concentraciones de 2,5 y 4 x 106 células (Fig. 1). Con respecto a este parámetro, los mejores resultados, desde el punto de vista productivo se alcanzaron en la línea de ratones Balb/c.
En el caso de la línea Ofbalb (F1), el mayor rendimiento correspondió a la concentración celular de 4 x 106, con 6,83 mL. En el caso de la línea Balb/c, la concentración de 2,5 x 106, resultó ser la de mejores resultados con 2,55 mL. En este parámetro, la línea Ofbalb (F1) reflejó mejores resultados, en comparación con la línea Balb/c (tabla 2).
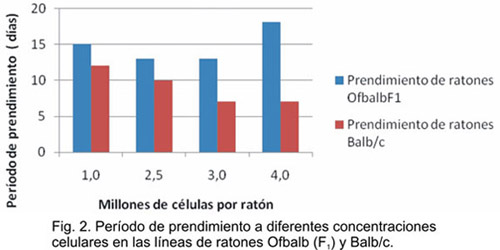
Las figuras 2 y 3 muestran, respectivamente, el período y el por ciento de prendimiento en cada uno de los grupos experimentales en las dos líneas de ratones consideradas. Los menores tiempos de prendimiento se obtuvieron en la línea Balb/c con inóculos de 3 y 4 x 106, mientras que en la línea Ofbalb (F1) se alcanzaron con inóculos de 2,5 y 3 x 106 (Fig. 2).
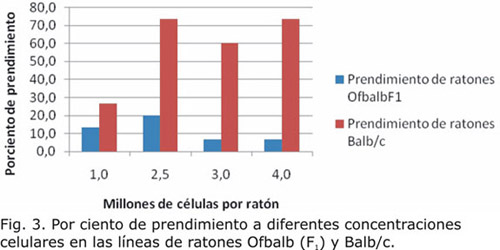
Por otra parte, en el caso de la línea Ofbalb (F1), la concentración de 2,5 x 106, con un 20 % de prendimiento, fue la de mejores resultados. En la línea Balb/c, las dos mejores concentraciones de inóculo estuvieron representadas por 2,5 y 4 x 106, con las que se alcanzó 73,3 % de prendimiento (Fig. 3).
Se demostró que, en sentido general, con la línea Balb/c se obtienen mejores resultados para este hibridoma, en particular (volúmenes colectados, así como el periodo y por ciento de prendimiento). Tomando en consideración los resultados de la prueba de Kruskall-Wallis (p< 0,05), los inóculos más adecuados fueron los correspondientes a 2,5 y 4 x 106 células.
DISCUSIÓN
Los reactivos hemoclasificadores, durante su producción no sufren un proceso de purificación por afinidad u otras técnicas, sino por filtración biológica, y las pérdidas proteicas son generalmente altas. Tomando en consideración este aspecto tecnológico, es importante optimizar los parámetros relacionados con la producción de LAM, y uno de los elementos esenciales es el modelo animal empleado.
La cavidad peritoneal del ratón representa un sitio idóneo para la producción de AcM debido a la posibilidad de formación de un fluido ascítico en respuesta al crecimiento tumoral, cuyo volumen puede fluctuar entre 2 y 10 mL por ratón y una concentración de AcM entre 5 y 15 mg/mL3.
Se ha planteado que el biomodelo Ofbalb (F1) es capaz de producir mayores rendimientos de ascitis tumoral rica en AcM, con el empleo de un menor número de animales,9 lo que constituye una consideración ética, importante para la producción de AcM en cantidades comercializables. Ello estaría relacionado estrechamente con la aplicación de los principios bioéticos referidos a las tres Rs (Refinamiento, Reemplazo y Reducción).11
La experiencia con los híbridos de primera generación obtenidos del apareamiento de Balb/c machos y Of1 hembras, denominados Ofbalb (F1),9 en la producción de reactivos hemoclasificadores se han limitado a los hibridomas anti-A10. No existen referencias relacionadas con el hibridoma C6 G4 (anti-B).
Los volúmenes de LAM colectados representan un criterio de gran importancia en el proceso de obtención de AcM.
La línea Ofbalb (F1) mostró mejores resultados en comparación con la línea Balb/c, respecto al rendimiento de LAM, con un mejor aprovechamiento de los animales positivos al hibridoma anti B, a pesar de la realización de una menor cantidad de extracciones. Este parámetro depende en gran medida de la línea genética utilizada y de las características individuales, ya que cada animal puede comportarse de manera diferente ante un mismo hibridoma y concentración celular. En este sentido, se plantea que los ratones híbridos entre Balb/c y otras cepas y razas son muy convenientes para la producción de ascitis, debido a su rendimiento.12 Se deben garantizar, además, las mejores condiciones ambientales, para evitar el estrés y de esta manera, contribuir a que se favorezcan las producciones establecidas.13
En la literatura relacionada con el tema se considera, en general, que un prendimiento por encima del 90% es adecuado. No obstante, pueden existir porcientos de prendimientos más bajos en dependencia de las condiciones existentes en cada instalación (temperatura, condiciones higiénico-sanitarias y alojamiento, entre otras) y del hibridoma utilizado. De modo que, cada laboratorio establece sus intervalos de normalidad; los resultados obtenidos se hallan dentro de los parámetros establecidos para LABEX/CIM según los Procedimientos Normalizados Operacionales.
Aunque, en sentido general, se demostró que con la línea Balb/c se obtienen mejores resultados para el hibridoma C6 G4 (anti-B), es necesario evaluar desde el punto de vista económico la factibilidad de la utilización de un inóculo de mayor concentración celular para obtener grandes volúmenes de LAM. Además, se debe valorar su incidencia en la eficiencia productiva y en la calidad del reactivo o producto final.
Agradecimientos
A los especialistas de los Departamentos de Producción de LAM, y de Productos Terminados y Cultivo Celular del LABEX-CIM por su cooperación y asistencia técnica en la realización de este trabajo.
REFERENCIAS BIBLIOGRÁFICAS
1. Voak D. Monoclonal antibodies as blood grouping reagents. Baillers Clin Haematol. 1990; 3:219-42.
2. Scott ML, Voak D. Monoclonal antibodies to human red blood cell group antigens. WHO Course in International Blood Group Reference Laboratory. Bristol: United Kingdom; 1997. June 2-6. p. 365-85.
3. Bencomo A, Alfonso Y, Alfonso ME, González R, Fernández J, Ballester A. Frecuencia de los grupos sanguíneos A1, A2, Aint, Ael, B y O en donantes de sangre. Rev Cubana Hematol Inmunol Hemoter. 1997;13:124-31.
4. Edelman L. Los anticuerpos monoclonales en inmunohematología, interés científico, aplicaciones prácticas y aspectos económicos de los reactivos empleados para la determinación de los grupos sanguíneos. Organización de las Naciones Unidas para el Desarrollo Industrial (ONUDI). Simposio Latinoamericano sobre la sangre y sus derivados. Cartagena: Colombia; 1984 Nov. Paper NRLA/83/117/18.
5. Kholer G, Milstein C. Continuos culture of fused cells secreting antibody of predefined specificity. Nature. 1975;256:495-7.
6. Urnadiz MP, Cuadrado E, Garrido F. Informe sobre el I Taller Internacional (y Simposio) sobre anticuerpos monoclonales contra antígenos de los eritrocitos y moléculas relacionadas. Inmunología. 1989;7:93-8.
7. Beck ML, Korth J, Kirkegaard J, Pierce S. Anomalous results of ABO blood grouping with monoclonal reagents. Transfusion. 1993;33:624.
8. Oriol R, Samuelsson BE, Messeter L. Antibodies serological behaviour and immunochemical characterization. J Immunogenet. 1990;17:279-99.
9. Cosme K. Producción de ascitis tumoral rica en anticuerpos monoclonales contra el antígeno de superficie del virus de la hepatitis B a partir de ratones híbridos de primera generación (Tesis Doctoral). Ciudad de La Habana: Centro de Ingeniería Genética y Biotecnología; 1999.
10. Esparraguera Y. Obtención de un reactivo hemoclasificador con el hibridoma anti-A IHI_15 en biomodelos murinos Ofbalb (F1) y Balb/c (Tesis de Maestría). Santiago de Cuba: Universidad de Oriente; 2006.
11. Balls M. Reduction, refinement, and replacement: The end of an era, new beginning, and new challenges. ATLA. 1995;23:744-5
12. Gavilondo JV. Anticuerpos monoclonales. La Habana: Elfos Scientae; 1995.
13. Marx U, Embleton M, Gruber F, Hansson U, Heder J. Monoclonal antibody production. ATLA. 1997;25:121-37.
Recibido: 26 de febrero de 2010.
Aprobado: 11 de junio de 2010.
Dra. Nelsa Esperanza Soria Peñalver (LABEX/CIM). Calle 23 y Carretera El Caney, Reparto Vista Alegre. Santiago de Cuba, Cuba. Teléfono: 53-22-642403. Correo electrónico: nelsa@cim.sld.cu