Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión impresa ISSN 0864-0300
Rev Cubana Invest Bioméd vol.30 no.4 Ciudad de la Habana sep.-dic. 2011
TRABAJO ORIGINAL
Nuevos modelos conceptual y matemático para el contorno de la onda de volumen de pulso arterial
New conceptual and mathematical forms for the contour of volume wave of arterial pulse
Ms. C. Alexander Pascau Simón,I Dr. CM. José E. Fernández-Britto Rodríguez,II Ph.D. John AllenIII
ICentro de Biofísica Médica, Departamento de Bioinformática. Universidad de Oriente, Santiago de Cuba, Cuba.
IICentro de Investigaciones y Referencia de Aterosclerosis. La Habana, Cuba.
IIIRegional Medical Physics Department, Freeman Hospital, United Kingdom.
RESUMEN
Introducción: El análisis del contorno de la onda de volumen de pulso arterial ha sido útil para el diagnóstico no invasivo de enfermedades cardiovasculares, pero los orígenes patofisiológicos que contribuyen a este contorno no están totalmente explicados. El objetivo de este trabajo fue hallar el nivel de coincidencia de un nuevo modelo conceptual simple, basado en las fuerzas hemodinámicas, con respecto a un nuevo modelo matemático aplicado a las diferentes clases de ondas de volumen de pulso arterial en dedos de miembros inferiores.
Métodos: la propuesta del modelo conceptual se basó en que este contorno es la suma de pares de gradientes de fuerzas hemodinámicas de acción, provenientes del corazón, la aorta y el distrito arterial periférico, y las de reacción, provenientes de la pared arterial músculo-elástica bajo estudio. El modelo matemático fue diseñado como un problema de programación no lineal, para hallar las 6 incógnitas numéricas de cada par de gradientes, bajo restricciones no lineales basadas en sus relaciones temporales. Se registraron los contornos desde los dedos de miembros inferiores, en pacientes en los que se pudieran observar las 4 clases de contornos de onda de volumen de pulso arterial conocidos. Se analizó la calidad de ajuste de 4 403 contornos de onda de volumen de pulso arterial experimentales, contra su onda de volumen de pulso arterial resultante del modelo matemático, desde 123 registros de 14 pacientes (7 mujeres).
Resultados: La clase III fue la predominante, las clases I y II fueron frecuentes en pacientes con menos riesgo cardiovascular y la clase IV, en los de mayor riesgo. El 64 % de las ondas de volumen de pulso arterial obtuvieron una bondad de ajuste de calidad > 95 % y el 36 % restante tuvo presencia de ondas oscilantes, provenientes del músculo liso.
Conclusiones: se acepta la coincidencia de ambos modelos para caracterizar morfológicamente el contorno de cualquier clase de onda de volumen de pulso arterial.
Palabras clave: Onda de volumen de pulso arterial, análisis del contorno, aterosclerosis, modelo matemático PNL.
ABSTRACT
Introduction: The analysis of volume wave contour of arterial pulse has been useful for non-invasive diagnosis of cardiovascular diseases, but the pathophysiological origins contributing to this contour are not totally explained. The objective of present paper was to find the coincidence level of a new simple conceptual form, based on the hemodynamic strengths regarding a new mathematical form applied to different classes of volume waves of arterial pulse in toe fingers.
Methods: The proposal of conceptual form was based on that this contour is the addition of pairs of action hemodynamic strengths gradients from the heart, aorta and the peripheral arterial zone and of the reactions coming from study musculoelastic arterial wall. The mathematical form was designed as a non-lineal programming problem to find the six numeral unknown quantities of each pair of gradients, under non-lineal restriction based on its temporary relations. The contours from toe fingers were registered in patients with four potential classes of volume wave known contours of arterial pulse. The fitting quality of 4 403 experimental above mentioned contours was analyzed versus the arterial pulse volume resulting from mathematical form of 123 registries of 14 patients (7 women).
Results: There was predominance of III class, the I and II ones were frequent in patients with less cardiovascular risk and the IV class in those of great risk. The 64% of the wave volume of arterial pulse had a quality fitting > 95% and the 36% had the presence of oscillating waves from skeletal muscle.
Conclusions: The coincidence of both forms is accepted to characterize in a morphologic way the contour of any class of wave volume of arterial pulse.
Key words: Wave volume of arterial pulse, contour analysis, atherosclerosis, PNL mathematical form.
INTRODUCCIÓN
El análisis del contorno de la onda de volumen de pulso arterial (OVP) ha sido de amplia aplicación para el diagnóstico no invasivo de enfermedades cardiovasculares. Su adquisición digital o registro se ha logrado mediante técnicas sencillas como la emisión y reflexión o transmisión de luz infrarroja, llamada fotopletismografía (FPG).1 Los orígenes patofisiológicos que contribuyen a los cambios de volumen sanguíneo, vistos en el contorno de la OVP, siguen siendo un tema de investigación abierto, específicamente los provocados por la actividad de las arterias periféricas músculo-elásticas.2-7 Por tanto, la interpretación en el diagnóstico de enfermedades vasculares, a partir del contorno de la OVP, no está totalmente explicada.1
Se han dado pasos para registrar la OVP, aplicando FPG, por sitios determinados de estas arterias, como en la femoral común.8 La aterosclerosis y sus consecuencias orgánicas constituyen la causa principal de los eventos cardiovasculares y ejercen una gran influencia en las paredes de las arterias músculo-elásticas.9 Se ha demostrado la presencia temprana de la aterosclerosis desde la niñez y la adolescencia, cuyo desarrollo se acelera en individuos que presentan factores de riesgo cardiovasculares modificables como la hipertensión y el tabaquismo.10,11 En las investigaciones actuales, se ha demostrado que las fuerzas hemodinámicas constituyen un factor clave de localización en la aterogénesis,12 y que es el trayecto arterial hacia el corazón, el encéfalo y los miembros inferiores donde más se localizan las placas de ateroma, en sus diferentes estados.9-11 Estas fuerzas son la expresión de fenómenos hemodinámicos derivados por el flujo sanguíneo, los que constituyen uno de los tres elementos básicos de la tríada de Virchow.13 Como consecuencia, la forma del contorno de la OVP es alterada directamente según el estado patológico que presenten las capas de estas arterias, junto con la manera en que se propagan estas fuerzas hemodinámicas, desde el mismo corazón, expresadas en la onda de presión, flujo y volumen sanguíneos.14 Un marcador atractivo e independiente de la aterosclerosis temprana y tardía es la disfunción endotelial (DE), que representa la pérdida gradual o total de la capacidad del endotelio vascular (importante monocapa celular más interna de los vasos sanguíneos) para modular el comportamiento anatomofisiológico de la pared arterial, ante cambios temporales del flujo y presión sanguíneos.15 Se ha llegado a ciertos avances teórico-experimentales en el conocimiento de la influencia anatómica del distrito vascular sobre el contorno de la OVP, simulados en modelos geométricos aplicando la dinámica de fluidos computacional; pero por la gran complejidad de la parte funcional del sistema cardiovascular ha sido difícil simular y pronosticar el funcionamiento de múltiples factores, incluido el endotelio vascular, para lograr así modelos que sean implementados en equipamiento médico, viables a la práctica clínica.12
En este trabajo se plantea que, de formularse un modelo conceptual simple, que considere un acercamiento más profundo sobre los orígenes patofisiológicos de la formación de la OVP y expresarlo matemáticamente, se obtendrían las variables numéricas que caractericen eficientemente el contorno de cualquier clase de OVP, en todo el distrito arterial. Por tanto, el objetivo de este trabajo fue hallar el nivel de coincidencia de un nuevo modelo conceptual simple con respecto a un nuevo modelo matemático, aplicado a las diferentes clases de OVP en dedos de miembros inferiores. Este nuevo modelo conceptual parte de la interacción de fuerzas hemodinámicas de acción y reacción las cuales, junto con otros múltiples factores presentes en la tríada de Virchow, regulan anatómicamente la pared arterial y, por ende, los cambios de volumen sanguíneo que modifican el contorno de la OVP.12,13 Esta interacción se analizó y validó mediante el diseño de un nuevo modelo matemático de regresión y algoritmo de optimización no lineal (PNL) en el cual los coeficientes a obtener del modelo se ajustan significativamente a las diferentes clases de OVP registradas en dedos de los miembros inferiores.
MÉTODOS
Actualidad en el origen y análisis del contorno de la onda de volumen de pulso
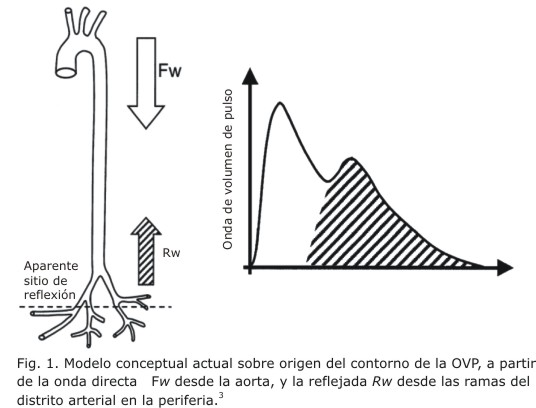
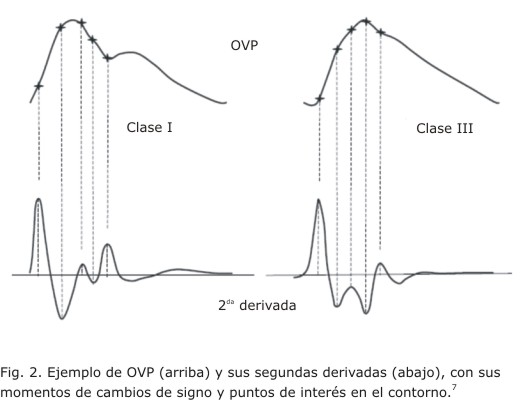
Se ha dado una explicación aproximada a la formación del contorno de la OVP. Se destacan, en general, las ondas directas Fw y las reflejadas Rw, formando así el contorno de la OVP16 (fig. 1). El análisis del contorno de la OVP se ha procesado matemáticamente desde la primera a la tercera derivada discreta por varios autores,6,7 con el objetivo de extraer rasgos distintivos, como la ubicación de los cambios de signo, ondas y sus puntos de interés (fig. 2), para calcular e interpretar índices numéricos como el índice de rigidez arterial (IRA) y el índice de reflexión (IR), con respecto a variables clínicas.2-5 Estos métodos y sus índices numéricos han tenido relación con los factores de riesgo cardiovascular. Sin embargo, ofrecen una explicación pobre con respecto al origen del contorno de la OVP.7 Además, estos métodos tienen la debilidad de no ser precisos cuando la OVP tiene un contorno muy atenuado (como suele suceder con los pacientes asintomáticos, con alto grado de riesgo cardiovascular, o los enfermos de aterosclerosis tardía y los de avanzada edad), donde no existe cambio de signo o es imprecisa la ubicación de puntos de inflexión en el descenso del contorno de la OVP.7,17 Se ha expresado el contorno de la OVP a través de una suma de funciones gausianas, aplicando PNL, pero no se explica en qué basamento fisiológico se apoya el modelo, además de la pobre bondad de ajuste que se obtiene para aproximar los coeficientes del modelo a clases de OVP sin puntos de inflexión en su descenso.17
Aportes al modelo conceptual actual sobre el origen del contorno de la OVP
El nuevo modelo conceptual sobre el origen y formación del contorno de la OVP que se propone, parte del concepto anterior. Las ondas Fw y Rw son de por sí fuerzas hemodinámicas, medidas y relacionadas por la presión, el flujo y el volumen sanguíneo arteriales donde, de este último, se origina el contorno de la OVP. Pero la relación fisiológica entre el estímulo (acción) de estas fuerzas hemodinámicas y la respuesta (reacción) que ofrece la pared arterial, regulada por múltiples factores, donde uno de los más importantes es el endotelio vascular, no ha sido aclarada.
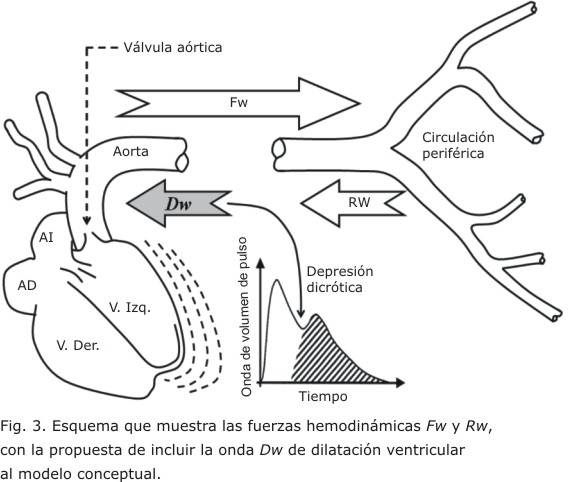
Por otro lado, en el concepto actual del origen del contorno de la OVP no se hace mención de la posible y evidente influencia del proceso de dilatación del ventrículo izquierdo en la circulación mayor (en cooperación con la arteria aorta y el cierre de la válvula aórtica), que origina así una tercera fuerza hemodinámica, en retroceso, que se denominó onda de dilatación ventricular Dw (fig. 3).
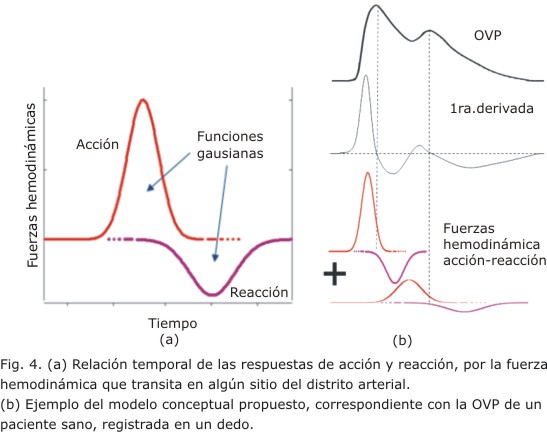
De esta forma se incorpora también esta fuerza Dw al nuevo modelo conceptual. Consecuentemente, se define el contorno de la OVP, según el sitio donde se registre, como: el resultado de la suma de pares de gradientes de fuerzas hemodinámicas de acción y reacción, donde las primeras son provenientes del corazón y la aorta (Fw, Dw) y el distrito arterial periférico (Rw) y las segundas son provenientes de la pared arterial músculo-elástica bajo estudio regulada por múltiples factores incluyendo el control, en algún grado, del endotelio vascular (fig. 4 (a y b)).
En un estado fisiológico saludable de la pared arterial, el endotelio vascular participa en el control de la interacción de cada par de gradientes de fuerzas hemodinámicas de acción y reacción. En este caso, las fuerzas de acción de las ondas Fw, Dw y Rw permiten estimular el endotelio vascular para vasodilatar y extender longitudinalmente la pared de la arteria, mientras que sus fuerzas de reacción son, entonces, las provocadas por el estímulo de esta monocapa para contraer y recuperar longitudinalmente la pared arterial. Otros factores de la pared arterial influyen en estas fuerzas de reacción, como el músculo liso, el colágeno y la adventicia.
La manera temporal y espacial en que interactúen estas fuerzas tiene importantes y vitales funciones para la vida humana, por ejemplo, permiten la propagación adecuada de la onda de presión por cada latido cardiaco, desde la aorta hasta todos los capilares, lo que favorece el intercambio metabólico entre la sangre y todos los tejidos.
Modelo matemático PNL para el contorno de la OVP
Basado en el modelo conceptual planteado, sobre el origen del contorno de OVP, donde las fuerzas hemodinámicas de acción y reacción son derivaciones de la primera derivada de la OVP, al ser estas como gradientes que actúan en la propagación de la onda de presión y en el metabolismo a nivel arterial, se propone el siguiente modelo matemático de optimización, como un problema de programación no lineal, para hallar las 6*p incógnitas que describen las funciones gausianas de estas fuerzas (1).
Minimizar:
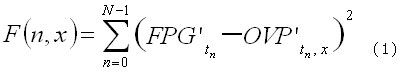
Donde:
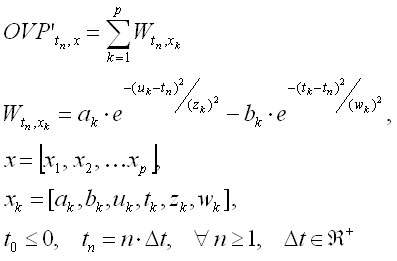
Sujeto a las restricciones siguientes:
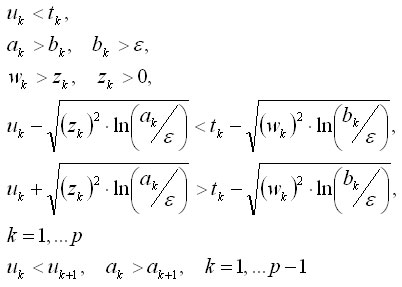
El vector x está constituido por una serie de vectores más pequeños xp, donde cada uno de estos describe la función de interacción W, entre funciones gausianas, de cada par de gradientes de fuerzas hemodinámicas de acción y reacción. La suma de todas estas fuerzas expresa la primera derivada de la función OVP (como OVP'). En cada función W, las variables (a, u, z) describen la magnitud, localización y duración temporal de la fuerza de acción respectivamente. Lo mismo ocurre para la fuerza opositora de reacción, a través de las variables (b, t, w). Las restricciones expresadas, que relacionan a estas variables, permiten obligar a que siempre la fuerza de acción ocurra antes de iniciarse la fuerza de reacción. La constante epsilon (e) permite controlar hasta qué magnitud ínfima será sensible la relación temporal descrita anteriormente.
Instrumentación
Para registrar la OVP de un paciente se utilizó la técnica de FPG, a través del pletismógrafo digital ANGIODIN®18, el cual captura las variaciones de volumen por el método de reflexión, con un fotodiodo a 850 nm y 3,5 mA. La señal FPG es pasada luego a un filtro analógico pasabanda, de 0,1 Hz a 15 Hz (filtro Butterworth 5to. orden) y fue digitalizada a una resolución de 8 bits y a 106 muestras por segundo. Los datos registrados se transmitieron, procesaron y archivaron en una PC, mediante su software auxiliar VAPLET®.19 El software permite exportar las OVP, marcadas latido a latido, para luego ser separadas y procesadas individualmente por otro sistema. Para hallar el índice de masa corporal (IMC) y otros parámetros antropométricos se utilizaron un tallímetro, una pesa y una cinta métrica.
Clasificación de las ondas de volumen de pulso según su contorno
Para clasificar el contorno de la OVP, el estudio se basó en el trabajo de Dawber20 y otros; las OVP, por su contorno, se agrupan en 4 clases en dependencia de lo que ocurra en el descenso de la OVP o período diastólico. Para realizar de forma automatizada esta clasificación, se diseñó e implementó un algoritmo sobre plataforma Matlab®,21 el cual detecta 4 puntos de interés, en forma secuencial y alternada, a partir de la 1ra. y la 2da. derivadas.
Pacientes y protocolo
El criterio de selección de un pequeño grupo de pacientes, perseguía una distribución equitativa de edades y de sexo, además de que estos incluyeran alguna combinación de factores de riesgo cardiovascular, de forma tal que se pudieran obtener ejemplos de contornos de OVP, agrupados por las 4 clases de contornos de OVP descritas. Los pacientes fueron preparados para ir al laboratorio en ayunas y sin ingerir medicamentos ni bebidas que alterasen el sistema nervioso o circulatorio.15 En posición decúbito supino y después de 10 minutos de adaptación al clima del laboratorio, se les registró hasta 2½ minutos de OVP en el pulpejo del dedo pulgar del miembro inferior derecho, para lo cual fue colocado adecuadamente el transductor de FPG, con el propósito de evitar su caída y la presión inducida en la superficie cutánea.1 Los registros de OVP, junto a otras mediciones, fueron obtenidos 1 o más veces, separados cada uno en visitas cada 7 días. La temperatura del local tuvo un valor promedio de 23±1 oC.
Algoritmo para resolver las incógnitas del modelo matemático
En base al protocolo diseñado, donde se registra la OVP en el dedo pulgar de los miembros inferiores, se estimó a p = 2, teniendo así un problema de programación no lineal de 12 incógnitas. Se desarrolló un algoritmo para separar y procesar las muestras registradas de la OVP, y hallar las incógnitas del modelo propuesto; se aplicó una programación cuadrática secuencial, a media escala, con búsqueda lineal y mediante el método Quasi-Newton.21 Por cada registro de OVP tomado de un paciente se separa cada OVP, desde su inicio de ascenso hasta el fin de diástole o descenso, se realiza un filtrado paso-bajo a la OVP' (OVPf'), se hallan los 4 extremos locales en OVPf', en dos máximos y dos mínimos. Luego, se conforma a xo como solución inicial factible y por último, se realiza el proceso interactivo de minimizar a F(n,x) (1).
Análisis estadístico sobre la bondad de ajuste del modelo de regresión
Para analizar la calidad de ajuste del modelo de regresión, ante cualquier clase de contorno de OVP, se procedió a utilizar el residual cuadrático ajustado (RCA). Este estadístico es generalmente el mejor indicador de la calidad de ajuste cuando se adicionen coeficientes, como puede suceder en el modelo propuesto.22 La expresión del RCA es:
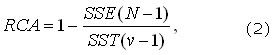
donde SSE es la suma de cuadrados por error y SST es la suma de cuadrados alrededor de la media estadística. N es el tamaño de la muestra de cada OVP extraída (1) y v= N6*p, ajustándose así estos estadísticos al tamaño de la muestra y el número de incógnitas de los vectores x1, x2,… xp. Los valores de RCA están entre 0 y 1. Un valor cada vez más cercano a 1 indica un mejor ajuste.
RESULTADOS
Pacientes analizados y clasificación de las OVP
Se analizaron OVP provenientes de 14 pacientes (7 hombres), con edad promedio de 35 ± 16 años (tabla). El grupo de pacientes presentó un balance adecuado de factores de riesgo cardiovascular. Se registraron y separaron individualmente 4 556 OVP. De estas, 153 no cumplen ninguno de los criterios de las clases definidas por Dawber20 y otros debido a que, en el momento de los registros, se observaron pequeños movimientos del pie con respecto al transductor de FPG, o saturación de la señal FPG debido a ritmos respiratorios acentuados, por parte de algunos pacientes. Por lo tanto, se analizaron los resultados de las 4 403 OVP restantes. La clase III fue la predominante en el grupo estudiado, con 3 453 casos (78,4 % del total). Le siguieron en orden las clases I (470), IV (322) y II (158).
Validación del modelo matemático
Al 100 % de las OVP clasificadas se les obtuvo sus respectivos coeficientes del modelo matemático, con una bondad de ajuste superior al 70 %; cerca del 64 % de las OVP fueron ajustadas con bondad de ajuste ³ 95 % y cerca del 91 % con ajuste ³ 85 %.
En la figura 5 se grafican estos resultados, pero desglosando los por cientos de OVP por sus clases. Los mejores ajustes por el modelo matemático y el algoritmo PNL fueron sobre las OVP de la clase IV, le siguieron las clases III, II y I; esto se explica porque la clase I presenta una mayor variación morfológica en el recorrido del contorno, que las restantes clases.
El modelo y el algoritmo PNL propuestos para caracterizar el contorno de las OVP de clases III y IV (fig. 6), ofrecen elementos lo suficientemente sólidos como para compararlos con los resultados obtenidos en otros trabajos.2,5-7,17
DISCUSIÓN
En el 36 % de las OVP, que alcanzaron una bondad de ajuste menor al 95 %, se observó la presencia de 1 a 3 ondas oscilantes con frecuencia de 2 a 20 Hz. Se sugiere que estas ondas provienen del músculo liso de la pared arterial, debido a tensiones oscilantes bajo condiciones fisiológicas o patofisiológicas, y también como situaciones ocupacionales o ambientales,23 esto se observó en 5 pacientes (4 mujeres y 1 hombre), Como consecuencia, los vectores de los residuales estadísticos de este grupo de OVP, R= FPG'OVP', describen estas ondas oscilantes pronunciadas, haciendo que el criterio RCA disminuya, Se indica que aquellas vibraciones con mayor frecuencia y energía perturban los resultados del algoritmo PNL, al encontrar este mínimos locales y no globales, lo que provoca los peores ajustes. En este caso, 3 mujeres y 1 hombre tuvieron OVP de clase I y II, el 9 % de las OVP con bondad de ajuste menor a 85 %.
Los resultados obtenidos a partir del modelo matemático propuesto, basado en el modelo conceptual, presentan ciertas ventajas. Cada contorno de OVP, tomado en zonas de microcirculación (dedos del pie o las manos), puede ser codificado por 12 variables. Se estima la presencia o la supuesta ausencia del punto de interés, relativo al momento de la onda dícrota, para cualquier clase de OVP, en la intersección a 0 resultante del segundo par de gradientes de acción y reacción, que representan a la onda Dw, Este punto es necesario para calcular índices numéricos tales como IRA e IR y no se requiere la obtención y procesamiento de la segunda o tercera derivada de la OVP.
La clase III fue la predominante en el grupo estudiado, siendo frecuentes las clases I y II en pacientes con menos riesgo cardiovascular y la clase IV en los de mayor riesgo, El 64 % de las OVP obtuvo una bondad de ajuste de calidad (95 %) y el 36 % restante tuvo presencia de ondas oscilantes, provenientes del músculo liso, las cuales no se consideraron en el modelo conceptual y matemático propuesto.
CONCLUSIONES
Es aceptable la coincidencia de ambos modelos para caracterizar morfológicamente el contorno de cualquier clase de OVP. Se sugiere que la formulación subsiguiente de un mejor modelo que separe las ondas oscilantes, haría que los resultados se acerquen más al fundamento del planteamiento y el objetivo anunciados. Los modelos propuestos presentan ventajas de procesamiento que bien pudieran ser comparadas con los publicados recientemente.2-7,17
Agradecimientos
A la técnica en Informática Yaima Hernández Alvarado, del Centro de Biofísica Médica, y a las enfermeras del Consultorio Médico de la Universidad de Oriente, Santiago de Cuba, por el apoyo para realizar la colección de la señal FPG, variables de examen físico y datos primarios.
REFERENCIAS BIBLIOGRÁFICAS
1. Allen J. Photoplethysmography and its application in clinical physiological measurement. Physiol Meas. 2007;28:R1-39.
2. Gunarathne A, Patel JV, Hughes EA, Lip GY. Measurement of stiffness index by digital volume pulse analysis technique: clinical utility in cardiovascular disease risk stratification. Am J Hypertens. 2008;21(8):866-72.
3. Gunarathne A, Patel JV, Gammon B, Hughes EA, Lip GY. Impact of mean arterial blood pressure on higher arterial stiffness indices in South Asians compared to white Europeans. J Hypertens. 2008;26(7):1420-6.
4. Wykretowicz A, Trojnarska O, Guzik P, Katarzyska A. Arterial stiffness in adult patients with cyanotic congenital heart disease. Congenit Heart Dis. 2007;2(2):134-8.
5. Chen JY, Tsai WC, Lin CC, Huang YY, Hsu CH, Liu PY, et al. Stiffness index derived from digital volume pulse as a marker of target organ damage in untreated hypertension. Blood Press. 2005;14(4):233-7.
6. Millasseau SC, Kelly RP, Ritter JM, Chowienczyk PJ. Determination of age-related increases in large artery stiffness by digital pulse contour analysis. Clinical Science. 2002;103:371-7.
7. Millasseau SC, Ritter JM, Takazawa K, Chowienczyk PJ. Contour analysis of the photoplethysmographic pulse measured at the finger. Journal of Hypertension. 2006;24:1449-6.
8. Loukogeorgakis S, Dawson R, Phillips N, Martyn CN, Greenwald SE. Validation of a device to measure arterial pulse wave velocity by a photoplethysmographic method. Physiol Meas. 2002;23:581-96.
9. Fernández-Britto JE. La lesión aterosclerótica: estado del arte a las puertas del siglo XXI. Rev Cubana Invest Bioméd. 1998;17(2):112-27.
10. Fernández-Britto JE, Castillo Herrera JA, Taquechel N, Barriuso A, Vilaú F. Aterosclerosis, colesterol y pared arterial: algunas reflexiones. Rev Cubana Invest Bioméd. 1999;18(3):169-75.
11. Fernández-Britto JE, Barriuso A, Chiang MT, Pereira A, Xavier HT, Castillo Herrera JA, et al. La señal aterogénica temprana: estudio multinacional de 4 934 niños y jóvenes y 1 278 autopsias. Rev Cubana Invest Bioméd. 2005;24(3).
12. Quarteroni A, Tuveri M, Veneziani A. Computacional vascular fluid dynamics: problems, models and methods. Comput Visual Sci. 2000;2:163-97.
13. Fernández-Britto JE. La lesión aterosclerótica y la tríada de Virchow en el siglo XXI. VI Congreso virtual hispanoamericano de anatomía patológica. 2004. Disponible en: http://conganat.uninet.edu/6CVHAP/conferencias/conf_britto.html [visitado Octubre 2009].
14. Li J K-J. Physiology and structural of arteries. In: Li J K-J. Arterial circulation: physical principles and clinical applications. Totowa, NJ: Humana Press Inc.; 2000.p. 13-32.
15. Simón A, Castro A, Kaski JC. Avances en el conocimiento de la disfunción endotelial y su aplicación en la práctica clínica. Rev Cubana Med. 2001;40(3):212-22.
16. Li J K-J. Arterial pulse transmission characteristics. In: Li J K-J. Arterial circulation: physical principles and clinical applications. Totowa, NJ: Humana Press Inc.; 2000. 69-128.
17. Rubins U. Finger and ear photoplethysmogram waveform analysis by fitting with Gaussians. Med Biol Eng Comput. 2008;46(12):1271-6.
18. Cuadra M, Corzo A, Pascau A, Ferrer O, García JC, Hernández D, et al. ANGIODIN® PD 3000, sistema microcontrolado para el diagnóstico de afecciones vasculares. Primer Congreso Latinoamericano de Ingeniería Biomédica. Mazatlán, México: 1998.
19. Pascau A, Ferrer O. Generador de reportes de pruebas hemodinámicas para el diagnóstico de enfermedades vasculares periféricas. Rev Cubana de Inform Méd. 2006;6(1). Disponible en: http://www.cecam.sld.cu/pages/rcim/revista_10 /articulos_htm/generador.htm
20. Dawber TR, Thomas HE Jr., McNamara PM. Characteristics of the dicrotic notch of the arterial pulse wave in coronary heart disease. Angiology. 1973;24:244-55.
21. ___. MATLAB. The language of technical computing. Version 6,5. MathWorks. Inc. 1984-2002.
22. Kutner MH, Nachtsheim CJ, Neter J, Li W. Applied linear statistical models. McGraw-Hill: International Edition; 2005. 6th ed. ISBN 007-112221-4.
23. Ljung B, Sivertsson R. Vibration-Induced Inhibition of Vascular Smooth Muscle Contraction. Blood Vessels. 1975;12:38-52.
Recibido: 8 de abril de 2011.
Aprobado: 22 de abril de 2011.
Ms. C. Alexander Pascau Simón. Departamento de Bioinformática, Centro de Biofísica Médica, Universidad de Oriente. Santiago de Cuba, Cuba. Correo electrónico: alexander.pascau@cbiomed.cu ; pascau_cu@yahoo.es