Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Investigaciones Biomédicas
versión impresa ISSN 0864-0300versión On-line ISSN 1561-3011
Rev Cubana Invest Bioméd vol.37 no.1 Ciudad de la Habana ene.-mar. 2018
ARTÍCULO ORIGINAL
Estudio de estabilidad acelerado del diagnosticador HemoCen Aerobio
Accelerated stability study of the HemoCen Aerobic diagnostician
Ana Iris Brito González, Claudio Rodríguez Martínez, Raisa Zhurbenko, Adelaida Ortega Surís
Centro Nacional de Biopreparados (BioCen). Bejucal, Mayabeque, Cuba.
RESUMEN
Introducción: la bacteriemia es una complicación grave de las infecciones bacterianas. Un diagnóstico temprano del microorganismo responsable permite aplicar tratamientos efectivos en menor intervalo de tiempo. Los hemocultivos son diagnosticadores clínicos diseñado para este fin.
Objetivo: realizar un estudio de estabilidad acelerado de un lote del hemocultivo HemoCen Aerobio que permita planificar su diseño en estante en condiciones reales.
Métodos: se formuló un lote del hemocultivo HemoCen Aerobio en el Centro Nacional de Biopreparados y se envasó asépticamente en los Laboratorios Biológicos Farmacéuticos. Se llevó a cabo un estudio de estabilidad acelerado por el Método de Arrenhius. Los frascos se conservaron durante 120 días a 15 °C, 30 °C y 50 °C. Se realizaron evaluaciones físico-químicas, organolépticas y capacidad de promoción de crecimiento de Staphylococcus aureus ATCC 25923 a los 7, 15, 30, 60 y 120 días.
Resultados: el estudio de estabilidad demostró que el pH y el color del medio se deterioran progresivamente en el tiempo cuando las temperaturas aumentan entre 30 °C y 50 °C. La promoción de crecimiento de Staphylococcus aureus resultó favorable con índices de recuperación entre 20 y 40 UFC·frasco-1.
Conclusiones: HemoCen Aerobio resulta funcional con un desempeño analítico satisfactorio, cuyos índices de recuperación microbiana se encuentran acorde a los valores reportados en bacteriemias de escasa magnitud. Estos resultados sientan las bases para planificar un estudio de estabilidad en estante en condiciones reales. Se estima un período de validez de 2 años.
Palabras clave: hemocultivo HemoCen Aerobio; estudio de estabilidad; promoción de crecimiento; temperature.
ABSTRACT
Introduction: bacteremia is a serious complication of bacterial infections. Early diagnosis of the causative organism allows applying appropriate treatments in a shorter time interval. Hemocultures are clinical diagnosticians designed for this purpose.
Objective: perform an accelerated stability study of a batch of HemoCen Aerobic hemoculture that allows planning its shelf designed in true conditions.
Methods: a batch of HemoCen Aerobic hemoculture was formulated at the National Bioproducts Center, BioCen, and aseptically packaged at the Biological Pharmaceutical Laboratories, LABIOFAM. An accelerated stability study was carried out by the Arrenhius Method. The bottles were stored for 120 days at 15 °C, 30 °C and 50 °C. Physicochemical, organoleptic and growth promotion capacity evaluations of Staphylococcus aureus ATCC 25923 were realized at 7, 15, 30, 60 and 120 days.
Results: the stability study demonstrated that the pH and the color of the medium progressively deteriorate over time as temperatures increase between 30 °C and 50 °C. Growth promotion of Staphylococcus aureus was favorable with recovery rates between 20 and 40 CFU bottle-1 .
Conclusion: HemoCen Aerobic is functional with a satisfactory analytical performance, which recovery rates are consistent with the values reported in bacteremia of low magnitude. These results provide the basis for planning a shelf stability study under real conditions. A durability period of 2 years was estimated.
Keywords: HemoCen Aerobic hemoculture; analytical performance; stability study; growth promotion, temperature.
INTRODUCCIÓN
La bacteriemia es una complicación grave de las infecciones bacterianas. Está muy asociada al uso de catéter1 y constituye uno de los factores que inciden en el aumento de las infecciones nosocomiales en la actualidad.2-5 Su detección es una de las prioridades del laboratorio de microbiología ya que se asocia con una elevada mortalidad que oscila entre el 20 y el 50 %.6-7
Los hemocultivos se consideran "el gold standard" o el método diagnóstico de elección, ante la sospecha de bacteriemia. 8-9 Estos juegan un papel importante en la recuperación y aislamiento de los microorganismos responsables de sepsis, pues establecen el diagnóstico de la bacteriemia y con él se permite conocer la sensibilidad del microorganismo a los antimicrobianos.
En el Centro Nacional de Biopreparados (BioCen) se diseñó y desarrolló, por primera vez en el país, la línea de medios para hemocultivos HemoCen Aerobio, para el diagnóstico de microorganismos aerobios en sangre. Para establecer su período de vida útil, es necesario llevar a cabo un estudio de estabilidad acelerado, que permita con posterioridad el diseño del mismo en tiempo real, con el cual se garantice la calidad del medio listo para el uso una vez introducido en la industria. Los resultados que deriven de este trabajo, pueden ser empleados para determinar la consistencia en el desempeño del diagnosticador, la cual se considera como la capacidad de proveer resultados confiables, bajo condiciones de funcionamiento o conservación diferentes, pero dentro del rango de parámetros recomendados. Además, comprobar la rudeza para mediciones cualitativas, quien refleja la capacidad del diagnosticador de proveer resultados confiables bajo condiciones extremas de funcionamientos, como son las temperaturas de almacenamiento no recomendadas. Este ensayo preliminar de evaluación del desempeño en condiciones diferentes de conservación, permite también predecir las posibles condiciones de almacenamiento y de funcionamiento del diagnosticador, previo al estudio de estabilidad en condiciones reales de almacenamiento. Para ello el objetivo de este trabajo es realizar un estudio de estabilidad acelerado de un lote del hemocultivo HemoCen Aerobio que permita planificar su diseño en estante en condiciones reales.
MÉTODOS
Se utilizó el medio para hemocultivo HemoCen Aerobio (BioCen, Cuba), formulado en el Departamento de Investigaciones de Medios de Cultivo de BioCen. Al medio formulado se le ajustó el pH a 7,3 ± 0,2 con una solución de hidróxido de sodio (Applichem, Alemania) al 40 % (p/v) en un pH metro (pH/ION METER PHM 240, Radiometer, Dinamarca). El proceso se continuó en una planta productiva de los Laboratorios Biológicos Farmacéuticos (LABIOFAM), con estricto cumplimiento de las Buenas Prácticas de Producción de diagnosticadores.10
La filtración esterilizante se ejecutó al botellón de cristal estéril de 10 L con una bomba peristáltica (JenCons, Inglaterra) conectada a un filtro de cartucho de 0,1 micras (Sartorius Sartoclean, Alemania). El llenado (80 mL) se realizó en una cabina de flujo laminar (ICEM, Cuba) a los frascos de vidrio transparente e incoloro de borosilicato clase I (Poly Labo, Alemania) con el volumen nominal de 118 ± 2 mL, retapados con tapones de clorobutilo de color gris de 20 mm, recubiertos con sello de aluminio y en su parte superior, cierre plástico de polipropileno Flip Off de color verde.
Como material biológico se empleó la cepa de la American Type Culture Collection (ATCC) Staphylococcus aureus 25923, microorganismo nutricionalmente exigente y uno de los aislados con mayor frecuencia en hemocultivos.11
Los frascos envasados, listos para el uso, se sometieron a un estudio de estabilidad acelerado, el cual se llevó a cabo por el Método de Arrenhius.12
Se evaluó un total de 30 muestras, a la temperatura de incubación de 15 °C, 30 °C y 50 °C. Los ensayos se realizaron con una frecuencia de 7, 15, 30, 60 y 120 días. El criterio de aceptación para el valor de pH fue 7,3 ± 10 % de deterioro admitido.13
En todas las etapas del estudio de estabilidad se determinaron los siguientes indicadores de la calidad: organolépticos (color y apariencia) por evaluación visual, pH empleándose el método potenciométrico con la utilización de un pHmetro pH/ION METER PHM 240 (Radiometer, Dinamarca) y el desempeño analítico del diagnosticador frente a S. aureus ATCC 25923.
Se observaron la transparencia y el color del medio HemoCen Aerobio. A la transparencia y al color se les asignó la puntuación siguiente: transparencia: desde 0 hasta 2 (0- turbio, no transparente; 1- ligeramente opalescente, no turbio; 2- transparente, brillante) y color: desde 0 hasta 3 (0- color muy oscuro, no permite visualizar el crecimiento; 1- color oscuro, permite visualizar el crecimiento; 2- color ligeramente más oscuro, permite visualizar el crecimiento; 3- color original). Para el desempeño analítico se estandarizó un cultivo fresco de S. aureus ATCC 25923 al 56 % de transmitancia (espectrofotómetro T70 UV/VIS Spectrometer, PG Instruments Ltd., United Kingdom), correspondiente a 2,5 x 108 UFC·mL -1. De seguida se realizaron diluciones decimales en solución salina estéril al 0,85 % (p/v), utilizándose cloruro de sodio (Applichem, Alemania). A partir de la dilución correspondiente a 2,5 x 102 UFC·mL -1 se tomaron 1,6 mL de la suspensión y se adicionaron a un matraz de Erlermeyer con 38,4 mL de solución salina estéril para obtener 40 mL de una suspensión con concentración aproximadamente de 10 UFC·mL-1. De esta última se inocularon 10 mL por cada frasco de HemoCen Aerobio conservado a las tres temperaturas del estudio, para garantizar la recuperación microbiana de inóculo por frasco de 10 a 100 UFC, el cual se establece en las directrices para el aseguramiento de la calidad de los medios de cultivo microbiológicos destinados a la clínica.14 En paralelo, 0,2 mL de la suspensión se inocularon en el Agar Triptona Soya (ATS) (BioCen, Cuba) para confirmar su pureza y determinar el valor real del inóculo (UFC·frasco-1) empleado en cada evaluación. Los frascos de HemoCen Aerobio inoculados se incubaron a 35 ± 2 °C hasta 15 días o hasta la aparición de la turbiedad y las placas de ATS se ubicaron a 35 ± 2 °C por 24 h en una incubadora Heraeus (Alemania).Todos los ensayos se realizaron por triplicado.
Los valores de puntuación obtenidos para el color y la transparencia del hemocultivo HemoCen Aerobio, conjuntamente con los valores de pH, se introdujeron en el programa estadístico de estabilidad acelerada 15 y se procesaron estadísticamente los resultados para estimar la durabilidad del medio HemoCen Aerobio.
RESULTADOS
Los frascos de HemoCen Aerobio conservados a las tres temperaturas de incubación, permanecieron transparentes y brillantes durante los 120 días del estudio de estabilidad acelerado.
El color del hemocultivo HemoCen Aerobio no varió en los frascos conservados a 15 °C. Los frascos que permanecieron a 30 °C sólo mostraron un ligero oscurecimiento del color a los 120 días del estudio, mientras que aquellos almacenados a 50 °C comenzaron a oscurecerse a partir de los 7 días del estudio, adquiriendo un color más intenso desde los 15 días de comenzado el mismo.
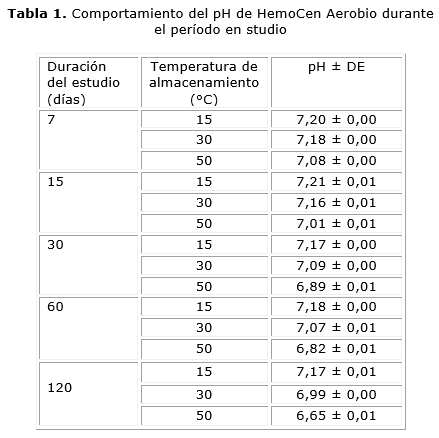
El aumento de la temperatura de almacenamiento condiciona el deterioro del pH. Este efecto es más evidente en el transcurso del tiempo (tabla 1), es por ello que al final del estudio, los frascos almacenados a 50 °C presentaron un valor promedio de pH de 6,65.
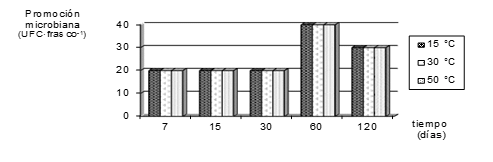
HemoCen Aerobio promovió satisfactoriamente el crecimiento de S. aureus ATCC 25923 en un período de 16 a 20 h de iniciadas las incubaciones, expresado en el desarrollo de la turbiedad en los frascos con los inóculos iniciales entre 30 ± 14 UFC·frasco -1 a lo largo del estudio (Fig.).
Fig. Capacidad de HemoCen Aerobio de promover el crecimiento de Staphylococcus aureus ATCC 25923 durante
el estudio de estabilidad acelerado.
El procesamiento estadístico de los resultados, permitió predecir un período de validez de HemoCen Aerobio de 24 meses (tabla 2).
Tabla 2. Tratamiento estadístico aplicado a los valores obtenidos
| Reacción orden 0 | primer orden | segundo orden | ||
| k0=(Co- Ct)/t | k1=(lnC0-LnCt)/t | k=(1/C-1/C0)/t | ||
| Temperatura (°C) | Temperatura (°K) | menosk0 | menosk1 | menosk2 |
| 15 | 288 | 0,000297506 | 4,14054E-05 | 5,76262E-06 |
| 30 | 303 | 0,001698247 | 0,000239511 | 3,37813E-05 |
| 50 | 323 | 0,004104323 | 0,000595755 | 8,65123E-05 |
| | | | | |
| | | Reacción orden 0 | primer orden | segundo orden |
| Temperatura (°C) | Temperatura (°K) | R2 | R2 | R2 |
| 15 | 288 | 0,611884898 | 0,612146945 | 0,61240845 |
| 30 | 303 | 0,926397419 | 0,928251458 | 3,37813E-05 |
| 50 | 323 | 0,896383808 | 0,90375982 | 8,65123E-05 |
| | | | | |
| | | Reacción orden 0 | primer orden | segundo orden |
| Temperatura (°K) | 1/T °K | Lnk0 | Lnk1 | Lnk2 |
| 288 | 0,003472222 | -8,120075286 | -10,09209829 | -12,06411873 |
| 303 | 0,00330033 | -6,378158878 | -8,336912907 | -10,29560362 |
| 323 | 0,003095975 | -5,49571442 | -7,425681874 | -9,355223626 |
| | | Reacción orden 0 | primer orden | segundo orden |
| | m=-Ea/R | -6892,301275 | -7004,984262 | -7118,812081 |
| | Ln A | 16,00763867 | 14,42472889 | 12,84574891 |
| | A=eLnA | 8954248,467 | 1838993,352 | 379173,4035 |
| | R2 | 0,94503567 | 0,94779648 | 0,950451728 |
| Temperatura (°C) | 1/T | K0 | K1 | K2 |
| 15 | 0,003472222 | 0,000361965 | 5,02684E-05 | 6,98079E-06 |
| 30 | 0,00330033 | 0,001183558 | 0,000167583 | 2,37321E-05 |
| 50 | 0,003095975 | 0,004840412 | 0,000701332 | 0,000101656 |
| | | Vida Media | | |
| Temperatura (°C) | 1/T | t1/2=C0/2k0 | t1/2=0,693/k1 | t1/2=1/C0k2 |
| 15 | 0,003472222 | 9945,712453 | 13785,98607 | 1031402,022 |
| 30 | 0,00330033 | 3041,676349 | 4135,261196 | 303386,0687 |
| 50 | 0,003095975 | 743,3939718 | 988,1194675 | 70794,35207 |
| | | 10 % de pérdida | | |
| Temperatura (°C) | 1/T | t10%=0,1C0/k0 | t10%=0,105/k1 | t10%=0,111/C0k2 |
| 15 | 0,003472222 | 1989,142491 | 2088,785768 | 114485,6244 |
| 30 | 0,00330033 | 608,3352699 | 626,5547266 | 33675,85363 |
| 50 | 0,003095975 | 148,6787944 | 149,7150708 | 7858,17308 |
| Temperatura de predicción del período de validez: 25 °C | Módulo de predicción (días) | |||
| 1/T °k | k0 | k1 | k2 | |
| 0,003355705 | 0,000808048 | 0,000113702 | 1,60006E-05 | |
| | t1/2=C0/2k0 | t1/2=0,693/k1 | t1/2=1/C0k2 | |
| | 4455,180909 | 6094,880462 | 449982,1804 | |
| | t10%=0,1C0/k0 | t10%=0,105/k1 | t10%=0,111/C0k2 | |
| | 891,0361818 | 923,4667366 | 49948,02202 | |
K= A*e-Ea/RT
DISCUSIÓN
Los medios de cultivo líquidos listos para el uso, destinados al diagnóstico de bacteriemias en hemocultivos, presentan la característica de ser transparentes y brillantes, lo cual favorece la interpretación de los resultados cuando el análisis se realiza cualitativamente, a partir de una inspección visual.
HemoCen Aerobio, al final del período estudiado, conserva su propiedad de ser transparente y brillante tal y como fue diseñado, lo cual evidencia que el producto fue desarrollado bajo estricto procesamiento aséptico y con materias primas de óptima calidad, que le garantizan la esterilidad y sus cualidades organolépticas.
El color es otro indicador de la calidad organoléptica, éste se afecta por efecto de las altas temperaturas y se debe a reacciones de pardeamiento que ocurren entre algunos aminoácidos y glúcidos presentes en la formulación.16 Estas reacciones pueden influir sobre la biodisponibilidad de los nutrientes en la composición,17 afectar en cierta medida la recuperación microbiana y con ello la funcionalidad del diagnosticador.
Los medios para hemocultivo aerobio están destinados a la recuperación tanto de bacterias como de levaduras, por lo que su valor de pH debe de estar acorde con las exigencias de tales microorganismos. La mayoría de las bacterias crecen en un rango de pH desde 5,4 hasta 8,5; incluidas en este grupo las que causan enfermedades en el hombre. 18 Este intervalo de pH se encuentra dentro del rango de pH óptimo de las levaduras que generalmente se desarrollan entre una ligera acidez y un pH neutron.19
Algunos autores refieren valores de pH de los hemocultivos, entre 7,0 y 7,6 (Oxoid Signal®, Inglaterra; Conda (España). Sin embargo, la literatura científica no hace énfasis en el pH como indicador de calidad de los diagnosticadores y sí se centra en las diferencias de composición, métodos de detección y grado de automatización.20
Las variaciones de pH que presenta HemoCen Aerobio durante el período evaluado, se deben a componentes de naturaleza reductora tales como L-cisteína y glúcidos presentes en la formulación, que interactúan en presencia del oxígeno libre de la atmósfera del frasco, originando la formación de nuevos compuestos y como consecuencia la disminución del pH.21 El aumento de las temperaturas acelera estos procesos.22 Esta es la causa por la que al final del estudio, el pH desciende sin afectar el índice de deterioro admitido para un diagnosticador al final de la durabilidad (hasta 6,57), según se establece en las regulaciones aprobadas por el CECMED para el estudio de estabilidad de productos farmacéuticos.13
HemoCen Aerobio es una excelente combinación de ingredientes que en su conjunto le aportan la calidad nutricional y las condiciones necesarias a la formulación para promover el metabolismo y el desarrollo de microorganismos aerobios exigentes que puedan estar presentes en muestras de sangre.23 Su composición, es una mezcla de bases nutritivas ricas en aminoácidos, péptidos de distintos pesos moleculares, vitaminas y minerales. El hidrolizado enzimático de caseína (HEC) es el componente mayoritario de HemoCen, con un aporte considerable de nitrógenos totales, aminoácidos libres y minerales entre los que se destacan, glutamina, arginina, leucina, asparagina, prolina, calcio y magnesio.24-25
La peptona de soya le aporta al medio, proteínas de alta calidad, un elevado contenido de vitaminas, carbohidratos y energía. Constituye además, una fuente importante de los aminoácidos lisina, arginina, leucina, isoleucina, prolina, serina, treonina, ácido aspártico y ácido glutámico, según plantean otros autores.26
La combinación de peptonas bacteriológicas P y Z, amplía el espectro de sustancias nutritivas de origen animal de naturaleza proteica, elevando el porcentaje de nitrógenos totales y amínicos, como elementos indispensables para el metabolismo celular, incrementa los niveles de macroelementos, microelementos y de sales.27
Los extractos de levadura y vegetal, elevan el valor nutricional de la formulación con la incorporación de carbohidratos fermentables como la glucosa, fructuosa, maltosa, sacarosa, maltotriosa y dextrinas, quienes pueden ser empleados como fuentes de energía en el metabolismo celular microbiano; estos además le aportan vitaminas y minerales, entre los que se destacan: potasio, fósforo, calcio y también aumentan los niveles de aminoácidos tales como cistina, cisteína y triptófano, importante para el metabolismo de ciertas especies de microorganismos.28
La L-cisteína es incorporada en la formulación de HemoCen, en calidad de agente reductor, ayudando a bajar el potencial redox del medio. Los factores de crecimiento Hemina y Menadiona, potencian la capacidad de promover el crecimiento de bacterias con requerimientos nutricionales especiales tales como Bacteroides malaninogenicus.29
En el estudio de estabilidad acelerado, HemoCen Aerobio demostró un desempeño analítico satisfactorio, debido a su capacidad de promover el crecimiento de S. aureus a concentraciones de inóculos inferiores a 100 UFC·frasco-1. Este resultado se manifiesta a lo largo del período evaluado, incluso al cabo de los 120 días del estudio, donde ya los valores de pH se encuentran al límite del valor mínimo permitido a consecuencia del deterioro que éste experimenta en el tiempo.
No existen diferencias en cuanto a la recuperación microbiana de los frascos provenientes de las distintas temperaturas de incubación a partir de una misma estandarización. Este comportamiento es similar para cada día del estudio.
La capacidad de HemoCen de recuperar la cepa de S. aureus en cada período ensayado y aún, al final del estudio donde ya las condiciones de pH se encuentran un tanto desfavorables, confirma que la composición nutricional del diagnosticador responde a las exigencias nutricionales de bacterias de gran interés en hemocultivo. Este resultado se corrobora con lo planteado anteriormente por otros autores en el 8th Congreso de Microbiología y Parasitología, sobre validación del desempeño clínico de HemoCen Aerobio donde además refiere la respuesta del diagnosticador frente a un grupo más amplio de microorganismos, aislados de pacientes con bacteriemias, entre los que se destacan Escherichia coli, Acinetobacter spp., Klebsiella pneumoniae, Serratia marcences, Acinetobacter calcoacetium-anitratum y levaduras.30
En cuanto a la consistencia en el desempeño del diagnosticador, en condiciones de conservación recomendadas a 15 °C se puede decir, que se mantienen el valor de pH y las características organolépticas, dentro de los criterios de aceptación pre-establecidos, durante los 120 días en que se llevó a cabo el estudio. La promoción de crecimiento del microorganismo objeto, se observó a partir de niveles muy bajos de concentración, desde las 16 h de incubación.
En los frascos conservados a temperatura de 30 °C y de 50 °C en condiciones de rudeza, o sea, fuera de los límites en las condiciones normales de funcionamiento, se observó un deterioro del pH y del atributo color a los 120 días de almacenamiento. Sin embargo, la detección del crecimiento (funcionalidad o desempeño diagnóstico), no se vio afectada por un aumento de la temperatura de conservación fuera de lo pre-establecido, lo que permite afirmar que incursiones cortas en condiciones no recomendadas de almacenamiento, como pueden ser fallos en la cadena de distribución y de almacenamiento, no afectarán la calidad del diagnosticador.
El estudio de estabilidad acelerado evidencia que, condiciones de almacenamiento tales como temperatura y pH, deben ser controladas para garantizar un período de validez estimado de 2 años. Fabricantes de medios para hemocultivos tales como Liofilchem y Britania, establecen tiempo de durabilidad similar al obtenido en este ensayo. Otros, como los Laboratorios Linsan, presentan hemocultivos con un período de validez de sólo 12 meses.
De forma general, HemoCen Aerobio resulta funcional con un desempeño analítico satisfactorio, cuyos índices de recuperación microbiana se encuentran acorde a los valores reportados en bacteriemias de escasa magnitud. Estos resultados sientan las bases para planificar un estudio de estabilidad en estante en condiciones reales.
Declaración de conflicto de intereses
Los autores declaran que no existe conflicto de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Martell Martorell L, Arencibia Núñez A. Infecciones intrahospitalarias en pacientes pediátricos con enfermedades hematológicas, 2006-2009. Rev Cubana Hematol Inmunol Hemoter. 2012;28(3):253-62.
2. Nautiyal A, Madhav NS, Sharma RK, Ojha A, Bhargava S. Review on nosocomial infections. Carib J Sci Tech. 2015;3:781-8.
3. Kumar G, Ahmad S, Taneja A, Patel J, Guddati AK, Nanchal R, et al. Severe sepsis in hematopoietic stem cell transplant recipients. Critical Care Med. 2015;43:41121.
4. Oliveros Navarro A, Uribe N, Sierra P, Jaimes F, González JM. Bacteriemia por enterobacterias resistentes a carbapenems. Estudio transversal. Infectio.2015;19:606.
5. Satlin MJ, Jenkins SG, Walsh TJ. The global challenge of carbapenemresistant Enterobacteriaceae in transplant recipients and patients with hematologic malignancies. Clin Infect Dis.2014;58:127483.
6. Krause I, Ashkenazi S. Gastrointestinal Infections in Pregnancy and Neonates. En: Kurjak A, Chervenak FA. Textbook of Perinatal Medicine. Vol 2. 3a ed. New Delhi: Jaypee Brothers Medical; 2015.
7. Manzur A, Ruiz MS, Fernández J, Bustos A, Amuchastegui R, Fonseca G, et al. Bacteriemia nosocomial en servicios de Cuidados Críticos y en Sala General. Actualizaciones en SIDA e Infectología. Buenos Aires. 2013;21(80):42-7.
8. Cattani ME, Posse T, Hermes RL, Kaufman SC. Rapid identification of microorganisms by mass spectrometry in a blood culture system. Comparison of two procedures. Rev Arg Microbiol. 2015;47:1905.
9. Dreyer AW. Blood Culture Systems: From Patient to Result. En: Azevedo L. Sepsis - An Ongoing and Significant Challenge. South Africa: InTech; 2012.
10. Regulación No. 20-2004. Buenas Prácticas para la producción de Diagnosticadores. CECMED. Cuba; 2004.
11. Kern WV. Usefulness of the CPG in the management of severe S. aureus infections. Enferm Infecc Microbiol Clin. 2015;33(9):577-8.
12. Centre for infections. Standards Laboratory in conjunction with the Regional Food, Waterand Environmental. HPA Standard Method; 2008.
13. Regulación No. 23-2000. Requerimientos de los estudios de estabilidad para el registro de productos farmacéuticos nuevos y conocidos. Cuba; 2000.
14. Guidelines for Assuring Quality of Medical Microbiological Culture Media. 2 ed. Australian Society for Microbiology; 2012.
15. Rodríguez C, Mayo O. Paquete estadístico SmartVal. Versión 1. BioCen; 2011.
16. Lupano CE. Modificaciones de componentes de los alimentos: cambios químicos y bioquímicos por procesamiento y almacenamiento. La Plata: Edulp; 2013.
17. Barreiro JA, Sandoval AJ. Operaciones de conservación de alimentos por bajas temperaturas. Caracas: Equinoccio; 2006.
18. Junco R, Rodríguez CM. Cultivo y crecimiento de los microorganismos. En: Llop A, Valdés-Dapena MM, Zuazo JL, eds. Microbiología y Parasitología Médicas Tomo I. La Habana: Ciencias Médicas; 2001.
19. Macola S. Generalidades de la micología. En: Llop A, Valdés-Dapena MM, Zuazo JL, eds. Microbiología y Parasitología Médicas Tomo I. La Habana: Ciencias Médicas; 2001.
20. Vetter EA, Torgerson CA, Feuker A, Hugnes JG, Harmsen WS, Schleck C, et al. Comparison of the BACTEC MYCO/F Lytic Bottle to the Isolater Tube, BACTEC Plus Aerobic F/Bottle and BACTEC Anaerobic Lytic/10 Bottle and Comparison of the BACTEC Plus Aerobic F/Bottle to the Isolater Tube for Recovery of Bacteria, Mycobacteria and Fungi from Blood. J Clin Microbiol. 2001;39(12):4380-6.
21. Laboratorios MICROKIT, S.L. Estudios sobre la caducidad de los medios de cultivo preparados herméticos. Técnicas de laboratorio. Madrid, España; 2003. p. 686-91. Disponible en: http://dialnet.unirioja.es/servlet.
22. Tortora GJ, Funke BR, Case CL. Metabolismo microbiano. Introducción a la Microbiología 9 ed. Buenos Aires: Médica Panamericana; 2007.
23. Zhurbenko R, Someillan D, Ortega A, López Y, Blanco AM, Torres M, et al. Evaluación comparativa de dos medios para hemocultivos para el aislamiento de microorganismos aerobios. Salud i Ciencia. 2016 [citado 12 Dic 2016]. Disponible en: www.siicsalud.com; doi: http://dx.doi.org/10.21840/siic/153101
24. Fallah M, Bahram S, Javadian SR. Fish peptone development using enzymatic hydrolysis of silver carp by-products as a nitrogen source in media. Food Sci Nut. 2015;3(2):153-7.
25. Meli F, Lazzi C, Neviani E, Gatti M. Effect of protein hydrolysates on growth kinetics and aminopeptidase activities of Lactobacillus. Curr Microbiol. 2014;68(1):82-7.
26. Hongfei Z, Fengling B, Fang Z, Walczak P, Xiangning J, Bolin Z, et al. Characterization of soybean protein hydrolysates able to promote the proliferation of Streptococcus thermophilus ST. J Food Sci. 2013;78(4):575-81.
27. Zhurbenko R, Rodríguez C, Lobaina T, López OD, Viera DR. Peptona papaínica de corazón de vaca como fuente de nutrientes para los microorganismos. Salud i Ciencia. 2015;21(5):531-5.
28. Lobaina T, Rodríguez C, Zhurbenko R. Caracterización de un extracto de Ipomoea batatas para ser utilizado en calidad de base nutritiva en medios de cultivo. Rev Cubana Med Trop. 2007;59(3).
29. Britania HEMORAB. Hemocultivos con Resinas. Laboratorios Britania S.A. Caba: Argentina; 2011. Rev 03-31655.
30. Zhurbenko R, Rodríguez C, Brito AI, Someillan D, Ortega A, López, et al. V alidación del desempeño clínico del medio para hemocultivo de producción nacional HemoCen Aerobio. 8vo Congreso cubano de Microbiología y Parasitología. 5to Congreso Nacional de Medicina Tropical and 5to Symposium Internacional de infecciones HIV/SIDA en Cuba; 2014.
Recibido: 8 de febrero de 2017.
Aprobado: 13 de marzo 2017.
Ana Iris Brito González. Centro Nacional de Biopreparados (BioCen). Bejucal, Mayabeque. Cuba.
Correo electrónico: anairis.brito@biocen.cu