Introducción
Desde 1969, K.W. Heaton,1 señaló la importancia de mantener los ácidos biliares en su lugar, conservando la integridad del sistema anatomo-funcional (hígado, conductos biliares: intrahepáticos/extrahepáticos, vesícula biliar, intestino delgado y circulación enterohepática), a lo cual se le suma en la actualidad la comprensión del control de su actividad biológica por transportadores y receptores nucleares, que mantienen la homeostasis e impiden su acción toxicológica sobre la mucosa intestinal. (2,3 Hecho que se refuerza desde 2008 con la publicación del libro BileAcid: Toxicology and Bioactivity, (4) de Gareth Jenkins y Laura J. Hardie, quienes compilaron los resultados de numerosas investigaciones, que aportan nuevos elementos teóricos y no solo contribuyen a actualizar el marco conceptual del sistema anatomo-funcional, sino también las acciones fisiológicas y los efectos tóxicos de los ácidos biliares en el ser humano.
En este sentido, el articulo tiene como objetivo principal describir la actualidad de los nuevos conocimientos sobre la actividad biológica y toxicológica de los ácidos biliares en el aparato digestivo, dirigido a cirujanos generales, gastroenterólogos, clínicos y fisiólogos que les permitan contextualizar el proceso inflamación-carcinogénesis relacionado con los efectos toxicológicos de los ácidos biliares.
Se realizó una revisión crítica y actual de todas las evidencias reportadas en bases de datos internacionales como PubMed, Medline, Scielo, LiLaC, Elservier, entre otras, que permitieron consultar artículos científicos publicados en revistas de alto impacto, así como bibliografía de primer nivel enviadas por los autores extranjeros entre el 2000 y 2019 y se redactó teniendo en cuenta los criterios más actuales sobre la actividad biológica y toxicológica de los ácidos biliares, que constituye un nuevo paradigma dentro de la fisiología del aparato digestivo.
Desarrollo
En este artículo se brindan las bases teóricas actuales que fundamentan la actividad biológica y toxicológica de los ácidos biliares; así como se ofrece la plataforma conceptual del proceso inflamación-carcinogénesis que se desencadena por el descontrol de la homeostasis de los ácidos biliares, haciendo énfasis en los aspectos relacionados con la biología molecular en la génesis de las lesiones en el aparato digestivo y la importancia de los ácidos biliares en la misma, lo que constituye un nuevo paradigma en la acción fisiológica de los ácidos biliares.
Ácidos biliares
Constituyen una gran familia de esteroides derivados del colesterol. Diariamente, el hígado sintetiza 0,5 g de ácidos biliares. (5 Las dos rutas principales de su síntesis a partir del colesterol se denominan: clásica y alternativa, donde la acción de un complejo enzimático provoca la deshidrogenación y reducción del núcleo del colesterol y origina los ácidos biliares primarios: ácido cólico y quenodeoxicólico. En el citoplasma de los hepatocitos son conjugados con el ácido glucurónico y taurocólico, y pasan a formar parte del contenido de las sales biliares, que son excretados y almacenados en la vesícula biliar formando micelas mixtas, encargadas de transportar fosfolípidos y colesterol del hígado al intestino. (6,7 Posteriormente, como respuesta a estímulos tantos mecánicos, hormonales (colecistoquinina, motilina) y nerviosos, generados por la ingestión de alimentos (grasas), son secretados hacia el duodeno, donde se producen cambios en su composición y ejercen la mayor parte de su actividad biológica. (8
Actividad biológica
Los ácidos biliares son moléculas anfipáticas, actúan como detergentes, actividad biológica descrita desde la antigüedad, la que facilita el transporte y la absorción de las grasas. (9
Estudios in vivo e in vitro desde la década del dos mil, evidencian que su actividad biológica comprende otras funciones: actúan como moléculas de señalización al activar rutas y modificar la transcripción génica celular, (10como sustancias proinflamatorias e inmunorreguladoras controlan y regulan la permeabilidad celular y paracelular, (11la microbiota, (12) la motilidad, la regeneración y la proliferación celular intestinal, modulan la liberación de diferentes enzimas pancreáticas y del catabolismo del colesterol, (13 ejercen una función pleotrópica al regular su propio metabolismo, así como el del colesterol, los lípidos, las lipoproteínas y el metabolismo energético14) y facilitan la absorción de iones de calcio. (15
En este sentido el concepto actual de la actividad biológica de los ácidos biliares se resume en dos de las funciones descritas: moléculas de señalización y modificadoras de la transcripción génica celular, las cuales mantienen la homeostasis del epitelio intestinal, y en condiciones fisiopatológicas se relacionan con el proceso inflamatorio-carcinogénesis del aparato digestivo.
Transportadores
Uno de los aspectos que en la actualidad evidencian el control de la actividad biológica a su llegada a la luz intestinal se basa en el conocimiento de los transportadores que regulan la absorción de los ácidos biliares. (16
En los primeros tramos del intestino delgado los ácidos biliares son absorbidos pasivamente en pequeñas cantidades, mientras que 95 % se absorbe a nivel de la mucosa del íleon terminal a través de transportadores apicales de ácidos biliares dependientes de iones sodio. Una vez dentro del citoplasma del enterocito, estos difunden hacia la membrana basolateral, donde se unen a un heterodímero TSOα/β, el cual los transporta y los expulsa hacia la circulación enterohepática, que los conduce hacia los sinusoides hepáticos y se unen a nivel de la membrana plasmática de los hepatocitos con un transportador de fosfatidilcolina dependiente de iones de sodio que facilita su paso hacia el citoplasma. De este modo los ácidos biliares retornan al hígado y permiten que una misma molécula de ácido biliar sea utilizada repetidamente, con lo que se minimiza el gasto energético que supondría su biosíntesis continua. (16) Así que, unos 3 g de ácidos biliares se reciclan de 4 a 12 veces al día, mientras que la pérdida a través de las heces (0,2-0,5 g/día) se repone por síntesis de novo en el hígado y con eso se mantiene una reserva constante de ácidos biliares en el organismo. (13
No obstante, a pesar de que la reabsorción de ácidos biliares en la mucosa del íleon terminal es eficaz, 5 % pasa al colon, donde son desconjugados y oxidado su grupo hidroxilo por la microbiota intestinal, formando los ácidos biliares secundarios: desoxicólico y litocólico. Por otro lado, la epimerización del ácido quenodesoxicólicoda origen a otro ácido denominado ácido ursodesoxicólico. (13
Es de resaltar que los ácidos biliares secundarios están ausentes en el estómago y en el intestino delgado, excepto cuando por condiciones anómalas, como la existencia de reflujo duodenogástrico e hipoacidez, pasan a la luz gástrica, donde los cambios de pH y el sobrecrecimiento bacteriano los desconjugan, invierten sus propiedades y los convierten en agentes toxicológicos, como ocurre en la gastritis alcalina. (17-19
En fin, el organismo humano a diferencia del resto de los animales cuenta con un sistema anatomo-funcional que controla la homeostasis de los ácidos biliares y su actividad biológica, de modo que los cambios estructurales y funcionales de este sistema contribuyen a la pérdida de este control y facilita su acción toxicológica, como se reporta en estudios realizados en pacientes con litiasis vesicular, colecistectomizados, síndrome de intestino corto, cirugía bariátrica, hepatopatías crónicas o derivaciones hepato-bilio-pancreáticas, síndrome de intestino irritable, entre otras. (20
Receptores
Desde la primera década del siglo xxi, diversos estudios biomoleculares relacionados con la homeostasis de los ácidos biliares han permitido identificar y caracterizar la existencia de cuatro receptores nucleares reconocidos por la comunidad científica, que pueden ser estimulados por los propios ácidos biliares y de esta manera mantener el equilibrio de su síntesis, absorción, detoxificación y secreción basolateral a partir del control del metabolismo del colesterol. (13,16) Estos receptores son identificados por sus siglas RXF(receptor X farnesoide), RXP (receptor X pregnano), RXH (receptor X de hígado) y el RVD (receptor vitamina D), que desempeñan una función reguladora y protectora en el organismo, especialmente en la actividad biológica de los ácidos biliares, por lo que investigaciones actuales reportan nuevas dianas terapéuticas para el control de sus funciones y de esta manera prevenir o amortiguar el proceso toxicológico y carcinogénico de los ácidos biliares en la luz intestinal. (21,22
Propiedades físico-químicas
Las propiedades físico-químicos de los ácidos biliares están dadas por ser conjugados, de pH alcalino, hidrófobos, con un PKa bajo, insolubles, detergentes endógenos fuertes, inductores de la señalización celular y, por tanto, reguladores de la microbiota intestinal, de la proliferación y la apoptosis celular. En condiciones fisiológicas, gracias a estas propiedades los ácidos biliares tienen naturaleza anfipática, por tanto, pueden mantenerse en la luz intestinal, ser solubles en agua y en pH ácidos, ser resistentes a la precipitación por iones de calcio y mezclarse con los alimentos, sin provocar daños epiteliales. (16,23
Una de las propiedades más estudiada de los ácidos biliares es su hidrofobicidad, la que es inversamente proporcional al número de grupos OH; un ejemplo de esto es el ácido litocólico que con un solo grupo OH en su estructura es altamente hidrofóbico y tóxico, mientras que el ácido desoxicólico y el ácido quenodeoxicólico con dos grupos OH y el ácido cólico con tres, son cada vez menos hidrofóbicos y menos tóxicos. Por otro lado, al ser detergentes fuertes, emulsionan las grasas tanto exógenas como endógenas, propiedad que justifica su acción toxicológica, tanto intracelular como extracelular cuando se encuentra en concentraciones altas en la luz intestinal. (4,6
Recientemente estudios realizados en animales reportan el cambio de las propiedades físico-químicas de los ácidos biliares cuando están conjugados con el glicolato y la taurina. La conjugación con el glicolato hace que los ácidos biliares sean insolubles durante el proceso digestivo al mezclarse con los alimentos en el intestino, lo cual hace que sean impermeables a las membranas epiteliales, lo que explica el por qué se mantienen en la luz intestinal sin provocar daños celulares, mientras que cuando están conjugados con la taurina son sulfónicos con propiedades detergentes fuertes, lo cual favorece su acción tóxica a nivel de las membranas celulares del intestino, hecho que en la actualidad se relaciona con el proceso de carcinogénesis intestinal. (24,25
En resumen, la actividad biológica de los ácidos biliares descansa sobre sus propiedades físico-químicas, las cuales garantizan sus funciones en el tracto gastrointestinal que no es otra que formar las micelas y emulsionar las grasas y las vitaminas liposolubles.
Acción toxicológica de los ácidos biliares
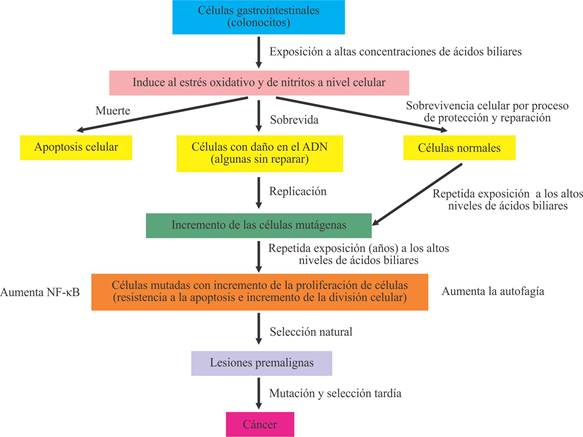
Evidencias actuales refuerzan cada vez más la acción toxicológica de los ácidos biliares. (26) Cuando las condiciones de su actividad biológica no son fisiológicas surge una secuencia de efectos tóxicoscapaces de provocar daño en concentraciones elevadas y mantenidas sobre las membranas plasmáticas y en el ADN celular, que generan estrés oxidativo, desnaturalización y plegamientos erróneos de proteínas, disminución de los niveles de los iones de calcio e hierro a través de su actividad quelante, e incluso la formación de estructuras secundarias en el ARN (Fig. 1). Por tanto, las alteraciones en su síntesis, transformación o transporte se traducen en trastornos metabólicos a nivel celular de la pared intestinal (inflamación, mutaciones, retardo de la apoptosis, lesiones premalignas y cáncer).
Cuando las concentraciones de los ácidos biliares sobrepasan los límites fisiológicos en la luz intestinal y sobresaturan los receptores, una parte queda libre e interactúa con las membranas lipídicas y desencadena una respuesta inflamatoria. (27,28
Desde finales de la década de los años noventa se ha evidenciado la capacidad de los ácidos biliares para activar diferentes rutas de señalización celular en diversos órganos del tracto digestivo (esófago, hígado, colon, entre otros) (29) que se traduce en alteraciones de la membrana plasmática celular, ejecutada a través de la activación de la proteína quinasa C, del receptor del factor de crecimiento epidérmico y de la β-catenina, lo que explica como los ácidos biliares penetran en la célula e interactúan con los organelos intracelulares (mitocondria y núcleo)y estimulan la producción de radicales libres de oxígeno y nitrógeno, que a su vez, por diversas vías, activan la apoptosis celular. (4,30-32
Los mecanismos de hiperproducción de radicales libres de oxígeno y nitrógeno por las células intestinales como respuesta a la exposición de los ácidos biliares elevados están relacionados con los cambios estructurales de la membrana plasmática, con su hidrofobicidad y su efecto detergente y al mismo tiempo con la activación de diferentes enzimas y receptores como: (4
Receptores del factor de crecimiento epidérmico y ácido graso sintetaza (Fas).
Factor de transcripción NF-κB.
Enzimas ciclooxigenasa y lipoxigenasa.
Enzimas NAD (P) H oxidasas, la fosfolipasa A2o la fosfolipasa C.
Promoción de salida de iones de calcio desde el retículo endoplásmico.
Inducción de la expresión del óxido nítrico sintetasa-3
Incremento de la producción de ácido araquidónico.
De todos estos mecanismos el mejor estudiado es la activación independiente de ligando de receptores como el ácido graso sintetaza. (4
El ácido graso sintetaza (Fas) activado provoca la rotura proteolítica de la procaspasa-8 y activa la caspasa-8. Esta última es un elemento importante no solo para la producción de los radicales libres de oxígeno sino también para la activación de la ruta extrínseca de apoptosis y para la ruptura proteolítica de Bid (BH3interacting-domaindeathagonist), que dan lugar al fragmento truncado de Bid (tBid), promotor de activación de la ruta intrínseca mitocondrial (Fig. 2). El daño mitocondrial originado por la activación de la caspasa-8 y del tBid, solo se ha podido demostrar en las líneas celulares del cáncer colorrectal estimuladas por el ácido desoxicólico y litocólico. (4
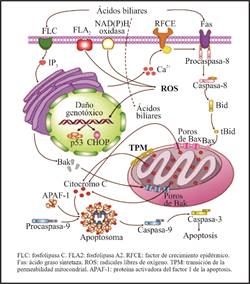
Fig. 2 Elementos con los que interactúan los ácidos biliares para desencadenar el proceso inflamatorio en las células epiteliales.
Los ácidos biliares son capaces de inducir la expresión de NF-κB a través de diferentes mecanismos en los que están implicados la enzima NAD (P) H oxidasa, la bomba sodio/potasio-ATPasa, el citocromo P450 y el calcio, así como el complejo respiratorio mitocondrial IV. (33) El factor de transcripción NF-κB es esencial en varios procesos celulares como inflamación, inmunidad, proliferación celular y apoptosis. Todo este proceso es responsable, al menos en parte, de la resistencia a la apoptosis delas células intestinales una vez que se desencadena la inflamación inducida por los niveles elevados de ácidos biliares en la luz intestinal.
Uno de los genes supresores de tumores más estudiado es el gen p53, ubicado en el cromosoma 17p, que muta en el 50-70 % de los tumores en humanos, donde la pérdida de la función supresora de tumor dela proteína p53 ocurre en un momento tardío de la carcinogénesis. (34 Dado que p53 está relacionado con la respuesta apoptótica a diferentes tipos de estrés celular (principalmente al daño en el ADN), se reporta que la resistencia a la apoptosis inducida por ácidos biliares es dependiente de la proteína p53.35 Aunque diferentes autores han intentado dilucidar la función de este factor de transcripción en la inducción de apoptosis por ácidos biliares en células colónicas, los datos obtenidos en diferentes líneas de cáncer colorrectal sugieren que el ácido desoxicólico es capaz de promover la apoptosis de forma independiente de la p53. (36
Conclusión
Los ácidos biliares en el intestino no solo regulan la digestión y absorción de las grasas, sino que desempeñan una función clave como moléculas de señalización en la modulación de la proliferación de células epiteliales, la expresión de genes y el metabolismo energético mediante la activación delos receptores nucleares, los que mantienen su homeostasis, que cuando se interrumpe promueve su acción toxicológica, que se traduce en trastornos metabólicos y en el proceso inflamación-carcinogénesis digestiva.